Курсовая по фарм химии. курсовая фх, 1804. Включая жидкостную хроматографию, в процессе разработки
 Скачать 202.74 Kb. Скачать 202.74 Kb.
|
ВВЕДЕНИЕВ фармацевтической промышленности все производимые продукты должны быть самого высокого качества, чтобы обеспечить наименьший риск для пациентов. Чтобы гарантировать, что товары проходят определенные стандарты, исследователи, производители и разработчики используют различные технические средства и аналитические методы, включая жидкостную хроматографию, в процессе разработки. Жидкостная хроматография - это аналитический метод, который используется для разделения определенного образца на отдельные компоненты. Разделение происходит при взаимодействии образца с подвижной (жидкой) и неподвижной фазами (колонкой). Различные части образца отделяются в зависимости от их полярности; они будут иметь различные уровни сродства к подвижной фазе, что приведет к миграции через колонку с разной скоростью. Смешанные компоненты помещаются в верхнюю часть колонки стационарной фазы, которая обычно представляет собой мелкодисперсное твердое вещество-адсорбент, такое как диоксид кремния. Она должна быть распределена равномерно, чтобы свести к минимуму наличие пузырьков воздуха, которые могут повлиять на результаты теста. Выход колонки закупоривают стеклом, ватой или пористой пластиной. При прохождении подвижной фазы смесь разделяется на полосы. Затем они могут быть собраны и проанализированы другими методами. Метод работает, когда компоненты в смеси притягиваются к поверхности адсорбента неподвижной фазы с различной степенью в зависимости от их индивидуальной полярности и их уникальных структурных характеристик; компонент с более высоким сродством к неподвижной фазе будет мигрировать вниз по колонке медленнее, чем компонент, который имеет большее сродство к подвижной фазе. (ВЭЖХ), которая прокачивает смесь образцов через колонку под высоким давлением. Алкилуреиды сульфокислот снижают уровень сахара в крови и потому используются для лечения диабета ІІ типа (ахрестического диабета). Известно более 15 тыс. сульфамидов с гипогликемическим действием, среди которых важное место занимают сульфанилмочевины и их производные (хлорпропамид, толбутамид, карбутамид, Глибенкламид). Одним из способов проверки качества алкилуреиды сульфокислот состоит в применении ВЭЖХ. ГЛАВА 1. ОБЗОР ЛИТЕРАТУРЫВысокоэффективная жидкостная хроматография в фармацевтикеВЭЖХ – это форма жидкостной хроматографии, которая обычно используется в фармацевтической промышленности, поскольку она может обеспечить точные результаты, которые требуются. Результаты могут быть использованы для количественного и качественного анализа готовых лекарственных препаратов и их ингредиентов в процессе производства. Это достигается путем разделения, количественной оценки и идентификации компонентов в смеси и может быть использовано для выявления идентичности лекарственного средства и мониторинга прогресса терапии заболевания. Одним из основных преимуществ ВЭЖХ является его способность выяснять структуру и определять количество примесей в фармацевтических препаратах. ВЭЖХ особенно подходит для соединений, которые не легко улетучиваются, термически нестабильны и имеют высокие молекулярные массы. Поэтому она может количественно определять препарат в его чистой и лекарственной форме[1]. Однако одним из недостатков ВЭЖХ является то, что ему должны предшествовать калибровочные испытания, которые могут увеличить затраты. Поскольку ВЭЖХ прост, специфичен, быстр, точен, его можно успешно и эффективно применять для рутинного анализа контроля качества лекарственных средств оптом и фармацевтической лекарственной формы. В целом жидкостная хроматография является полезным аналитическим инструментом для установления компонентов рецептуры лекарственного средства, позволяя исследователям количественно определить рецептуру и определить, есть ли какие-либо примеси в продукте. 1.2 Производные алкилуреидов сульфокислотВ настоящее время известно более 15 000 сульфамидных производных, обладающих гипогликемическим действием. Идея их создания зародилась в результате изучения побочных эффектов сульфаниламидов, одним из которых было снижение содержания сахара в крови. Наибольшую гипогликемическую активность проявили сульфонилмочевины и их производные (сульфонилтиомочевины, сульфонилсемикарбазиды, сульфонилтиосемикарбазиды, сульфонамидомочевины), а также гетериламиды сульфокислот (сульфонамидооксадиазолы, сульфонамидотиадиазолы, сульфонамидопиримидины). Установлено также, что противодиабетическим действием обладают бигуаниды. Общую формулу производных сульфонилмочевины можно представить следующим образом (рис 1.1): 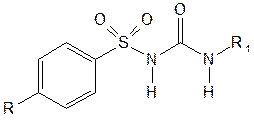 Рис.1.1 –Общая формула производных сульфонилмочевины Гипогликемическое действие обусловливает наличие группы (рис 1.2). 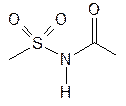 Рис.1.2 – Группасульфонилмочевины Исходными продуктами синтеза алкилуреидов сульфокислот служат производные анилина или толуола. Синтез включает получение сульфаниламида, который затем сочетают с производными мочевины (рис 1.3): 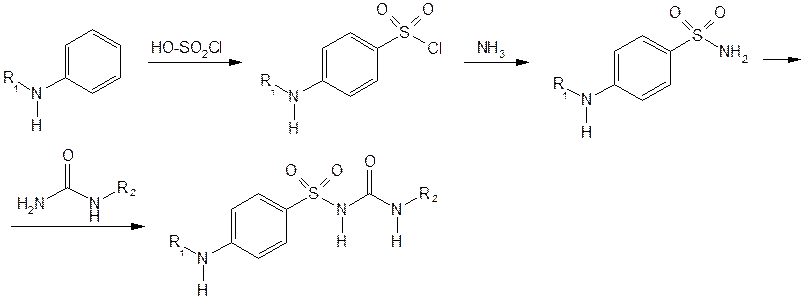 Рис.1.3 – Синтез алкилуреидов сульфокислот Производные сульфонилмочевины (табл. 1.1) представляют собой белые кристаллические вещества .Они практически нерастворимы в воде, растворимы или мало растворимы в этаноле. Для идентификации алкилуреидов сульфокислот (гликлазида, глипизида, глибенкламида и др.) используют ИК-спектроскопию. ИК-спектры лекарственных веществ, растертых в вазелиновом масле, регистрируют в области 4000–650 см–1. Они должны соответствовать спектрам стандартных образцов. Подлинность производных сульфонилмочевины можно установить методом спектрофотометрии в УФ-области по расположению максимумов поглощения и по удельному показателю поглощения. Раствор карбутамида в этаноле имеет максимум при 269 нм, в 0,1 М растворе хлороводородной кислоты – при 266 и 272 нм, а в 0,1 М растворе гидроксида натрия — при 255 нм. УФ-спектр раствора гликлазида имеет максимум поглощения при 228 нм, раствора глибенкламида в метаноле – три максимума (227, 273 и 293 нм), наибольшее значение удельного показателя поглощения (597) при длине волны 227 нм. Для подтверждения подлинности глипизида и гликвидона устанавливают идентичность УФ-спектров поглощения спектрам стандартных образцов этих лекарственных веществ. Подлинность глипизида устанавливают также методом ВЭЖХ по времени удерживания испытуемого вещества, которое должно быть сопоставимым со временем удерживания стандарта [7]. Для подтверждения подлинности гликвидона используют метод ТСХ. Основное пятно на хроматограмме должно соответствовать по расположению и интенсивности флуоресценции основному пятну стандартного образца. Методом ВЭЖХ в гликлазиде устанавливают допустимое содержание примесей (не более 0,2%) других производных сульфонилмочевины. Примесь остаточных растворителей (этилацетата) определяют методом ГЖХ. Подлинность производных сульфонилмочевины устанавливают также с помощью химических реакций. При нагревании карбутамида в растворе гидроксида калия происходит гидролиз с образованием аммиака, который можно обнаружить по запаху или по изменению окраски лакмусовой бумаги (рис 1.5). 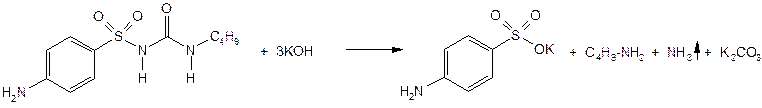 Рис.1.5 – Гидролиз карбутамида с образованием аммиака Аналогичный химический процесс происходит при испытании в тех же условиях глибенкламида, гликлазида и др. Реакция гидролиза происходит также при кипячении производных сульфонилмочевины с разбавленной серной кислотой. Последующее добавление 30%-ного раствора гидроксида натрия приводит к выделению жирных капель аминов, имеющих характерный запах. После более продолжительного нагревания (10–30 мин) в присутствии 50%-ной серной кислоты (с обратным холодильником), последующего охлаждения и нейтрализации выделяется осадок сульфамида. Общая схема гидролиза карбутамида, гликлазида, глибенкламида в кислой среде (рис 1.6). 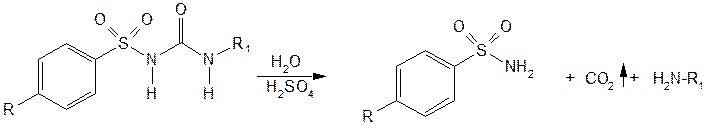 Рис.1.6 – Общая схема гидролиза карбутамида, гликлазида, глибенкламида в кислой среде Наличие серы устанавливают после спекания со смесью карбоната и нитрата калия. Затем плав растворяют в хлороводородной кислоте и в фильтрате открывают сульфат-ион. В том же фильтрате обнаруживают хлорид-ионы, образующиеся при разрушении глибенкламида. Сульфамидную группу в глибенкламиде обнаруживают по образованию комплексного соединения с ионом меди (II), выпадающего в виде осадка зеленовато-голубого цвета. Из раствора карбутамида в этаноле под действием сульфата меди (II) выпадает окрашенный мелкокристаллический осадок, который постепенно обесцвечивается. Карбутамид при нагревании с 0,2%-ным раствором нингидрина в бутиловом спирте приобретает фиолетовое окрашивание. Карбутамид и глибенкламид могут быть идентифицированы с помощью цветных и микрокристаллоскопических реакций. В качестве реактивов для этой цели используют 10%-ный раствор иодида калия, 5%-ный раствор хлорида кадмия, железо- и медноиодидный комплексы, 1%-ный раствор в этаноле a-нафтола в присутствии концентрированной серной кислоты [8]. При взаимодействии указанных лекарственных веществ с аллоксаном в присутствии солей кальция образуются окрашенные производные пурпуровой кислоты. Эту реакцию используют в среде диметилформамида для спектрофотометрического определения при длине волны 480 нм. Раствор карбутамида в хлороводородной кислоте с раствором фосфорномолибденовой кислоты в азотной кислоте образует осадок в виде желто-зеленых хлопьев, которые постепенно превращаются в мелкие кристаллы. Карбутамид дает ряд других реакций, подтверждающих его подлинность. При пиролизе его кристаллов выделяется аммиак, а плав приобретает фиолетово-красный цвет. После обработки плава этанолом раствор окрашивается в красновато-фиолетовый цвет. При нагревании кристаллов карбутамида и резорцина с 1 мл серной кислоты смесь окрашивается в темно-красный цвет, после разбавления водой и добавления щелочи появляется желто-зеленая флуоресценция. Карбутамид отличается от других производных сульфонилмочевины наличием первичной ароматической аминогруппы в молекуле. Способы его испытаний по этой функциональной группе такие же, как и при анализе сульфаниламидов. Для испытания подлинности используют реакцию диазотирования и азосочетания с b-нафтолом в щелочной среде. Появляется красное окрашивание. Количественное определение гликлазида выполняют методом неводного титрования в среде безводной уксусной кислоты, используя в качестве титранта 0,1 М раствор хлорной кислоты, устанавливая конечную точку потенциометрическим методом. Этим методом количественно определяют и другие производные сульфонилмочевины. Метод ВЭЖХ используют для количественного определения глипизида по стандартному образцу. Подвижной фазой служит буферный раствор (водные растворы мононатрийфосфата и гидроксида натрия до pH 6) в смеси с метанолом (55:45). Детектируют на спектрофотометре при длине волны 225 нм. Гликвидон и другие производные сульфонилмочевины в лекарственных формах количественно определяют методом УФ-спектрофотометрии в указанных выше максимумах поглощения. Хранят лекарственные вещества в сухом, защищённом от света месте, при температуре до 25 °C. Большинство из них относятся к списку Б. Производные сульфонилмочевины стимулируют образование инсулина b-клетками поджелудочной железы, понижая при этом содержание сахара в крови. Назначают при различных формах сахарного диабета в виде таблеток; карбутамид по 0,5 г, глибенкламид по 0,005 г, гликлазид по 0,08 г, глипизид по 0,005 и 0,01 г, гликвидон по 0,03 г [9]. 1.3 Стабильность в фармацевтических препаратахИзучение стабильности в фармацевтических препаратах жизненно важно из-за необходимости избегать потенциально токсичных продуктов разложения. В таких исследованиях необходимо продемонстрировать, что содержание сопротивления в препарате не изменилось со временем. Также, если деградация имеет место, необходимо будет идентифицировать и количественно оценивать продукты деградации. Хорошей иллюстрацией этого являются условия жидкостной хроматографии, разработанные для определения пилокарпина в офтальмологических растворах. Идентичные условия используются для определения продуктов разложения пилокарпина. Часто, когда соединение существует в различных изомерных формах, оно представляет собой смесь изомеров. Альтернативно может быть потребность контролировать образцы одного изомера для обеспечения его чистоты. В обоих случаях важно иметь возможность отделять изомеры с помощью жидкостной хроматографии. Это особенно важно для веществ сопротивления, в виду того что изомеры почти наверняка будут иметь различные фармакологические и иногда токсикологические свойства. Энантиомеры - это типы изомеров, которые вызвали большой интерес, когда резкие тератогенные эффекты талидомида (дети, рожденные матерями, которые принимали талидомид, родились с усеченными конечностями) были приписаны одному из двух энантиомеров, присутствующих в лекарственном веществе. Энантиомеры имеют идентичные физико-химические свойства и поэтому не могут быть разделены на обычной хроматографии. Таким образом, при жидкостном хроматографическом разделении энантиомеров необходимо использовать «хиральный селектор». Это может принимать форму хирального деривационного агента, хиральной добавки подвижной фазы или хиральной стационарной фазы [10]. ГЛАВА 2 АНАЛИЗ ЛЕКАРСТВЕННЫХ СРЕДСТВ, ПРОИЗВОДНЫХ АЛКИЛУРЕИДОВ СУЛЬФОКИСЛОТ ПРИ ПОМОЩИ ВЭЖХСтабильность карбутамида,гликлазида и иглибенкламида испытывались в различных условиях. Были проведены следующие испытания: Стабильность в кислых условиях: 50 мг каждой соли взвешивали в мерную колбу (100 мл) и добавляли 2 мл 1н HCl. Затем колбу выдерживали либо при комнатной температуре в течение 5 часов, либо при 80°С в течение 5 часов. После окончания каждого эксперимента охлаждения до комнатной температуры добавлялось 2 мл 1N NaOH и добавлялась подвижная фаза до 100 мл. Результат определялся с помощью ВЭЖХ. Стабильность при основных условиях: 50 мг соответствующей соли взвешивались в мерную колбу (100 мл) и добавлялось 2 мл 1н NaOH. Затем колбу выдерживают либо при комнатной температуре в течение 5 часов, либо при 80°С в течение 5 часов. После окончания каждого эксперимента иохлаждения до комнатной температуры добавлялось 2 мл 1н HCl и добавлялась подвижная фаза до 100 мл..Результат определяют с помощью ВЭЖХ. Стабильность в окислительных условиях: 50 мг соответствующей соли взвешивалось в мерной колбе (100 мл) и добавлялось 2 мл 3%H2О2. Затем колбу выдерживалась либо при комнатной температуре в течение 5 часов, либо при 80°С в течение 5 часов. После окончания каждого эксперимента иохлаждения до комнатной температуры добавлялась подвижная фаза до 100 мл. Результат определяют с помощью ВЭЖХ. Во всех случаях измерения ВЭЖХ проводили при следующих условиях с УФ-детектированием: Таблица 2.1– Характеристики колонки ВЭЖХ
Результаты этих испытаний обобщены в следующих таблицах 2.2-2.5. Таблица 1.1– Результаты испытаний ВЭЖХ карбутамида
В таблица 2.2-2.4 представлены цифры, которые показывают растворимость лекарственных средств в различных средах. Очевидно, что гликлазида обладает сравнимой и, в щелочных условиях, даже значительно повышенной стабильностью по сравнению с иглибенкламидом и карбутамидом.  Рис. 2.1 Хроматограмма раствора субстанции гликлазида ЗАКЛЮЧЕНИЕСегодня ВЭЖХ представляет собой хорошо оформленный инструментальный метод, который широко применяют в фармацевтической промышленности, поскольку она может обеспечить точные результаты, которые требуются. Результаты могут быть использованы для количественного и качественного анализа готовых лекарственных препаратов и их ингредиентов в процессе производства. Это достигается путем разделения, количественной оценки и идентификации компонентов в смеси и может быть использовано для выявления идентичности лекарственного средства и мониторинга прогресса терапии заболевания. В ходе данной работы: 1. Проведен обзор литературы по теме «Применение метода ВЭЖХ в фармацевтическом анализе лекарственных средств. 2. На основе полученных данных можно сделать вывод, что ВЭЖХ является наиболее полноценным методом качественного и количественно определения состава лекарственных веществ; 3. Рассмотрен на примере работы Стороженко С.Е. "Разработка состава и технологические исследования инновационных лекарственных форм на базе гипогликемического средства – гликлазида " качественный состав лекарственных препаратов, производных алкилуреидов сульфокислот. Другие формы ВЭЖХ, которые используются в фармацевтической промышленности, включают ВЭЖХ с обращенной фазой, денатурирующий и иммобилизованный ферментный реактор (IMER). Ее также можно использовать в сочетании с другими аналитическими методами для дальнейшего выяснения компонентов смесей [2]. ВЭЖХ-УФ использует УФ в качестве формы обнаружения. Преимущество этого метода заключается в том, что он не требует сложной обработки и процедур, обычно связанных с традиционным хроматографическим методом, что делает его менее трудоемким и экономичным. Однако некоторые компоненты могут иметь слабые УФ-хромофоры, если используется УФ-детектирование, или полностью удерживаться на жидкостной хроматографической колонке. Для обнаружения компонентов диодная матрица и детектор быстрого сканирования полезны для идентификации пиков и контроля чистоты пиков. Вместо этого флуоресцентные и электрохимические детекторы значительно более чувствительны к соответствующим аналитам и более селективны, чем УФ-детекторы для многих соединений [3]. Наиболее чувствительным методом детекции ВЭЖХ является восстановительное электрохимическое детектирование, которое дало отличные результаты при исследовании некоторых классов лекарственных средств. Другой метод, с которым можно сочетать ВЭЖХ - это масс-спектрометрия (ВЭЖХ / МС); хроматограф присоединяется через интерфейс к масс-спектрометру. Эта форма анализа может исследовать широкий спектр компонентов, включая те, которые являются термически лабильными, проявляют высокую полярность или имеют высокую молекулярную массу. Компоненты, элюированные из колонки, вводятся в масс-спектрометр на специализированном интерфейсе. Двумя наиболее распространенными интерфейсами, используемыми для ВЭЖХ / МС, являются интерфейсы ионизации электрораспылением и химической ионизации атмосферного давления. это процентное содержание вещества в лекарственном препарате. Чем выше его количество, тем лучше оно растворяется в среде например в организме человека. Соответственно стабильность этого препарата при той или иной температуре, с которой он не выделяется | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
