Влияние фосфора на рост и развитие растений
 Скачать 1.37 Mb. Скачать 1.37 Mb.
|
|
Министерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего образования «Нижегородский государственный архитектурно-строительный университет» (ННГАСУ) Кафедра водоснабжения, водоотведения, инженерной экологии и химии Курсовая работа по дисциплине «Биохимия, биофизика и физико-химические основы жизнедеятельности» Тема: «Влияние фосфора на рост и развитие растений» Выполнил: Бревнов Никита Евгеньевич Студент 1 курса очной формы обучения, группы ЭП-44 Проверил: кандидат технических наук, доцент кафедры водоснабжения, водоотведения, инженерной экологии и химии Патова Мария Александровна Нижний Новгород 2021 Содержание Введение…………………………………………………………………….4 1.Теоретическая часть………………………………………………….…..5 1.1 История открытия фосфора……………………………………..5 1.2 Свойства………………………………………………………….7 1.2.1 Физические свойства…………………………………...7 1.2.2 Химические свойства…………………………………..7 1.2.3 Вывод……………………………………………………8 1.3 Биологическая роль……………………………………………..9 1.4 Области применения…………………………………………...11 1.4.1 Применение в медицине………………………………11 1.4.2 Применение в промышленности……………………..11 1.4.3 Применение в сельском хозяйстве…………………...12 1.4.4 Вывод…………………………………………………..13 1.5 Влияние фосфора на растения…………………………….…..14 1.5.1 Реакции в почве………………………………………..14 1.5.2 Недостаток …………………………………………….14 1.5.3 Избыток………………………………………………..14 1.5.4 Тестирование в почве…………………………………15 1.6 Получение……………………………………………................16 2.Практическая часть. Исследование влияния фосфора на рост семян…………………………17 2.1Методика……………….………………………………………..17 2.1.1Препарат дигидроортофосфат калия………………….17 2.1.2 Оценка влияния на рост семян…………………….….17 2.1.3 Итоги эксперимента…………………………….……..20 Вывод……………………………………………………………………..21 Список литературы………………………………………………………22 Введение Один из главных и значимых элементов в питании растений – это фосфор. Он входит в состав как минеральных, так и органических соединений, находящихся в растениях. В наибольшей потребности фосфора растения нуждаются на самых ранних этапах своего развития, во время формирования корневой системы, а также в фазе цветения и плодоношения. Критической в отношении фосфорного питания для всех культур является фаза всходов, когда слабая корневая система способна поглощать фосфорные соединения лишь на ограниченной ей территории. Недостаток фосфора в этот период вызывает в дальнейшем серьезные изменения в ростовых и репродуктивных процессах растений. Актуальность Я считаю, что выбранная мной тема всегда является актуальной, например, в сельском хозяйстве, где скорость и качество прорастания растений зависит от количества фосфора в почве. Цель работы: изучить влияния фосфора на рост и развитие растений. Задачи: Изучить физико-химические свойства фосфора. В ходе анализа различных литературных источников изучить основные функции, влияние на физиологические процессы растений, естественные источники и применение в различных областях. Провести эксперимент, в результате которого изучить влияние фосфора на рост растений. 1.Теоретическая часть 1.1 История открытия фосфора В 1669 г. гамбургский алхимик-любитель Бранд, разорившийся купец, мечтавший с помощью алхимии поправить свои дела, подвергал обработке самые разнообразные продукты. Предполагая, что физиологические продукты могут содержать "первичную материю", считавшуюся основой философского камня, Бранд заинтересовался человеческой мочой. Он собрал около тонны мочи из солдатских казарм и выпаривал ее до образования сиропообразной жидкости. Эту жидкость он вновь дистиллировал и получил тяжелое красное "уринное масло". Перегнав это масло еще раз, он обнаружил на дне реторты остаток "мертвой головы" (Caput mortuum), казалось бы ни к чему непригодной. Однако, прокаливая этот остаток длительное время, он заметил, что в реторте появилась белая пыль, которая медленно оседала на дно реторты и явственно светилась. Бранд решил, что ему удалось извлечь из "маслянистой мертвой головы" элементарный огонь, и он с еще большим рвением продолжил опыты. Превратить этот "огонь" в золото ему, конечно, не удалось, но он все же держал в строгом секрете свое открытие фосфора (от греч.- свет и "несу", т.е. светоносца). Однако о секрете Бранда узнал некто Кункель, служивший в то время алхимиком и тайным камердинером у саксонского курфюрста. Кункель попросил своего сослуживца Крафта, отправлявшегося в Гамбург, выведать у Бранда какие-либо сведения о фосфоре. Крафт, однако, сам решил воспользоваться секретом Бранда. Он купил у него секрет за 200 талеров и, изготовив достаточное количество фосфора, отправился в путешествие по Европе, где с большим успехом демонстрировал перед знатными особами свечение фосфора. В частности, в Англии он показывал фосфор королю Карлу II и ученому Бойлю. Тем временем Кункелю удалось самому приготовить фосфор способом, близким к способу Бранда, и в отличие от последнего он широко рекламировал фосфор, умалчивая, однако, о секрете его изготовления. В 1680 г. независимо от предшественников новый элемент был получен знаменитым английским физиком и химиком Робертом Бойлем, который, так же как и Кункель, опубликовал данные о свойствах фосфора, но о способе его получения сообщил в закрытом пакете лишь Лондонскому королевскому обществу (это сообщение было опубликовано только через 12 лет, уже после смерти Бойля), а ученик Бойся – А. Ганквиц изменил чистой науке и вновь возродил «фосфорную спекуляцию» в виде широкой производственной деятельности по изготовлению этого вещества: 50 лет он широко торговал фосфором по весьма высокой цене. В Голландии, например, унция (31,1 г) фосфора стоила в то время 16 дукатов. По поводу природы фосфора высказывались самые фантастические предположения. В XVIII в. фосфором занимались многие крупные ученые и среди них Маргграф, усовершенствовавший способ получения фосфора из мочи путем добавления к последней хлорида свинца (1743). 1.2 Свойства 1.2.1 Физические свойства Фосфор (P) – вследствие высокой активности в свободном состоянии в природе не встречается. Электронная конфигурация 1S2 2S2 2P6 3S2 3P3 Фосфор – неметалл (то, что раньше называли металлоид) средней активности. На наружной орбите атома фосфора находятся пять электронов, причем три из них не спарены. Поэтому он может проявлять валентности 3–, 3+ и 5+. Для того чтобы фосфор проявлял валентность 5+, необходимо какое-либо воздействие на атом, которое бы превратило в не спаренные два спаренных электрона последней орбиты. Фосфор часто называют многоликим элементом. Действительно, в разных условиях он ведет себя по-разному, проявляя то окислительные, то восстановительные свойства. Многоликость фосфора – это и его способность находиться в нескольких аллотропных модификациях. 1.2.2 Химические свойства. Фосфор занимает 15 место в периодической таблице Менделеева и входит в одну группу с азотом, мышьяком и сурьмой. Хотя на валентном уровне он и имеет целых 5 электронов, однако 5 связей образуются довольно редко. Фосфор – очень химически активный элемент, особенно белый фосфор. Как следствие он может вступать в самые разнообразные химические реакции, выступая как в качестве окислителя (с элементами, расположенными ниже и левее в таблице Менделеева), так и восстановителя (с элементами, расположенными выше и правее в таблице Менделеева). При взаимодействии с кислородом воздуха образуются оксиды – ангидриды соответствующих кислот: 4P +3O2 > 2P2O3 4P + 5O2 > 2P2O5 При взаимодействии фосфора с галогенами образуются галогениды с общей формулой PHal3 и PHal5: 2P + 3Cl2 > 2PCl3 2P + 5Cl2 > 2PCl5 При взаимодействии фосфора с серой образуются сульфиды: 2P + 3S > P2S3 2P + 5S > P2S5 При взаимодействии с металлами фосфор проявляет свойства окислителя, продукты реакции называют фосфидами. Например, кальций и магний реагируют с фосфором с образованием фосфидов кальция и магния: 2P + 3Ca > Ca3P2 2P + 3Mg > Mg3P2 1.2.3 Вывод Фосфор является необходимым элементом питания растений. Он входит в состав нуклеиновых кислот, мембран, фосфолипидов. Фосфор является элементом энергосистемы, входит в состав макроэргических соединений. Как запасающее вещество откладывается в семенах растений. Если в минеральном питании недостает фосфора, то падает активность фотосинтеза, дыхания, так как нарушается синтез хлорофилла. 1.3 Биологическая роль. Фосфор является обязательной составной частью живой клетки растений, он входит в состав нуклеиновых кислот, которые участвуют в таких важных процессах жизнедеятельности растительных организмов, как синтез белков и передача наследственных свойств. В свою очередь, нуклеиновые кислоты образуют в растительных организмах комплексы с белками, так называемые нуклеопротеиды, участвующие в построении клеточных ядер. Фосфор содержится также в веществах, определяющих направление и скорость биохимических процессов в растениях, — в витаминах, гормонах, ферментах. Как показали исследования последнего времени, особенно велика роль фосфора в процессах дыхания растений и синтеза углеводов — крахмала, сахаров. Кроме того, фосфор входит в состав других органических соединений, имеющих большое значение в жизни растений: фосфатидов, фитина, сахарофосфатов и др. Фосфатиды — вещества, сходные с жирами, но отличающиеся от них наличием фосфора и азота. Фосфатиды являются частью протоплазмы и играют важную роль в процессах проникновения и обмена веществ в клетках растений. Больше всего их находится обычно в зародышах семян растений. В семенах пшеницы фосфатидов в среднем содержится 0,6–0,7 %, в семенах гороха 1,1–1,3 и в семенах люпина синего около 2,2 %. Фитин, представляющий собой кальциево-магниевую соль инозитфосфорной кислоты, является запасным веществом в семенах растений. Содержание его довольно значительно и составляет, например, в семенах льна 1,6 %, подсолнечника 2,0 %. При прорастании семян фитин разлагается, при этом образуются более простые соединения фосфорной кислоты, используемые проростками и молодыми растениями для питания. В последние годы установлена большая роль фосфора в накоплении энергии, за счет которой осуществляются многие важнейшие процессы в растительном организме. Считают, что энергия света, необходимая для синтеза органического вещества в растениях, предварительно накапливается в сложном органическом соединении — аденозинтрифосфорной кислоте. В состав этой кислоты входят три остатка молекул фосфорной кислоты, последовательно соединенных так называемыми макроэргическими связями, то есть связями, несущими большой запас энергии. В процессах биохимического обмена веществ остатки фосфорной кислоты могут с помощью ферментов отщепляться от аденозинтрифосфорной кислоты и переноситься на другие соединения вместе с энергией, которую они несут. Неорганические соединения фосфора имеются во всех частях растений — стеблях, листьях, цветках, корнях и семенах. Количество неорганических фосфатов может сильно изменяться в зависимости от степени обеспеченности растений фосфором и от фазы развития растений. Накопление неорганического фосфора в стеблях растений — один из признаков достаточной обеспеченности растений фосфорной пищей. Неорганические соединения фосфора могут накапливаться в растениях в виде солей калия, кальция и магния. Они служат запасными фосфорсодержащими веществами и используются по мере надобности на построение органических соединений, в виде которых обычно и находится большая часть фосфора в растении. Регулируя уровень фосфатного питания растений, можно в определенной мере управлять темпами их роста и развития и, что часто не менее важно, изменять качество урожая. Участие фосфора в углеводном обмене растений позволяет с помощью фосфорных удобрений воздействовать на повышение содержания сахара в корнях сахарной свеклы, крахмала в клубнях картофеля и т. д. Элементы пищи растений, в том числе и фосфор, могут поглощаться не только через корни, но и через листья. При внекорневом питании фосфаты быстро передвигаются в другие части растений, включая и корни. С помощью метода меченых атомов было установлено, что часть поступившего в растения фосфора вновь выделяется через корни. Большая часть растений в первый период жизни обладает слабой способностью усваивать труднорастворимые фосфаты. Поступление фосфора в достаточном количестве с момента прорастания семян усиливает рост корневой системы, вследствие чего резко возрастает способность растений обеспечивать себя питательными веществами и влагой из почвы. Растения быстрее развиваются, а усвоенная ими фосфорная кислота используется более продуктивно, так как большая часть ее при этом направляется на образование репродуктивных органов. Обильное питание растений фосфором значительно ускоряет образование зерна и существенно изменяет соотношение между соломой и зерном у злаков в пользу последнего. На долю фосфора приходятся обычно десятые доли процента от веса сухих растений. Наиболее богаты им семена растений, в стеблях и листьях фосфора значительно меньше. В то время как количество фосфора в репродуктивных органах довольно постоянно, в стеблях и листьях оно может изменяться в весьма широких пределах в зависимости от условий питания растений. 1.4 Области применения. Фосфор содержится земной коре, также фосфор есть и в морской воде. Он способен образовывать 190 минералов. Фосфор называют элементом жизни, так как содержится в животных тканях, зеленых растениях, белках и так далее. 1.4.1 Применение в медицине. На сегодняшний день из фосфора получают класс терапевтических потенциальных средств, которые лечат заболевания мягких тканей и костей, сопровождающихся нарушением обмена кальция – биофосфонаты. Каждый элемент имеет свой спектр активности. Они устойчивы к энзиматическому гидролизу, обладают сродством к ионам металлов, образовывают нерастворимые и растворимые хелатные агрегаты и комплексы. Самым распространенным и применяемым является этидронат. Он эффективный при нарушениях в организме обмена кальция. Его применяют при прогрессирующем оссифицирующем миозите, при болезни Педжета, при остеопорозах, гетерогенной оссификации и опухолевом остеолизе. 1.4.2 Применение в промышленности. Ортофосфорную кислоту используют широко. Ее применяют для производства комбинированных и фосфорных удобрений, которые повышают урожайность сельскохозяйственных культур, придают растениям устойчивости к неблагоприятным климатическим условиям и зимостойкости. Кроме того, удобрения прекрасно действуют на почву, способствуют структурированию, изменению растворимости содержащихся веществ в почве, развитию почвенных бактерий, подавлению образования органических вредных веществ. В пищевой промышленности ортофосфорная кислота также используется. Она приятная на вкус и в разбавленном виде ее добавляют в мармелад, лимонад, сиропы для улучшения вкусовых качеств. Подобными свойствами обладают соли фосфорной кислоты. Например, гидрофосфаты кальция являются составляющей хлебопекарных порошков, повышает вкус хлеба и булочек. На основе ортофосфорной кислоты производят фосфодревесные негорючие плиты, огнезащитные краски, фосфатный негорючий пенопласт. Соли фосфорной кислоты защищают от радиации, умягчают воду, устраняют котельную накипь и входят в состав моющих средств. Фосфорорганические соединения (пластификаторы, экстрагенты, смазочные вещества, абсорбенты) используются в холодильных установках и как присадка к пороху. Алкилфосфаты выступают в роли поверхностно-активных веществ, антифриз, специальных удобрений, антикоагулянтов латекса. Из красного фосфора делают спички. Вместе с клеем и толченым стеклом его наносят на боковые части спичечной коробки. Фосфид цинка (Zn3 Р2) применяется для борьбы с грызунами. Из белого фосфора производят зажигательные бомбы, дымообразующие снаряды, шашки, гранаты, дымовые завесы. 1.4.3 Применение в сельском хозяйстве. Большинство (80–90%) добываемой фосфатной руды идет на получение удобрений. В 1799 было доказано, что фосфор необходим для нормальной жизнедеятельности растений. Накапливаясь в биомассе, фосфор исчезает из почвы. Ежегодно мировой урожай уносит с полей несколько миллионов тонн фосфора, наряду с азотом и калием, поэтому необходимо возобновление его ресурсов в плодородном слое. В древние времена люди удобряли почву навозом, костями и гуано. Первое искусственное фосфорное удобрение – суперфосфат – было получено в Англии в 1839 Лаузом, а в 1842 там же было организовано его первое промышленное производство. В России первое предприятие по производству суперфосфата появилось в 1868. Сейчас его получают, обрабатывая апатит серной кислотой: Ca10(PO4)6F2 + 7H2SO4 = 3Ca(H2PO4)2 + 7CaSO4 + 2HF. Побочно получающийся сульфат кальция не отделяют. Более ценный продукт – двойной суперфосфат, так как в нем содержится в три раза больше фосфора по массе, его получают обработкой апатита фосфорной кислотой: Ca10(PO4)6F2 + 14H3PO4 +10H2O = 10Ca(H2PO4)2·H2O +2HF. Доля производства удобрений, содержащих в своем составе только один фосфор, падает, и все больше производится комплексных удобрений, содержащих два или три питательных элемента. Большая часть фосфорных удобрений, производимых в России, приходится на аммофос, диаммофос и азофоску. Ежегодное мировое производство фосфорных удобрений на начало 21 в. составило 41 млн. тонн, а суммарное количество всех удобрений – 190 млн. тонн. Основными производителями фосфорных удобрений являются Марокко, США и Россия, а основными потребителями – страны Азии, Латинской Америки и Западной Европы. Необходимый состав вносимого удобрения и его эффективность зависят от характеристик почвы, например, рН, но растворимость фосфатных удобрений определяет время, за которое происходит его усвоение растениями, и долю усвоенного фосфора, которая обычно мала и составляет около 20%. 1.4.4 Вывод Фосфор является важнейшим биогенным элементом и в то же время находит очень широкое применение в различных сферах: в фармакологии, в быту, в создании удобрений. 1.5 Влияние фосфора на растения 1.5.1 Реакции в почве. Фосфор содержится в почвах как в органической форме, так и в неорганической (минеральной) форме, и его растворимость в почве низкая. Существует равновесие между твердым фосфором в почве и фосфором в почвенном растворе. Растения могут поглощать только фосфор, растворенный в почвенном растворе, а поскольку большая часть почвенного фосфора существует в виде стабильных химических соединений, в любой момент времени для растений доступно лишь небольшое количество фосфора. Когда корни растений удаляют фосфор из почвенного раствора, часть фосфора, адсорбированного на твердой фазе, высвобождается в почвенный раствор для поддержания равновесия. Типы соединений фосфора, которые существуют в почве, в основном определяются ее pH, а также типом и количеством минералов в почве. Минеральные соединения фосфора обычно содержат алюминий, железо, марганец и кальций. В кислых почвах фосфор имеет тенденцию реагировать с алюминием, железом и марганцем, в то время как в щелочных почвах преобладает фиксация с кальцием. Оптимальный диапазон pH для максимальной доступности фосфора составляет 6.0-7.0. Во многих почвах разложение органических материалов и растительных остатков способствует увеличению количества фосфора в почве. 1.5.2 Недостаток Симптомы дефицита фосфора включают задержку роста и темно-фиолетовый цвет старых листьев, замедление цветения и развития корневой системы. У большинства растений эти симптомы проявляются, когда концентрация фосфора в листьях ниже 0.2%. 1.5.3 Избыток Избыток фосфора в основном препятствует усвоению других элементов, таких как железо, марганец и цинк. Чрезмерное удобрение фосфором является обычным явлением, и многие производители применяют излишне высокие количества фосфорных удобрений, особенно когда используются сложные удобрения или когда поливная вода подкисляется фосфорной кислотой. 1.5.4Тестирование в почве. Уровень содержания фосфора в почве дает меру способности почвы поставлять фосфор в почвенный раствор. Почвенный тест не измеряет общее количество фосфора в почве, потому что доступное количество фосфора намного меньше, чем общее количество. Он также не измеряет фосфор в почвенном растворе, потому что количество фосфора в почвенном растворе обычно очень мало и не отражает надлежащим образом количество фосфора, которое растения потенциально могут поглотить в течение вегетационного периода. Тест на фосфор почвы на самом деле является показателем, который помогает предсказать потребность культуры в удобрениях. Рекомендации по внесению удобрений определены на основе множества полевых испытаний на многих почвах и культурах. Различные методы тестирования приводят к различным значениям, которые необходимо интерпретировать соответствующим образом. Например, результат 25 ppm фосфора, полученный с помощью метода тестирования «Olsen», может иметь иную интерпретацию, чем такой же результат, полученный с помощью метода тестирования «Bray». Но на этом путаница не заканчивается - разные лаборатории, использующие один и тот же метод тестирования, могут определять разные интерпретации одних и тех же значений. Правильный отбор пробы почвы очень важен для получения результатов, которые действительно отражают уровень доступного фосфора. Например: Глубина отбора проб почвы - Поскольку фосфор в почве не подвижен, пробы, взятые с верхнего слоя почвы, обычно показывают более высокое количество фосфора, чем пробы, взятые из недр. Способы внесения удобрений - Большая часть внесенного в почву фосфора остается в пределах 1-2 дюймов от места нанесения. Следовательно, точное место отбора проб может значительно повлиять на результат. 1.6 Получение фосфора. Получение. Фосфор получают из апатитов или фосфоритов в результате взаимодействия с коксом и кремнезёмом при температуре около 1600 °С: 2Ca3(PO4)2 + 10C + 6SiO2 → P4 + 10CO + 6CaSiO3 или Ca3(PO4)2 + 3SiO2+5C = 3CaSiO3+5CO+2P. Образующиеся пары фосфора конденсируются в приёмнике под слоем воды в аллотропическую модификацию в виде белого фосфора. Вместо фосфоритов для получения элементарного фосфора можно восстанавливать углём и другие неорганические соединения фосфора, например, в том числе, метафосфорную кислоту: 4HPO3 + 10C → P4 + 2H2O + 10CO 2.Практическая часть. Исследование влияния фосфора на рост семян. 2.1Методика. Я решил провести эксперимент с семенами овса, выращивая их в течении пяти дней в чашках петри с использованием увлажненной бумаги. 2.1.1Препарат дигидроортофосфат калия. Дигидроортофосфат калия (KH2PO4). Это порошок белого цвета. Как его получить? Добавляют нужное количество ортофосфорной кислоты к гидроксидам. Дигидроортофосфат калия получают обработкой 50-55% ортофосфорной кислоты твердым ацетатом калия при молярном соотношении ацетата калия и фосфорной кислоты, равном (1-1,09):1, в течение 10-15 мин с последующим отделением осадка продукта от маточника и его сушкой. Можно использовать в качестве удобрений для растений. Перед применением нужно разводить и брать правильные дозировки, чтобы не навредить растениям. 2.1.2 Оценка влияния на рост семян. Для проведения своего эксперимента я взял период 5 дней. Ход эксперимента: Для проведения эксперимента я взял 3 чашки петри для контроля (вода), для 1% раствора и 0,5% раствора (KH2PO4) и специальную бумагу. Отобрал одинаковые по форме и здоровые семена овса для каждой чашки по 15 штук. Поместил семена овса в чашки петри и поставил их в одно и тоже место, для того чтобы они могли прорастать в одинаковых условиях. Смачивал специальную бумагу по мере ее высыхания, в среднем один раз в сутки. По истечению 5 дней провел подсчет корней и стеблей овса. Сделал вывод о влиянии фосфора на рост семян. Таблица 1 «Учёт прорастания семян и их описание»
При определении энергии прорастания и всхожести семян учитывают также поражение семян плесневыми грибами. Средний процент пораженных семян определяют визуально и устанавливают степень поражения в соответствии с таблицей:
Посчитать энергию прорастания семян по формуле: E=Nпроростков/Nобщее*100% Энергия прорастания семян: Для воды: E= 10/15*100%=66,7% Для KH2PO4 (1%): E= 9/15*100%=60% Для KH2PO4 (0,5%): E=13,3% 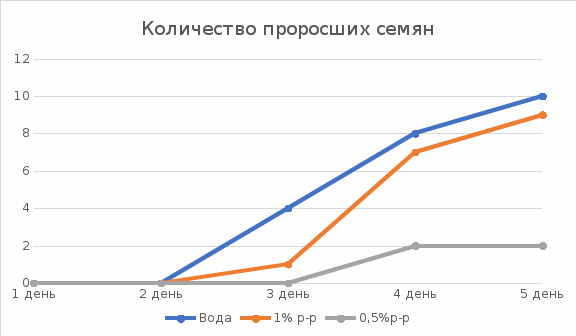 2.1.3 Итоги эксперимента. В ходе проделанного эксперимента можно сделать вывод, что при опыте с уменьшением концентрации дигидроортофосфата калия ростовые процессы тормозятся, длина корешка уменьшается. Степень поражения семян плесневыми грибами слабая до 5 %. Вывод. Фосфор – это элемент, который необходим для каждого растения и выполняет важную биологическую роль в их жизни. С помощью литературных и интернет-источником я изучил физико-химические свойства фосфора, области его применения и его влияние на рост и развитие растений. А именно, на примере, дигидроортофосфата калия удалось выяснить, что растения, в моем случае овёс, благоприятно чувствуют себя при удобрении. Хотя семян, которые прорастали в воде выросло больше, у семян, которые увлажнялись дигидроортофосфотом калия 1% концентрации наблюдался резкий рост в период с 3 на 4 день, что доказывает факт положительного влияния фосфора на рост растений. Но с уменьшением концентрации дигидроортофосфата калия ростовые процессы замедляются, и длина корешка уменьшается, поэтому требуются правильные дозировки концентраций. Данный способ, с использованием дигидроортофосфата калия и других фосфатов можно применять в качестве удобрения для подкормки растений. Список литературы Л.Ю. Аликберова, Н.Г. Завьялов "Актуальная геохимия" С-Пб., «АСТ-ПРЕСС» 2001г. М.Х. Карапетьянц М.Х. С.И. Дракин "Общая и неорганическая химия" издательство «Химия» - 2000 г. Пурдела Д., Вылчану Р. «Химия органических соединений фосфора». Корбридж Д. Фосфор. Основы химии, биохимии, технологии. Ягодин Б.А., Жуков Ю.П., Кобзаренко В.И. Агрохимия/Под ред. Б.А. Ягодина. — М.: Колос, 2002. Агрохимия. Учебник/В.Г. Минеев, В.Г. Сычев, Г.П. Гамзиков и др.; под ред. В.Г. Минеева. — М.: Изд-во ВНИИА им. Д.Н. Прянишникова, 2017 [Электронный ресурс] офиц. сайт – Режим доступа: https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%BE%D1%80 [Электронный ресурс] офиц. сайт – Режим доступа: https://ru.wikipedia.org/wiki/%D0%94%D0%B8%D0%B3%D0%B8%D0%B4%D1%80%D0%BE%D0%BE%D1%80%D1%82%D0%BE%D1%84%D0%BE%D1%81%D1%84%D0%B0%D1%82_%D0%BA%D0%B0%D0%BB%D0%B8%D1%8F [Электронный ресурс] офиц. сайт – Режим доступа: https://www.activestudy.info/fosfornyj-obmen-i-rost-rastenij/ [Электронный ресурс] офиц. сайт – Режим доступа: https://chem.ru/fosfor.html [Электронный ресурс] офиц. сайт – Режим доступа: http://referatwork.ru/refs/source/ref-128184.html [Электронный ресурс] офиц. сайт – Режим доступа: https://fb.ru/article/201434/fosfor-i-ego-soedineniya-prakticheskoe-primenenie-soedineniy-fosfora |














