влияние ph. Влияние рн буровых сточных вод на их очистку электрокоагуляцией
 Скачать 0.66 Mb. Скачать 0.66 Mb.
|
|
ВЛИЯНИЕ рН БУРОВЫХ СТОЧНЫХ ВОД НА ИХ ОЧИСТКУ ЭЛЕКТРОКОАГУЛЯЦИЕЙ Одним из эффективных методов очистки буровых сточных вод вод (БСВ), образующихся при строительстве скважин и представляющих наибольшую опасность для окружающей среды из-за высокой подвижности и аккумулирующей способности к загрязнителям, является электрокоагуляционный метод. Он позволяет очищать БСВ от взвешенных веществ, нефти, нефтепродуктов, органических химреагентов и других загрязнителей. Основные закономерности и особенности электрокоагуляционной очистки БСВ достаточно хорошо изучены. Однако установлена необходимость строгого учета всех факторов, влияющих на эффективность очистки в целом. Рассмотрена значимость такого показателя, как рН среды возможность варьирования им для управления процессом в целях повышения глубины очистки, что крайне важно при проектировании технологии водоочистки. Для очистки влияния глубины рН БСВ на эффективность электрокоагуляционной очистки были выполнены исследования с использованием электрокоагулятора с растворимым алюминиевым анодом. Опыты проводили с наиболее характерной сточной буровой водой, которая была отобрана из амбара-накопителя одной из бурящихся скважин Бухаранефтегаз. Она имела следующие показатели (г/л): взвешенные вещества (ВВ)-3,683; нефть и нефтепродукты (НП)-0,458;бихроматная окисляемость или химическое потребление кислорода (ХПК)-1,487г/л; удельная электропроводимость при № 11 (80) ноябрь, 2020 г. 23 температуре 200С (χ)-3700μS см-1 ; рН-7,85; содержание ионов Сl – и НСО3 соответственно 0,9372 и 4575 г/л. Для достижения требуемого значения рН в исследуемую БСВ вводили расчетное количество едкого натра. При этом содержание взвешенных веществ, нефти, нефтепродуктов и других компонентов сточной воды оставалось постоянным в течении всей серии опытов рН БСВ изменялся в пределах 7.85…12,48. Эксперименты проводили при оптимальных токовых и гидродинамических режимных параметрах: плотность тока составляла 1,0 A/дм, линейная скорость потока в межэлектродном пространстве электрокоагулятора-2,5м/ч, что соответствует времени пребывании стока в электролизере 120 с или пропускной способности 2 м 3 /ч . Влияние на электрокоагуляцию исследуемого фактора оценивали по степени очистки БСВ от основных загрязнителей- взвешенных веществ αвв Кроме того контролируемым показателем процесса являлся показатель «удельные энергозатраты» Wуд. Результаты экспериментов приведены в таблице и на рисунке Они свидетельствуют о высокой эффективности процесса очистки по основным загрязнителям во всем исследуемым интервале рН. При этом установлено определенное влияние активной реакции среды сточной воды на эффект очистки. Так с ростом рН до 9,8…10,0 cтепень очистки БСВ от ВВ и НП практически не изменяется и составляет соответственно 98,3100 и 99,2-100%( см.таблицу). 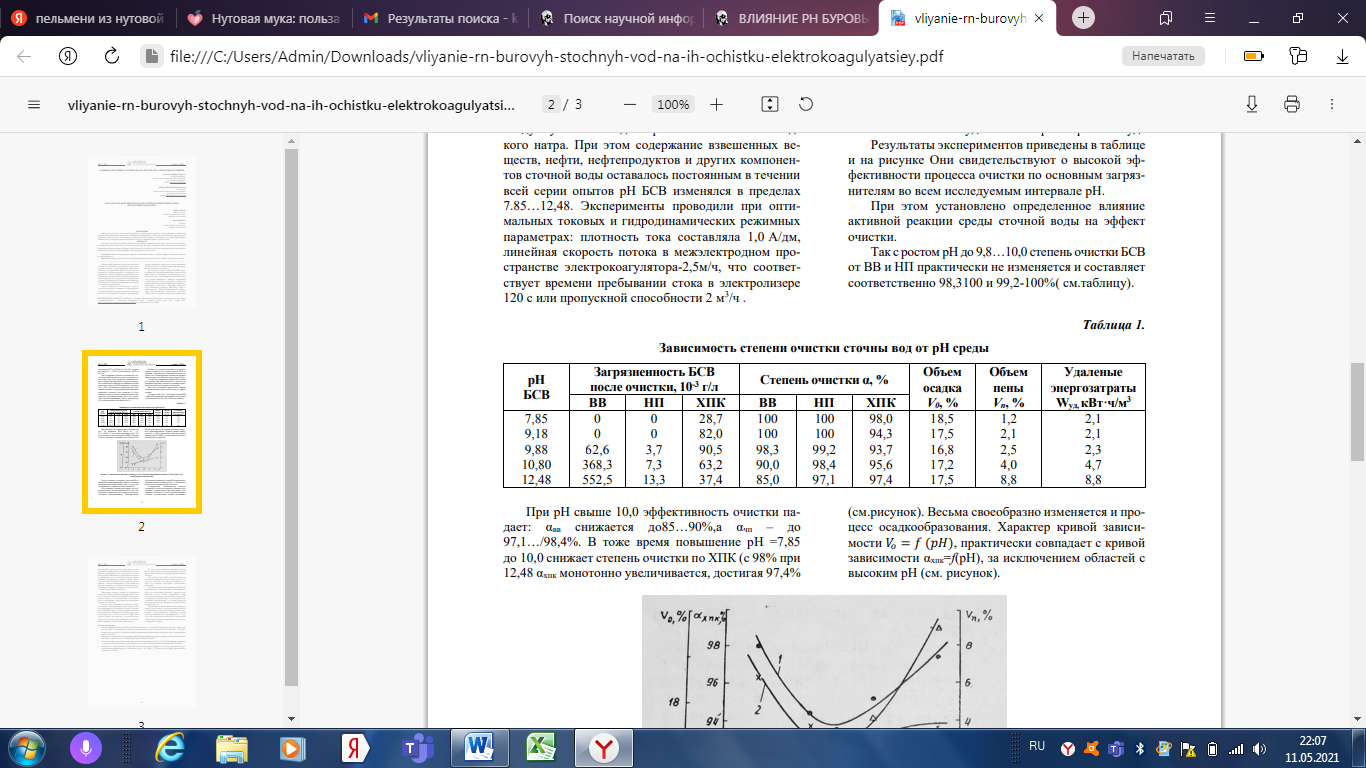 При рН свыше 10,0 эффективность очистки падает: αвв снижается до85…90%,а αчп – до 97,1…/98,4%. В тоже время повышение рН =7,85 до 10,0 снижает степень очистки по ХПК (с 98% при 12,48 αхпк монотонно увеличивается, достигая 97,4% (см.рисунок). Весьма своеобразно изменяется и процесс осадкообразования. Характер кривой зависимости 𝑉𝑜 = 𝑓 (𝑝𝐻), практически совпадает с кривой зависимости αхпк=f(pH), за исключением областей с высоким рН (см. рисунок). 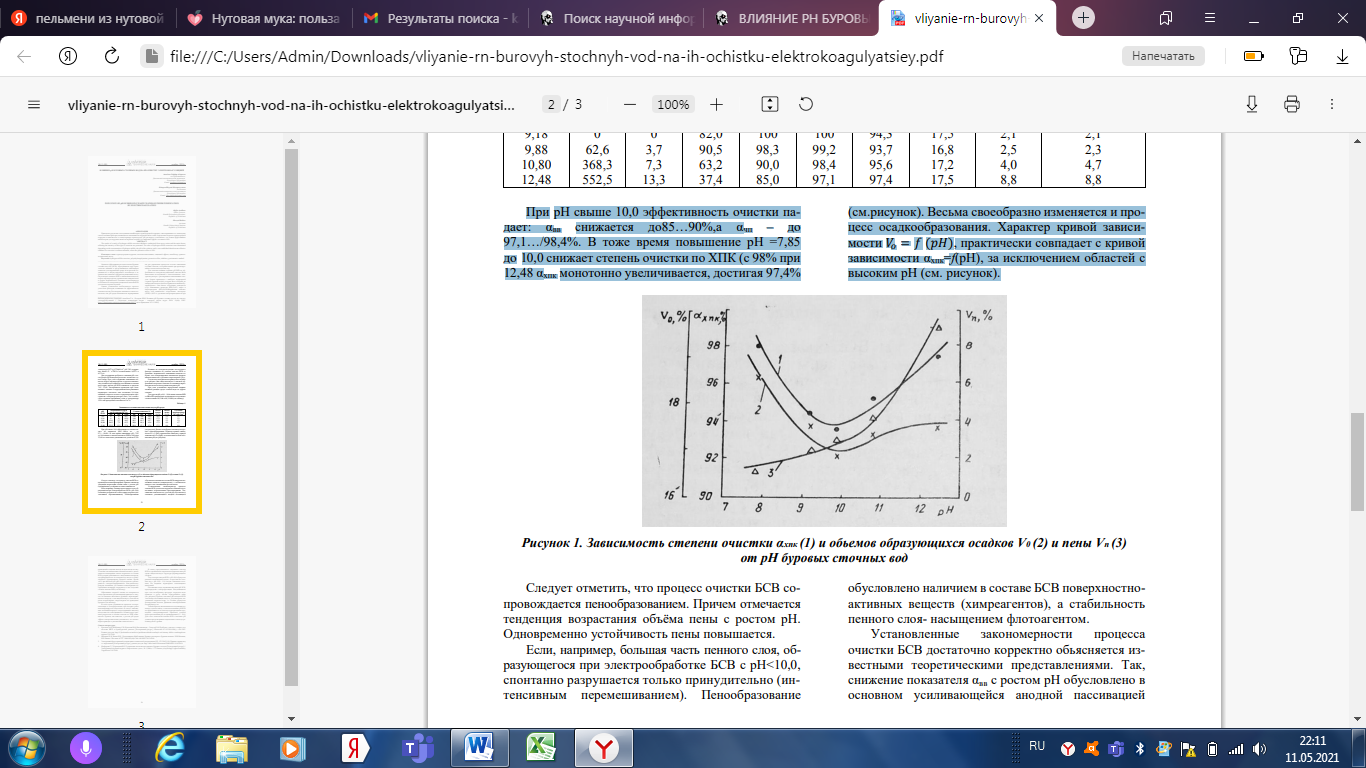 Следует отметить, что процесс очистки БСВ сопровождается пенообразованием. Причем отмечается тенденция возрастания объёма пены с ростом рН. Одновременно устойчивость пены повышается. Если, например, большая часть пенного слоя, образующегося при электрообработке БСВ с рН˂10,0 спонтанно разрушается только принудительно (интенсивным перемешиванием). Пенообразование обусловлено наличием в составе БСВ поверхностноактивных веществ (химреагентов), а стабильность пенного слоя- насыщением флотоагентом. Установленные закономерности процесса очистки БСВ достаточно корректно обьясняется известными теоретическими представлениями. Так, снижение показателя αвв с ростом рН обусловлено в основном усиливающейся анодной пассивацией приводящей к падению выхода металла анода по току. Усиление пассивационных явлений связано с увеличением концентрации ионов гидроксила в составе БСВ, которые размещаются с выделением кислорода, адсорбирующегося на поверхности анода и стимулирущего формирование окисной пленки. Кроме того, при высоких рН (рН>10,0) возрастает растворимость электрогенерированного коагулянта-гидроксида алюминия, что снижает концентрацию адсорбционно-активной гидроокиси и как следствие степень очистки БСВ (см.таблицу). Образование окисной пленки на поверхности анода при высоких рН (пассивация) приводит к тому, что он начинает выполнять функцию нерастворяющегося электрода, о чем свидетельствует, в частности, резко возрастающие энергозатраты на проведение процесса (см.таблицу). В этом случае усиливаются процессы электроокисления и электрофлотации, при которых резко интенсифицируется выделение на аноде окисляющих агентов(кислорода и хлорсодержащих веществ), вследствие чего находящаяся в сточных водах органика разлагается и степень очистки по ХПК повышается. Причем, как известно, с ростом рН среды эффект электроокисления усиливается, что закономерно приводит к увеличению показателя αхпк. В пользу представленного механизма очистки БСВ от органических загрязнителей при высоких рН среды свидетельствует структура формирующихся осадков. Так если при очистке БСВ с рН˂10,0 образуется рыхлый хлопьевидный осадок, то при очистке сточных вод с рН=10,0…11,0 осадок становится плотным, без видимых характерных хлопьевидных включений. Пассивация анода, вызванная высоким рН БСВ, предопределяет электрофлотацию. Выделяющиеся при этом газообразные продукты гидролиза воды приводят к росту обьема образующейся пены (см. рисунок). Причем, чем выше рН исходной БСВ тем сильнее пассивация анода и, следовательно, интенсивней гидролиз воды, т.е. больше образуется флотирующих агентов. Динамика пенообразования подтверждает это. Таким образом, выполненные исследования позволяют сделать вывод о заметном влиянии рН БСВ на эффективность их очистки и рекомендовать проведение электрохимической обработки сточной воды при значениях рН, не превышающих 9,5…10,0. Для этого технология очистки БСВ с высоким рН должна предусматривать подкисление стоков до рекомендуемого уровня. Список литературы: 1. Ермолин А.Ф.,Шабанова С.В.,Куксанов В.Ф.,Васильевская., Сагитов Р.Ф./Проблема очистки сточных вод системы ЖКХ в Оренбургском регионе [Электронный ресурс] //Известия ОГАУ.2016.№4(), с.201-202- Режима доступа: http://Cyberleninka.ru/article/n//problema-ochistki-stochnyh-vod-sistemy zhkh-v orenburgskomregione-3.05.2018. 2. Мельник И.В.,Чиник И.И / Детоксикация обработанных буровых растворов и буровых шламов / И.В.Мельник, И.И.Чиник // Вестник АГТУ. 2008.№3(44)с.106-169 ISSN 1812-9498. 3. Электронный фонд правовой и нормативно-технической документации: РД -153-39-031-98. Правила охраны вод от загрязнения [Электронный ресурс] -режим доступа: http://doks/cntd.ru/document/200056059.14.04.2018. 4. Ягафарова Г.Г.,Барахнина В.Б./Утилизация экологически опасных буровых отходов [Электронный ресурс] // Электронный научный журнал» Нефтегазовое дело», № 1,2006,с.1-17-Режим доступа:htpp://ogbus.ruauthory Yagafarova-3.05.2018. ПРИМЕНЕНИЕ ЭЛЕКТРОКОАГУЛЯЦИИ В ОЧИСТКЕ СТОЧНЫХ ВОД НЕФТЕПЕРЕРАБАТЫВАЮЩИХ ПРЕДПРИЯТИЙ В основе электрохимических методов очистки сточных вод лежит электролиз веществ, то есть химические превращения с использованием электрической энергии. Они возможны в растворах электролитов, электропроводность которых обусловлена присутствием ионов, способных передвигаться под воздействием электрического поля. На скорость электрохимической реакции влияют состав сточных вод, их температура, гидродинамические условия, материал электродов, наличие примесей, отлагающихся на электроде и другие причины. Электрохимическая коагуляция является одним из основных методов очистки нефтесодержащих сточных вод. При электрокоагуляции гидроокиси металлов получают в результате растворения анода и дальнейшего гидролиза перешедших в раствор ионов металлов. Образующиеся при этом гидроокиси обладают повышенной активностью и сорбционной способностью, что обеспечивает эффективную коагуляцию дисперсных примесей с участием продуктов электролиза. Образовавшиеся хлопьевидные структуры флотируются на поверхность жидкости пузырьками образовавшегося при электролизе газа или выносятся из электрокоагуляционного аппарата потоком обрабатываемой сточной воды с последующим отстаиванием или фильтрованием [1]. Механизм электрокоагуляции последовательно включает в себя следующие операции: электрофоретическое концентрирование, то есть направленное движение заряженных частиц примесей и концентрирование их у поверхности электродов; растворение электрода и образование гидроокисей металлов; поляризационная коагуляция дисперсных частиц; упаковка первичных агрегатов по мере накопления частиц гидроокисей и флокуляционная; флотация образовавшихся агрегатов пузырьками газов. Эффективность электрокоагуляции зависит от материала электродов, анодной плотности тока, состава и скорости движения обрабатываемой жидкости в межэлектродном пространстве. Серьезной помехой электрокоагуляции является образование на электродах окисных пленок – анодная пассивация. Для очистки нефтесодержащих сточных вод аноды изготовляются из алюминия или железа. Расход электроэнергии N для анодного растворения металла зависит от плотности j (рис.1) и расстояния между электродами [2]. Рис. 1 Расход электроэнергии N при анодном растворении 1 кг алюминия (1) и 1 кг железа (2) в зависимости от плотности тока j Как видно из рис.1, с уменьшением расстояния расход электроэнергии снижается. Обычно плотность тока принимают до 200 – 300 А/м2 , расстояние между электродами 10 – 20 мм, скорость движения воды между электродами должна быть не менее 0,03 – 0,05 м/с. Теоретический расход электроэнергии при рекомендуемом напряжении 3 – 12 В составляет, Вт*ч: при растворении 1 г железа 2,9, при растворении 1 г алюминия 12. Растворение в воде 1 г железа эквивалентно введению в сточную воду 3,58 г сернокислого железа Fe2(SO4)3, а растворение 1 г алюминия – 6,33 г сернокислого алюминия Al2(SO4)3. Электрокоагуляционная очистка воды производится в электролизерах в основном с вертикальным расположением электродов, выполняемых чаще всего в виде блока прямоугольных пластин толщиной 5 – 10 мм. Соединение электродов, осуществляется по монополярной схеме (рис.2). Возможно соединение их по биполярной и комбинированным схемам. При отсутствии источников постоянного тока питание электролизеров осуществляется выпрямленным током, для чего в составе установки предусматриваются выпускаемые промышленностью выпрямители. С целью обеспечения безопасности работающего персонала на одну электролитическую ячейку не должно подаваться напряжение более 36 В [3]. Рис. 2 Устройство электролизера для электрохимической коагуляцией: 1 – вода; 2 – электроды По характеру потоков воды в электролизерах они могут быть однопоточные, многопоточные и смешанные с горизонтальным или вертикальным направлением движения жидкости. Конструктивные варианты электрокоагуляционных установок различны. Промышленная электрокоагуляционная установка для очистки нефтесодержащих сточных вод представлена на рис.3 [4]. Основной элемент электрокоагулятора — электродная камера со сменным набором стальных или алюминиевых (дюралюминиевых) электродов чередующейся полярности, в зазорах между которыми (шириной 5–20 мм) протекает обрабатываемая вода со скоростью не менее 0,5 м/с. Как и в электролизерах, в электрокоагуляторах электроды могут располагаться горизонтально или вертикально с зазором 10–16 мм, что зависит от условий размещения и монтажа, а также от расходов обрабатываемой воды. В электрокоагуляторах с меньшими плотностями электрического тока в связи с незначительным пенообразованием можно принимать ширину межэлектродных каналов менее 15 мм, и при обосновании не предусматривать устройств для удаления пены. При больших плотностях электрического тока ширина межэлектродных каналов должна принимается не менее 15–20 мм. Для удаления скоплений пены в каналах предусматриваются различные устройства, в частности, продувка сжатым воздухом [5]. Аноды и катоды выполняются в виде пластин из алюминия, его сплавов, не содержащих медь, или стали. Подключение пластин к источнику тока может быть параллельным или последовательным. В первом случае все электроды действуют как монополярные, во втором — промежуточные пластины работают биполярно. Последовательное же подключение позволяет работать при меньших значениях электрического тока. Наряду с пластинчатыми иногда используют засыпные электроды из стальной стружки. Несмотря на некоторые преимущества (большая поверхность, низкая стоимость), засыпные электроды применяются редко, поскольку они засоряются гидроксидами металлов и плохо регенерируются. Выбор материала для электродов зависит от технологических особенностей процессов очистки. Рис. 3 Электрокоагуляционная установка для очистки нефтесодержащих вод: 1 – трубопровод подачи сточных вод; 2 – резервуар электрокоагулятора; 3 – пакет плоских стальных электродов; 4 – отстойник; 5 – выпуск очищенных вод; 6 – выпрямитель электрического тока; 7 – выпуск сточныхвод С целью интенсификации процесса электрокоагуляции может использоваться конструкция виброэлектрокоагулятора. Применение вибрационных колебаний среднего диапазона частот практически исключает пассивацию электродов, снимает диффузионные ограничения во всем рабочем объеме, облегчает удаление газов и образующихся осадков, выгружаемых периодически через специальный клапан без остановки аппарата. Эксплуатационные работы включают: усреднение по расходам и качеству воды, поступающей в электрокоагулятор; корректировку качества воды (очистка от грубодисперсных примесей, корректировка рН и солевого состава); поддержание расчетного режима рециркуляции воды в контуре электрокоагулятора, если это предусмотрено схемой обработки; контроль значений и поддержание на нужном уровне электрических параметров — силы тока, напряжения; соблюдение режима переполюсовок электродов для депассивации и способа равномерного растворения всех электродов; очистку межэлектродного пространства от отложений и пены; удаление образующейся при электролизе пены; своевременную замену электродов; контроль за состоянием газовой среды и обеспечение эффективной работы системы вентиляции; правильное содержание сооружений для последующей очистки воды (отстойники, флотаторы, фильтры) [6]. При электрокоагуляции образуется очень рыхлый, плохо уплотняющийся осадок. Для его обезвоживания применяют отстаивание, центрефугирование, флотацию, термическую сушку. Электрохимические методы, и в том числе электрокоагуляция, имеют следующие преимущества: не требуют применения реагентов, не увеличивают солесодержание воды, упрощают технологические схемы очистки, улучшают условия эксплуатации, позволяют сравнительно просто решать вопросы автоматизации. Наряду с этим электрокоагуляция не лишена и существенных недостатков. К их числу относятся сравнительно большая потребность в электроэнергии, значительный расход листового металла, образование на поверхности электродов окисных пленок, засорение пространства между электродами продуктами электрокоагуляции. Образование отложений на электродах в результате электродах в результате электрофоретического концентрирования дисперсной фазы и гидроокисей приводит к снижению скорости и эффективности электрокоагуляции [7]. Для уменьшения вредных последствий этого явления предусматривают барботаж воздуха через межэлектродное пространство, устройство вращающихся щеток, вращающихся дисковых электродов и пр. Для борьбы с пассивацией электродов осуществляется их переплюсовка, добавка в жидкость анионов, вытесняющих кислород из пассивирующих соединений и образующих растворимые соединения, например, Cl. С целью интенсификации процесса очистки воды с применением электролизеров предложены следующие сочетания электролизеров с другими: - электролизер-отстойник; - гальванокоагулятор-электролизер; - электролизер-флотатор. Эффективность очистки воды и электролизере-отстойнике по взвешенным веществам составляет 95,5 %, а по нефтепродуктам – 83 %, в электролизерефлотаторе по нефтепродуктам – 95,5 %. Литература: 1. Воловник Г.И., Коробко М.И. Электрохимическая очистка воды. — Хабаровск: Изд-во ДВГУПС, 2002. 2. Каратаев О. Р., Новиков В. Ф., Шамсутдинова З. Р. Проблема аналитического контроля и экологической безопасности водоснабжения // Вестник Казанского технологического университета 2013, С. 52-54. 3. Мосин О.В. Технологический расчет установок электрофлотации воды // Журнал С.О.К., №1/2014 4. Ерусалимская Л.Ф., Смепченко А.В. / Сравнение эффективности обеззараживания воды электролизом и хлорированием // Гигиена и санитария. 1989, №11, с. 73-75. 5. Смола В. И. Поглощение двуокиси серы природными цеолитами. - М.: Полиграф сервис, 2009, 319с. 6. Назаров В. Д., Гурвич Л. М., Русакович А. А. Водоснабжение в нефтедобыче: Учебное пособие. Уфа. ООО «Виртуал», 2003. 163с. 7. Вахидова И.М., Шайхиев И.Г., Гильманов Р.З., Вахидов Р.М., Мусин Р.З./ Очистка сточных вод производства калиевой соли 4,6 динитробензофуроксана окислением // Вестник Казанского технологического университета. 2013. № 19. С. 49-52. ОЧИСТКА СТОЧНЫХ ВОД ОТ ПРИМЕСЕЙ ТОЛУОЛА И АЦЕТОНА ЭЛЕКТРОЛИЗОМ ПОД ДАВЛЕНИЕМ КИСЛОРОДА Ацетон и толуол являются многотоннажными продуктами органического синтеза и находят применение в различных отраслях народного хозяйства. В результате технологических процессов ежегодно в окружающую среду попадает около двадцати миллионов тонн суммарного количества выбросов ацетона, остальные выбросы ацетона, подлежащие оценке, связаны с образованием побочных продуктов, образующихся в результате фоторазложения органических соединений (около двадцати миллионов тонн в год) или попадают в окружающую среду из промышленных предприятий в виде конечного продукта (59 тыс. тонн в год) [1]. Исходя из этого представляет большой практический интерес разработка эффективных технологий очистки сточных вод, содержащих указанные органические растворители. Для обезвреживания сточных вод, содержащих данные органические соединения, успешное применение находят электрохимические методы. Однако недостатком этих методов является относительно высокий расход электроэнергии. Кроме того, полезное применение нашел только анодный процесс, а катодной реакцией является выделение водорода. В последние годы возник существенный интерес к развитию эффективных деструктивных электрохимических технологий, позволяющих полезно использовать оба электродных процесса за счет одновременного использования анодного окисления органических соединений и их непрямого окисления продуктами катодного восстановления кислорода, обладающих высокой окислительной активностью [2]. В отличие от прямого электрохимического окисления органических веществ, протекающего в области высоких анодных потенциалов, где практически всегда существуют проблемы коррозионной стойкости электродных материалов, термодинамической устойчивости водных растворов электролитов, при непрямом окислении такие проблемы не возникают, так как процесс катодной генерации окислителей протекает при сравнительно высоких катодных потенциалах, а химическая реакция протекает в гомогенной среде [3]. Известно [3], что расход электроэнергии для обезвреживания органических токсикантов в сточных водах пропорционален их концентрации и числу электронов, необходимых для деструкции до углекислого газа. Расход электроэнергии на электросинтез пероксида водорода из кислорода, согласно [4], составляет около 4,5 кВт×ч в расчете на один килограмм 100% H2O2. Отсюда следует, что использование метода непрямого окисления при низких концентрациях (перед направлением на биологические очистные сооружения) органических субстратов – «хвостов», содержащихся в сточных водах, электрохимически генерируемым H2O2 экономически целесообразно. Поскольку при атмосферном давлении катодное восстановление кислорода протекает с низким выходом по току, перспективным является проведение процесса при повышенном давлении. Преимущества электролиза под давлением перед проведением процесса при атмосферном давлении известны [5, 6]. В этом случае открываются новые возможности осуществления электродной реакции с участием газообразного кислорода, растворимость которого при повышенных давлениях возрастает и соответственно при этом снижаются диффузионные ограничения подачи кислорода к электродной поверхности. Настоящая работа, нацеленная на решение задачи максимального полезного использования как катодного, так и анодного электродных процессов, развивает направление исследований по интенсификации технологии очистки сточных вод. Давление в системе для проведения исследований электрохимических процессов создается подачей кислорода в автоклав из баллона высокого давления или за счет накопления газа в автоклаве при протекании электролиза. Вентиль для впуска и выпуска газа и манометр закреплялись непосредственно на корпусе автоклава. Здесь же крепились и изолированные выводы электродов. В работе использовали автоклав ёмкостью 500 мл, рассчитанный на 10,0 МПа. Электролиз проводили в автоклаве – электролизёре с мембраной, схема которого приведена на рис. 1. Мембраной служила катионообменная мембрана марки МК-40. Объём анодной камеры – 300 мл, катодной – 250 мл. В качестве анода служил платиновый электрод площадью 8 см2 , в качестве катода использовали графитовую ткань с видимой поверхностью 50 см2 . Электролиз проводили под давлением 0,5 МПа, при плотности тока 0,1 А/см2 , в течение одного часа. После электролиза растворы из анодной и катодной камер анализировали на остаточное содержание толуола и ацетона на газовом хроматографе TRACE-2000 (фирма «CE Instruments», Италия) с пламенно-ионизационным детектором. Рис. 1. Схема диафрагменного электролизера - автоклава: 1 – стальной корпус; 2 – мембрана; 3 – электроды; 4 – болты; 5 – манометр; 6 – трубка для регулирования подачи газа; 7 – вентиль В связи с тем, что интенсификация электрохимического процесса направлена на повышение эффективности деструкции за счет полезного использования анодной и катодной реакций, была проведена серия экспериментов в диафрагменном электролизере под давлением 0,5 МПа. Результаты представлены на рис. 2 и 3 в виде зависимости концентрации толуола и ацетона от количества пропущенного электричества в катодной и анодной камерах. Рис. 2. Изменение концентрации ацетона в анодной (1) и катодной (2) камерах в зависимости от количества пропущенного электричества Как видно из рис. 2, окисление ацетона протекает более интенсивно в анодной камере, что связано с прямой деструкцией ацетона на ОРТА. Одновременно с анодным разрушением в катодной камере также идет интенсивное разрушение ацетона, что связано с участием активных продуктов восстановления кислорода в окислительном процессе. Рис.3 Изменение концентрации толуола в анодной (1) и катодной(2) камерах в зависимости от количества пропущенного электричества На рис. 3 представлены данные по изменению концентрации толуола в анодной и катодной камерах электролизера в зависимости от количества пропущенного электричества. Разрушение толуола в анодной камере идет более интенсивно чем в катодной камере, как и в случае с окислением ацетона. Как видно из рис. 2 и 3 до 0,5 А∙ч наблюдается практически прямолинейная зависимость между пропущенным количеством электричества и концентрацией растворителя, свидетельствующая о том, что практически весь ток идет на процесс деструкции. По мере увеличения количества электричества и снижения концентрации толуола наблюдается изменение прямолинейной зависимости. При этом часть тока тратится на процесс выделения кислорода и водорода. Анализ содержания толуола в анодной камере показал, что разрушение толуола при пропускании 0,5 А∙ч значительно более интенсивно, чем в катодной камере и после пропускания 1,0 А∙ч. Таким образом, полученные экспериментальные данные позволяют утверждать, что проведение электролиза под давлением кислорода позволяет интенсифицировать процесс за счет катодного восстановления кислорода до активных промежуточных продуктов, которые окисляют толуол и ацетон. БИБЛИОГРАФИЧЕСКИЙ СПИСОК 1. Toluene. Eur. Chem. 2002. 76, № 1995, прил., с.27. 2. Корниенко В.Л., Колягин Г.А. Непрямое электрохимическое окисление органических веществ интермедиатами восстановления кислорода // Электрохимия. 2003. Т. 39. № 12. С. 1462 – 1470. 3. Do J – S., Yen W – S., In situ electro oxidative degradation of formaldehyde with electro generated hydrogen peroxide and hypochlorite ion // I . Appl. Electro – chem. –1998. V. 28. Рp. 703 – 710 . 4. Химия и технология пероксида водорода / Под ред. Г. А. Серышева. – Л.: Химия, 1984 . 200 с. 5. Алиев З.М., Харламова Т.А., Томилов А.П. Научные основы и перспективы использования электролиза при повышенном давлении // Изв. вузов Сев.-Кав. региона. Техн. науки. 2004. Спец. выпуск. – С.44 – 51. 6. Харламова Т.А., Алиев З.М., Исаев А.Б. Очистка сточных вод от красителей электролизом под давлением // Известия вузов. Химия и химическая технология. 2004. Т. 47. Вып. 8. С. 56 – 58. |
