Биохимия (зачет). Вопрос 1 Первичная структура белков
 Скачать 4.52 Mb. Скачать 4.52 Mb.
|
|
Вопрос 1 Первичная структура белков. Специфичность первичной структуры белков. Конформация пептидных цепей белков (вторичная и третичные структуры). Дисульфидные, водородные, гидрофобные и ионные связи в стабилизации конформации белковой молекулы. Четвертичная структура белков. Примеры строения белков с четвертичной структурой. Понятие о протомере. Кооперативные изменения конформации протомеров при функционировании белков (гемоглобин, протеинкиназа). П 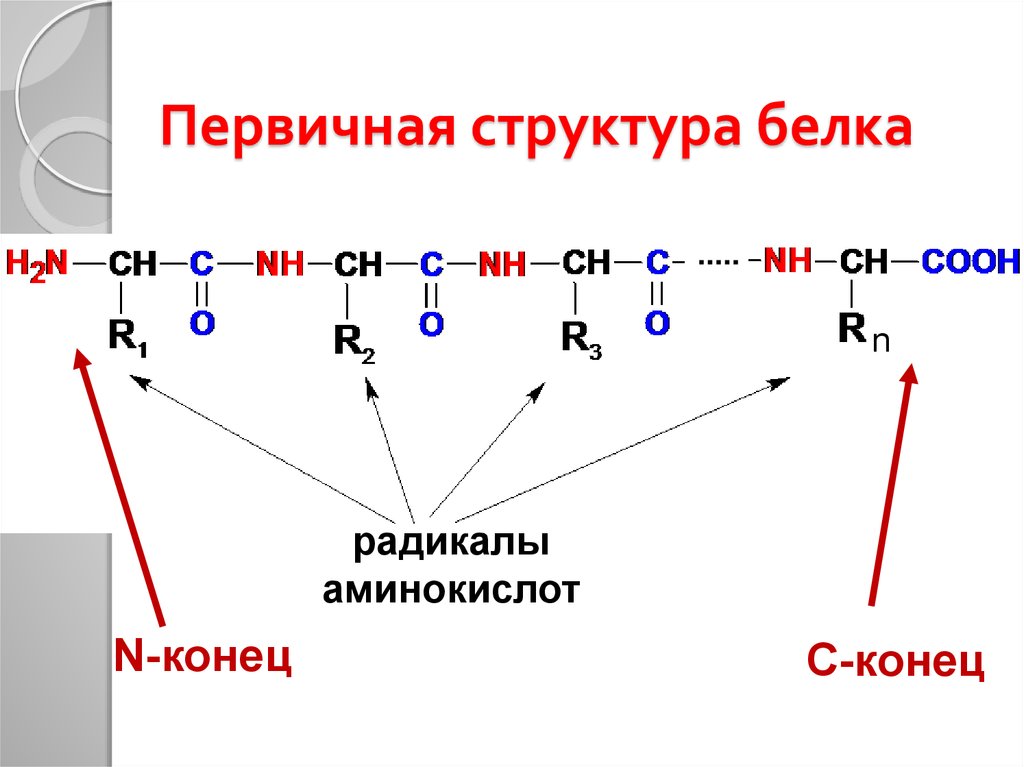 ервичная структура — линейная последовательность аминокислот, соединенных пептидными связями. Имеет вид нити. У нее два конца: N-конец (свободная NH2 -группа) и С-конец (свободная СООН-группа) Вторичная структура — пространственная укладка первичной цепи. Она имеет два вида: а) альфа-спираль — правозакрученная спираль цепи, фиксируемая водородными связями между группами СО и NН основной пептидной цепи. Эта форма характерна для белков человека и высших животных; б) бета-структура — несколько (до 6) параллельно расположенных пептидных цепей (направленных в обратные стороны относительно друг друга), соединенных между собой теми же поперечными водородными связями между СО и NН. Третичная структура — укладка вторичной спирали в более компактную форму. Чаще это самая удобная форма в природе — шарик, по-латински — глобула. Не забывайте, что человек — ходячий водный раствор, и все его белки находятся в водной среде. Третичная форма — это округлое образование, все гидрофобные (нерастворимые) радикалы которой находятся внутри глобулы, скрыты от окружающей водной стихии, а гидрофильные, наоборот — торчат наружу, покрывая все тело глобулы (как иглы ежа), притягивая воду к себе, создавая плотную гидратную оболочку. Третичную структуру стабилизируют 4 вида связей: а) водородные — образуются между радикалами с участием водорода. Например: ОН-группа серина и азот гистидина; б) электрофильные — возникают между разнозаряженными частицами аминокислот. Пример: положительно заряженный лизин и отрицательная аспарагиновая кислота. Примечание: не стоит называть электрофильные связи — ионными, это грубая ошибка; в) гидрофобные — формируются между радикалами гидрофобных аминокислот (их список приведен в классификации); г) дисульфидные — единственный вид ковалентных связей в третичной структуре. Образуется между двумя остатками аминокислоты цистеин, формирующих мостик: S-S. Четвертичная структура — характерна далеко не для всех протеинов (для большинства белков высшей структурой является третичная). Представляет собой объединение нескольких глобул воедино, их число всегда четное, от двух до нескольких тысяч. Такой белок называют мультимером (или олигомером), а каждую из его глобул — протомером, или субъединицей. Связи четвертичной структуры: а) водородные; б) электрофильные; в) гидрофобные. Замечу, что все связи в третичной и четвертичной структурах образуются только между радикалами аминокислот. Таким образом, мы видим, что в белковой структуре имеются два вида ковалентных (прочных) связей: пептидная и дисульфидная и три вида нековалентных (слабых) связей: водородные, электрофильные и гидрофобные. Классическим примером мультимера является гемоглобин (Hb), молекула которого построена из 4-х протомеров, каждый их которых имеет в своем составе небелковую часть — гем, с ионом железа в центре. Именно гем отвечает за связывание и транспорт кислорода. Выделяют 4 основных типа гемоглобина: HbА1 — гемоглобин взрослого, его молекула построена из двух α- и двух β-субъединиц. На его долю приходится более 90% общего гемоглобина. HbА2 — минорный. 2 α и 2 δ частицы. 1% от общего Hb. HbF — фетальный (2 α, 2 γ). Является основным гемоглобином плода. HbP — эмбриональный (2 α, 2 ε). Преобладает у эмбриона. Протомер - отдельная полипептидная цепь в третичной структуре, не выполняющая функцию белка. Протомер (субъединица) – это часть олигомерного белка, состоящая из одной полипептидной цепи. Причем, каждая полипептидная цепь такого белка имеет собственную первичную, вторичную и третичную структуру и приобретает собственную конформацию. Кооперативными изменениями конформации протомеров называются изменения конформации всего олигомерного белка после присоединения лиганда к одному из протомеров, приводящее к изменению функциональных свойств белка в целом. Для гемоглобина это означает, что кооперативные изменения конформации его протомеров ускоряют присоединение кислорода в легких и облегчают отщепление кислорода в тканях: - присоединение кислорода через Fe2+ к одному протомеру (оксигенация гемоглобина) вызывает перемещение Fe2+ в плоскость гема; одновременно перемещается и остаток Гис F8, связанный с ним. Это влечет изменение конформации данного протомера, а также остальных субъединиц гемоглобина и их активных центров, то есть вследствии конформационной лабильности изменяется конформация и свойства всего белка; - измененная конформация белка облегчает связывание второй молекулы кислорода со следующим протомером, что вызывает дополнительные кооперативные изменения конформации протомеров и еще более облегчает связывание со следующей молекулой 02. Четвертая молекула кислорода присоединяется к оставшемуся протомеру в 300 раз легче, чем первая. - последовательное отщепление кислорода (дезоксигенация) в тканях изменяет на каждом этапе конформацию всех протомеров и облегчает диссоциацию последующих молекул 02. Кривая диссоциации оксигемоглобина имеет выраженный S-образный характер и отражает положительный кооперативный эффект взаимодействия протомеров (субъединиц) в тетрамер-ной молекуле гемоглобина при его оксигенации. Гемоглобин имеет S-образную кривую насыщения, которая показывает, что субъединицы белка работают кооперативно, и чем больше кислорода они отдают, тем легче идет диссоциация остальных молекул 02; этот процесс зависит от изменения парциального давления 02 в тканях. Кривая насыщения (диссоциации) миоглобина - простая гипербола, отражает функции миоглобина - обратимое связывание с кислородом, высвобождаемым гемоглобином, депонирование его и освобождение в случае интенсивной физической нагрузки; не зависит от посторонних факторов Вопрос 2 Структура и функция пантотеинфосфата. Суточная потребность в витамине В3. 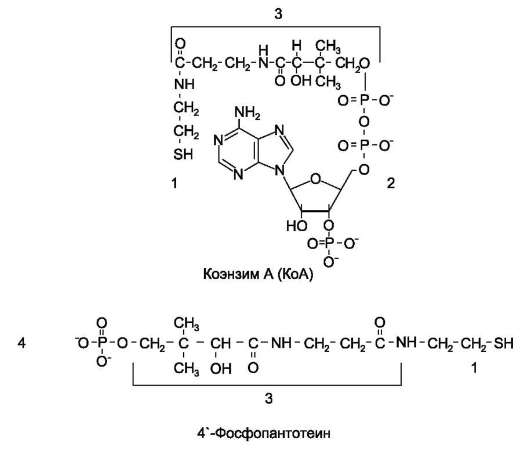 Строение КоА и 4'-фосфопантотеина. 1 - тиоэтаноламин; 2 - аденозил-3'-фосфо-5'-дифосфат; 3 - пантотеновая кислота; 4 - 4'-фосфопантотеин (фосфорилированная пантотеновая кислота, соединённая с тиоэтаноламином). Биологические функции: используется в клетках для синтеза коферментов: 4-фосфопантотеина и КоА. 4-фосфопантотеин - кофермент пальмитоилсинтазы. КоА участвует в переносе ацильных радикалов в реакциях общегопути катаболизма, активации жирных кислот, синтеза холестерина и кетоновых тел синтеза ацетилглюкозаминов, обезвреживания чужеродных веществ в печени. Суточная потребность- 10-12 мг. Вопрос 3 Классификация белков. Протеины и протеиды. Характеристика отдельных протеинов: альбумины, глобулины, протамины, гистоны, проламины и глютелины. Характеристика отдельных протеинов: фосфопротеины, гликопротеины, нуклеопротеины, металлопротеины. До настоящего времен нет единой и стройной классификации, учитывающей различные параметры белков. В основе имеющихся классификаций обычно лежит один признак. Так, белки можно классифицировать: -по форме молекул (глобулярные или фибриллярные); -по молекулярной массе (низкомолекулярные, высокомолекулярные и др.); -по химическому строению (наличие или отсутствие небелковой части); -по выполняемым функциям (транспортные, защитные, структурные белки и др.); -по локализации в клетке (ядерные, цито-плазматические, лизосомальные и др.); -по локализации в организме (белки крови, печени, сердца и др.); -по возможности адаптивно регулировать количество данных белков: белки, синтезирующиеся с постоянной скоростью (конститутивные), и белки, синтез которых может усиливаться при воздействии факторов среды (индуцибельные); -по продолжительности жизни в клетке (от очень быстро обновляющихся белков, с Т1/2 менее 1 ч, до очень медленно обновляющихся белков, Т1/2 которых исчисляют неделями и месяцами); -по схожим участкам первичной структуры и родственным функциям (семейства белков). Классификация белков по химическому строению Простые белки Некоторые белки содержат в своём составе только полипептидные цепи, состоящие из аминокислотных остатков. Их называют "простые белки". Примером простых белков - гистоны; в их составе содержится много аминокислотных остатков лизина и аргинина, радикалы которых имеют положительный заряд. Сложные белки Очень многие белки, кроме полипептидных цепей, содержат в своём составе небелковую часть, присоединённую к белку слабыми или ковалентными связями. Небелковая часть может быть представлена ионами металлов, какими-либо органическими молекулами с низкой или высокой молекулярной массой. Такие белки называют "сложные белки". Прочно связанная с белком небелковая часть носит название простетической группы. Простетическая группа может быть представлена веществами разной природы. Например, белки, соединённые с гемом, носят название гемопротеины. В состав гемопротеинов, кроме уже рассмотренных выше белков гемоглобинов и миоглобина, входят ферменты - цитохромы, каталаза и пероксидаза. Гем, присоединённый к разным белковым структурам, выполняет в них характерные для каждого из белков функции (например, в составе гемоглобина переносит О2, а в составе цитохромов - электроны). Белки, соединённые с остатком фосфорной кислоты, называют фосфопротеинами. Фосфорные остатки присоединяются сложноэфирной связью к гидроксильным группам серина, треонина или тирозина при участии ферментов, называемых протеинкиназами. В состав белков часто входят углеводные остатки, придающие белкам дополнительную специфичность и часто уменьшающие скорость их ферментативного протеолиза. Такие белки носят название гликопротеинов. Многие белки крови, а также рецепторные белки клеточной поверхности относят к гликопротеинам. Белки, функционирующие в комплексе с липидами, называют липопротеинами, а в комплексе с металлами - металлопротеинами. Сложный белок, состоящий из белковой части (апопротеин) и небелковой части (простетическая группа), называют "холопротеин". Классификация белков по функциям 1. Ферменты - специализированные белки, ускоряющие течение химических реакций. Благодаря ферментам в клетке скорости химических реакций возрастают в миллионы раз. Так как ферменты, как и любые белки, имеют активный центр, они специфически связывают определённый лиганд (или группу похожих лигандов) и катализируют определённый тип химического превращения данной молекулы. Например, протеолитический фермент трипсин разрушает в белках пептидные связи, образованные карбоксильной группой основных аминокислот - аргинина или лизина. Фермент рибонуклеаза расщепляет фосфоэфирную связь между нуклеотидами в полинуклеотидной цепи. 2. Регуляторные белки - большую группу белковых гормонов, участвующих в поддержании постоянства внутренней среды организма, которые воздействуют на специфические клетки-мишени. Например, гормон инсулин выделяется в кровь при повышении концентрации глюкозы в крови после еды и, стимулируя использование глюкозы клетками, снижает концентрацию глюкозы до нормы, т.е. восстанавливает гомеостаз. Кроме того, к регуляторным относят белки, присоединение которых к другим белкам или иным структурам клетки регулирует их функцию. Например, белок кальмодулин в комплексе с четырьмя ионами Са2+ может присоединяться к некоторым ферментам, меняя их активность. Регуляторные ДНК-связывающие белки, присоединяясь в определённые моменты к специфичным участкам ДНК, могут регулировать скорость считывания генетической информации. 3. Рецепторные белки Сигнальные молекулы (гормоны, нейромедиаторы) действуют на внутриклеточные процессы через взаимодействие со специфическими белками-рецепторами. Так, гормоны, циркулирующие в крови, находят клетки-мишени и воздействуют на них, специфично связываясь с белками-рецепторами, обычно встроенными в клеточную мембрану. Для гидрофобных регуляторных молекул, проходящих через клеточную мембрану, рецепторы локализуются в цитоплазме клеток. 4. Транспортные белки Многие белки крови участвуют в переносе специфических лигандов из одного органа к другому. Часто в комплексе с белками переносятся молекулы, плохо растворимые в воде. Так, белок плазмы крови альбумин переносит жирные кислоты и билирубин (продукт распада тема), а гемоглобин эритроцитов участвует в переносе О2 от лёгких к тканям. Стероидные гормоны переносятся в крови специфическими транспортными белками. Транспортные белки участвуют также в переносе гидрофильных веществ через гидрофобные мембраны. Так как транспортные белки обладают свойством специфичности взаимодействия с лигандами, их набор в клеточной мембране определяет, какие гидрофильные молекулы могут пройти в данную клетку. С помощью белков-переносчиков в клетку проникают глюкоза, аминокислоты, ионы и другие молекулы. 5. Структурные белки Некоторые белки, расположенные определённым образом в тканях, придают им форму, создают опору, определяют механические свойства данной ткани. Например, как уже говорилось выше, главным компонентом хрящей и сухожилий является фибриллярный белок коллаген, имеющий высокую прочность. Другой структурный белок (эластин) благодаря своему уникальному строению обеспечивает определённым тканям свойство растягиваться во всех направлениях (сосуды, лёгкие). 6. Защитные белки Некоторые белки, в частности иммуноглобулины, обладают способностью узнавать и связывать чужеродные молекулы, вирусные частицы и бактерии, в результате чего происходит их нейтрализация. Кроме того, комплекс чужеродной частицы с иммуноглобулином легко узнаётся и уничтожается клетками иммунной системы. Защитными свойствами обладают белки свёртывающей системы крови, например фибриноген, тромбин. Они участвуют в формировании тромба, который закупоривает повреждённый сосуд и препятствует потере крови. 7. Сократительные белки Некоторые белки при выполнении своих функций наделяют клетку способностью либо сокращаться, либо передвигаться. К таким белкам относят актин и миозин - фибриллярные белки, участвующие в сокращении скелетных мышц. Другой пример таких белков - тубулин, из которого построены клеточные органеллы - микротрубочки. Микротрубочки в период деления клетки регулируют расхождение хроматид. Микротрубочки - важные элементы ресничек и жгутиков, с помощью которых клетки передвигаются. Простые белки (протеины) и сложные белки (протеиды) [((про них выше я уже указала))] 1. Альбумины глобулярные белки, молекулярная масса 70 000, растворимы в воде, ИЭТ 5, высаливаются 100% сульфатом аммония, синтез в печени. Функции альбуминов депо белка в организме, осморегуляция, неспецифическая защита, транспорт лекарств, металлов, холестерина, билирубина, желчных пигментов, гормонов. 2. Глобулины глобулярные белки, молекулярная масса 150 000 дальтон, растворимы в солевых растворах, ИЭТ 7, имеют ряд фракций, высаливаются 50% сульфатом аммония, синтезируются в печени и В-лимфоцитах. Функции глобулинов ферменты, транспорт витаминов, гормонов, металлов, защита (иммунитет), γ -глобулины являются антителами. 3.Гистоны связаны с ДНК, молекулярная масса 20 000, ИЭТ 8, богаты лиз, арг, гис, имеют положительный заряд, содержат тирозин, защищают ДНК от нуклеаз. 4.Протамины молекулярная масса 5000, ИЭТ 11, содержат много арг, лиз, имеют положительный заряд, не содержат тирозин, являются белковым компонентом нуклеопротеинов. Проламины Проламины – белки растительного происхождения, содержатся в клейковине семян злаковых растений, где выполняют роль запасных белков. В их состав входит большое количество глутаминовой кислоты и пролина (отсюда название проламин). Проламины почти не содержат глицина и лизина, что делает невысокой их пищевую ценность. Характерной особенностью проламинов является то, что они не растворимы в воде, солевых растворах, щелочах, хорошо растворимы в 60-80% растворе этилового спирта (это связано с наличием большого количества неполярной аминокислоты пролина), в то время как все другие белки денатурируют и выпадают в осадок. К ним относятся глиадин (белок пшеницы, ржи), гордеин (белок ячменя), зеин (белок кукурузы), авенин (белокян овса), эдестин (белок конопли). Проламины практически отсутствуют в бобовых и масличных культурах. Глютелины Глютелины – белки растительного происхождения, характеризующиеся высоким содержанием аминокислот пролина и глутаминовой кислоты. Глютелины играют важную роль в питании человека, т. к. их питательная ценность высока. Они присутствуют в семенах злаковых культур вместе с проламинами. Глютелины занимают промежуточное положение между проламинами и глобулинами. Глютелины растворяются в разбавленных кислотах и щелочах, не растворяются в воде, спирте и разбавленных солевых растворах. Представителями данного класса простых белков является оризенин (белок риса), глютелин (белок кукурузы) и глютенин (белок пшеницы). У риса 80% всего белка приходится на глютелины (оризенин), этим можно объяснить высокое содержание лизина в белке рисового зерна. Эти белки в ржаной муке не образуют клейковины, что обусловлено качественным различием белков ржи и пшеницы. |
