Дыхание и обмен веществ. Вопросы коллоквиума по разделам Физиология крови
 Скачать 2.87 Mb. Скачать 2.87 Mb.
|
|
14. Коагуляционный гемостаз. Стадии коагуляционного гемостаза, их характеристика. Свёртывание крови – ферментативный, каскадный, матричный процесс перехода растворимого белка фибриногена в нераствр. фибрин. Матричный – т.к. активация факторов гемокоагуляции осущ. на матрице. Матрицей могут быть фосфолипидов мембран разрушенных ФЭК (тромбоцитов) и обломки клеток тканей. О 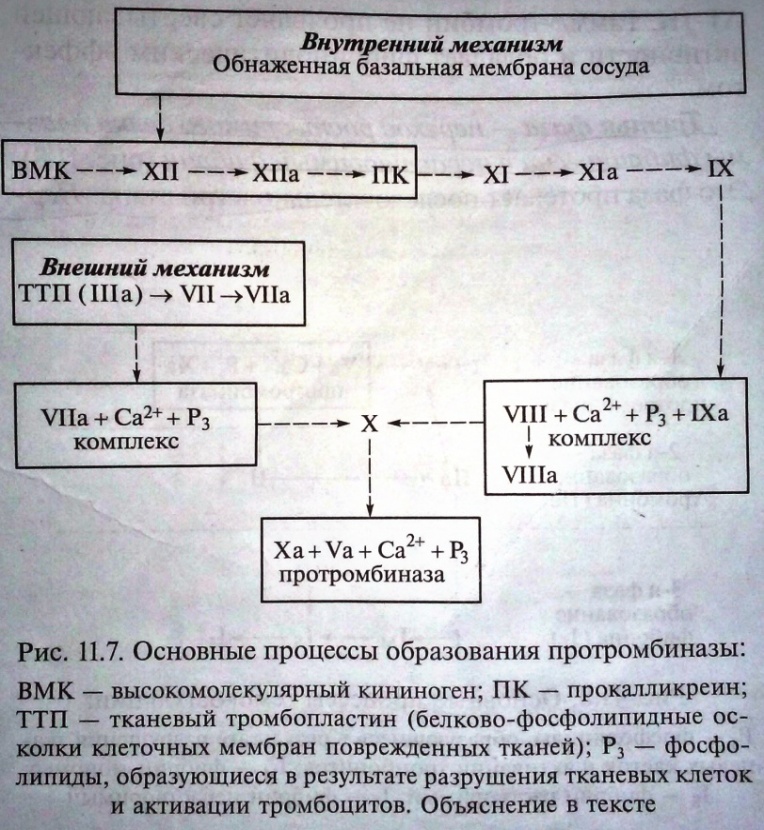 сущ. в 3 фазы: сущ. в 3 фазы:1) Первая фаза – образование протромбиназы. Начинается с активации XII фактора плазмы, затем каскадная активация др. факторов и заканчивается активацией X плазм. фактора с образованием протромбиназы. Реакция осущ. по 2м механизмам. В  нутр. механизм образования начинается с повреждения стенки сосуда и активации плазм. фактора XII за счёт контакта его с «-»-о заряженной поверхностью базальной мембраны, коллагеном, ВМК, калликреином, фактором Р3 – фосфолипидными осколками мембран тромбоцитов. Активный фактор XIIа превращает плазм. фактор XI в активную форму (XIа) также в присутствии Р3 и ВМК. Фактор XIа активирует плазм. фактор IX (IXа). В дальнейшнем образуется комплекс факторов IXа, VIII, Ca2+ и фактора Р3, который активирует фактор X (Xa). Образовавшийся по внеш. и внутр. механизму Xа взаимодействует с плазм. фактором V, Са2+ и фактором Р3, в результате чего образуется комплекс, который наз. протромбиназой. нутр. механизм образования начинается с повреждения стенки сосуда и активации плазм. фактора XII за счёт контакта его с «-»-о заряженной поверхностью базальной мембраны, коллагеном, ВМК, калликреином, фактором Р3 – фосфолипидными осколками мембран тромбоцитов. Активный фактор XIIа превращает плазм. фактор XI в активную форму (XIа) также в присутствии Р3 и ВМК. Фактор XIа активирует плазм. фактор IX (IXа). В дальнейшнем образуется комплекс факторов IXа, VIII, Ca2+ и фактора Р3, который активирует фактор X (Xa). Образовавшийся по внеш. и внутр. механизму Xа взаимодействует с плазм. фактором V, Са2+ и фактором Р3, в результате чего образуется комплекс, который наз. протромбиназой.Внешн. механизм образования осущ. при поступлении тканевого тромбопластина (фосфолипид. осколки мембран поверждён. клеток) в кровоток из повреждён. тканей и сосуд. стенки, взаимодействия его с плазм. фактором VII и ионами Са2+. Образуется кальциевый комплекс, который превращ. X в Xa. 2) Вторая фаза – образование активного фермента тромбина. Он образуется из протромбина при действии на него тромбиназы: происходит протеолиз протромбина и образуются α-, β- и γ-тромбин. Наиболее активный - α-тромбин, он оказывает выраженное коагуляционное действие. Однако α-тромбин быстро игнибируется естественными антикоагулянтами, особенно комплексом гепарин-АТ-III. Свёртывающим действием обладают также β- тромбин, но он оказывается резистентным к гепарину и АТ-III. γ-тробимн не проявл. свёрт. активности и обладает фибринолитическим эффектом. 3) Третья фаза – переход растворимого белка плазмы фибриногена в нерастворимый фибрин. Эта фаза происходит в 3 этапа. 1-ый этап – протеолитический: тромбин, обладая эстеразной активностью, отщепляет от α- и β- цепей молекулы фибриногена 2 пептида А, затем 2 пептида В, в результате образуются фибрин-мономеры. 2-ой этап – полимеризационный: в основе этого неферментатив. этапа лежит спонтанный самосборочный процесс, приводящий к агрегации фибрин-мономеров с образованием фибрин-полимера (фибрин-S); его волокна легко лизируются не только под влиянием плазмина, но и комплексных соединений, обладающих неферментатив. фибринолитической активностью. 3-ий этап – ферментативный: фибриназа (XIII) дополнительно «прошивает» полимеры фибрина S, в результате растворимый фибрин S переходит в нераствор. фибрин I. Благодаря этого сгусток становится резистентным к действию мочевины и фибринолитических агентов и лучше фиксируется в повреждённом сосуде. В процессе превращения фибриногена в фибрин большую роль играют эритроциты: в их присутствии процесс ускоряется. В результате свёртывания крови образуется сгусток. Он сост. из нитей фибрина и осевших в них ФЭК, глав. образом эритроцитов. Кровяной сгусток закрывает просвет повреждённого сосуда. Сгусток, прикреплённый к стенке сосуда – тромб. Сгусток и тромб в дальнейшем подвергаются 2м воздействиям: 1) ретракции (сокращению) и 2) фибринолизу (растворению). Ускорение и замедление процесса свёртывания крови – гипер- и гипокоагуляция. 15. Функциональная система, обеспечивающая поддержание жидкого состояния крови. Свертывающая, противосвертывающая и фибринолитическая системы, их функц. взаимодействие. Факторы, поддерживающие жидкое состояние крови: 1) Тромборезистентность эндотелия стенки сосуда; Тромборезистентность эндотелия сосудов обеспечивается за счет антиагрегантных, антикоагулянтных и фибринолитических свойств. 2) Неактивное состояние плазменных факторов свертывания крови; 3) Присутствие в крови естественных антикоагулянтов; 4) Наличие системы фибринолиза; 5) Непрерывный циркулирующий поток крови. Ф 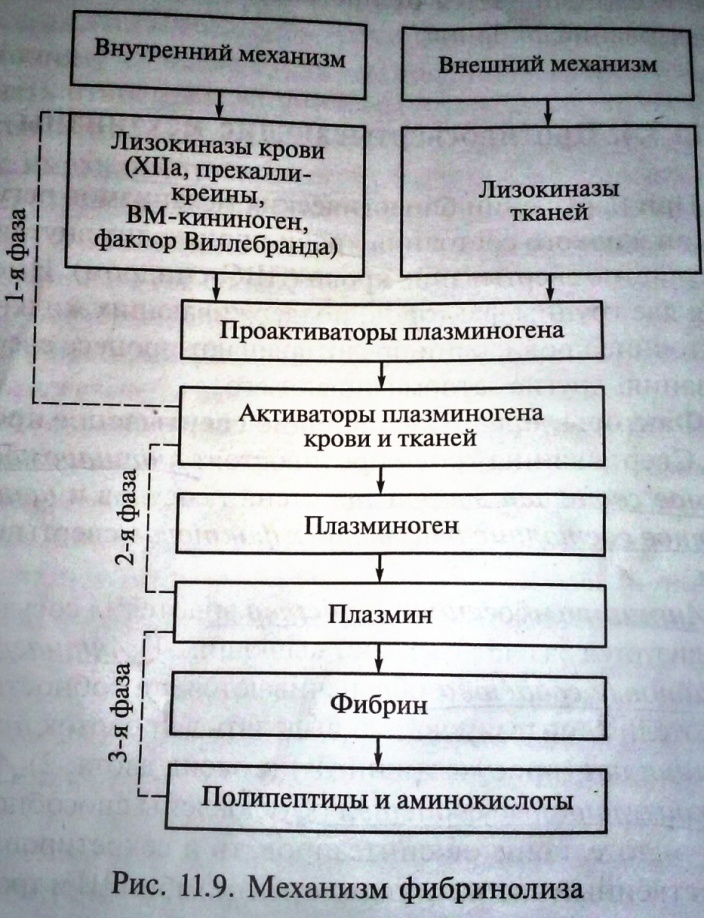 ИБРИНОЛИЗ – совокупность процессов, осущ. расщепление нитей фибрина, образовавшихся в процессе свертывания крови, на растворимые комплексы и восстановление просвета кровеносных сосудов. ИБРИНОЛИЗ – совокупность процессов, осущ. расщепление нитей фибрина, образовавшихся в процессе свертывания крови, на растворимые комплексы и восстановление просвета кровеносных сосудов.Основные компоненты фибринолиза. Фермент плазмин (фибринолизин) находится в крови в неактивном состоянии в виде плазминогена (профибриглизина); явл. протеолитич. ферментов, относящимся к β1-глобулинам, расщепляет фибрин, фибриноген, некоторые плазм. факторы свёртывания крови и др. белки плазмы крови. Активаторы плазминогена относятся к глобулинам. 2 группы активаторов – прямого и непрям. действия. Активаторы прямого действия непосредственно переводят плазминоген в активную форму плазмин (кислые и щелочные фосфатазы, трипсин, урокиназа). Активаторы непрям. дейсвтия в плазме крови в виде профибринолизинкиназы. Для его активации нужны лизокиназы тканей и плазмы (XIIа). Активаторы также есть в ткани: матка, лёгкие, щит. железа, надпочечники. Ингибиторы фибринолиза (антиплазмины) – альбумины. 2 группы. 1-ая: антиплазмины, тормозящие действие активного фермента фибринолизина; 2-ая: ингибирующие превращение профибринолизина в фибринолизин. Основным быстродействующим ингибитором явл. α2-макроглобулин. Также ингибиторы: α2-антиплазмин, α1-хемотрипсинн, Ат-III, С1-эстеразный ингибитор. Ферментативный фибринолиз. 3 фазы: 1) 1 фаза – лизокиназы, поступающие в крови из тканей и ФЭК, превращают проактиватор плазминогена в активное состояние – активатор плазминогена. Эта реакция осущ. в результате отщепления от проактиватора ряда аминок-т. 2) 2 фаза – превращение плазминогена в плазмин в результате действия активатора на молекулу плазминогена, от которой отщепляется липидный ингибитор. 3) 3 фаза – под влиянием плазмина фибрин расщепляется до полипептидов (высокомол. фрагменты Х и У, низкомолекул. – D и Е) и амин-к-т. Эти фрагменты – продукты деградации фибриногена/фибрина (ПДФ) - обладают выраженным антикоаг. действием. Они не только ингибируют тромбин, но и тормозят процессы образование протромбиназы и полимеризации фибрина, адгезию и агрегацию тромбоцитов. Активация фибринолиза осущ. по 2м путям: внеш. и внутр. По внешнему пути активация осуществляется за счет лизокиназ тканей, тканевых активаторов плазминогена. В первую очередь, это относится к активатору, который образуется эндотелием сосудистой стенки, что облегчает его поступление в кровоток. В сосудистом русле активаторы оказывают свое специфическое действие на плазминоген. При физ. нагрузках, стрессовых состояниях организма наблюдается усиление поступления тканевых активаторов в кровоток. Внутренний путь активации фибринолиза значительно сложнее внешнего. В нем участвуют проактиваторы и активаторы фибринолиза, обнаруженные в форменных элементах крови, ХIIа фактор, прекалликреин, высокомолекулярный кининоген (ВМК), фактор Виллебранда. Комплекс XIIа + ВМК способен превращать проактиваторы в активаторы плазминогена или же действовать непосредственно на профермент и переводить его в плазмин. В процессе растворения фибринового сгустка значительную роль играют лейкоциты. За счет фагоцитарной активности они способны захватывать фибрин, лизировать его и выделять в окр. среду продукты его деградации. Лизис фибрина в лейкоцитах осуществляется содержащимися в гранулах фибринолитическими протеазами до высокомолекулярных фрагментов X и Y без участия плазмина. Неферментативный фибринолиз. Фибринолитическим эффектом обладают комплексные соединения гепарина с некоторыми гормонами, биогенными аминами и тромбогенными белками крови. Неферментативным способом осуществляется процесс расщепления нестабилизированного фибрина (фибрин S), в результате чего он из фибриллярной формы превращается в глобулярную, и в результате этого сосудистое русло очищается от промежуточных продуктов образования фибрина. ПРОТИВОСЁРТЫВАЮЩИЕ МЕХНИЗМЫ. При нарушении био. механизмов регуляции жидкого состояния крови происходит внутрисосудистое свертывание кровИ. Имеется 2 группы факторов, поддерживающих жидкое состояние крови. 1) Факторы, предотвращающие свертывание крови. Свертыванию крови противостоят антитромбогенное свойство эндотелия стенки сосудов и неактивное состояние плазм. факторов свертывания. Антитромбогенное св-во эндотелия сосудов реализуется за счет трех составляющих. - антиагрегационные св-ва обеспечиваются способностью эндотелия синтезировать и выделять в кровоток простациклин (простагландин12) и оксид азота. - антикоагулянтные св-ва обусловлены способностью эндотелиоцитов синтезировать и секретировать естеств. антикоагулянт антитромбин III и тромбомодулин. Последний связывает активный фермент тромбин и за счет этого нарушается процесс образования фибрина при свертывании крови. Комплекс тромбомодулин-тромбин активируется также естественным антикоагулянтом — протеином С, образующимся в печени. - фибринолитические св-ва закл. в способности эндотелиоцитов синтезировать и секретировать в кровоток тканевой активатор плазминогена, который является мощным активатором системы фибринолиза. 2) Факторы, тормозящие свёртывание крови: первичные, синтез. в печени, лёгких и др. органах, постоянно циркулир. в крови, и вторичные, образующиеся в процессе свертывания крови и фибринолиза. Первичные антикоагулянты. В интиме крупных сосудов преимущ. локализован гликопротеид антитромбин-III (АТ-III). Биосинтез осущ. в печени и эндотелиоцитах. АТ-III тормозит активность тромбина, факторов IХа, Ха, ХIа, ХIIа, плазмина и калликреина. Гепарин усиливает ингибирующий эффект АТ-III. Гепарин - гликозаминогликан, синтезируется в базофильных клетках крови и тканей, а также в тучных клетках соед. ткани. Гепарин содержится почти во всех тканях организма и явл. антикоагулянтом прямого и широкого спектра действия. Он проявляет свой антикоагулянтный эффект на факторы гемокоагуляции непосредственно в крови. Гепарин тормозит процесс образования протромбиназы, блокирует превращение протромбина в тромбин, препятствует взаимодействию тромбина с фибриногеном, т.е. тормозит протекание всех фаз процесса гемокоагуляции. Антикоагулянтный эффект гепарина объясняется его способностью образовывать комплексные соединения с тромбогенными белками — протромбином, тромбином, фибриногеном. Разрушение гепарина осуществляется ферментом гепариназой. Антикоагулянтное действие гепарина проявляется в присутствии его кофактора — АТ-III. Протеин С образуется в печени и секретируется в кровь в неактивном виде; гликопротеид. Активация неактивной формы протеина С осуществляется комплексом тромбомодулин-тромбин. Антикоагулянтные свойства активного протеина С связаны с тем, что он инактивирует активные плазменные факторы Va и VIIIa и этим тормозит образование тромбина и фибрина в процессе свертывания крови. Протеин S образуется эндотелиоцитами печени, тромбоцитами и является К-зависимым белком. Он является кофактором протеина С, так как в его присутствии ускоряется процесс инактивации фактора VIIIа. Антитромбин IV(а2-макроглобулин). Вторичные антикоагулянты — отработавшие факторы свертывания (фибрин, ХIа и Va, фибринпептиды А и В, отщепляемые от фибриногена), а также продукты фибринолиза (антитромбин VI). 16. Группы крови как проявления иммунной специфичности организма. Разновидности групп, систем крови. Резус-фактор, их значение для акушерской и хирургической практики. 1) К. ландштейнер и Я. Янский в 1901-1904 гг. установили существование в эритрцитах людей особых антигенов – агглютиногенов и предположили наличие в сыворотке крови соотв. им антигенов – агглютининов. Антигены – высокомол. полимеры естеств. или искусств. происхождения, которые несут признаки генетически чужеродной информации. Групповую принадлежность крови обусловливают изоантигены (у человека 200). Они объединяются в групповые антигенные системы. Главными носителями антигенных св-с явл. эритроциты. Антитела – иммуноглобулины, образующиеся на введение антигена. Антитела способны взаимодействовать с одноименными антигенами и вызывать агглютинацию. Различные группы крови объединяют в системы, в частности АВ0, Rh-hr. Известен еще целый ряд антигенных систем, наибольшее значение из которых имеют Келл-Челлано, Даффи, Кидд, MNSs. К ним. как и к антигенам Rh-hr, нет естественных антител. Антигенные системы АВО и Rh-hr имеют большое клиническое значение, так как иммунологический конфликт по указанным системам является наиболее частой причиной осложнений, наблюдающихся при переливании крови. Система АВО. Антигены (агглютиногены) А и В явл. полисахаридами, они находятся в мембране эритроцитов и связаны с белками и липидами. Кроме указанных агглютиногенов в эритроцитах может содержаться антиген 0, у которого антигенные свойства выражены слабо и в крови нет одноименных ему агглютининов. Антитела (агглютинины) α и β находятся в плазме крови. Одноименные агглютиногены и агглютинины в крови одного и того же человека не встречаются. Если же в эксперименте смешать в пробирке кровь с одноименными агглютиногенами и агглютининами, то произойдет реакция агглютинации — склеивание и разрушение (гемолиз) эритроцитов. Деление людей по группам крови в системе АВО основано на различных комбинациях агглютиногенов эритроцитов и агглютининов плазмы. Известно 4 группы крови: 1 - 0αβ, 2 – Аβ, 3- Вα, 4- АВ. В эритроцитах обнаружены разновидности агглютиногенов А и В: агглютиногены А1-7, В1-6 (отличаются по антигенным св-вом). Найдены также агглютинины α1 и α2 – экстраагглютинины. 2) Система резус-фактор была открта в 1937-1940 гг. К. Ландштейнером и А. Винером. Антигены системы резус (Rh) явл. липопротеидами. Эритроциты 85% людей содержат Rh-агглютиноген – Rh+ кровь. В эритроцитах 15% людей резус-антигена нет – Rh- крови. В наст. вр. описано 6 разновидностей системы резус. Наиболее важные: Rh0 (D), rh (C), rh’’ (E); самые активный антиген D, по которому и определяется резус-принадлежность. Главная особенность системы резус сост. в том, что она не имеет ественных антител. Антирезус – антитела формируются при переливании Rh- человеку Rh+-ой крови, что недопустимо. Опасность для плода. Если мать резус-отрицательна, а отец резус-положителен, то плод может быть резус-положительный. При нарушении целостности сосудистого плацентарного барьера в период беременности резус-положительным плодом в организме матери могут вырабатываться антирезус-агглютинины. Это происходит вследствие того, что эритроциты Rh+ крови плода попадают в Rh- кровь матери и вызывают выработку у нее Rh-антител. Последние, проникая через плаценту в кровь плода, могут вызвать агглютинацию его эритроцитов с последующим их гемолизом. В результате этого у новорожденного развивается тяжелая гемолитическая анемия, характеризующаяся низким содержанием гемоглобина и снижением количества эритроцитов. Открытие резус-фактора имело большое практическое значение, так как позволило предупреждать возможные гемотрансфузионные реакции при переливании крови одноименных групп. 17. Физиологические основы переливания крови. Кровезамещающие растворы, их использование в медицинской практике. 1) Иммунный конфликт по системе АВ0 может произойти при встрече одноимённых агглютиногенов и агглютининов. При этом происходит агглютинация. Иммунный конфликт может наблюдаться: - при переливании крови несовместимой в групповом отношения; - при наличии в переливаемой крови иммунных анти-А- и анти-В-антител; - присутствие в переливаемой крови экстраагглютининов α1 и α2; - при переливании больших кол-в крови (более 200 мл) группы 0 (I) лицам с др. группами крови. При переливании крови необходимо предупредить встречу одноимённых антител и антигенов. При этом у донора образают внимание на эритроциты с содержащимися в ним агглютиногенами, а у реципиента – на плазму с находящими в ней агглютининами. Необходимо переливать только одногруппную кровь, в экстренных случаях возможно применение правила Оттенберга. Детям можно переливать только одногруппную кровь. 2) Иммунный конфликт по антигенной системе резус происходит в следующих случаях: 1) при повторном переливании резус-отрицательному человеку (реципиенту) резус-положительной крови; 2) в случаях беременности, когда женщина резус-отрицательна, а плод резус-положителен. Если кровь резус-положительного донора переливать резус-отрицательному реципиенту, то в организме последнего начнут образовываться специфические по отношению к резус-фактору антитела — антирезус-агглютинины. При повторном переливании резус-положителъной крови этому реципиенту у него может наблюдаться гемотрансфузионный шок вследствие агглютинации эритроцитов донора и их гемолиза. Резус-отрицательным реципиентам необходимо переливать только резус-отрицательную кровь. 18. Значение дыхания для организма. Основные этапы дыхания. Дыхание - совокупность процессов, включающх поступление в организм О2, использование его для окисления орган. вещ-в с освобождением энергии и выделением СО2 в окр. среду. В среднем в состоянии покоя человек потребляет в течение минуты 50 мл О2 и выделяет 230 мл СО2. Зн-е дыхания закл. в обеспечении организма энергией. Источником энергии явл. орган. соедин., поступающие в организм с пищевыми вещ-вами, а дыхание обеспечивает высвобождение этой энергии. Главным поставщиком энергии явл. процесс аэробного окисления. Фун-и дых. системы:
Различают несколько этапов дыхания: 1) газообмен между альвеолами и окр. средой - вентиляция лёгких. 2) газообмен между кровью организма и газовой смесью, находящейся в лёгких. 3) транспорт газов кровью - О2 от лёгких к тканям, СО" от тканей организма к лёгким. 4) газообмен между кровью и тканями организма - О2 поступает к тканям, а СО2 из тканей - в кровь. 5) потребление О2 тканями с образованием СО2 и воды - тканевое (внутр.) дыхание. Совокупность 1-го и 2-го этапов дыхания - это внешнее дыхание, обеспечивающее газообмен между окр. средой и кровью. Оно осущ. с помощью внешнего звена системы дыхания, вкл. лёгкие с воздухоносными путями, грудную клетку и мышцы, приводящие её в движение. Прочие этапы дыхания осущ. посредством внутр. звена системы дыхания, вкл. кровь, ССС, органеллы клеток, обеспечивающих тканевое дыхание. 19. Внешнее дыхание. Биомеханика вдоха и выдоха. Давление в плевральной полости, его изменения при вдохе и выдохе. Внешнее дыхание. 1) Лёгкие. Главная фун-я – газообмен между организмом и окр. средой. Функц. единица – ацинус (300 тыс.): вкл. дых. бронхиолы, переходящие в альвеол. ходы и мешочки с альвеолами (d=0,3-0,4 мм, 300-350 млн, 80 м2). Совокупность альвеол. ходов и мешочков, несущих на себе альвеолы, где происходит газообмен м/ду газовой смесью и кровью организма, наз. дыхательной зоной. Недых. ф-и (№31). 2) Воздухоносные пути. - Газообменная фун-я – обеспеч. доставку атмосферного воздуха в газообменную область. Они начинаются с отверстий носа, полости рта до 16 генерации бронхиол. 17,18,19 – дых. бронхиолы (переходная зона). 2% альвеол. - Негазообменные фун-и: очищение вдыхаемого воздуха (кашлевой, чихательный рефлексы), увлажнение вдых. воздуха до 100% (слизь), согревание воздуха, терморегуляция за счёт теплоиспарения, конвекции и теплопродукции. 3) Грудная клетка явл. герметической полостью для лёгких. Она предохраняет их от высыхания и механ. повреждения. Экскурсиями гр. клетки обеспечивают сужение и расширение лёгких, а значит, их вентиляцию. 4) Дых. мышцы. Инспираторные: диафрагма, наруж. межорёберные и внутр. межхрящевые мышцы. Экспираторные: абдоминальные (внутр. и нар. косые, прямая ипоперечная) и внутр. межрёб. (5. Сурфактант содержит фосфолипиды, триглицериды, холестерин, протеины и углеводы. Ученьшает поверх. натяжение жидкости, предотвращает слипание альвеол во время вдоха. Защитная фун-я. Облегчает диффузию О2.) Отриц. давление в плевральной полости - величина, на которую давление в плеврал. щели ниже атмосферного. В норме это (-4)-(-8) мм рт. ст. Изменение давления в самих лёгких при вдохе – на -2 мм рт. ст., при выдохе – на +2 мм рт. ст. При макс. вдохе давление увел. до – 20 мм рт. ст., при макс. выдохе приближается к нулю, становясь почти равным атмосфер. давлению (760 мм рт.ст.). Вследствие растянутого состояния лёгких возникает сила, стремящаяся вызвать их спадение – эласт. тяга лёгких (ЭТЛ). Т.к. плеваральная щель не сообщ. с атмосферой, давление в ней ниже атмосферного на величину ЭТЛ: при вдохе – на 8 мм рт. ст., при выдохе – на 4 мм. рт. ст. Пневмоторакс – пат. состояние, возникающее при нарушении гермитичности плевр. щели, в результате чего атм. воздух заполняет плевр. щель, оказываясь между висц. и париет. листками плевры. Вдох. 1 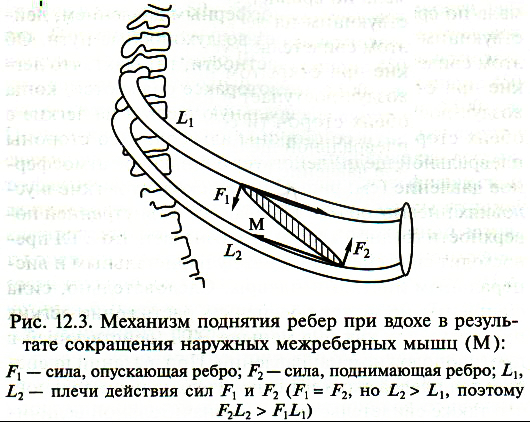 ) Расширение грудной клетки при вдохе обеспечивается сокращением инспираторных мышц и происходит в трех направлениях: вертикальном, фронтальном (в стороны) и сагиттальном. В вертикальном направлении гр. клетка расширяется в основном за счет сокращения диафрагмы и смещения ее сухожильного центра вниз. Диафрагмальная мышца — главная дыхательная мышца: в норме вентиляция легких на 2/3 осуществляется за счет ее движений. Диафрагма участвует в обеспечении кашлевой реакции, рвоты, натуживания, икоты, в родовых схватках. При спокойном вдохе купол диафрагмы опускается примерно на 2 см, при глубоком дыхании — до 10 см. У здоровых молодых мужчин разница между окружностью грудной клетки в положении вдоха и выдоха составляет 7—10 см, у женщин — 5—8 см. ) Расширение грудной клетки при вдохе обеспечивается сокращением инспираторных мышц и происходит в трех направлениях: вертикальном, фронтальном (в стороны) и сагиттальном. В вертикальном направлении гр. клетка расширяется в основном за счет сокращения диафрагмы и смещения ее сухожильного центра вниз. Диафрагмальная мышца — главная дыхательная мышца: в норме вентиляция легких на 2/3 осуществляется за счет ее движений. Диафрагма участвует в обеспечении кашлевой реакции, рвоты, натуживания, икоты, в родовых схватках. При спокойном вдохе купол диафрагмы опускается примерно на 2 см, при глубоком дыхании — до 10 см. У здоровых молодых мужчин разница между окружностью грудной клетки в положении вдоха и выдоха составляет 7—10 см, у женщин — 5—8 см.Расширение гр. клетки в сагиттальном направлении и в стороны происходит при поднятии ребер вследствие сокращения наружных межреберных и межхрящевых мышц. Наружные межреберные мышцы при сокращении с одинаковой силой (F) тянут верхнее ребро вниз, а нижнее поднимают вверх. Однако система из каждой пары ребер поднимается вверх, так как момент силы, направленной вверх (F2), больше момента силы, направленной вниз (F1), поскольку плечо нижнего ребра (L2) больше верхнего (L1): F1= F2, но L2> Lx, поэтому P2 • L2> Fx- Lx. Так же действуют и межхрящевые мышцы. В обоих случаях мышечные волокна ориентированы таким образом, что точка их прикрепления к нижележ. ребру расположена дальше от центра вращения, чем точка прикрепления к вышележ. ребру. Расширению грудной клетки способствуют и силы ее упругости: в процессе выдоха грудная клетка сильно сжимается, вследствие чего стремится расшириться. Поэтому энергия при вдохе расходуется только на преодоление прироста величины ЭТЛ и брюшной стенки, а ребра поднимаются сами, обеспечивая примерно до 60 % жизненной. 2) Главная причина расширения легких при вдохе — атмосферное давление воздуха, действующее на легкое только с одной стороны — через воздухоносные пути. Вспомогательную роль выполняют силы сцепления (адгезии) висцерального и париетального листков плевры. Сила, с которой легкие прижаты к внутренней поверхности грудной клетки атмосферным воздухом, равна Ратм - Рэтл. (В целях улучшения восприятия материала, изменением давления в самих легких (при вдохе на -2 мм рт. ст., а при выдохе на +2 мм рт. ст. можно пренебречь.) Снаружи на грудную клетку действует Ратм, но на легкие это давление не передается, и на них действует только одностороннее атмосферное давление через воздухоносные пути. Так как снаружи на грудную клетку действует Ратм, а изнутри разница (Ратм - Рэтл), при вдохе необходимо преодолеть прирост силы ЭТЛ. Поскольку при вдохе ЭТЛ увеличивается вследствие расширения (растяжения) легких, то увеличивается и отриц. давление в плевральной щели. Расширению легких при вдохе способствует еще одна сила — сила сцепления между висцеральным и париетальным листками плевры, но она крайне малап о сравнению с атмосферным давлением. 3) Поступление воздуха в легкие при их расширении является результатом некоторого (на 2 мм рт. ст.) падения давления в альвеолах. Кроме того, увеличение ЭТЛ при вдохе обеспечивает дополнительное расширение бронхов. Вслед за вдохом плавно начинается выдох. Скорость движения воздуха в трахее и главных бронхах составляет 100 см/с, далее она быстро падает вследствие суммарного расширения воздухоносных путей и в дыхательных бронхах составляет 0,2 см/с. Выход. При описании выдоха необходимо объяснить причины одновременно происходящих процессов: 1) сужение грудной клетки; 2) сужение легких; 3) изгнание воздуха из легких в атмосферу. Экспираторными являются внутренние межреберные мышцыи мышцы брюшной стенки. Спокойный выдох осуществляется без непосредственной затраты энергии. Сужение грудной клетки обеспечивают ЭТЛ и эласт. тяга стенки живота. При вдохе растягиваются легкие, вследствие чего возрастает ЭТЛ. Кроме того, диафрагма опускается вниз и оттесняет органы брюшной полости, растягивая при этом стенку живота и увеличивая ее эластическую тягу. Как только прекращается поступление нервных импульсов к мышцам вдоха по диафрагм. и межреб. нервам, прекращается возбуждение мышц, вследствие чего они расслабляются. Гр. клетка суживается под влиянием ЭТЛ и постоянно имеющегося тонуса мышц стенки живота, при этом органы брюшной полости оказывают давление на диафрагму. Вследствие происходящих процессов легкие сжимаются. Поднятию купола диафрагмы способствует также ЭТЛ. Давление воздуха в легких возрастает на 2 мм рт. ст. в результате уменьш. их объема, и воздух из легких изгоняется в атмосферу. Уменьшение давления равно силе ЭТЛ, так как с внутренней стороны реальное давление, оказываемое воздухом на грудную клетку, равно Ратм _ Рэтл, а снаружи на грудную клетку действует Ратм. Этот перепад давлений (РЭтл) действует и на вдохе, и на выдохе, но вдоху он препятствует (преодоление ЭТЛ), а выдоху способствует. Иными словами, ЭТЛ сжимает грудную клетку, как пружину. 20. Понятие легочных объемов, емкостей, их величины. Резервные возможности системы дыхания. Объемы. 1) Дыхательный объем (ДО) — это объем воздуха, который человек вдыхает и выдыхает при спокойном дыхании, при этом продолжительность одного цикла дыхания составляет 4—6 с, акт вдоха проходит несколько быстрее. Такое дыхание называется эйпное. 500 мл. 1 мин=12-16 дых. циклов. 2) Резервный объем вдоха (РО вдоха) — максимальный объем воздуха, который человек может дополнительно вдохнуть после спокойного вдоха. 1,8-2,0 л. 3) Резервный объем выдоха (РО выдоха) — максимальный объем воздуха, который можно выдохнуть после спокойного выдоха. 1,2-1,4 л. 4) Остаточный объем (ОО) — объем воздуха, остающийся в легких после макс.выдоха. 1,2-1,5л. 5) Минутный объем воздуха (МОВ) — это объем воздуха, проходящего через легкие за 1 мин. Он составляет в покое 6-8 л, частота дыхания — 14-18 в 1 минуту (около 8 л/мин). При интенсивной мышечной нагрузке МОВ может достигать 100 л. 6) Максимальная вентиляция легких (МВЛ) — это объем воздуха, который проходит через легкие за 1 мин при максимально возможной глубине и частоте дыхания. МВД может достигать у молодого человека 120-150 л/мин, а у спортсменов — 180 л/мин, она зависит от возраста, роста, пола. При прочих равных условиях МВД характеризует проходимость дыхательных путей, а также упругость грудной клетки и растяжимость легких. Ёмкости легких – совокупность нескольких объёмов. 1) Жизненная емкость легких (ЖЕЛ) — это наибольший объем воздуха, который можно выдохнуть после макс. вдоха. Вкл. в себя ДО, РО входа и выхода. У молодых людей должную величину ЖЕЛ можно рассчитать по формуле: ЖЕЛ = Длина тела (м) -2,5 (л). ЖЕЛ мужчин = 3,5-5,0 л. ЖЕЛ женщин = 3,0-4,0 л. 2) Функциональная остаточная емкость (ФОЕ) — кол-во воздуха, остающееся в легких после спокойного выдоха; ФОЕ равна сумме ОО и РО выдоха. 2500 мл. 3) Общая емкость легких (ОЕЛ) — объем воздуха, содержащийся в легких на высоте максимального вдоха; ОЕЛ = ЖЕЛ + + ОО. Как и другие объемы и емкости, ОЕЛ весьма вариабельна и зависит от пола, возраста и длины тела. Так, у молодых людей в возрасте 20 — 30 лет она равна в среднем около 6 л, у мужчин в 50 — 60 лет — в среднем около 5,5 л. 4) Ёмкость вдоха (Е вд.) = ДО + РО вхоха = 2,0-2,5 л. Из всех перечисленных величин наибольшее практическое значение имеют: ДО, ЖЕЛ и ФОЕ. ЖЕЛ является показателем подвижности грудной клетки и растяжимости легких: при различных патологических процессах ЖЕЛ может сильно уменьшаться. Однако значительное уменьшение ЖЕЛ не обязательно ведет к ухудшению оксигенации крови и уменьшению удаления углекислого газа, так как даже при максимальной физической нагрузке используется не более 60 % ЖЕЛ. Этот показатель также весьма вариабелен и зависит от длины тела, пола (у женщин — на 25 % меньше), возраста (после 40 лет ЖЕЛ снижается). ФОЕ обеспечивает стабилизацию альвеолярной газовой смеси, несмотря на то что она обновляется порциями. ФОЕ сохраняет некоторый резерв кислорода при вынужденной задержке дыхания, например при нырянии, при действии веществ с едким запахом, в результате чего происходит произвольное или непроизвольное прекращение дыхания. При пневмотораксе большая часть остаточного воздуха выходит, а в легком остается минимальный объем воздуха. Этот воздух задерживается в так называемых воздушных ловушках, так как часть бронхиол спадается раньше альвеол (концевые и дыхательные бронхиолы не содержат хрящей). Поэтому легкое взрослого человека и дышавшего новорожд. ребенка не тонет в воде (тест для определения в суд.-мед. экспертизе, живым ли родился ребенок: легкое мертворожденного тонет в воде, так как не содержит воздуха). Резервные возможности системы внешн. дыхания проявл. в способности увел. либо произвольно, либо во время физ. работы, либо в условиях изменений газ. среды объём вдоха (РО вдоха может увел. до 1900-3300 л) и объём выхода (РО выхода может увел. до 700-1000 мл) относительно ДО, величина которого в покое равна 500 мл. Все 3 объёма составляют ЖЕЛ, которая явл. тренируемой величиной. Нпр., в зависимости от характера физ. упражнений или вида спорта величина ЖЕЛ может превышать в 1,5 раза аналог. показатель у нетренированного человека. Кислородная ёмкость крови (КЁК) – один из показат. резерв. возможностей; кол-во О2, которое может быть связано кровью при полном её насыщении. Зависио от: кол-ва Hb, t тела (при нагревании крови КЁК уменьш.). КЁК измеряется объёмом О2 в мл, который может связаться гемоглобином 100 мл крови. 1г Hb связывает 1,34 мл О2. 2 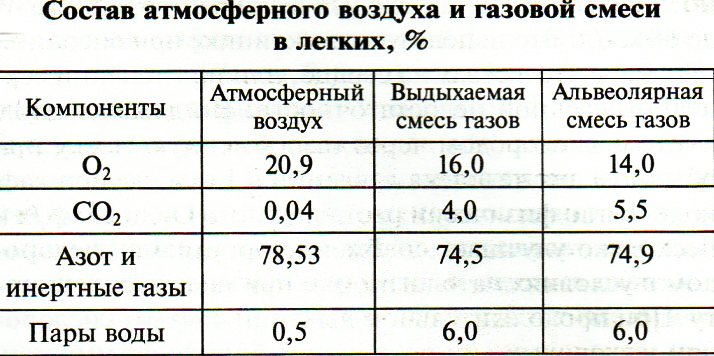 1. Состав вдыхаемого, выдыхаемого и альвеолярного воздуха. Анатомическое, физиологическое и функциональное мертвые пространства. 1. Состав вдыхаемого, выдыхаемого и альвеолярного воздуха. Анатомическое, физиологическое и функциональное мертвые пространства.Дых. средой для человека явл. атмосферный воздух, состав которого отличается постоянством. В 1 л сухого воздуха содержится 780 мл азота, 210 мл О2 и 0,3 мл СО2. Остальные 10 мл приходятся на инертные газы: аргон, неон, гелий, криптон, ксенон и водород. Газообмен в легком ведет к изменению его газового состава по сравнению с составом атмосферного воздуха. В покое человек потребляет около 250 мл 02 и выделяет около 230 мл С02, поэтому в альвеолярном воздухе уменьшается количество 02 и увеличивается содержание С02. Изменения содержания 02 и С02 в альвеолярной смеси газов являются следствием потребления организмом 02 и выделения С02. В выдыхаемом воздухе количество 02 несколько возрастает, а С02 — уменьшается, по сравнению с альвеолярной газовой смесью вследствие того, что к ней добавляется воздух воздухоносного пути, не участвующий в газообмене и, естественно, содержащий С02 и 02 в таких же количествах, как и атмосферный воздух. Азот в газообмене не участвует, некоторое увеличение содержания его в альвеолярном воздухе является относительным — объем выдыхаемого воздуха несколько меньше объема вдыхаемого. Это объясняется тем, что С02 выделяется из организма несколько меньше, чем потребляется 02, из-за различного содержания углерода и кислорода в различных окисляемых веществах организма. На долю инертных газов в атмосферном воздухе приходится около 1 %. Кровь, обогащенная 02 и отдавшая С02, из легких поступает в левую половину сердца и по артериям и капиллярам разносится по всему организму, отдавая в различных органах и тканях О 2 и получая из них С02. Анатомически мёртвое пространство – воздухопроводящая зона, которая не участвует в газообмене (верхние дых. пути, трахея, бронхи, терминальные бронхиоллы). АМП выполняет ряд важных фун-ий: нагревает вдыхаемый атм. воздух, задерживает около 30% выдыхаемого тепла и воды. Во время спокойного вдоха объёмом 500 мл в альвеолы поступает только 350 мл. Остальные 150 мл задерживаются в АМП. Составляя в среднем 1/3 дых. объёма, мертвое пространство снижает на эту величину эффективность альвеолярной вентиляции при спокойной дыхании. В тех случаях, когда при выполнении физ. работы дых. объём увел. в несколько раз, объём АМП практически не влияет на эффективность альв. вентиляции. Альвеолярное мёртвое пространство – физиолог. состояние, при котором в здоровом лёгком некоторое кол-во апикальных альвеол вентилируются нормально, но частично либо полностью не перфузируются кровью. Также АлМП может возникнуть при анемии, лёгочной эмболии или эмиземе. Физиолог. (функц.) мёртвое пространство – сумма АМП и альвеолярного мёртвого пространства. 22. Аэрогематический барьер. Диффузионная способность легких. Диффузия газов в средах организма, роль парциального давления, парциального напряжения газов в газообмене. Процесс переноса О2 и СО2 через альвеолярно-капиллярную мембрану осущ. путём его физиолог. диффузии, т.е. из области выск5ого в область низкого парц. давления. Аэрогематический барьер – барьер между альвеолярным воздухом и кровью, образован эндотелиоцитами и базальной мембраной капилляров, прослойками интерстиц. ткани, базальной мембраной альвеолярного эпителия, альвеоцитами (I типа – плоскими, выстилающими 95% поверхности альвеол, и II типа – крупными, округлыми клетками СС зернистой цитоплазмой, продуцирующими сурфактант) и альвеолярной жидкостью. Сурфактант – эпителий альвеол – интерстиция – эндотелий капилляров – плазма – эритроцит. Газообмен осущ. за счёт диффузии газов через аэрогематический барьер. 1) I этап: перенос гахов по концентрационному градиенту через аэрогематический барьер. 2) II этап: связывание газов в крови лёгочных капилляров.
В легких газообмен осуществляется с помощью диффузии: СО2 выделяется из крови в альвеолы, 02 поступает из альвеол в венозную кровь, пришедшую в легочные капилляры из всех органов и тканей организма. При этом венозная кровь, богатая С02 и бедная 02, превращается в артериальную, насыщенную 02 и обедненную СО2. Газообмен между альвеолами и кровью идет непрерывно, но во время систолы он более активный, чем во время диастолы. Газообмен в альвеолах происходит в результате разности парц. давлений Ро2, и Рсо2 в альвеолярной смеси газов и напряжений этих газов в крови. Парциальное давление газа— это часть общего давления газовой смеси, приходящаяся на долю данного газа. Напряжение газа – величина, характеризующая силу стремления молекул растворённого газа выйти из водной среды в газовую. напряжение газа в жидкости зависит только от парц. давления г  аза над жидкостью, и они равны между собой. Парциальное давление газа в смеси, согласно закону Дальтота, прямо пропорционально его объемному содержанию. Для его расчета необходимо от общего давления газовой смеси вычислить процент, равный содержанию этого газа в смеси. При этом необходимо учесть парциальное давление водяных паров. Так, например, парциальное давление водяных паров в газовой смеси в альвеолах при температуре тела 37 °С составляет 47 мм рт. ст., на долю давления газовой смеси приходится 760 - 47 = 713 мм рт. ст. Поскольку процентное содержание кислорода в альвеолярной смеси равно 14 %, то аза над жидкостью, и они равны между собой. Парциальное давление газа в смеси, согласно закону Дальтота, прямо пропорционально его объемному содержанию. Для его расчета необходимо от общего давления газовой смеси вычислить процент, равный содержанию этого газа в смеси. При этом необходимо учесть парциальное давление водяных паров. Так, например, парциальное давление водяных паров в газовой смеси в альвеолах при температуре тела 37 °С составляет 47 мм рт. ст., на долю давления газовой смеси приходится 760 - 47 = 713 мм рт. ст. Поскольку процентное содержание кислорода в альвеолярной смеси равно 14 %, тоРо2= 713*14 /100 = 99,82 = 100 мм рт.ст. Pо2 и Рсо2 в альвеолах и капиллярах уравниваются. СО2 диффундирует в альвеолы в 20—25 раз быстрее О2 вследствие его лучшей растворимости в жидкости и мембранах. Поэтому обмен С02 в легких происходит достаточно полно, несмотря на небольшой градиент парц. давления этого газа и его напряжения — всего 6 мм рт. ст. (для О2 — до 60 мм рт. ст.). Факторы, способствующие диффузии газов в легких. 1) Огромная поверхность контакта легочных капилляров и альвеол (до 120 м2). Альвеолы - пузырьки d=0,3—0,4 мм, образованные эпителиоцитами. Каждый капилляр контактирует с 5 —7 альвеолами. 2) Большая скорость диффузии газов через тонкую (около 1 мкм) легочную мембрану. Выравнивание Р02 в альвеолах и крови в легких происходит за 0,25 с; кровь находится в капиллярах легких около 0,5 с, т. е. в 2 раза больше. Скорость диффузии С02 в 23 раза больше, чем 02, т. е. имеется высокая степень надежности в процессах газообмена в организме. 3) Интенсивные вентиляция легких и кровообращение. Интенсивность вентиляции различных отделов легких зависит от положения тела: в вертикальном положении лучше вентилируются нижние отделы, в горизонтальном — отделы легких, находящиеся снизу (в положении на спине — дорсальные, на животе — вентральные, на боку — тоже нижней части легких). Это объясняется тем, что отделы легких, находящиеся снизу, сжаты под действием собственного веса, так как они не имеют жесткого каркаса, а отделы легких, находящиеся сверху, растянуты. Поэтому при вдохе нижние отделы легких имеют большую возможность расправляться. Примерно так же изменяется и кровообращение в легких (верхушка легких в положении сидя ниже на 15 %, стоя — на 25 %, чем в средних отделах). Лучшее кровоснабжение легких имеет место в положении лежа на спине, что необходимо учитывать при сердечно-легочной недостаточности. 4) Корреляция между кровотоком в участке легкого и его вентиляцией. Если участок легкого плохо вентилируется, то кровеносные сосуды в этой области суживаются и даже полностью закрываются. Это осуществляется с помощью механизмов местной саморегуляции — посредством реакций гладкой мускулатуры: при снижении в альвеолах Р02 возникает вазоконстрикция. В нормальных условиях у здорового человека активно функционирует примерно 1/7 часть альвеол, эти активно функционирующие участки легких непрерывно меняются. Тот факт, что одновременно функционирует лишь часть альвеол, весьма важен. При поражении части легкого или даже всего легкого и невозможности излечения терапевтическими средствами, одно легкое можно удалить полностью. Оставшееся легкое обеспечит газообмен, достаточный для удовлетворительной жизнедеятельности организма. 2  3. Транспорт кислорода кровью. Кривая диссоциации оксигемоглобина, факторы, влияющие на процесс образования и диссоциации оксигемоглобина. Понятие кислородной емкости крови. 3. Транспорт кислорода кровью. Кривая диссоциации оксигемоглобина, факторы, влияющие на процесс образования и диссоциации оксигемоглобина. Понятие кислородной емкости крови.Практически весь О2 (200 мл/л) переносится кровью в виде хим. соединения с гемоглобином. В физически растворенном состоянии транспортируется только 3 мл/л 02. Свойства гемоглобина — переносчика О2. Этот красный кровяной пигмент в эритроцитах обладает свойством присоединять кислород, когда кровь находится в легком (оксигенация), и отдавать О2, когда кровь проходит по капиллярам всех органов и тканей организма. Гемоглобин – хромопротеид, Mr=64 500 Да, тетрапирольное соединение. Кислород образует обратимую связь с гемом, причем валентность железа не изменяется. При этом восстановленный гемоглобин (Нb) становится окисленным Нb02, точнее, НЬ(02)4. Каждый гем присоединяет по одной молекуле кислорода, поэтому одна молекула гемоглобина связывает четыре молекулы 02. Содержание гемоглобина в крови у мужчин 130— 160 г/л, у женщин 120— 140 г/л. Количество 02, которое может быть связано (КЁК) у мужчин, составляет около 200 мл/л, у женщин оно на 6—8 % меньше. 1 г гемоглобина способен максимально связать 1,34 мл О2. Учитывая, что нормальное содержание гемоглобина составляет 15 г/100 мл, можно рассчитать, что в 100 мл крови максимально может содержаться 20Д мл 02, связанного с гемоглобином. Данная величина называется кислородной емкостью крови (КЕК): КЕК = [НЬ] х 1,34 мл Ог/гНb/100 мл крови. Наиболее важным параметром, определяющим количество кислорода, связанного с гемоглобином, является насыщение гемоглобина кислородом — сатурация (SaO2), который рассчитывают по формуле: 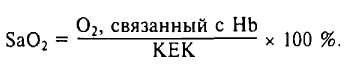 При Рао2, равном 100 мм рт.ст., насыщение гемоглобина кислородом артериальной крови составляе около 97 %. В венозной крови (РО2 = 40 мм рт.ст.) Sa02 приблизительно равна 75 %. Гем может подвергаться не только оксигенации, но и истинному окислению. При этом Fe2+ = Fe3+ - метгемоглобин. В крови человека он содержится в незначительных количествах, но при некоторых заболеваниях, отравлениях определенными ядами, действии некоторых лекарст. его содержание увел. Опасность таких состояний заключается в том, что окисленный Hb очень слабо диссоциирует (не отдает 02 тканям) и, естественно, не может присоединять дополнительно молекулы 02, т. е. он теряет способность переносить кислород. Также опасно соединение гемоглобина с угарным газом (СО) — карбоксигемоглобин, поскольку сродство гемоглобина к СО в 300 раз больше, по сравнению с кислородом, и НЬСО диссоциирует в 10 000 раз медленнее, чем НЬ02. Образование оксигемоглобина происходит в капиллярах легких очень быстро. Время полунасыщения гемоглобина кислородом составляет всего лишь 0,01 с. Главным фактором, обеспечивающим образование оксигемоглобина, является высокое Ро2 в альвеолах (100 мм рт. ст.). При увеличении Ро2 от 40 до 60 мм рт. ст. насыщение достигает 90 %. При возрастании Pо2 свыше 60 мм рт. ст. дальнейшее насыщение гемоглобина идет очень медленно и постепенно приближается к 96 — 98 %, никогда не достигая 100 %. З 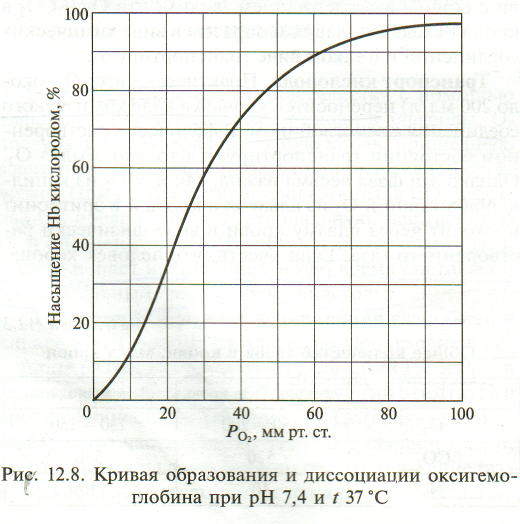 ависимость насыщения гемоглобина О2 от парциального напряжения О2 может быть представлена графически в виде кривой диссоциации оксигемоглобина. Кривая имеет сигмовидную форму, при этом нижняя часть кривой (Рао2<60 мм рт.ст.) имеет крутой наклон, а верхняя часть (Рао2 > 60 мм рт.ст.) относительно пологая. Нижний участок кривой диссоциации оксигемоглобина показывает, что при снижении РаО2 продолжается насыщение гемоглобина кислородом, т.е. ткани продолжают извлекать достаточное количество О2 из крови. Верхняя пологая ависимость насыщения гемоглобина О2 от парциального напряжения О2 может быть представлена графически в виде кривой диссоциации оксигемоглобина. Кривая имеет сигмовидную форму, при этом нижняя часть кривой (Рао2<60 мм рт.ст.) имеет крутой наклон, а верхняя часть (Рао2 > 60 мм рт.ст.) относительно пологая. Нижний участок кривой диссоциации оксигемоглобина показывает, что при снижении РаО2 продолжается насыщение гемоглобина кислородом, т.е. ткани продолжают извлекать достаточное количество О2 из крови. Верхняя пологая |
