сосать лежать. Реферат по физике Носов. Взаимное превращение жидкостей и газов
 Скачать 373.9 Kb. Скачать 373.9 Kb.
|
|
МИНИСТЕРСТВО ОБРАЗОВАНИЯ АРХАНГЕЛЬСКОЙ ОБЛАСТИ государственное бюджетное профессиональное образовательное учреждение Архангельской области «Техникум судостроения и машиностроения» (ГБПОУ АО «Техникум судостроения и машиностроения») РЕФЕРАТ Дисциплина ОУДП.02 «Физика» Тема: «Взаимное превращение жидкостей и газов» Выполнил студент 2 курса группы 223/224 Носов Никита Сергеевич Руководитель Волошина Светлана Борисовна преподаватель физики г. Северодвинск 2022 г. ОГЛАВЛЕНИЕ ВВЕДЕНИЕ 4 1.АГРЕГАТНОЕ СОСТОЯНИЕ 6 Состояние вещества, характеризующееся способностью или неспособностью сохранять объем и форму, наличием или отсутствием дальнего и ближнего порядка называется агрегатным состоянием. 6 Выделим 3 вида агрегатных состояний. 6 газообразное, 6 жидкое, 6 твердое. 6 Газ - не имеет собственного объема и формы. Расстояние между молекулами значительно больше размеров молекул. Силы притяжения между молекулами отсутствуют. 6 Жидкости - сохраняют объем, но изменяют форму. Расстояние между молекулами равно размеру самих молекул. Силы притяжения между молекулами равно размеру самих молекул. 6 Твердое - сохраняет свою форму и объем. Молекулы расположены в определенном порядке, плотно друг к другу. Силы притяжения между молекулами очень велики. 6 Термодинамические процессы перехода вещества из одного состояния в другое, называемые фазовыми переходами, это и есть изменение агрегатного состояния. 6 6 2.ИСПАРЕНИЕ 7 Испарение – это переход из жидкости в газ. При этом это термодинамический процесс, то есть такой, который происходит под воздействием температурных колебаний. Именно вследствие испарения количество любой жидкости в любой незакрытой емкости будет постепенно уменьшаться. 7 С точки зрения молекулярно-кинетической теории, испарение – это процесс, при котором с поверхности жидкости вылетают наиболее быстрые молекулы, кинетическая энергия которых превышает энергию их связи с остальными молекулами жидкости. Это приводит к уменьшению средней кинетической энергии оставшихся молекул, т. е. к охлаждению жидкости. 7 Особенностью испарения является тот факт, что оно может иметь разную направленность тепловых потоков. Они могут идти: 7 из глубины жидкости к поверхности, а затем в воздух, 7 только из жидкости к поверхности, 7 к поверхности из воды и газовой среды одновременно, 7 к площади поверхности только от воздуха. 7 Скорость испарения жидкости зависит от: 7 температуры (чем выше температура жидкости, тем большей скоростью обладают ее молекулы); 7 от площади поверхности испаряющейся жидкости (чем больше площадь поверхности, тем большее число быстрых молекул покидает жидкость); 7 от наличия ветра над поверхностью жидкости. 7 Так как при испарении жидкость покидают наиболее быстрые молекулы, обладающие соответственно большей кинетической энергией, средняя кинетическая энергия молекул жидкости уменьшается, значит температура жидкости при испарении понижается. 8 Испарение является фазовым переходом. При испарении часть жидкости или твердого тела преобразуется в пар. Вещество в газообразном состоянии, которое находится в динамическом равновесии с жидкостью, называется насыщенным паром. При этом изменение внутренней энергии тела равняется: 8 ΔU=±mr, 8 где m – это масса тела, r – это удельная теплота парообразования 8 8 3.КОНДЕНСАЦИЯ 9 Кипение — это интенсивное парообразование, которое происходит при нагревании жидкости не только с поверхности, но и по всему объёму. 12 ЗАКЛЮЧЕНИЕ 14 Переходы вещества из одного агрегатного состояния в другое играют важную роль не только в природе, но и в технике. Так, воду, превращенную в пар, можно использовать в паровых турбинах на электростанциях. Из расплавленных металлов на заводах получают различные сплавы: сталь, чугун, латунь и т. д. Для понимания этих процессов надо знать, что происходит с веществом при изменении его агрегатного состояния и при каких условиях это изменение возможно. 14 СПИСОК ЛИТЕРАТУРЫ 15 ВВЕДЕНИЕ ФИЗИКА - наука о наиболее общих законах природы, материи, о её структуре, движении и правилах. Понятия физики и её законы лежат в основе всего естествознания. Является точной и очень сложной наукой. В физике принято считать, что взаимные превращения жидкостей и газов являются процессом перехода вещества из одного состояния в другое. Жидкостью называют вещество, находящееся в жидком агрегатном состоянии, занимающем промежуточное положение между твердым и газообразным состояниями. А физическое тело, которое в особом состоянии, всегда стремится равномерно заполнить весь внутренний объем пространства, где оно заключено называется газ. 1.АГРЕГАТНОЕ СОСТОЯНИЕ Состояние вещества, характеризующееся способностью или неспособностью сохранять объем и форму, наличием или отсутствием дальнего и ближнего порядка называется агрегатным состоянием. Выделим 3 вида агрегатных состояний. газообразное, жидкое, твердое. Газ - не имеет собственного объема и формы. Расстояние между молекулами значительно больше размеров молекул. Силы притяжения между молекулами отсутствуют. Жидкости - сохраняют объем, но изменяют форму. Расстояние между молекулами равно размеру самих молекул. Силы притяжения между молекулами равно размеру самих молекул. Твердое - сохраняет свою форму и объем. Молекулы расположены в определенном порядке, плотно друг к другу. Силы притяжения между молекулами очень велики. Термодинамические процессы перехода вещества из одного состояния в другое, называемые фазовыми переходами, это и есть изменение агрегатного состояния. 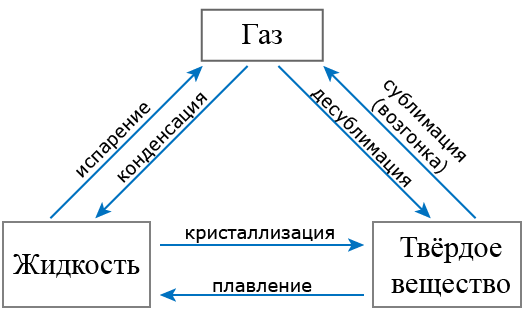 2.ИСПАРЕНИЕ Испарение – это переход из жидкости в газ. При этом это термодинамический процесс, то есть такой, который происходит под воздействием температурных колебаний. Именно вследствие испарения количество любой жидкости в любой незакрытой емкости будет постепенно уменьшаться. С точки зрения молекулярно-кинетической теории, испарение – это процесс, при котором с поверхности жидкости вылетают наиболее быстрые молекулы, кинетическая энергия которых превышает энергию их связи с остальными молекулами жидкости. Это приводит к уменьшению средней кинетической энергии оставшихся молекул, т. е. к охлаждению жидкости. Особенностью испарения является тот факт, что оно может иметь разную направленность тепловых потоков. Они могут идти: из глубины жидкости к поверхности, а затем в воздух, только из жидкости к поверхности, к поверхности из воды и газовой среды одновременно, к площади поверхности только от воздуха. Скорость испарения жидкости зависит от: температуры (чем выше температура жидкости, тем большей скоростью обладают ее молекулы); от площади поверхности испаряющейся жидкости (чем больше площадь поверхности, тем большее число быстрых молекул покидает жидкость); от наличия ветра над поверхностью жидкости. Так как при испарении жидкость покидают наиболее быстрые молекулы, обладающие соответственно большей кинетической энергией, средняя кинетическая энергия молекул жидкости уменьшается, значит температура жидкости при испарении понижается. Испарение является фазовым переходом. При испарении часть жидкости или твердого тела преобразуется в пар. Вещество в газообразном состоянии, которое находится в динамическом равновесии с жидкостью, называется насыщенным паром. При этом изменение внутренней энергии тела равняется: ΔU=±mr, где m – это масса тела, r – это удельная теплота парообразования 3.КОНДЕНСАЦИЯ Конденсацией называется переход вещества из газообразного в жидкое состояние. Молекулы жидкости, покинувшие ее в процессе испарения, находятся в воздухе в состоянии непрерывного теплового движения. Так как движение молекул хаотичное, то какая-то часть молекул вновь попадает в жидкость. Число таких молекул тем больше, чем больше давление пара над жидкостью. Пар конденсируется. Процесс превращения пара в жидкость идет с выделением некоторого количества тепла. Скорость конденсации зависит от: рода жидкости, наличия центров конденсации и от температуры. Температура вещества в процессе конденсации не изменяется. Температура конденсации паров вещества равна температуре кипения этого вещества. Процессы испарения и конденсации в закрытой системе (сосуде): 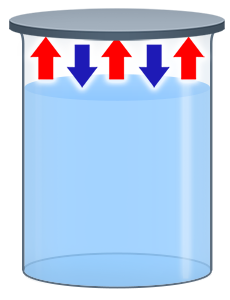 Конденсация может происходить и тогда, когда пар не соприкасается с жидкостью. Именно конденсацией объясняется, например, образование облаков: молекулы водяного пара, поднимающиеся над землей, в более холодных слоях атмосферы группируются в мельчайшие капельки воды, скопления которых и представляют собой облака. Следствием конденсации водяного пара в атмосфере являются также дождь и роса. 4.НАСЫЩЕННЫЙ ПАР Насыщенный пар — это пар, который находится в состоянии динамического равновесия со своей жидкостью.Динамическое равновесие – это состояние при котором число молекул, покидающих поверхность жидкости за некоторый промежуток времени будет равно в среднем числу молекул пара, возвратившихся за то же время в жидкость Пар, не достигший состояния динамического равновесия с жидкостью, называется ненасыщенным. Свойства: при постоянной температуре плотность и давление насыщенного пара не зависит от его объема; при неизменном объеме плотность насыщенного пара растет с повышением температуры и уменьшается с понижением температуры; давление насыщенного пара растет с температурой быстрее, чем по линейному закону. Давление и плотность насыщенного пара — это максимальные давление и плотность, которые может иметь пар при данной температуре. Иными словами, давление и плотность насыщенного пара всегда превышают давление и плотность ненасыщенного пара. 5.НЕНАСЫЩЕННЫЙ ПАР Если в пространстве, содержащем пары какой-либо жидкости, может происходить дальнейшее испарение этой жидкости, то пар, находящийся в этом пространстве, является ненасыщенным. Пар, не находящийся в состоянии равновесия со своей жидкостью, называется ненасыщенным. Ненасыщенный пар можно простым сжатием превратить в жидкость. Как только это превращение началось, пар, находящийся в равновесии с жидкостью, становится насыщенным.  При уменьшении объема давление ненасыщенного пара увеличивается (участок 1—2) подобно тому, как изменяется давление при уменьшении объема идеального газа. При определенном объеме пар становится насыщенным, и при дальнейшем его сжатии происходит превращение его в жидкость (участок 2—3). В этом случае над жидкостью уже будет находиться насыщенный пар. Как только весь пар превратится в жидкость, дальнейшее уменьшение объема вызовет резкое увеличение давления (жидкость малосжимаемая). Однако пар превращается в жидкость не при любой температуре. Если температура выше некоторого значения, то, как бы мы ни сжимали газ, он никогда не превратится в жидкость. 6.КИПЕНИЕ Кипение — это интенсивное парообразование, которое происходит при нагревании жидкости не только с поверхности, но и по всему объёму. Кипение от начала до конца происходит при определенной и постоянной для каждой жидкости температуре. Температура кипения зависит от внешнего давления. Чем больше внешнее давление, тем выше температура кипения. Кипение начинается при температуре, при которой давление насыщенного пара в пузырьках сравнивается и становится чуть больше давления в жидкости. Пример кипения: в воде растворены молекулы воздуха (газов). При нагревании этот растворенный газ выделяется в виде воздушных пузырьков на дне и стенках сосуда.  С повышением температуры жидкости внутри этих пузырьков испаряется вода, они увеличиваются в размерах. Достигнув определённого размера, пузырьки отрываются от поверхности. Если вода прогрета недостаточно, то пузырьки пара в холодных слоях схлопываются. А если температура достаточная, то они достигают поверхности воздуха или жидкости и лопаются, выпуская пар. В этот момент слышен шум, предшествующий обычно кипению. При определённой температуре вода закипает. Температуру, при которой жидкость кипит, называют температурой кипения. Вовремя кипения температура жидкости не изменяется, так как вся энергия расходуется на парообразование. Температура кипения жидкости зависит от двух факторов: от рода жидкости; от внешнего давления.  При уменьшении давления воздушным пузырькам легче всплывать, кипение происходит при меньшей температуре. Именно поэтому высоко в горах (на высотах 6000 — 8000 м) не варят суп или мясо, а пользуются готовыми консервами, т.к. температура кипения воды меньше 100 °С. ЗАКЛЮЧЕНИЕ Переходы вещества из одного агрегатного состояния в другое играют важную роль не только в природе, но и в технике. Так, воду, превращенную в пар, можно использовать в паровых турбинах на электростанциях. Из расплавленных металлов на заводах получают различные сплавы: сталь, чугун, латунь и т. д. Для понимания этих процессов надо знать, что происходит с веществом при изменении его агрегатного состояния и при каких условиях это изменение возможно. СПИСОК ЛИТЕРАТУРЫ Физика: учебник для 10 кл. общеобразоват. Учреждений Г. Я. Мякишев, Б. Б. Буховцев, Н. Н. Сотский. 2006 год https://ru.wikipedia.org/wiki/ https://resh.edu.ru/subject/lesson/4740/conspect/15519/ |
