Задача Подавляющее большинство протеиногенных аминокислот дают синее окрашивание с нингидрином, а пролин и оксипролин желтое. Объясните это различие, принимая во внимание химизм нингидриновой пробы и особенности структуры протеиногенных аминокислот.
 Скачать 2.68 Mb. Скачать 2.68 Mb.
|
Задача 11.Фермент (10мкг) с молекулярной массой 500.000 г/моль превращает 9,6 мкмоль субстрата в минуту при температуре 25С. Подсчитайте число оборотов. Ответ. Молярная активность (число оборотов фермента) – количество молекул субстрата, которое превращается в продукт одной молекулой фермента (при полном насыщении субстратом) за единицу времени. 9,6/60:10/50000=800сек-1 Задача 12.Сколько граммов субстрата с молекулярной массой 672 г/моль может преобразовать фермент, если его активность составляет 5 нКат, а время инкубации – 20 сек. Ответ. 6721011 г. Задача 13.
Проанализируйте данные экспериментов по определению скорости ферментативной реакции при различных концентрациях субстрата, а также в присутствии ингибитора. По имеющимся данным, представленным в таблице, постройте график Лайнуивера–Берка, определите Кm фермента и тип ингибирования. Ответ: 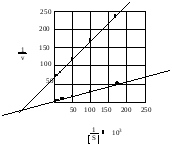 График Лайнуивера-Берка – график двойных обратных величин ( 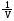 против против 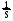 ). ).Отрезок на горизонтальной оси = -1/Кm Отрезок на вертикальной оси = 1/Vmax Тип ингибирования неконкурентный, т.к. в присутствии ингибитора Кm (т.е. сродство фермента к субстрату ) не изменилась. Задача 14. Проанализируте графики Михаэлиса-Ментен и Лайнуивера-Берка. Отметьте Кm, Vmax и определите тип ингибирования: 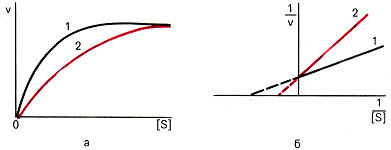 Ответ: 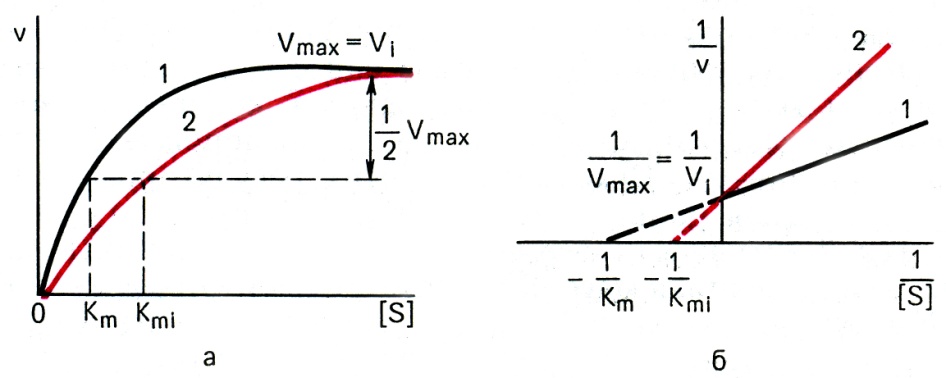 Отрезок на оси абсцисс = Кm (график Михаэлиса-Ментен) или-1/Кm (график Лайнуивера-Берка). Отрезок на оси ординат = Vmax или 1/Vmax соответственно. В присутствии ингибитора Кm увеличилась (т.е. сродство фермента к субстрату снизилось), а Vmax не изменилась. Следовательно, тип ингибирования конкурентный. Задача 15. В процессе подготовки животных к зимней спячке изменяется фосфолипидный бислой мембран. Эти изменения выражаются в первую очередь в увеличении содержания ненасыщенных жирных кислот в составе фосфолипидов.Как увеличение полиненасыщенных жирных кислот влияет на структуру бислоя при понижении температуры? Какие преимущества для метаболизма приносит такое изменение жирнокислотного состава и фосфолипидов? Ответ: Ненасыщенные жирные кислоты имеют более низкую температуру плавления, т.е. они находятся в жидком состоянии при более низких температурах, вследствие этого более подвержены катаболизму, лучше растворяются в липидах и выполняют роль разобщителей тканевого дыхания и окисления. Последнее необходимо для согревания тела. Задача 16. Известно, что в мембранах бактерий часто встречаются окси- и циклопропансодержащие жирные кислоты, а в мембранах термоацидофильных, метанобразующих архебактерий – нетипичные липиды, содержащие изопреноидные цепи, метильные концы которых соединены ковалентными связями. Сравните с составом липидов мембран животных клеток, объясните, насколько целесообразно такое строение. Ответ: В мембранах бактерий отсутствует холестерин, который обеспечивает прочность внешней мембране эукариотической клетки. Изопреноидные цепи нетипичных липидов бактерий своими концами ковалентно связываются и обеспечивают повышенную прочность липидного бислоя. В составе сложных липидов бактерий отсутствют ненасыщенные жирные кислоты, но имеются разветвленные и циклопропансодержащие жирные кислоты, при этом температура фазового перехода « кристалл – жидкий кристалл» увеличивается, а упаковка становится более рыхлой, что позволяет бактериям существовать в широком диапазоне температур и обеспечивать обмен крупными молекулами со средой обитания. Задача 17. В лечении больного запланировано воздействие на метаболизм через аденилатциклазную систему. Какое воздействие оказывают на нее различные гормоны? Ответ: Воздействие на метаболизм клетки через аденилатциклазную систему оказывают многие гормоны нестероидного ряда. Активируют аденилатциклазу: адреналин, норадреналин, глюкагон, АКТГ, тироксин, подавляют: простагландины, инсулин. Задача 18. Эстрогены – гормоны стероидной природы, используются для гормонзаместительной терапии при угасании функции яичников, а также при остеопорозе, атеросклерозе и других заболеваниях у женщин. Однако, при длительном и бесконтрольном их применении возможно развитие онкологических заболеваний – рака матки и молочных желез. Объясните механизм действия стероидных гормонов на органы-мишени. Ответ: Цитозольные рецепторы эстрогенов находятся в клетках матки, молочных желез, печени, костной ткани , сердце , сосудах и головном мозге. Комплекс цитозольный рецептор – эстроген проникает через ядерную мембрану и усиливает процесс транскрипции мРНК. Вслед за этим усиливается синтез белков в гормонкомпетентных клетках (анаболический эффект гормона). Риск развития рака молочной железы и матки при монотерапии эстрогенами возрастает в 4-6 раз. Задача 19. Больной жалуется на неутолимую жажду, употребление большого объёма жидкости, значительное количество мочи (6–8 л в сутки). При обследовании найдено: глюкозы в крови 5,2 ммоль/л, кетоновых тел нет. Моча бесцветная, плотность 1,002, сахара нет. Назовите возможные причины полиурии (большого количества мочи). Ответ: Полиурия, низкая плотность мочи, отсутствие гипергликемии и глюкозурии позволяют предполагать несахарный диабет. Его причиной является дефицит вазопрессина (антидиуретического гормона). Задача 20. У больного, страдающего тиреотоксикозом, удалена одна доля щитовидной железы. После операции симптомы тиреотоксикоза исчезли, но появились судорожные сокращения мышц лица и конечностей. Почему? Ответ: Во время операции вместе с долей щитовидной железы были удалены паращитовидные железы, в которых вырабатывается паратгормон. Он способствует повышению содержания кальция в крови за счет резорбции (вымывания) его из костной ткани и повышени реабсорбции из первичной мочи в почках, увеличивает выведение с мочой фосфата. Удаление паращитовидных желез снизило выработку паратгормона, уровень кальция в крови понизился, появились судороги. Задача 21. Пациент жалуется на сильную слабость, повышенную утомляемость. Часто бывают явления гипогликемии. Усилена пигментация кожи. Имеется анемия, лимфоцитоз, эозинофилия. Уменьшена реабсорбция натрия из мочи. О недостаточности каких гормонов можно думать? Ответ: Высокая утомляемость, частые гипогликемические состояния, повышенная пигментация кожных покровов и др. симптомы характерны для первичной хронической недостаточности коры надпочечников (болезни Аддисона). Задача 22. О недостаточности каких гормонов может свидетельствовать обнаружение у больного устойчивого повышения экскреции с мочой ионов натрия и хлора? Ответ: Уровень натрия и калия в крови и моче регулируется минералкортикоидами. Основным минералкортикоидом в организме человека является альдостерон. Он стимулирует реабсорбцию натрия и выведение калия. Задача 23. С пищей в организм ребенка поступило 80г белка в сутки. С мочой за это же время выделилось 16 г азота. Каков азотистый баланс у ребенка, о чем он свидетельствует? Ответ: Вспомним, что азотистый баланс– это соотношение азота, поступившего в организм с пищей (N1) и азота, выделенного из организма за сутки (N2). Если N1=N2 , то это азотистое равновесие, которое характерно для здорового взрослого человека. ЕслиN1>N2 , то это положительный азотистый баланс, который характерен для детей, беременных женщин, в период выздоровления. Если N1 Известно, что в 100 г белка содержится 16 г N, а из условия задачи известно, что с пищей в организм ребенка поступило 80г белка. На основании этого мы можем составить следующую пропорцию: 100 г белка – 16 г N 80 г белка – Х Х = 12,8 г Следовательно, при N1=N2 с мочой должно выделяться 12,8 г азота. Но т.к. это ребенок, то у него в норме должно быть N1>N2. Из условия задачи известно, что его N2=16 г, т.е. N1 Задача 24. Сколько липидов растительного и животного происхождения должен содержать рацион человека, если энерготраты составляют 3500 ккал, а на долю энерготрат, обеспечиваемых липидами, приходится 22% всей необходимой энергии? Ответ: Для решения задачи необходимо: а) найти количество энергии, продукцию которого должны обеспечить липиды: 3500 ккал – 100% Хккал – 22 % Х=770 ккал; б) найти количество липидов, которое обеспечит высвобождение 770 ккал: 1г – 9,3 ккал Х–770 ккал Х = 82,8г; в) известно, что рацион должен содержать 2/3 животного и 1/3 растительного жира, поэтому соответствующие доли от 82,8 г составят 55,2 г и 27,6 г. Задача 25. Препараты витамина К (викасол) используются в медицине как антигеморрагические средства. Эффективны ли они для остановки кровотечения, или могут применяться только как средства, предупреждающие кровотечения? Ответ: Препараты витамина К используются как средства, предупреждающие кровотечения, поскольку витамин К относится к непрямым коагулянтам, участвующим в образовании в печени факторов свертывания II, VII,IX X. Участие заключается в -карбоксилировании остатков глутаминовой кислоты в ходе постсинтетического «дозревания» белков свертывания крови. Дополнительная карбоксильная группа необходима для взаимодействия с ионами Са++ (факторы II, VII, IX, X являются Са++-зависимыми). Задача 26. Отмечено, что у некоторых больных с хроническими заболеваниями почек развивается остеомаляция. Объясните механизм возникновения так называемого ренального рахита. Эффективно ли в этом случае назначение препаратов витамина D? Ответ: В основе ренального рахита лежит снижение способности вырабатывать активную форму витамина Д3 – 1,25-диоксихолекальциферол [1,25(ОН)2D3], так как 1α-гидроксилирование протекает именно в ткани почек. Наиболее эффективным в данном случае является применение не самого холекальциферола, а его активного метаболита – [1,25(ОН)2D3]. Задача 27.Ацетильный остаток, меченный 14С по обоим углеродным атомам (14СН314СОКоА), окисляется в цикле лимонной кислоты. Проследите судьбу радиоактивной метки. Определите, в каком соединении будет обнаруживаться 14С после первого оборота цикла. В ходе какого оборота ЦТК будет выделяться 14СО2? Ответ: В результате альдольной конденсации щавелевоуксусной кислоты и меченого по указанным положениям ацетила образуется лимонная кислота со следующим распределением радиоактивной метки  Углеродные атомы, имеющие происхождение из меченого ацетила, в ходе первого оборота цикла окисляться не будут, поэтому радиоактивная метка будет обнаруживаться в центральных атомах регенерированного ЩУК (НООС-14СН214СО-СООН). В ходе второго оборота, после конденсации ацетила и меченого ЩУК, будет образовываться лимонная кислота:  поэтому, в ходе второго оборота меченые углероды окислительному декарбоксилированию подвергаться не будут и выделится ЩУК со следующим распределением радиоактивной метки НООС-СН214СО-14СООН. Таким образом, 14СО2 будет выделяться в ходе третьего оборота цикла. Задача 28. Бактерии, обитающие в корневых клубеньках растения гороха, потребляют свыше 20% всего АТФ, образуемого этим растением. Назовите причину, которой можно было бы объяснить, почему эти бактерии потребляют так много АТФ. Ответ: Бактерии в корневых клубеньках находятся в симбиозе с растением: растение поставляет АТФ и восстановительные эквиваленты, а бактерии-ионы аммония, получаемые путем восстановления атмосферного азота. На это восстановление затрачивается большое количество АТФ. Поэтому эти бактерии и потребляют так много АТФ. Задача 28. Подсчитайте количество АТФ, которое теоретически может образоваться при окислении янтарной кислоты до щавелевоуксусной при условии, что митохондрии не разобщены. Ответ: Окисление сукцината до оксалоацетата сопровождается восстановлением одной молекулы ФАД и одной молекулы НАД. Последующее окисление ФАДН2 в дыхательной цепи сопряжено образованием 2 молекул АТФ (Р/О2), а окисление НАДН+H+ 3 молекул (Р/О3). Следовательно, энергетический выход окисления сукцината до яблочной кислоты 5 молекул АТФ. Задача 30. В эксперименте с изолированными митохондриями в качестве субстрата дыхания используется изоцитрат. Определите: а) коэффициент Р/О; б) коэффициент Р/О при одновременном присутствии в среде сукцината и амитала натрия; в) как изменится коэффициент Р/О при добавлении к среде тиреоидных гормонов? Ответ: Изолимонная кислота окисляется НАД-зависимой дегидрогеназой, следовательно, коэффициент Р/О будет близок к 3. В присутствии в среде амитала (производное барбитуровой кислоты) передача электронов от изоцитратдегидрогеназы будет заблокирована и дыхание будет поддерживаться за счет окисления сукцината. Сукцинатдегидрогеназа - ФАД зависимый фермент, передает электроны непосредственно на Ко Q, следовательно, коэффициент Р/О составит 2. Тиреоидные гормоны обладают свойством разобщать окисление и фосфорилирование, поэтому в их присутствии коэффициент Р/О будет снижаться (3). Задача 31. Фотосинтез протекает в клетках растений, водорослей и фототрофных бактерий. У большинства из них фотосинтез сопровождается использованием в качестве доноров электронов Н2О и выделением О2. И только у аноксигенных бактерий Anoxyphotobacteria, вместо Н2О роль доноров ē могут выполнять некоторые восстановленные соединения, например, Н2S. Что при этом образуется? Ответ: При этом образуется сера: СО2 + 2Н2S → (СН2О) + Н2О + 2S Задача 32. С4-путь (цикл Хетча-Слэка-Карпилова), отличается присутствием дополнительной начальной стадии – фиксации СО2 в составе оксалоацетата (4С). Эту реакцию катализирует ФЕП-карбоксилаза - более активный фермент, чем рибулозо-дифосфат-карбоксилаза. Но этот путь требует дополнительных стадий и затрат энергии: на фиксацию 1 СО2 затрачивается 5АТФ вместо 3-х в С3-пути. Однако С4-растения (кукуруза, сахарный тростник, сорго, многие сорняки) растут гораздо быстрее, чем С3-растения (пшеница, рожь, овес, рис и др.). Объясните почему? Ответ: Причина в фотодыхании – расточительном процессе, характерном только для С3-растений. Это происходит за счет оксигеназной активности рибулозодифосфаткарбоксилазы. О2 конкурирует с СО2 за активный центр карбоксилазы, в результате чего часть рибулозодифосфата превращается в фосфогликолат. Этого не происходит у С4-растений, т.к. большинство из них произошли из тропических стран, где высокое испарение влаги заставило выработать механизм закрывания устьиц, через которые ткани вентилируются газами в самые жаркие часы дня (при максимальном солнечном освещении). С4-растения запасают СО2 в составе малата или аспартата (образуются из ЩУК в цикле Хетча-Слэка-Карпилова), а затем расходуют по мере надобности. В этом случае концентрация СО2 всегда высокая и отсутствует конкуренция с О2, т.к. он поступает в клетки в ограниченном количестве при закрывании устьиц. Задача 33. Известно, что помимо таких углеводов как крахмал, сахароза, лактоза пища должна содержать группу полисахаридов, объединяемых в группу так называемых балластных веществ или пищевых волокон. Какие полисахариды входят в эту группу? Каково их значение для нормального питания? Ответ: Желудочно-кишечный тракт не содержит ферментов, способных расщеплять такие полисахариды как целлюлоза (клетчатка) и инулин . В то же время не перевариваемые углеводы - основной компонент пищевых волокон - необходимый компонент питания, поскольку они стимулируют моторику ЖКТ, ускоряют развитие чувства насыщения, способны адсорбировать холестерин, некоторые токсические вещества. К пищевым волокнам относится также лигнин – сложный полимер, состоящий из фенилпропаноидных единиц, а также пектиновые вещества и альгиновые кислоты, обладающие желеобразующими свойствами. Рекомендуемое потребление пищевых волокон составляет 25 г в день для женщин и 38 г – для мужчин. Химическая структура некоторых полисахаридов, относящихся к группе пищевых волокон. Целлюлоза – полимер, состоящий из D – глюкопиранозных остатков, соединенных β (1→4) гликозидными связями: 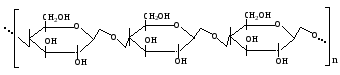 Мr от 400 000 до 1-2 млн Мr от 400 000 до 1-2 млн Инулин – полисахарид, накапливающийся в клубнях растений, состоит из D – фруктофуранозных звеньев, соединенных β (1→2) связями Пектиновые вещества – растительные полисахариды производные пектовой (полигалактуроновой) кислоты: 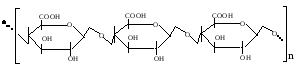 Альгиновые кислоты – полисахариды бурых водорослей, состоящие из остатков D – маннуроновой и D - гулуроновой кислот, связанных β (1→4) гликозидными связями. Задача 34. На включении одного остатка глюкозы в структуру гликогена затрачивается 2 макроэргические связи – 2 молекулы АТФ. И все же, почему, несмотря на «затратность» биосинтеза гликогена, главное клеточное топливо хранится в виде полисахарида, а не в форме свободной глюкозы? Чем объясняется большая разветвленность гликогена, по сравнению с запасным полисахаридом растений – крахмалом? Ответ: 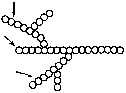 (стрелками указаны точки действия гликогенфосфорилазы) Глюкоза растворима в воде, следовательно, обладает осмотическими свойствами. Свободная глюкоза в количествах, равноценных количеству гликогена, приводила бы к осмотическому шоку – лизису клеток. Большая разветвленность гликогена объясняется механизмом его мобилизации. Гликогенфосфорилаза отщепляет путем фосфоролиза концевые нередуцирующие остатки глюкозы. Следовательно, большая разветвленность обеспечивает более быстрый приток глюкозы – главного энергетического субстрата. Задача 35. Л. Пастер – французский химик и микробиолог IXX века впервые описал следующий феномен: в отсутствии кислорода ткани, способные окислять глюкозу, утилизируют ее гораздо быстрее, чем при достаточном парциальном давлении О2. Объясните механизм этого явления, обозначаемого ныне как эффект Пастера, или ингибирование гликолиза тканевым дыханием. Ответ: Эффект Пастера объясняется гораздо меньшей эффективностью анаэробного распада глюкозы – гликолиза, который в анаэробных условиях является единственным источником АТФ. Энергетический выход гликолиза составляет всего 2 моля АТФ на моль глюкозы, тогда как аэробное окисление даст 36 молекул АТФ на 1 молекулу глюкозы. Таким образом, в анаэробных условиях больше глюкозы должно окисляться, чтобы обеспечить энергетические потребности клеток. Задача 36. Алкогольная интоксикация сопровождается гипогликемией и повышенным содержанием лактата в крови. Чем объясняются эти метаболические нарушения при действии алкоголя? Ответ: Примерно 90% принятого алкоголя метаболизируется в печени НАД – зависимым ферментом алкогольдегидрогеназой:  Для окисления 125 г этилового спирта требуется столько же НАД+, сколько и для окисления 500 г глюкозы, поэтому, после приема алкоголя соотношение [НАД+]/ [НАДН+Н+] резко снижается вследствие значительного увеличения концентрации восстановленной формы кофермента. Это ведет к смещению лактатдегидрогеназной реакции в сторону образования лактата: пируват + НАДН+Н+ лактат +НАД + Пируват – один из главных субстратов глюконеогенеза, поэтому снижение его концентрации резко замедляет скорость синтеза глюкозы, что является причиной гипогликемии. Задача 37. Установлено, что при обычном питании фруктоза обеспечивает примерно 10% энергетической ценности пищи. Особенно богаты этим моносахаридом фрукты и мед. Фруктоза отличается от глюкозы гораздо большей скоростью окисления, даже у больных сахарным диабетом фруктоза выводится из крови с такой же скоростью, как и у здоровых лиц. Объясните, почему фруктоза метаболизируется быстрее, чем глюкоза? Ответ: В ткани печени фруктоза «вливается» в гликолиз на уровне триозфосфатов:  Таким образом, фруктоза «обходит» две регуляторные, медленные реакции гликолиза – гексокиназную и фруктокиназную, поэтому окисляется значительно быстрее. Равная скорость выведения фруктозы у больных сахарным диабетом и здоровых объясняется тем, что транспорт фруктозы в клетки не зависит от инсулина. Инсулин также не влияет на активность фруктокиназы, «запускающей» метаболизм фруктозы. Задача 38. Являются ли инсулин и адреналин в управлении углеводным обменом в печени антагонистами или синергистами? Имеет место косвенное или прямое взаимодействие? Ответ: Инсулин ускоряет переход глюкозы из крови в клетки и ее превращение по основному пути. Адреналин ускоряет выход глюкозы из депо в печени, где она находится в форме гликогена. В этом случае гормоны действуют в одном направлении, хотя и на разных этапах обмена глюкозы. С другой стороны, инсулин угнетает глюконеогенез и активирует образование гликогена. Синергизм в первом и антагонизм во втором случаях являются косвенными – гормоны влияют на один процесс разными путями. Задача 39. Для определения количества липидов в суточном рационе необходимо произвести их экстрагирование. С помощью каких веществ можно это сделать? Ответ: Липиды очень разнообразны по своему строению, общим для них является растворение в органических растворителях, таких как хлороформ, ацетон, эфир и др. Эти вещества можно использовать для экстрагирования жира. Задача 40. В результате плохого хранения сливочного масла вкус его ухудшился. Какие процессы обусловливают прогоркание масла? Как можно количественно оценить качество масла? Ответ: Качество и вкус масла определяются содержанием в нем витаминов, пигментов и свободных жирных кислот, особенно таких как масляная, валериановая, пропионовая и др., имеющие неприятный запах и вкус. Содержание последних возрастает при гидролизе жира, интенсивность которого зависит от условий хранения. Количество жирных кислот определяется т.н. «кислотным числом», которое устанавливается стандартом. Задача 41. У пациентов со сниженной секрецией бикарбонатов поджелудочной железой даже при нормальной продукции липазы и колипазы развивается стеаторея - выделение непереваренного жира с калом. Чем объясняется стеаторея у больных со сниженной секрецией бикарбонатов? Ответ: Панкреатическая липаза активна в пределах рН от 6-8. Бикарбонаты способствуют нейтрализации кислотной пищевой кашицы, поступающей из желудка в тонкий кишечник. Кроме того, смещение рН в щелочную сторону способствует ионизации желчных кислот, а следовательно усиливает их амфифильность и эмульгирующие свойства.Недостаточность бикарбонатов приводит к снижению расщепления жира. Задача 42. Два взрослых здоровых человека (А и Б) за один прием пищи получили (в граммах):
Как изменится липопротеиновый спектр плазмы крови испытуемых через 2,5 часа после еды? Ответ: В плазме крови испытуемого А наиболее значительно будет увеличено содержание ЛПОНП – частиц, ответственных за транспорт эндогенных, т.е. синтезированных in vivo липидов (главным образом триацилглицеринов) из печени в периферические ткани. Строение липопротеиновой частицы плазмы крови: 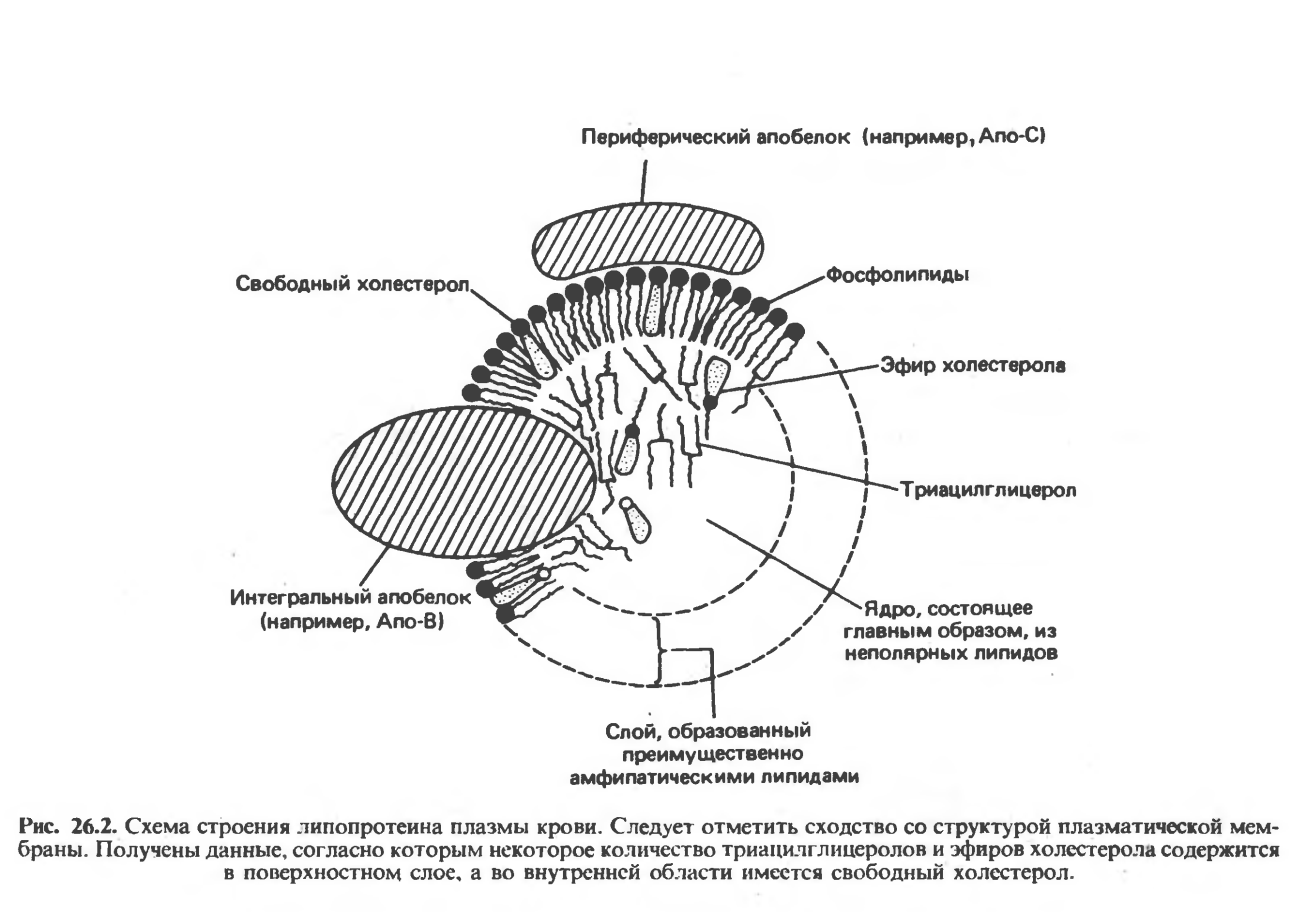 Большая доза принятых углеводов (почти соответствующая суточной потребности – 400 г) будет активно включаться в липогенез. Образующиеся в ткани печени триглицериды разносятся в эктрагепатические ткани в составе ЛПОНП. В плазме крови испытуемого Б будет так же увеличена концентрация ЛПОНП (по тем же причинам), а также концентрация хиломикронов, т.к. последние ответственны за транспорт экзогенных, т.е. принятых с пищей триглицеридов. Функция плазменных липопротеинов – транспорт гидрофобных липидов в гидрофильной среде плазмы крови. Задача 43. Больные с наследственным дефектом ацил – СоА- дегидрогеназы страдают от приступов гипогликемии и гипокетонемии, которые случаются после 6-7 часового голодания. Объясните происхождение этих симптомов у больных. Ответ: Митохондриальный фермент ацил- КоА-дегидрогеназа запускает процесс β-окисления жирных кислот: 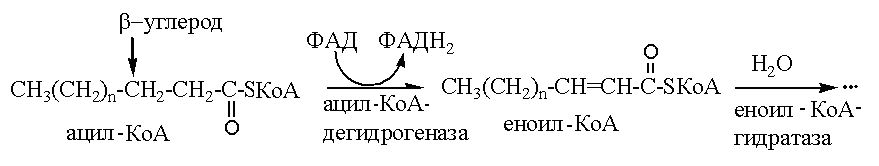 Поэтому у больных с наследственным дефектом ацил- КоА- дегидрогеназы процесс β-окисления жирных кислот нарушен. Снижение утилизации жирных кислот - основного источника энергии при голодании – ведет к повышенному использованию глюкозы. Вследствие этого у таких больных быстро развивается гипогликемия. Снижение синтеза кетоновых тел объясняется уменьшением концентрации ацетил-КоА - конечного продукта β- окисления и исходного продукта для синтеза кетоновых тел. Задача 44. Рассчитайте количество АТФ, которое может образоваться при полном окислении тристеарина. Ответ: Тристеарин представляет по химической природе простой триглицерид, при гидролизе которого образуется одна молекула глицерола и три остатка стеариновой кислоты. При полном окислении глицерола образуется 19 молекул АТФ. Стеариновая кислота является насыщенной жирной кислотой следующего строения С17Н35СООН..Рассчитать количество АТФ, образующееся при полном окислении одного моля стеариновой кислоты можно по формуле А = 17 ( n : 2) – 6, где А- количество АТФ, n – число атомов углерода в жирной кислоте. Итого: 147·3=441; 441 + 19 =460 АТФ. Задача 45. Потребление жира рыб северных морей рекомендуется больным с гиперхолестеринемией и повышенным риском тромбообразования. Объясните действие такой диеты. Ответ: Морская рыба богата длинноцепочными полиненасыщенными жирными кислотами семейства ω – 3. Обозначение омега –3 указывает на то, что первая двойная связь расположена у С3 при отсчете углеродных атомов от концевой метильной группы. Представителем ω – 3 семейства является эйкозопентаеновая кислота (20:5, Δ 3,6,9,12,15) 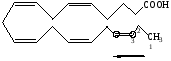 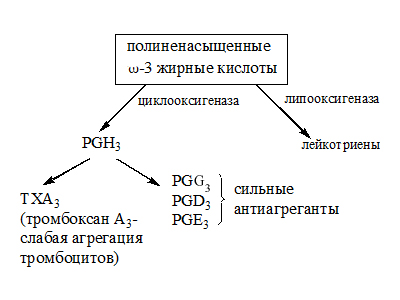 Жирные кислоты семейства ω-3 являются предшественником биологически активных соединений – эйкозаноидов, и в частности, простагландина G3 (PGG3) или простациклина, который является мощным ингибитором агрегации тромбоцитов Полиненасыщенные жирные кислоты положительно влияют на жидко-кристалическое состояние биомембран. Благодаря цис – конфигурации двойных связей, молекулы указанных жирных кислот «изломаны», что увеличивает «текучесть» биомембран. 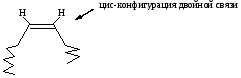 Задача 46. Каковы различия в обмене холестерина у вегетарианцев и людей, рационы которых включает много мяса, молока, яиц? Для ответа: А. напишите схему синтеза холестерина Б. напишите схему регуляции холестерина В. объясните происхождение субстратов для синтеза холестерола. Г. Объясните какова роль ЛПОНП, ЛПНП, и ЛПВП в транспорте холестерола. Ответ: 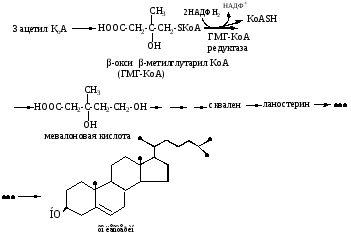
Конечный продукт – холестерин является аллостерическим ингибитором ключевого фермента – ГМГ- КоА – редуктазы
ЛПВП, образуемые в плазме крови и содержащие преимущественно эфиры холестерина можно считать переносчиками холестерина из периферических тканей (и других липопротеинов) в печень, где холестерин метаболизируется и частично выделяется в составе желчи. Благодаря высокому содержанию в ЛПВП фермента ЛХАТ холестерин этерифицируется и «прячется» в гидрофобном ядре этих частиц, освобождая место для новых молекул холестерина. Таким образом, ЛПВП работают как своеобразные «мусорщики», извлекающие излишки холестерина из периферических тканей и других липопротеидных частиц. При содержании 2-3 г холестерина в суточной пище синтез эндогенного холестерина почти полностью прекращается. Богаты холестерином такие продукты как жирное мясо, яйца, молоко. При питании растительной пищей, в которой холестерина мало, главное значение имеет биосинтез эндогенного холестерина (in vivo). Задача 47. Здоровых взрослых крыс длительное время содержали на искусственной белковой диете, исключающей метионин и лизин. Как изменится у этих животных азотистый баланс? Поясните ответ. Ответ: Фонд свободных аминокислот организма наполняется из трех источников – белков пищи, белков собственных тканей и за счет синтеза из углеводов и кетоновых тел. Последний пункт справедлив только в отношении заменимых аминокислот. Метионин и лизин относятся к незаменимым аминокислотам, т.е. аминокислотам, которые не могут быть синтезированы в организме. Если отсутствует хотя бы одна из неземенимых аминокислот, синтез белка прекращается, поэтому в условиях, когда пища не содержит какую-либо незаменимую аминокислоту (или аминокислоты), их единственным источником становятся белки собственных тканей, распад тканевых белков усиливается, что приводит к развитию отрицательного азотистого баланса. 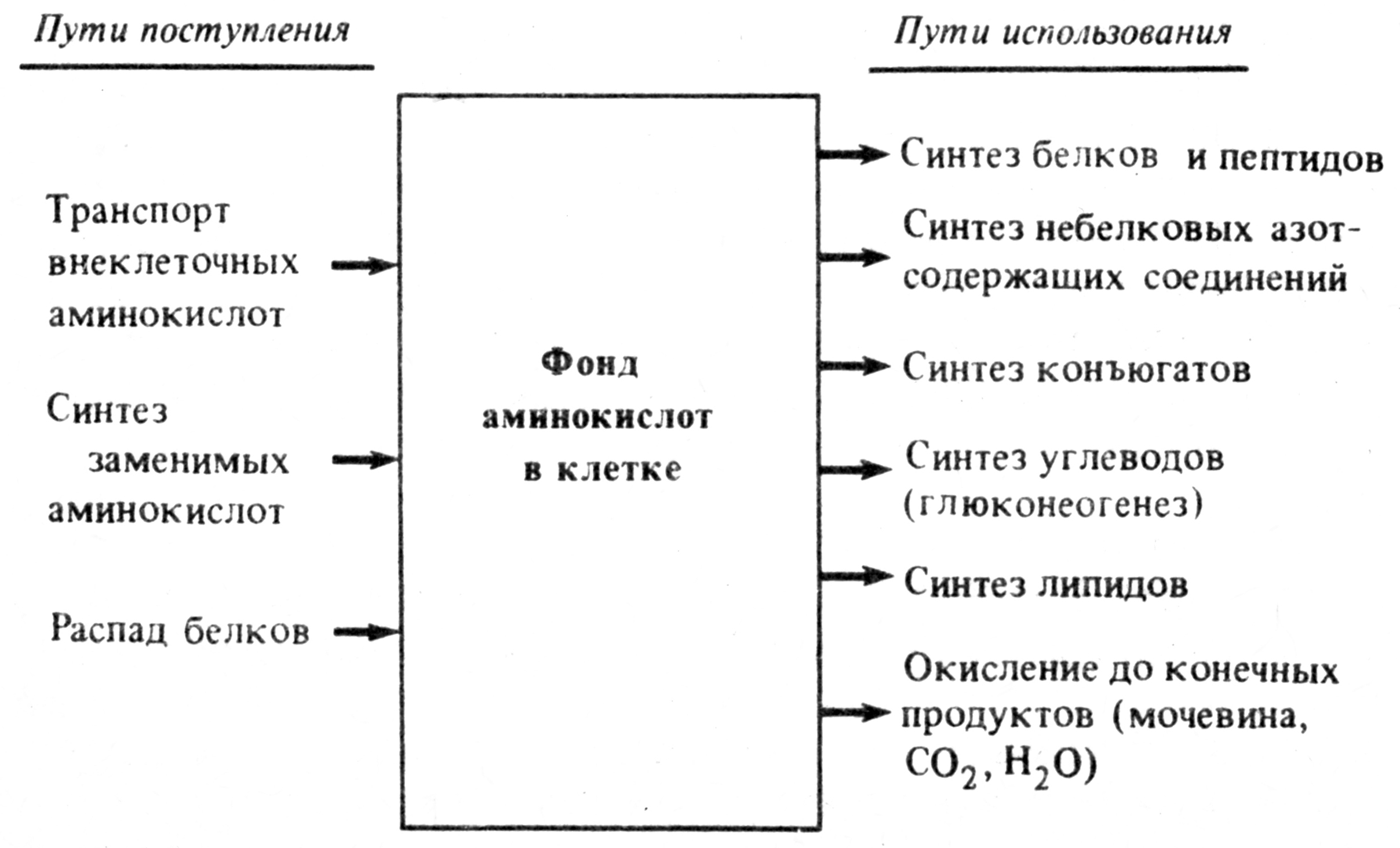 Задача 48. Подпишите протеолитические ферменты желудочно-кишечного тракта, способные принять участие в протеолизе пептидов: 1. тир-вал-тир-лиз-ала-ала-фен-арг-асп-асп-три-ала-сер-мет-фен-арг 2. ала-лиз-лей-глу-тир-ала-ала-асп-три-мет-фен-глу-асп-три-иле-гли Укажите специфичность их действия. Ответ: 1. тир-вал-тир-лиз-ала-ала-фен-арг-асп-асп-три-ала-сер-мет-фен-арг 6b 1 4 3 1 1 4 3 2 1 4 1 1 5b ↓ сер-мет 7 2. ала-лиз-лей-глу-тир-ала-ала-асп-три-мет-фен-глу-асп-три-иле-гли 6а 3 1 1 4 1 1 4 1 4 2 1 4 5а ↓ ала-асп 7 1 – пепсин (расщепляет пептидные связи: Х-фен, Х-тир, Х-три, ала-ала, ала-сер, лей-глу) 2 – гастриксин (расщепляет пептидные связи, образуемые дикарбоновыми АК) 3 – трипсин (расщепляет пептидные связи: арг-Х; лиз-Х) 4 – химотрипсин (расщепляет связи: фен-Х; тир-Х; три-Х) 5а – карбоксипептидаза А (отщепляет с С-конца одну аминокислоту: ароматическую или алифатическую) 5б – карбоксипептидаза В (отщепляет с С-конца лиз или арг) 6а – аланинаминопептидаза (отщепляют аланин с N-конца. 6б – лейцинаминопептидаза (отщепляет с N-конца любую аминокислоту) 7 – дипептидаза (расщепляют дипептиды) Примечание: Х – любая аминокислота. Задача 49. При дезаминировании аланина образуется пировиноградная кислота. Каков энергетический эффект полного окисления аланина (в молях АТФ на моль кислоты)? Ответ: Дезаминирование аланина через переаминирование с последующим участием НАД-дегидрогеназы в дыхательной цепи будет сопровождаться синтезом трех молей АТФ на моль аминокислоты. Образовавшаяся пировиноградная кислота пройдет обычный путь окисления: окислительное декарбоксилирование с образованием ацетил-КоА и распадом ацетила в ЦТК. Подсчитайте энергетический эффект окисления пировиноградной кислоты и прибавьте 3 моля АТФ, синтезированных за счет энергии, высвободившейся при окислительном дезаминировании аланина. (18 АТФ). Задача 50. Глутаминовая кислота в процессе окислительного дезаминирования превращается в α-кетоглутаровую. Каков энергетический эффект полного окисления 1 моля глутаминовой кислоты (в молях АТФ)? Ответ: Принцип решения тот же, что и в задаче 1: дезаминирование глутаминовой кислоты осуществляется при участии НАД-дегидрогеназы, а образующаяся при этом α-кетоглутаровая кислота сгорает в ЦТК. Подсчитайте ее энергоотдачу и прибавьте 3 моля АТФ. Для подсчета энергоотдачи необходимо написать частные реакции ЦТК. (12 АТФ). Задача 51. Если инкубировать аспарагиновую кислоту, содержащую метку (14С) в альфа-положении, с тканью печени, то в составе какого соединения обнаружится метка? Ответ: Аспарагиновая кислота может вступать в реакцию переаминирования, однако отсутствие кетокислот исключает эту возможность. Следует вспомнить роль аспарагиновой кислоты в биосинтезе мочевины и проследить судьбу углеродсодержащего остатка: найти в схеме биосинтеза мочевины конечный продукт орнитинового цикла, углеродный скелет которого принадлежит аспарагиновой кислоте, – он и будет содержать метку. Задача 52. В каких соединениях обнаружится радиоактивная метка, принадлежащая атому углерода в углекислоте (Н2СО3), если ее инкубировали с печеночной тканью, осуществляющей тканевое дыхание? Ответ: СО2 утилизируется печеночной тканью главным образом для синтеза мочевины через карбамоилфосфат. Проследите судьбу этого атома углерода в орнитиновом цикле и назовите все продукты, в состав которых последовательно войдет метка (последний из них - мочевина). Задача 53. Нормальные клетки Е. coliсинтезируют все аминокислоты, но некоторым ауксотрофным мутантам, не способным к синтезу определенных аминокислот, для оптимального роста необходимо вводить эти аминокислоты в питательную среду. Аминокислоты нужны не только для синтеза белков; некоторые из них требуются для биосинтеза других азотсодержащих клеточных компонентов. Допустим, у нас имеются три ауксотрофных мутанта, лишенных способности синтезировать одну из трех аминокислот-глицин, глутамин или аспартат. Синтез каких азотсодержащих продуктов (помимо белков) будет нарушен у каждого из этих мутантов? Ответ: Бактериальные мутанты, которые не способны синтезировать глицин, аспарагиновую или глутаминовую кислоты, обычно требуют добавки пуринов аденина и гуанина. Кроме того, для ауксотрофов по аспартату и глутамату необходимо, чтобы в среде содержались уридин и цитозин, а для ауксотрофов по Gly дополнительные пиримидины не нужны. Задача 54. Аминокислота метионин используется как лекарственный препарат с липотропным эффектом (удаляет из печени избыток жира) при жировом гипотозе, токсических поражениях печени, хроническом алкоголизме. Введение метионина при атеросклерозе вызывает снижение содержания в крови холестерина и повышения фосфолипидов. Объясните терапевтические эффекты метионина. Для ответа на этот вопрос: 1 - перечислите биологические функции метионина, 2 - напишите реакцию активации метионина 3 - напишите схему участия активного метионина в синтезе сложных липидов. Ответ: Аминокислота метионин является донором подвижной метильной группы в реакциях метилирования. Примерами реакций трансметилирования протекающих с участием метионина, являются превращение норадреналина в адреналин, гуанидинацетата в креатин, синтез мелатонина, метилирование азотных оснований нуклеотидов. Активной формой метионина (точнее его метильной группы) являются S- аденозилметионин, который образуется следующим образом: 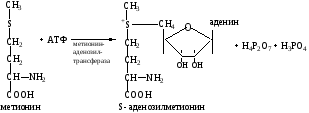 Синтез сложных липидов (фосфолипидов) также включает реакцию метилирования с участием S- аденозилметионина: 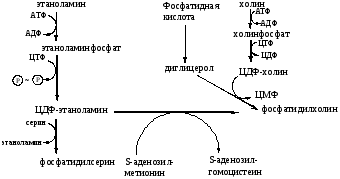 Задача 55. Укажите место радиоактивной метки в пуриновом ядре, биосинтез которого протекал в присутствии глутамина: а) содержащего радиоактивный углерод в альфа-положении, б) радиоактивный азот в аминогруппе, в) радиоактивный азот в амидогруппе. Ответ: Только азот амидогруппы используется в биосинтезе пуринового ядра, занимая позиции 3 и 9. Радиометка в других позициях в молекуле глутамина появиться в пуриновом основании не может: 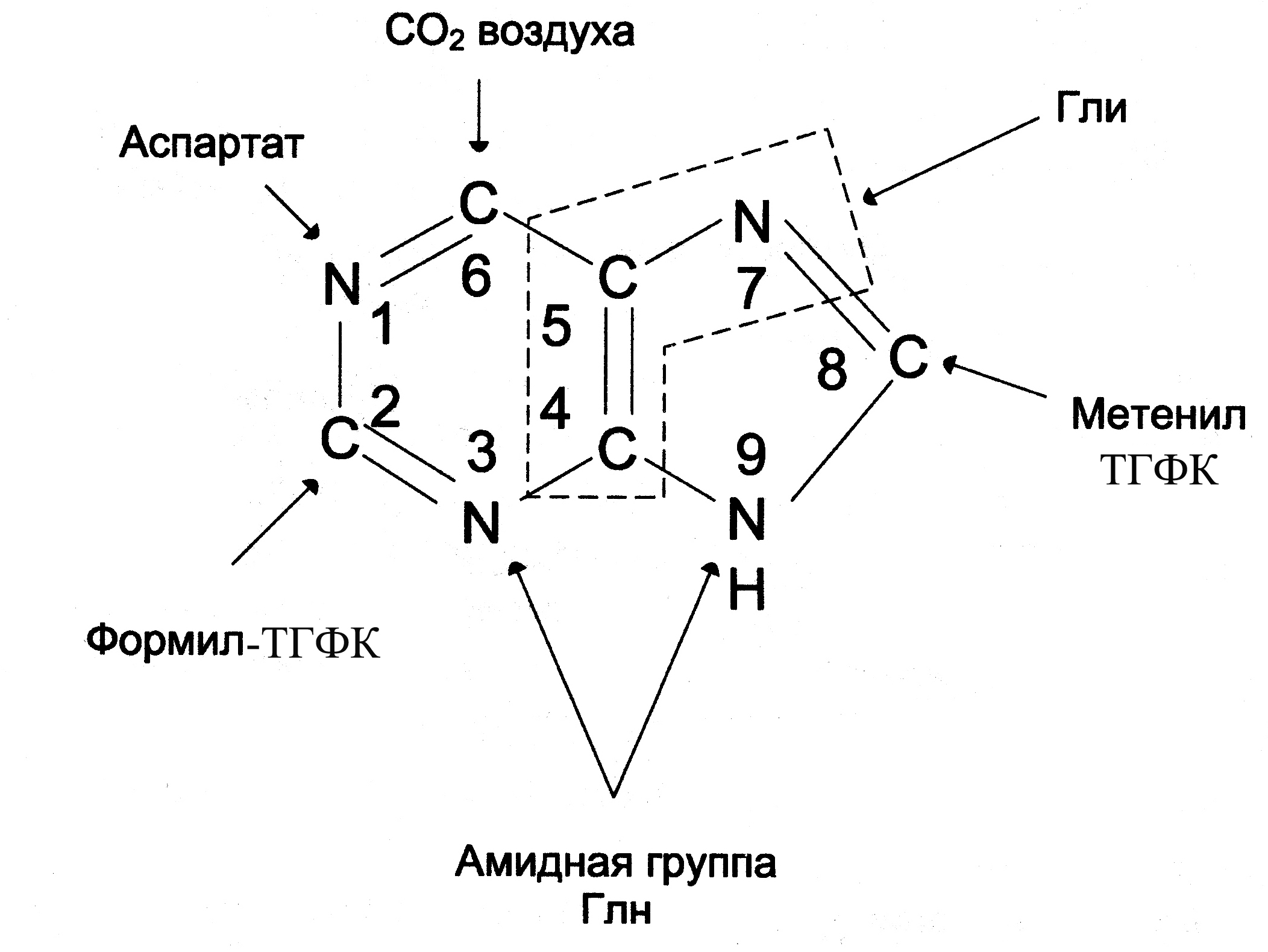 Задача 56. Урацил, содержащий в положении 6 радиоактивный атом углерода (14С), подвергся распаду в тканях при нормальном течении процесса. В составе какого соединения и в какой функциональной группе обнаружится 14С? Ответ: 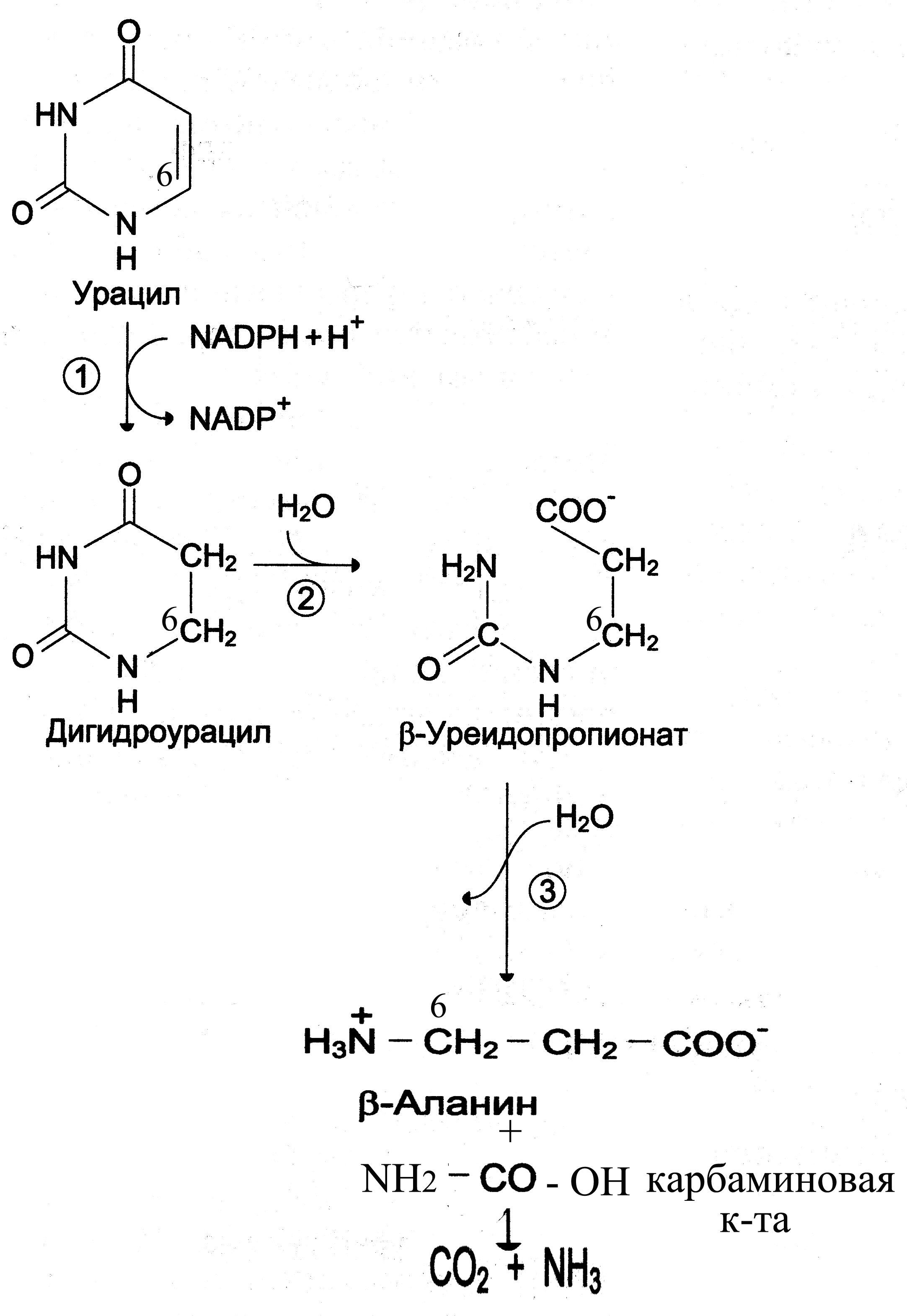 Проследите судьбу атома углерода в позиции 6. Это позволит ответить на вопрос задачи. Задача 57. Используя триплетную карту, предскажите аминокислотную последовательность пептидов, синтезируемых в рибосомах в присутствии следующих матриц, считая, что считывание начинается с первого триплета на левом конце. а) GGUCAGUCGCUCCUGAUU б) UUGGAUGCGCCAUAAUUUGCU в) CAUGAUGCCUGUUGCUAC г) AUGGACGAA Ответ: У эукариотов: a) Gly-Gln-Ser-Leu-Leu-Ile; 6) Leu-Asp-Ala-Pro; в) His-Asp-Ala-Cys-Cys-Туг; г) Met-Asp- Glu У прокариотов: fMet-Asp-Glu Задача 58. В большинстве соматических клеток после завершения репликации хромосом 5’-концы дочерних цепей ДНК недостроены, т.к. после удаления праймеров эти фрагменты оказываются недореплицированными. В эмбриональных клетках такого не наблюдается. Как осуществляется восстановление 5’-концов дочерних цепей в быстро делящихся клетках? Опишите фермент, ответственный за достройку 5’-концов ДНК этих клеток, механизм его функционирования; объясните, почему ДНК-полимеразы ß не могут осуществить эту достройку; укажите, почему укорочение дочерних цепей не опасно для большинства клеток человека. Ответ: Достройку 5-концов цепей ДНК обеспечивает фермент теломераза (нуклеотидилтрансфераза). Фермент содержит в активном центре фрагмент РНК, служащий матрицей при синтезе теломерных повторов хромосом быстро делящихся клеток. С помощью РНК фермент комплементарно присоединяется к 3-концу недостроенной дочерней цепи ДНК. Теломераза по принципу комплементарности последовательно удлиняет 3-конец цепи ДНК в направлении 53 на один гексануклеотид ГГГТТА. Затем фермент смещается по цепи ДНК на один теломер и начинает синтез нового фрагмента ГГГТТА. ДНК-полимераза В не может заменять теломеразу, потому что не может вести синтез цепи ДНК от 3- к 5-концу. В большинстве соматических клеток теломерная ДНК имеет длину, достаточную для времени жизни клетки и её потомства, а потому укорочение дочерних цепей не представляет опасности. Задача 59. Большинству аминокислот соответствует больше чем один кодон, больше чем одна тРНК и больше чем один анти-кодон. Напишите все возможные антикодоны для четырех глициновых кодонов: (5') GGU (3), GGC, GGA и GGG. а) На основании вашего ответа скажите, какие из положений антикодона определяют в первую очередь его специфичность в случае глицина? б) Какие из кодон-антикодоновьгх пар содержат «качающуюся» пару оснований? в) В какой из кодон-антикодоновых пар все три пары оснований образованы за счет прочных водородных связей? г) Использование какой из кодон-антикодоновых пар в биологическом синтезе белка наименее вероятно? Почему? Ответ:
а) Ha 5'-конце и в середине антикодона. б) «Качающиеся» пары оснований будут образовывать со своими кодонами аптикодоны (5') GGG, ICC и UCC. в) В парах, в образовании которых принимают участие антикодоны (5')ACG, GCC, UCC и CCC. г) Наименее вероятно использование пар, в которых участвуют антикодоны, указанные в п. в), поскольку тРНК, содержащие эти антикодоны, из-за прочного связывания всех трех антикодоновых оснований будут освобождаться из комплекса с более низкой скоростью, чем другие тРНК для Gly. Задача 60. Определите минимальные энергетические затраты (в расчете на число высокоэнергетических фосфатных групп), необходимые для биосинтеза Р-глобиновой цепи гемоглобина (146 остатков) из всех аминокислот, АТР и GTP. Сравните ваш ответ с расходами энергии на биосинтез линейной цепи гликогена, включающей 146 остатков глюкозы, соединенных α(1 → 4)-связью, и синтезируемой из глюкозы в присутствии АТР. Какова, исходя из ваших ответов, дополнительная энергетическая стоимость Р-глобиновой молекулы, обусловленная тем, что в отличие от гликогена при ее построении необходимо реализовать определенную генетическую информацию? Ответ: По меньшей мере 583 высокоэнергетические фосфатные группы; может быть и больше в зависимости от количества ошибок, выявленных и исправленных аминоацил-тРНК-синтетазами. На исправление каждой ошибки затрачиваются две высокоэнергетические фосфатные группы. Чтобы синтезировать из аминокислот белок, эукариотическая клетка должна осуществить синтез как минимум 20 активирующих ферментов, 70 рибосомных белков, 4 рибосомных РНК, не менее 20 тРНК и не менее 10 вспомогательных ферментов. В то же время для синтеза α(1→4)-цепи гликогена из глюкозы необходимо всего 4-5 ферментов. Задача 61. В гемоглобине серповидных эритроцитов в 6-м положении β-цепи гемоглобина А вместо глутаминовой кислоты (присутствующей в нормальном гемоглобине А) обнаружен валин. Какое изменение, произошедшее в кодоне для глутаминовой кислоты, привело к ее замене на валин? Ответ: В ДНК два кодона для Glu-(5')TTC и (5')СТС и четыре кодона для Val-(5')TAC, (5')САС, (5)ААС и (5)GAC. Замена аминокислоты в гемоглобине серповидных эритроцитов может быть обусловлена изменением одного основания: (5')ТТС (Glu) → (5')TAC (Val) или (5')CTC(Glu) → (5')CAC (Val). Гораздо менее вероятны изменения двух оснований: (5')ТТС → (5')САС, (5')ААС и (5')GAC или (5')СТС → (5')ТАС, (5')ААС и (5')GAC. Задача 62. Очень важные доказательства, подтверждающие правильность расшифрованного генетического кода, были получены при изучении природы мутаций, приводящих к замене одного остатка в аминокислотной последовательности белка. Какая из перечисленных ниже замен одной аминокислоты на другую согласуется с генетическим кодом? Какая из замен не может быть результатом изменения одного-единственного основания в мРНК? Почему? а) Phe → Leu б) Lys → Ala в) Ala → Thr г) Phe → Lys д) Не → Leu е) His → Glu ж) Pro → Ser Ответ: (а), (в), (д) и (ж); замены (б), (г) и (е) не могут быть результатом изменения в одном основании; для (б) и (е) требуется замена двух оснований, а для (г) необходимо заменить все три основания. |
