Диплом Закономерности изменения физических свойств анаэробных герметиков различного состава. Диплом 4 курс. Закономерности изменения физических свойств анаэробных герметиков различного состава Дипломная работа Научный
 Скачать 331.85 Kb. Скачать 331.85 Kb.
|
Глава 1. Принципы, механизм действия и разработки анаэробных композиций(Обзор литературы) Анаэробные композиции (клеи и герметики) – это жидкие составы на основе производных акриловой или метакриловой кислоты, которые поли- меризуются без доступа воздуха с образованием твердых продуктов. [1] В состав таких композиций входят акриловые мономеры и олигомеры, инициирующие системы, стабилизаторы (ингибиторы) и функциональные добавки (загустители, красители). Вязкость, в зависимости от выбранных компонентов, может колебаться в пределах от 10 мПа·с до 1000 Па·с. Герметики нашли широкое применение во многих отраслях народного хозяйства в основном для: -пропитки пористого литья, сварных швов, пресованных изделий; -контровки, стопорения резьбовых соединений; -фиксации скользящих соединений; -уплотнение резьбовых и гладких соединений. [2] Применение анаэробных герметиков в машиностроении позволяет экономить высококачественные марки металла, сократить количество металлообрабатывающих станков, повысить качество изделий, интенсифицировать и упростить технологический процесс производства, снизить себестоимость продукта. Широкое использование анаэробных уплотняющих составов повышает надежность изделий, резко сокращает брак готовой продукции, удлиняет время работы машин до капитального ремонта и позволяет ремонтировать технику на местах. 1.1 Принцип действия анаэробных композиций1.1.1 Общий механизм реакции полимеризации анаэробных композицийДля начала реакции полимеризации в анаэробных композициях, требуется выполнить три условия: соответствующая температура; контакт с металлом; изоляция от воздуха. Контакт с металлом дает начало стадии инициирования, которая включает в себя две реакции (Схема 1.1): образование свободного радикала, посредством взаимодействия перекиси и металла и присоединение этого радикала к мономеру. [3] Схема 1.1 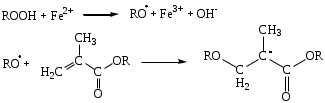 После того, как радикал присоединился к мономеру, происходит быстрая стадия роста цепи (Схема 1.2). Стоит заметить, что анаэробные композиции предназначены для использования при комнатных температурах. При температуре окружающей среды равной 10°С, скорость сшивки значительно снижается, а при 5°С она почти равна нулю. Напротив, повышение температуры до 55 °С приводит к слишком быстрой полимеризации, что усложняет процесс использования композиций. [3, 4] Схема 1.2 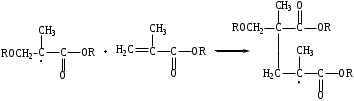 При использовании в составе диметакрилаты (три- и тетраметакрилаты), возможна перекрестная полимеризация (Схема 1.3), а также образование трёхмерных структур. Обрыв цепи происходит после рекомбинации радикальных частиц с образованием неактивных макромолекул. Схема 1.3 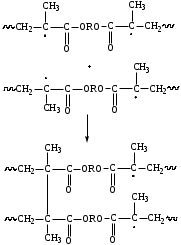 При этом следует отметить, что скорость образования начальных радикалов заметно увеличивается при переходе от алюминия к цинку, железу, меди и коррелирует с электродным потенциалом металла (Рисунок 1.1). [5] Рисунок 1.1. Кинетические кривые распада ГПК в присутствии ДМПТ-БСИ (1), Fe (2), ДМПТ-БСИ-Al (3), ДМПТ-БСИ-Zn (4), ДМПТ-БСИ-Fe (5), ДМПТ-БСИ-Cu (6). [ДМПТ]=[БСИ]=0,044 моль/л. Содержание металлов 0,025 г/мл, температура 50° 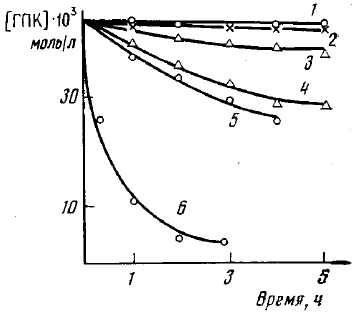 1.1.2 Роль кислородаКислород является ингибитором реакции полимеризации для анаэробных герметиков. Для того, чтобы понять роль кислорода был предложен следующий механизм. Он включает в себя сравнение скоростей реакций в присутствии кислорода (3-6) и без него (1-2). R· + M → RM· RM· + M → RM2· → R(M)n R· + O2 → ROO· RM· + O2 → RMOO· ROO· + M → ROOM· ROO· + ROO· → инертная макромолекула Где М – мономер, R· - инициирующий радикал, RM· - мономерный радикал, ROO· - пероксидный радикал. Из исследования [3] следует, что скорость реакций 4 и 6 выше, чем 2 и 5 соответственно. А т.к., образующиеся активные исходные радикалы мало используются на стадии ростацепи и большинство пероксидных радикалов превращаются в инертные вещества, полимеризация не происходит. 1.1.3 Роль инициирующей системыВысокую скорость полимеризации анаэробных композиций обеспечивают инициирующие системы, состоящие из пероксидного инициатора и ускорителя. Одними из самых эффективных признаны системы, в состав которых входят гидропероксиды, третичные ароматические амины и сульфамиды. [6] Из работы [5] следует, что начальная скорость полимеризации увеличивается с ростом донорной и снижением акцепторной способности заместителей в амине. Предполагаемое взаимодействие БСИ с третичными ароматическими аминами можно представить следующим образом: 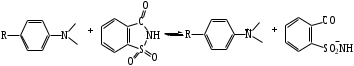 Установлено, что полимеризация с заметной скоростью происходит только при одновременном присутствии ГПК, БСИ и амина и сильно зависит от природы заместителей в бензольном кольце последних. Исследования продуктов взаимодействия порошков меди, железа, цинка и алюминия с БСИ и ДМПТ в органических растворителях (ИК-спектроскопия, элементный анализ) показало, что во всех случаях образуются соли соответствующих металлов с БСИ (сахаринаты). При изучении кинетики образования сахарината железа было обнаружено, что в отсутствии ДМПТ этот процесс замедляется (Рисунок 1.2). Рисунок 1.2. Накопление сахарината железа в дизобутиратетриэтилен-гликоля в присутствии 0,025 г/мл порошка железа и 0,1 моль/л БСИ (1), а также смеси 0,1 моль/л БСИ с 0,1 моль/л ДМПТ (2) при 80°С в атмосфере аргона. 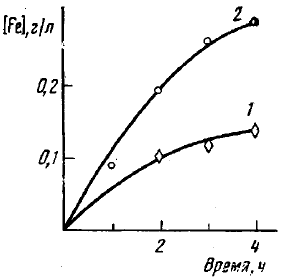 Логично предположить следующую схему взаимодействия металлов с компонентами инициирующей системы (где С-сахаринат): 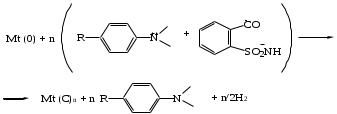 Сахаринат металла в дальнейшем реагирует с гидропероксидом с образованием алкоксильного радикала, который в свою очередь является инициатором реакции полимеризации. |
