иммнитет. Иммунная система Иммунная система
 Скачать 92.45 Kb. Скачать 92.45 Kb.
|
|
Иммунная система Иммунная система — система органов, существующая у позвоночных животных и объединяющая органы и ткани, которые защищают организм от заболеваний, идентифицируя и уничтожая опухолевые клетки и патогены. Иммунная система распознаёт множество разнообразных возбудителей — от вирусов до паразитических червей — и отличает их от биомолекулсобственных клеток. Распознавание возбудителей усложняется их адаптацией и эволюционным развитием новых методов успешного инфицирования организма-хозяина. Среди органов иммунной системы различают: 1. Центральые: вилочковая железа (тимус), костный мозг, бурса (у птиц). 2. Периферические: кров, лимфа, селезенка, лимфатические узлы. 3. Система лимфоэпителиальных образований: скопления лимфоидной ткани слизистых оболочек желудочно-кишечного тракта, дыхательных и мочеполовых путей. 1. Центральные органы иммунной системы: В центральных органах иммунной системыпроисходит лимфопоэз [от греч. lympha. прозрачная жидкость и poiesis, производить] — дифференцировка из клеток-предшественниц, размножение и созревание иммунокомпетентных клеток. В ходе дифференцировки лимфоциты начинают экспрессировать рецепторы, в дальнейшем способные связываться с Аг. В центральных органах отбираются и выживают те лимфоциты, которые толерантны к собственным Аг. Периферические органы иммунной системы 2. В периферических органах иммунной системы зрелые лимфоциты взаимодействуют между собой, со вспомогательными клетками и Аг. Здесь макрофаги и зрелые Т- и В-лимфоциты участвуют в иммунном ответе, появляются эффекторные клетки и клетки памяти. Иммунные реакции с участием циркулирующих в крови Аг протекают в селезёнке. Клетки лимфатических узлов реагируют с Аг, циркулирующем в лимфе. 3. Система лимфоэпителиальных образований: 1. Лимфоидные образования глотки - это 6 миндалин лимфоидного глоточного кольца. Каждая миндалина - это довольно крупное скопление лимфоидной ткани. Поверхность миндалин неровная, как будто изрыта оврагами. Эти складки называют криптами. Они задерживают частички пищи, пыли и т.д. Микроорганизмы попадая сюда, могут размножаться, что служит сигналом для запуска иммунологических реакций. 2. Лимфоидные образования пищевода. В толще складок слизистой оболочки пищевода, а также между ними, в глубине его борозд расположены лимфоидные узелки. Находясьна пути пищевых масс, а, следовательно, и антигенного воздействия, лимфоидные узелки осуществляют контроль и защиту стенок органа от генетически чужеродного материала. Лимфоидные узелки формируют цепочки на всем протяжении органа, повторяя извилистый ход складок. Кроме того, в стенках пищевода присутствуют так называемые диффузно рассеянные клетки лимфоидного ряда, залегающие между цепочками. 3. Лимфоидные образования желудка. В слизистой оболочке желудка обнаруживаются лимфоциты, относящиеся к В- и Т- популяциям, плазматические клетки и макрофаги. На разных этапах онтогенеза скопления лимфоидных узелков в различных частях желудка колеблется. 4. Лимфоидные образования кишечника. Лимфоидные образования в стенках толстой и тонкой кишок имеют анатомические особенности. Строение и имммунологическая функция этих органов соответствуют физиологическому назначению тонкой и толстой кишок.Лимфоидный аппарат включает в себя: лимфоидные (пейеровы бляшки), одиночные лимфоидные узелки, диффузно расположенные лимфоциты. У начала толстой кишки, располагается червеобразный отросток с его лимфоидными узелками. 5. Лимфоидные образования органов дыханияВ стенках органов дыхания, в которые вместе с воздухом попадают чужеродные частицы, имеется хорошо развитый аппарат иммунной защиты. Это скопления лимфоидной ткани расположенные в слизистой оболочке гортани, трахеи и бронхов под покровным эпителием, а также рассеянные в слизистой оболочке довольно многочисленные клетки лимфоидного ряда, получившие название лимфоидной ткани, ассоциированной с бронхами. Скопления лимфоидной ткани (лимфоидные узелки) зависит от возраста, а также функционального состояния организма 6. Лимфоидные образования мочевыводящих путей. Лимфоидные скопления (узелки) в стенках мочевыводящих путей выполняют "сторожевые" функции по отношению к тем чужеродным веществам, которые попадают в них извне восходящим путем или образуются в верхних их отделах. А также лимфоидный ткань кожи. Функции иммунной системы 1. Распознавания чужеродных и собственных измененных макромолекул (антигенов); 2. Удаление из организма антигенов и несущих их клеток; 3. Запоминание контакта с конкретными антигенами, определяющее их быстрое удаление при повторном поступлении в организм. Клетки иммунитета системы 1. Клетки иммунитета системы по строении :
1. Клетки иммунитета системы по функции :
Лейкоциты Лейкоциты- белые кровяные клетки; неоднородная группа различных по внешнему виду и функциям клеток крови человека или животных, выделенная по признакам наличия ядра и отсутствия самостоятельной окраски. Главная сфера действия лейкоцитов — защита. Они играют главную роль в специфической и неспецифической защите организма от внешних и внутренних патогенных агентов, а также в реализации типичных патологических процессов.Все виды лейкоцитов способны к активному движению и могут переходить через стенку капилляров и проникать в межклеточное пространство, где они поглощают и переваривают чужеродные частицы. Этот процесс называется фагоцитоз, а клетки, его осуществляющие, — фагоциты. Фагоциты- нейтрофилы, эозинофилы, моноциты, дендритные клетки и тучные клетки. По морфологическим признакам лейкоциты, окрашенные по Романовскому — Гимзе, со времён Эрлиха традиционно делят на две группы: Зернистые лейкоциты, или гранулоциты — клетки, имеющие крупные сегментированные ядра и обнаруживающие специфическую зернистость цитоплазмы; в зависимости от способности воспринимать красители они подразделяются на нейтрофильные, эозинофильные и базофильные; Незернистые лейкоциты, или агранулоциты — клетки, не имеющие специфической зернистости и содержащие простое несегментированное ядро, к ним относятся лимфоциты и моноциты. Функция лейкоцитов: Нейтрофилы 1. Нейтрофилы способны к фагоцитозу, причём являются микрофагами, то есть способны поглощать лишь относительно небольшие чужеродные частицы или клетки. 2. Нейтрофилы содержат большое количество миелопероксидазы, фермента, который способен окислять анион хлора до гипохлорита — сильного антибактериального агента (особенно к бактериам, грыбам, но к вирусам слабый). Миелопероксидаза как гем-содержащий белок имеет зеленоватый цвет, что определяет зеленоватый оттенок самих нейтрофилов, цвет гноя и некоторых других выделений, богатых нейтрофилам 3. Погибшие нейтрофилы вместе с клеточным детритом из разрушенных воспалением тканей и гноеродными микроорганизмами, послужившими причиной воспаления, формируют массу, известную как гной. Эозинофилы 1. Эозинофилы, как и нейтрофилы, способны к фагоцитозу, причём являются микрофагами 2. Эозинофилы способны поглощать и связывать гистамин и ряд других медиаторов аллергии и воспаления, активирует тчных клеток. 3. Главнейшее их свойство — экспрессия Fc-рецепторов, специфичных для Ig E. Физиологически это проявляется в мощных цитотоксических, а не фагоцитарных, свойствах эозинофилов, и их активном участии в противопаразитарном иммунитете. Однако, повышенная продукция антител класса E может привести к аллергической реакции немедленного типа (анафилактический шок), что является главным механизмом всех аллергий такого типа. Базофилы 1. Базофилы принимают активное участие в развитии аллергических реакций немедленного типа (реакции анафилактического шока). Гранулы базофилов содержат большое количество гистамина, серотонина, лейкотриенов, простагландинов и других медиаторов аллергии и воспаления. 2. Базофилы обладают способностью к хемотаксису и фагоцитозу. Кроме того, по всей видимости, фагоцитоз не является для базофилов ни основной, ни естественной (осуществляемой в естественных физиологических условиях) активностью. 3. Базофилы способны к экстравазации (эмиграции за пределы кровеносных сосудов), причём могут жить вне кровеносного русла, становясь резидентными тканевыми лаброцитами (тучными клетками). 4. Активируется эозинофилами крови, у базофилах есть рецептор к IgE. Моноциты 1. Осуществляют противоопухолевый, противовирусный, противомикробный, противозачаточный и противопаразитарный иммунитет, производя цитотоксины, интерлейкин (ИЛ-1-8-12), фактор некроза опухоли (ФНО), интерферон, ИЛ-1 является пирогенами, оны повышает температуры тела. 2. Фагацитоз с помошью протеаз, окись азота, лизасомные ферменты 3. Участвуют в регуляции гемопоэза (кроветворения) 4. Принимают участие в формировании специфического иммунного ответа организма(синтезирует белков комплемента, антиген презентация). 5. Моноциты, выходя из кровяного русла, становятся макрофагами, которые наряду с нейтрофилами являются главными «профессиональными фагоцитами». Лимфоциты Лимфоциты — главные клетки иммунной системы, обеспечивают гуморальный иммунитет (выработка антител), клеточный иммунитет (контактное взаимодействие с клетками-жертвами), а также регулируют деятельность клеток других типов.По функциональным признакам различают три типа лимфоцитов: B-клетки, T-клетки, NK-клетки. B-клетки распознают чужеродные структуры (антигены), вырабатывая при этом специфические антитела (белковые молекулы, направленные против конкретных чужеродных структур). T-киллеры выполняют функцию регуляции иммунитета. Т-хелперы стимулируют выработку антител, а Т-супрессоры тормозят её. NK-лимфоциты осуществляют контроль над качеством клеток организма. При этом NK-лимфоциты способны разрушать клетки, которые по своим свойствам отличаются от нормальных клеток, например, раковые клетки. Т- лимфоциты 1. Т-хелперы (от англ. helper — помощник) — T-лимфоциты, главной функцией которых является усиление адаптивного иммунного ответа. Выделяют несколько подтипов Т-хелперов: Т-хелперы 0 (Th0) — «наивные», недифференцированные Т-хелперы; Т-хелперы 1 (Th1) — преимущественно способствуют развитию клеточного иммунного ответа, активируя Т-киллеры; основной выделяемый цитокин — интерферон-гамма; Т-хелперы 2 (Th2) — активируют В-лимфоциты, способствуя развитию гуморального иммунного ответа; продуцируют интерлейкины 4, 5 и 13; Особенности: 1. Активируют Т-киллеры, B-лимфоциты, моноциты, NK-клетки, презентируя им фрагменты чужеродного антигена при прямом контакте, а также гуморально, выделяя цитокины. 2. Основным фенотипическим признаком Т-хелперов служит наличие на поверхности клетки молекулы CD4. Они связывются с MHC-II, соотвествии с эти развивается: 1. Th0 активируется- дифференцируется на Th1 и Th2. 2. Свыязывается с рецептором вируса ВИЧ. 3. Т-хелперы распознают антигены при взаимодействии их Т-клеточного рецептора(ТcR) с антигеном, связанным с молекулами главного комплекса гистосовместимости 2 класса (MHC-II). 4. Т хеперы имеет клеточный память(распазнають антиген при повторном поступлении) 5. Th0 с помощью ИЛ-2 образуется Th1, Th1 с помощью интерферонов активирует макрофагов, а также Th0 с помошью ИЛ-4 и 10 образуется Th2, Th2 с помощью ИЛ-4 активирует В лимофцитов(образуется плазматические клетки), и с помощью ИЛ -5 активирует плазматических клеток(образуется иммуноглобулины) 2. Т-киллеры. Т-киллеры, цитотоксические T-лимфоциты, CTL (англиц. killer «убийца») — вид Т-лимфоцитов, осуществляющий лизис повреждённых клеток собственного организма. Мишени Т-киллеров — это клетки, поражённые внутриклеточными паразитами (к которым относятся вирусы и некоторые виды бактерий), опухолевые клетки. Т-киллеры являются основным компонентом антивирусного иммунитета. Осоенности: 1. Т-киллеры непосредственно контактируют с повреждёнными клетками и разрушают их. В отличие от NK-клеток, T-киллеры специфически распознают определённый антиген и убивают только клетки с этим антигеном. 2. Большинство цитотоксических T-клеток относится к субпопуляции CD8+(имеет рецепторы CD8+), и распознает антиген, презентированный в ассоциации с молекулами MHC класса I, но меньшая их часть (примерно 10 %), относящаяся к субпопуляции CD4+(имеет рецепторы CD4+), способна распознавать антиген в ассоциации с молекулами MHC класса II. Опухолевые клетки, лишённые MHC I, Т-киллерами не распознаются. 3. Активированные Т-киллеры убивают клетки с чужеродным антигеном, к которому имеют рецептор, вставляя в их мембраны перфорины (белки, образующие широкое незакрывающееся отверстие в мембране) и впрыскивая внутрь токсины (гранзимы). В некоторых случаях Т-киллеры запускают апоптоз заражённой клетки через взаимодействие с мембранными рецепторами. 4. Пролиферация ТК осуществляется с помощью ИЛ-2. 3. Т-супрессоры. Регуляторные Т-лимфоциты, Т-регуляторные клетки, Т-супрессоры (англ. regulatory T cells, suppressor T cells, Treg) — центральные регуляторы иммунного ответа. Основная их функция — контролировать силу и продолжительность иммунного ответа через регуляцию функции Т-эффекторных клеток (Т-хелперов и Т-киллеров). Особенности: - Важным маркером Т-регуляторных клеток является экспрессия на их поверхности рецептора к цитокину IL-2 — CD25, соответственно их обозначают как CD25+-клетки. - Различают несколько разных типов регуляторных Т-клеток: естественные Т-регуляторные клетки (T-reg1) и индуцибельные Т-регуляторные клетки (iT-reg). Индуцибельные Т-регуляторные клетки образуются под влиянием различных факторов на периферии, например, в региональных лимфатических узлах. - Для супрессии иммунного ответа клетки Тreg выделяют цитокины: TGF-beta, IL-10, IFNγ, IL-35. Мишенями действия Тreg-клеток являются как Т-эффекторные клетки, так и дендритные клетки. Важным механизмом также служит захват IL-2 при помощи CD25 — рецептора к IL-2 и секвестрация рецептора у эффекторных Т-клеток, что препятствует активации после связывания комплекса MHC с антигеном, так как известно, что IL-2 является основным аутокринным стимулирующим фактором, поддерживающим дифференцировку и клональную экспансию Т-клеток. В- лимфоциты B-лимфоци́ты (B-клетки, от bursa fabricii птиц, где впервые были обнаружены) — функциональный тип лимфоцитов, играющих важную роль в обеспечении гуморального иммунитета. При контакте с антигеном или стимуляции со стороны T-клеток некоторые B-лимфоциты трансформируются в плазматические клетки, способные к продукции антител. Другие активированные B-лимфоциты превращаются в B-клетки памяти. Помимо продукции антител, В-клетки выполняют множество других функций: выступают в качестве антигенпрезентирующих клеток, продуцируют цитокины и экзосомы. Характерной особенностью В-клеток является наличие поверхностных мембраносвязанных антител, относящихся к классам IgM и IgD. В комплексе с другими поверхностными молекулами иммуноглобулины формируют антигенраспознающий рецептивный комплекс — B-клеточный рецептор, ответственный за узнавание антигена. Также на поверхности В-лимфоцитов расположены антигены МНС класса II, важные для взаимодействия с Т-клетками, также на некоторых клонах В-лимфоцитов присутствует маркер CD5, общий с Т-клетками. Рецепторы компонентов системы комплемента C3b (Cr1, CD35) и C3d (Cr2, CD21) играют определённую роль в активации В-клеток. Следует отметить, что маркеры CD19, CD20 и CD22 используются для идентификации В-лимфоцитов. Также на поверхности В-лимфоцитов обнаружены Fc-рецепторы. Активруется с помощью Т хелперов. NK-клетки Естественные киллеры, натуральные киллеры, NK-клетки (англ. Natural killer cells (NK cells)) — большие гранулярные лимфоциты, обладающие цитотоксичностью против опухолевых клеток и клеток, заражённых вирусами. В настоящее время NK-клетки рассматривают как отдельный класс лимфоцитов. NK выполняют цитотоксические и цитокин-продуцирующие функции. NK являются одним из важнейших компонентов клеточного врождённого иммунитета. Основная функция NK — уничтожение клеток организма, не несущих на своей поверхности MHC1 и таким образом недоступных для действия основного компонента противовирусного иммунитета — Т-киллеров. Уменьшение количества MHC1 на поверхности клетки может быть следствием трансформации клетки в раковую или действия вирусов, таких как папилломавирус и ВИЧ. C помощью гамма интерферонов активирует макрофагои и дифференсаци Т лимфоцитов Прочие клетки Макрофаги: макрофаги- вид моноцитов вне крови(таканевые формы). Они по локализации называетсы по разному: Дендритные клетки- макрофаги кожи, клетки Купфера- макрофаги печени, альфеоларные макрофаги, Гистоциты- макрофаги соединительной ткани, макрофаги селезенки, лимфоузлов. Их функция как и у моноцитов. Иммунитет Иммунитет (лат. immunitas) — это способ защиты организма от действия различных веществ и организмов, вызывающих деструкцию его клеток и тканей, характеризующийся изменением функциональной активности преимущественно иммуноцитов с целью поддержания гомеостаза внутренней среды. 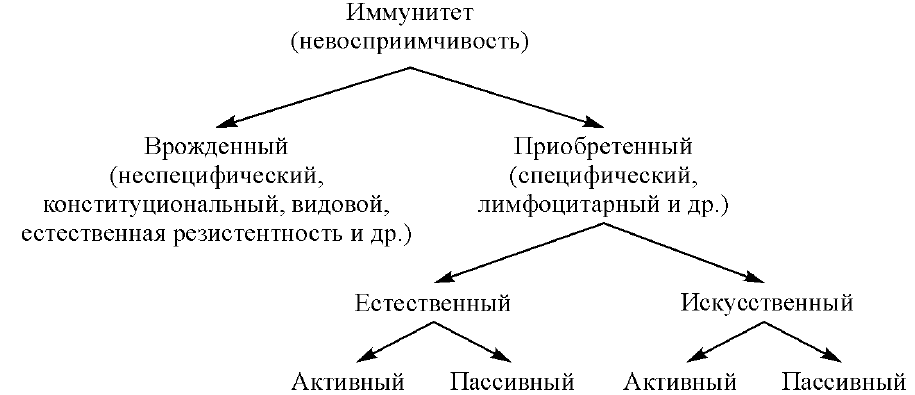 Классификация
Вроженный(неспецифический ) иммунитет Врождённый (неспецифический) иммунитет обусловлен способностью идентифицировать и обезвреживать разнообразные патогены по наиболее консервативным, общим для них признакам. Осуществляется большей частью клетками миелоидного ряда, не имеет строгой специфичности к антигенам, не имеет клонального ответа, не обладает памятью о первичном контакте с чужеродным агентом. Виды: 1. Барьеры: физическая- кожа, слизистая оболочка, химическая- ферменты кишечника, желч, сальные и потовые железа. 2. Система комплемента 3. Фагацитоз Приобретенный(специфический) иммунитет Способность организма обезвреживать чужеродные и потенциально опасные микроорганизмы (или молекулы токсинов), которые уже попадали в организм ранее. Представляет собой результат работы системы высокоспециализированных клеток (лимфоцитов), расположенных по всему организму. 1. Естественный иммунитет: 1. Активный (после перенесённого заболевания), 2. Пассивный иммунитет при передаче антител ребёнку от матери(с молозивом матери или внутриутробным способом. 2. Искусственный иммунитет: 1. Активный после прививки (введение вакцины) и 2. Пассивный после введение сыворотки. Клеточный иммунитет и гумаральный иммунитет Это такой тип иммунного ответа, в котором не участвуют ни антитела, ни система комплемента. В процессе клеточного иммунитета активируются макрофаги, натуральные киллеры, антиген-специфичные цитотоксические Т-лимфоциты, и в ответ на антиген выделяются цитокины. Иммунная система исторически разделена на две части — систему гуморального иммунитета и систему клеточного иммунитета. В случае гуморального иммунитета, защитные функции выполняют молекулы, находящиеся в плазме крови(иммуноглобулины), но не клеточные элементы. В то время как в случае клеточного иммунитета защитная функция связана именно с клетками иммунной системы. Лимфоциты кластера дифференцировки CD4 или Т-хелперы осуществляют защиту против различных патогенов Фагоцитоз Фагоцитоз (др.-греч. φαγεῖν «пожирать» + κτος «клетка») — процесс, при котором клетки (простейшие, либо специально предназначенные для этого клетки крови и тканей организма — фагоциты) захватывают и переваривают твёрдые частицы. Фагоцитоз, наряду с пиноцитозом, является одним из видов эндоцитоза. У некоторых клеток он используется для получения полезных веществ, и для одноклеточных организмов гомологичен питанию. У многоклеточных животных этот процесс взял на себя функцию удаления отходов и патогенов. Этапы: 1. Хемотаксис(). В реакции фагоцитоза более важная роль принадлежит положительному хемотаксису. В качестве хемоаттрактантов выступают продукты выделяемые микроорганизмами и активированными клетками в очаге воспаления (цитокины, лейкотриен В4, гистамин), а также продукты расщепления компонентов комплемента(С3а, С5а), протеолитические фрагменты факторов свертывания крови и фибринолиза (тромбин, фибрин), нейропептиды, фрагменты иммуноглобулинов и др. Однако, «профессиональными» хемотаксинами служат цитокины группы хемокинов. Ранее других клеток в очаг воспаления мигрируют нейтрофилы, существенно позже поступают макрофаги. Скорость хемотаксического перемещения для нейтрофилов и макрофагов сопоставима, различия во времени поступления, вероятно, связаны с разной скоростью их активации. 2. Адгезияфагоцитов к объекту. Обусловлена наличием на поверхности фагоцитов рецепторов для молекул, представленных на поверхности объекта (собственных или связавшихся с ним). При фагоцитозе бактерий или старых клеток организма хозяина происходит распознавание концевых сахаридных групп — глюкозы, галактозы, фукозы, маннозы и др., которые представлены на поверхности фагоцитируемых клеток. Распознавание осуществляется лектиноподобными рецепторами соответствующей специфичности, в первую очередь маннозосвязывающим белком и селектинами, присутствующими на поверхности фагоцитов.В тех случаях, когда объектами фагоцитоза являются не живые клетки, а кусочки угля, асбеста, стекла, металла и др., фагоциты предварительно делают объект поглощения приемлемым для осуществления реакции, окутывая его собственными продуктами, в том числе компонентами межклеточного матрикса, который они продуцируют.Хотя фагоциты способны поглощать и разного рода «неподготовленные» объекты, наибольшей интенсивности фагоцитарный процесс достигает при опсонизации, то есть фиксации на поверхности объектов опсонинов к которым у фагоцитов есть специфические рецепторы — к Fc-фрагменту антител, компонентам системы комплемента, фибронектину и т. д. 3. Активация мембраны. На этой стадии осуществляется подготовка объекта к погружению. Происходит активация протеинкиназы С, выход ионов кальция из внутриклеточных депо. Большое значение играют переходы золь-гель в системе клеточных коллоидов и актино-миозиновые перестройки. 4. Погружение(эндоцитоз). Происходит обволакивание объекта. 5. Образование фагосомы. Замыкание мембраны, погружение объекта с частью мембраны фагоцита внутрь клетки. 6. Образование фаголизосомы. Слияние фагосомы с лизосомами, в результате чего образуются оптимальные условия для бактериолиза и расщепления убитой клетки. Механизмы сближения фагосомы и лизосом неясны; вероятно, происходит активное перемещение лизосом к фагосомам. 7. Киллинг и расщепление. Велика роль клеточной стенки перевариваемой клетки. Основные вещества, участвующие в бактериолизе: пероксид водорода, продукты азотного метаболизма, лизоцим и др. Процесс разрушения бактериальных клеток завершается благодаря активности протеаз, нуклеаз, липаз и других ферментов, активность которых оптимальна при низких значениях pH. 8. Выброс продуктов деградации. Фагоцитоз может быть: завершённым (киллинг и переваривание прошло успешно); незавершённым (для ряда патогенов фагоцитоз является необходимой ступенью их жизненного цикла, например, у микобактерий и гонококков). Антитела Антитела (иммуноглобулины, ИГ, Ig) — белковые соединения плазмы крови, образующиеся в ответ на введение в организм человека или теплокровных животных бактерий, вирусов, белковых токсинов и других антигенов. Связываясь активными участками (центрами) с бактериями или вирусами, антитела препятствуют их размножению или нейтрализуют выделяемые ими токсические вещества. Антитела являются особым классом гликопротеинов, имеющихся на поверхности B-лимфоцитов в виде мембраносвязанных рецепторов и в сыворотке крови. Антитела являются важнейшим фактором специфического гуморального иммунитета. Антитела используются иммунной системой для идентификации и нейтрализации чужеродных объектов — например, бактерий и вирусов. Антитела выполняют две функции: антиген-связывающую и эффекторную (вызывают тот или иной иммунный ответ, например, запускают классическую схему активации комплемента).Антитела синтезируются плазматическими клетками, которыми становятся некоторые В-лимфоциты, в ответ на присутствие антигенов. Для каждого антигена формируются соответствующие ему специализировавшиеся плазматические клетки, вырабатывающие специфичные для этого антигена антитела. Антитела распознают антигены, связываясь с определённым эпитопом — характерным фрагментом поверхности или линейной аминокислотной цепи антигена.Антитела состоят из двух лёгких и двух тяжёлых цепей. У млекопитающих выделяют пять классов антител (иммуноглобулинов) — IgG, IgA, IgM, IgD, IgE, различающихся между собой по строению и аминокислотному составу тяжёлых цепей и по выполняемым эффекторным функциям. Функции Иммуноглобулины всех изотипов бифункциональны. Это означает, что иммуноглобулин любого типа распознает и связывает антиген, а затемусиливает уничтожение и/или удаление иммунных комплексов, сформированных в результате активации эффекторных механизмов. Одна область молекулы антител (Fab) определяет её антигенную специфичность, а другая (Fc) осуществляет эффекторные функции: связывание с рецепторами, которые экспрессированы на клетках организма (например, фагоцитах); связывание с первым компонентом (C1q) системы комплемента для инициации классического пути каскада комплемента. 1. IgG является основным иммуноглобулином сыворотки здорового человека (составляет 70-75 % всей фракции иммуноглобулинов), наиболее активен во вторичном иммунном ответе и антитоксическом иммунитете. Благодаря малым размерам (коэффициент седиментации 7S, молекулярная масса 146 кДа) является единственной фракцией иммуноглобулинов, способной к транспорту через плацентарный барьер и тем самым обеспечивающей иммунитет плода и новорождённого. В составе IgG 2-3 % углеводов; два антигенсвязывающих Fab-фрагмента и один FC-фрагмент. Fab-фрагмент (50-52 кДа) состоит из целой L-цепи и N-концевой половины H-цепи, соединённых между собой дисульфидной связью, тогда как FC-фрагмент (48 кДа) образован C-концевыми половинами H-цепей. Всего в молекуле IgG 12 доменов (участки, сформированные из β-структуры и α-спиралей полипептидных цепей Ig в виде неупорядоченных образований, связанных между собой дисульфидными мостиками аминокислотных остатков внутри каждой цепи): по 4 на тяжёлых и по 2 на лёгких цепях. 2. IgM представляют собой пентамер основной четырёхцепочечной единицы, содержащей две μ-цепи. При этом каждый пентамер содержит одну копию полипептида с J-цепью (20 кДа), который синтезируется антителообразующей клеткой и ковалентно связывается между двумя соседними FC-фрагментами иммуноглобулина. Появляются при первичном иммунном ответе B-лимфоцитами на ранее неизвестный антиген; составляют до 10 % фракции иммуноглобулинов. Являются наиболее крупными иммуноглобулинами (970 кДа). Содержат 10-12 % углеводов. Образование IgM происходит ещё в пре-B-лимфоцитах, в которых первично синтезируются из μ-цепи; синтез лёгких цепей в пре-B-клетках обеспечивает их связывание с μ-цепями, в результате образуются функционально активные IgM, которые встраиваются в поверхностные структуры плазматической мембраны, выполняя роль антиген-распознающего рецептора; с этого момента клетки пре-B-лимфоцитов становятся зрелыми и способны участвовать в иммунном ответе. 3. IgA сывороточный IgA составляет 15-20 % всей фракции иммуноглобулинов, при этом 80 % молекул IgA представлено в мономерной форме у человека. Основной функцией IgA является защита слизистых оболочек дыхательных, мочеполовых путей и желудочно-кишечного тракта от инфекций. Секреторный IgA представлен в димерной форме в комплексе с секреторным компонентом, содержится в серозно-слизистых секретах (например в слюне, слезах, молозиве, молоке, отделяемом слизистой оболочки мочеполовой и респираторной системы). Содержит 10-12 % углеводов, молекулярная масса 500 кДа. 4. IgD составляет менее одного процента фракции иммуноглобулинов плазмы, содержится в основном на мембране некоторых В-лимфоцитов. Функции до конца не выяснены, предположительно является антигенным рецептором с высоким содержанием связанных с белком углеводов для В-лимфоцитов, ещё не представлявшихся антигену. Молекулярная масса 175 кДа. 5. IgE в свободном виде в плазме почти отсутствует. Способен осуществлять защитную функцию в организме от действия паразитарных инфекций, обуславливает многие аллергические реакции. Механизм действия IgE проявляется через связывание с высоким сродством (10−10М) с поверхностными структурами базофилов и тучных клеток, с последующим присоединением к ним антигена, вызывая дегрануляцию и выброс в кровь высоко активных аминов (гистамина и серотонина — медиаторов воспаления), на чем основано применение аллергических диагностических проб. Молекулярная масса 200 кДа. 6. IgY обнаружены в крови кур и яичном желтке. Система комплемента Система комплемента — комплекс сложных белков, постоянно присутствующих в крови. Это каскадная система протеолитических ферментов, предназначенная для гуморальной защиты организма от действия чужеродных агентов, она участвует в реализации иммунного ответаорганизма. Является важным компонентом как врождённого, так и приобретённого иммунитета. Функции:
|
