Наименование проекта Напиток Байкал пить или не пить (выявление концентрации лимонной кислоты в напитке Байкал)
 Скачать 3.7 Mb. Скачать 3.7 Mb.
|
|
Шифр: 1401 Наименование проекта: Напиток «Байкал» пить или не пить? (выявление концентрации лимонной кислоты в напитке «Байкал») Антиплагиат: 64% Оглавление Введение……………………………………………………………………………….3 I. Теоретическая часть……………………………………………………………..4 История создания напитка…………………………………………………….4 Состав напитка………………………………………………………………....5 II. Экспериментальная часть…………………………………………………………6 2.1. Эксперимент 1……………………………………………………………………6 2.2. Наблюдения и результаты……………………………………………………….9 2.3. Погрешности в измерениях……………………………………………………...11 2.4. Вывод……………………………………………………………………………...12 2.5. Эксперимент 2…………………………………………………………………….12 2.6. Наблюдения и результаты……………………………………………………….14 2.7. Вывод……………………………………………………………………………..21 2.8. Вывод по экспериментальной части……………………………………………21 Заключение……………………………………………………………………………22 Список литературы…………………………………………………………………...23 Введение Организм человека на 60% состоит из воды. Для поддержания водного равновесия мы пьем каждый день. Кто-то предпочитает кофе, кто-то чай, соки, газировку. Как правило, сладкие газированные напитки употребляют в больших количествах дети и подростки. Основа напитка составляет вода. Помимо воды в напитках содержатся другие вещества, оказывающие воздействие на наш организм. Это воздействие может быть положительным или отрицательным, в зависимости от регулярности и объемов употребления того или иного напитка. Здоровому человеку небольшое количество газированной воды не повредит. Но частое употребление больших количеств сладкой газированной воды может неблагоприятно отразиться на здоровье. Проблема исследования заключается в том, что в наше время недостаточное внимание уделяется негативному влиянию газированных напитков на эмаль зубов. Гипотеза: если часто употреблять сладкие газированные напитки, то можно остаться без зубов. Цель: провести исследование методами химического анализа на концентрацию лимонной кислоты в напитке «Байкал». Задачи: Изучить разные источники информации по истории создания и составу напитка «Байкал»; Ознакомиться с основами гравиметрического и титриметрического анализа; Провести химические эксперименты по определению концентрации лимонной кислоты в напитке; Оценить полученные результаты, погрешность измерений, сделать вывод о точности методик; Ознакомиться с негативным влиянием лимонной кислоты на зубную эмаль; Объект: газированный напиток «Байкал» Предмет: концентрация лимонной кислоты в напитке. Новизна. Я видела много проектов на похожие темы. Актуальность моего проекта заключается в том, что до меня никто не проверял количество лимонной кислоты в напитке «Байкал» и сразу двумя методами. Теоретическая часть . История создания напитка «Байка́л» — сильногазированный тонизирующий напиток, разработанный в СССР как местный аналог «Кока-колы» и «Пепси-колы». История напитка Байкал начинается в 1973 году, когда партией было поручено создать аналог американских напитков Кока-Кола и Пепси. Из-за того, что люди не доверяли составу зарубежного напитка, который продавался в союзе за 45 копеек, вокруг него ходили страшные легенды. Да и привыкли москвичи к тому, что у всего западного есть свой аналог в Союзе, который и вкуснее, и здоровее, и дешевле. Конечно, были у нас напитки собственного производства всех расцветок: «Дюшес», «Крюшон», «Тархун», «Ситро», «Буратино». Одна беда – не было среди них только коричневого, только та самая «Кола», которую нашей назвать было никак нельзя. Для этого подключили лучшие силы – «Всесоюзный научно-исследовательский институт пивобезалкогольной и винодельческой промышленности» (ВНИИ ПБП). Задача была поставлена труднейшая: 1. Чтобы новый напиток был коричневого цвета. 2. Чтобы он изготавливался только из отечественных составляющих. 3. Чтобы при всем при этом его можно было еще и пить. Новый напиток должен был занять достойное место в ряду советской безалкогольной продукции. Первая и основная сложность, с которой столкнулись ученые-химики - это выбор ингредиентов. Орехи колы никогда не росли на территории Союза, они предпочитают жаркий тропический климат, которым не славится ни Россия, ни другие советские республики. Состав напитка В 1973 году был создан такой напиток Всесоюзным научно-исследовательским институтом пиво-безалкогольной промышленности (ВНИИ ПБП). Состав напитка был создан в СССР, на рынке с 1973 года. С 1991 года выпускается в России  Новый напиток всех очаровал. Потребитель на ура принял «Байкал», а люди его быстро распробовали и оценили. Впервые «Байкал» был выпущен заводом безалкогольных напитков в Москве в 1973 году. Состав и технология приготовления нового советского напитка «Байкал» являлись служебной тайной. II. Экспериментальная часть Для подтверждения нашей гипотезы мы решили в качестве эксперимента использовать методы гравиметрия и титримитрия для определения концентрации лимонной кислоты в напитке "Байкал". Гравиметрия – метод количественного химического анализа, основанный на точном измерении массы вещества. Гравиметрический метод заключается в определении массы некоторого компонента в образце, подвергаемом анализу. Для этого производят точное взвешивание вещества в устойчивой конечной форме, в которую переведен измеряемый компонент. Его должно быть можно легко отделить и взвесить. Титриметрический метод анализа основан на измерении объема раствора известной концентрации (титранта), вступившего в реакцию с исследуемым веществом. 2.1. Эксперимент 1 Цель: Рассчитать концентрацию лимонной кислоты в напитке «Байкал». Средства измерений, вспомогательное оборудование, реактивы, материалы: Весы аналитические Пипетка Мора вместимостью 50 см3 Пипетка Пастера Цилиндр вместимостью 10 см3 Часы Плита нагревательная Воронка лабораторная диаметром 75 мм Колба коническая вместимостью 250 см3 Стакан лабораторный вместимостью 250 см3 Палочка стеклянная Аммиак водный Вода дистиллированная Газированная вода «Байкал» Хлорид кальция, раствор с массовой долей 11,1 % Фильтровальная бумага «синяя лента» Ход эксперимента: Пипеткой Мора мы отобрали аликвотную часть газированной воды объемом 50 см3 и поместили в стакан вместимостью 250 см3. Эксперимент проводили в трёх параллелях.  В качестве реагента (осадителя) мы взяли раствор хлористого кальция (CaCl2) с массовой долей 11,1 %. Цилиндром добавили 10 см3 осадителя к пробам.   Поставили стаканы на нагревательную плиту, нагрели до кипения.  К кипящим растворам добавили по 2 капли аммиака водного. Продолжили кипятить пробы в течение 10 минут.  5. По истечении этого времени поместили пробы на кипящую водяную баню на 30 минут. 6. Горячие пробы отфильтровали на предварительно высушенный при 105 °С фильтр «синяя лента», промыли осадок цитрата кальция на фильтре горячей дистиллированной водой до отрицательной реакции на хлорид-ионы нитратом серебра.   7. Осадок высушили при температуре 105˚С в течении двух часов и после этого взвесили. Наблюдения и результаты
Найдем массу лимонной кислоты в исследуемых пробах: 2C6H8O7 + 3CaCl2 = Ca3(C6H5O7)2↓ + 6HCl  𝜈ур. 2 моль 1 моль 𝜈ур. 2 моль 1 моль 𝜈 моль 𝜈ос. =   ; ;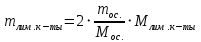 Mос. = 40,08⋅3 + (12,0108⋅6 + 1,00795⋅5 + 15,9994⋅7)⋅2 = 498,44 г/моль Млим. кисл. = 12,0108⋅6 + 1,00795⋅8 + 15,9994⋅7 = 192,12 г/моль mлим.к-ты 1 =  = 0,0017 г = 0,0017 гmлим.к-ты 2 =  = 0,0021 г = 0,0021 гmлим.к-ты 3 =  = 0,0018 г = 0,0018 гНайдем концентрацию лимонной кислоты в исследуемой газированной воде: С  С – концентрация лимонной кислоты, г/дм3 mлим. кисл. – масса лимонной кислоты, г; V – объём газированной воды, взятый для анализа, см3; 1000 – коэффициент пересчёта с см3 на дм3. С1 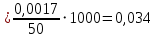 г/дм3 г/дм3С2  г/дм3 г/дм3С3  г/дм3 г/дм3Найдем среднее значение:   Найдем расхождение между определениями:   Полученное расхождение указывает на то, что наше определение проведено с погрешностью. Погрешности в измерениях В аналитической химии выделяют грубые, систематические и случайные погрешности. Грубые (промахи) возникают из-за ошибок оператора или неправильной работы оборудования. Грубые погрешности делают измерение недостоверным. В нашем случае мы считаем, что указанный вид погрешности отсутствовал. Измерения проводились строго по выбранной нами методике, используемое оборудование было исправно, работали на оборудовании корректно, показания считывали верно. Систематические погрешности возникают из-за влияния измерительных приборов на исследуемые процессы. В нашем случае вклад в точность методики от систематической погрешности следующая: погрешность используемых измерительных приборов (весы, пипетка, цилиндр). Случайная погрешность – это ошибка в измерениях, которая носит неконтролируемый характер и труднопредсказуема. В нашем эксперименте к таковой отнесем: - неточное доведение до метки при взятии аликвоты газированной воды; - неколичественный перенос пробы из пипетки в стакан; - неколичественный перенос осадка из стакана на фильтр; - потери при промывании осадка; - потери при высушивании осадка; - изменение температуры при проведении анализа и т.д. 2.4. Вывод Газированная вода – многокомпонентный напиток, поэтому вместе с цитратом кальция в ходе эксперимента мы могли осадить и другие соли кальция, что могло внести определенную неточность в определение концентрации лимонной кислоты в напитке. В нашем случае лимонную кислоту мы осаждали хлоридом кальция, в результате образовался нерастворимый в воде цитрат кальция. Несмотря на вышеперечисленное, мы считаем, что данный метод может быть использован для определения концентрации лимонной кислоты в газированной воде. Эксперимент 2 Далее, для подтверждения нашей гипотезы мы решили в качестве эксперимента использовать титриметрический метод определения концентрации лимонной кислоты в напитке "Байкал". В нашем эксперименте в качестве титранта мы использовали раствор NaOH с молярной концентрацией 0,1 моль/дм3. Титриметрический анализ проводят до конечной точки титрования (КТТ), добавляя небольшое количество раствора из бюретки к исследуемому веществу. Конечную точку титрования идентифицируют по изменению цвета индикатора или какого-либо физико-химического свойства. В нашем случае конечную точку титрования мы фиксировали с помощью рН-метра, в точке эквивалентности при этом происходит резкий скачок рН. Объем титранта, при котором наблюдается скачок и есть конечный результат. Цель: Рассчитать концентрацию лимонной кислоты в напитке «Байкал». Средства измерений, вспомогательное оборудование, реактивы, материалы: рН-метр Бюретка вместимостью 25 см3 Пипетка Мора вместимостью 50 см3 Стакан лабораторный вместимостью 250 см3 Магнитная мешалка Магнитный якорь Газированная вода «Байкал» Раствор NaOH молярной концентрации 0,1 моль/дм3 Ход эксперимента: Пипеткой Мора мы отобрали аликвотную часть газированной воды объемом 50 см3 и поместили в стакан вместимостью 250 см3. Эксперимент проводили в трёх параллелях.  В пробу опустили магнитный якорь и поместили ее на магнитную мешалку. Выбрали такую скорость у мешалки, чтобы водоворот был едва заметен. Опустили в стакан электрод рН-метра таким образом, чтобы он не касался стенок стакана, а якорь не бил по электроду. Замерили рН исследуемой пробы. Бюретку с раствором NaOH молярной концентрации 0,1 моль/дм3 устанавливаем так, чтобы капли из крана не попадали на электрод. Приступили к титрованию: титрант добавляем небольшими порциями, фиксируем показания рН-метра и считываем показания с бюретки. Вблизи точки эквивалентности (рН 8,2 – 10,0) титрование проводим по каплям. Наблюдения и результаты Для того, чтобы точно найти объем титранта, при котором происходит скачок рН, мы будем строить кривые ΔрН/ΔV = f(V) Проба 1
 На кривой титрования мы наблюдаем пик, в этой точке происходит резкий скачок рН, следовательно, объем в этой точке – эквивалентный. Vэкв.1=10,1 см3 Проба 2
 Vэкв.2=10,0 см3 Проба 3
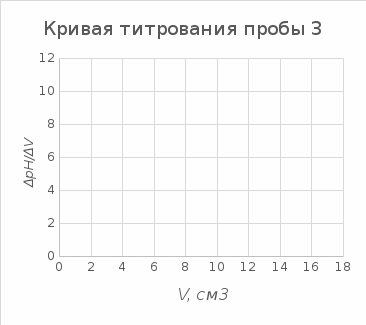 Vэкв.3=10,0 см3 Найдем массу лимонной кислоты в исследуемых пробах: C6H8O7 + 3NaOH = Na3C6H5O7 + 3H2O  𝜈ур. 1 моль 3 моль 𝜈ур. 1 моль 3 моль 𝜈 моль 𝜈NaOH =   ; ; Млим. кисл. = 12,0108⋅6 + 1,00795⋅8 + 15,9994⋅7 = 192,12 г/моль mлим.к-ты 1 = 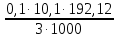 = 0,0647 г = 0,0647 гmлим.к-ты 2 =  = 0,0640 г = 0,0640 гmлим.к-ты 3 =  = 0,0640 г = 0,0640 гНайдем концентрацию лимонной кислоты в исследуемой газированной воде: С  С – концентрация лимонной кислоты, г/дм3 mлим. кисл. – масса лимонной кислоты, г; V – объём газированной воды, взятый для анализа, см3; 1000 – коэффициент пересчёта с см3 на дм3. С1  г/дм3 г/дм3С2  г/дм3 г/дм3С3  г/дм3 г/дм3Найдем среднее значение:   Найдем расхождение между определениями:   Полученное расхождение указывает на то, что наше определение проведено с погрешностью. Также, как и в предыдущем эксперименте вклад в точность методики от систематической и случайной погрешностей. Систематическая погрешность при титровании: погрешность используемых измерительных приборов (рН-метр, пипетка, бюретка). К случайной погрешности в нашем эксперименте отнесем: - неточное доведение до метки при взятии аликвоты газированной воды; - неточное считывание показаний с бюретки; - изменение температуры при проведении анализа и т.д. 2.7. Вывод Данный метод позволяет провести определение с большей точностью. Но при титровании мы определяем не только лимонную кислоту, но и все остальные кислоты, которые могли находиться в газированной воде (по крайней мере, угольная), хотя перед экспериментом мы дегазировали напиток. Поэтому данный метод пригоден для определения кислотности напитка, а определять лимонную кислоту следует все-таки гравиметрическим методом, а титрование раствором гидроксида натрия не подходит для определения лимонной кислоты в пробах, содержащих другие кислоты. Вывод по экспериментальной части Проведя два эксперимента по определению лимонной кислоты в газированном напитке методами гравиметрии и титриметрии, мы пришли к выводу, что концентрация лимонной кислоты в газированной воде «Байкал» равна 0,037 г/дм3. В эксперименте 2 перед титрованием мы измеряли рН газированной воды «Байкал», среднее значение составило 2,88, что означает, что среда достаточно кислая. Заключение В большинстве газированных напитков в составе присутствуют кислоты, которые являются разрушителем зубной эмали. Даже в диетической газировке, также имеется вредная кислота. Человек, часто употребляющий большое количество газированных напитков, подвергает защитный слой зубов разрушительному процессу. Среди органических кислот, растворяющих кристаллы апатитов, значительным воздействием обладает лимонная кислота, т. к. она в наибольшей степени из всех органических кислот влияет на растворимость гидроксиапатита, образуя с кальцием комплекс. Под действием лимонной кислоты, входящей в состав напитка «Байкал», кальций из гидроксиапатита будет переходить в более растворимую форму – цитрат, что увеличит деминерализацию зубной эмали.  Ca10(PO4)6(OH)2 + C6HgO7 Ca9H2(PO4)6(OH)2 + Ca3(C6H5O7)2 Ca10(PO4)6(OH)2 + C6HgO7 Ca9H2(PO4)6(OH)2 + Ca3(C6H5O7)2Включение чужеродных катионов в кристаллическую решетку увеличивает растворимость гидроксиапатита. Кислота растворяет минеральные вещества в зубной эмали, от чего зубы становятся непрочными, более чувствительными и более склонными к разрушению. Употребление напитков с высокой кислотностью на протяжении длительного времени (особенно маленькими глотками) в результате может привести к разрушению зубной эмали. Поэтому стоматологи рекомендуют пить газированные напитки через соломинку — тогда жидкость попадает сразу в заднюю часть полости рта и не вступает в контакт с зубами настолько агрессивно. Цель достигнута, поставленные задачи выполнены. Во время своей работы я познакомилась с двумя методами лабораторного анализа титриметрия и гравиметрия, научилась использовать их на практике. Список литературы: https://nsportal.ru/ap/library/nauchno-tekhnicheskoe-tvorchestvo/2011/08/28/izuchenie-kislotnosti-gazirovannykh-napitkov https://raven-yellow.livejournal.com/293852.html https://pikabu.ru/story/sdelano_v_sssr_legendarnaya_gazirovka_baykal_istoriya_sozdaniya_unikalnogo_napitka_iz_prirodnyikh_komponentov_napominanie_bayan_7927037 |
