Поверхностные явления. ), поверхность эритроцитов (25003800 м
 Скачать 16.79 Mb. Скачать 16.79 Mb.
|
|
ПРЕДИСЛОВИЕ В 1932 году выдающийся физико-химик Н.П.Песков писал: «Поверхность раздела – необычайно интересная вещь. Это и есть единство противоположностей. Молекулы, лежащие на поверхности, принадлежат обеим фазам. В этом смысле они сосредотачивают в себе все те противоположные свойства, которые имеются в этих фазах». Действительно, прилежащие слои резко отличаются по многим физико-химическим характеристикам (удельной энергии, плотности, электрической проводимости и др.) от свойств фаз в глубине их объема. Отличия связаны с определенной ориентацией молекул в поверхностных слоях и иным энергетическим состоянием их в сравнении с молекулами в объеме. Кроме того, в многокомпонентных системах (например, в растворах) состав поверхностного слоя, как правило, не совпадает с составом объемных фаз. Особенности поверхностных слоев обусловлены наличием избытка поверхностной энергии. Процессы, протекающие на границе раздела фаз, называются поверхностными. К ним относятся адсорбция, смачивание, адгезия. Изучение физических и химических взаимодействий в поверхностных слоях необходимо для развития многих областей науки и практики. Поверхностные явления используются, например, в гетерогенном катализе, очистке жидкостей, извлечении ценных ионов металлов из разбавленных растворов, печатании, сварке металлов, пищевой промышленности и т.д. Живые организмы представляют собой системы с очень развитыми поверхностями раздела, к которым относят кожные покровы (1,5-1,6 м2), поверхность эритроцитов (2500-3800 м2), поверхность капилляров печени (400 м2), поверхность альвеол (около 1000 м2) и т.д. Многие жизненно важные биохимические процессы в организме протекают на поверхности биологических мембран, поэтому для понимания их механизма необходимо знание основных закономерностей, которым подчиняются поверхностные явления. Важное значение поверхностных явлений для фармации определяется тем, что большинство лекарственных форм являются дисперсными системами с большой удельной поверхностью: порошки, таблетки, эмульсии, суспензии и т.д. Вопросы рациональной технологии, стабилизации, хранения, повышения эффективности терапевтического действия неразрывно связаны с исследованиями в области физикохимии поверхностных явлений. АДСОРБЦИЯ ПРИРОДА ПОВЕРХНОСТНОЙ ЭНЕРГИИ Поверхностный слой, возникающий на границе раздела различных фаз, согласно Гиббсу, представляет собой промежуточную фазу толщиной всего в несколько молекулярных диаметров. В ряде случаев поверхностный слой имеет толщину, примерно равную диаметру молекулы, и в этом случае его называют мономолекулярным. Поверхностными явлениями называют процессы, происходящие на границе раздела фаз и обусловленные особенностями состава и строения поверхностного слоя. Молекулы, атомы, ионы, находящиеся на поверхности раздела фаз, не равноценны по своему положению таким же частицам, находящимся в глубине фазы. Удобно рассмотреть в качестве примера систему, состоящую из жидкости и газа. 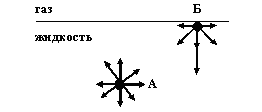 Рис. 1 Схема возникновения поверхностной энергии Молекула А (рис 1.) внутри жидкости окружена со всех сторон другими молекулами. Силы взаимодействия при этом взаимно уравновешиваются, равнодействующая равна нулю. У поверхностных молекул силы, действующие со стороны жидкой и газообразной фаз, неодинаковы. Молекулярные взаимодействия в вертикальном направлении не уравновешены. Вследствие этого равнодействующая молекулярных сил не равна нулю и направлена вглубь жидкой фазы. Эту силу часто называют внутренним давлением. Чем сильней различаются межмолекулярные взаимодействия в граничащих фазах, тем больше внутреннее давление. Для жидкостей на границе с воздухом внутреннее давление очень велико, например, для воды р = 14800 атм. Внутреннее давление стремится втянуть молекулу вглубь жидкости. Чтобы образовать межфазную поверхность, необходимо перевести часть молекул из объема жидкости на поверхность. Для этого надо совершить работу против внутреннего давления. Очевидно, что чем оно больше, тем больше энергии требуется затратить. Эта энергия сосредотачивается в молекулах, находящихся на поверхности, и называется свободной поверхностной энергией. Свободная поверхностная энергия зависит от количества частиц на поверхности раздела, а потому прямо пропорциональна площади раздела фаз и удельной энергии межфазной поверхности. F = σ · S при V, T – const G = σ · S при p, T – const где σ - удельная свободная поверхностная энергия, которая равна работе, которую надо совершить, чтобы увеличить площадь межфазной поверхности на единицу. Она зависит от природы контактирующих фаз и температуры. В зависимости от агрегатного состояния контактирующих фаз различают поверхностные явления для подвижной и неподвижной поверхности раздела. В системах газ-жидкость и жидкость-жидкость поверхность раздела подвижна, так как частицы поверхности раздела постоянно обновляются вследствие теплового движения молекул каждой фазы. Удельную свободную поверхностную энергию для подвижных поверхностей раздела фаз называют коэффициентом поверхностного натяжения и обозначают σг/ж или σж/ж, где [σ] = Дж/м2 или (Н·м)/м2 = Н/м. Существуют различные методы экспериментального определения поверхностного натяжения σ. Например: 1. Метод наибольшего давления образования пузырька,в котором измеряется давление, при котором пузырек газа проскакивает через воду (р0), а затем через исследуемую жидкость (рх). 2. Метод капиллярного поднятия. В нём измеряется высота h, на которую поднимается жидкость плотностью d по капилляру радиусом r.
Поверхностное натяжение характеризует различия в интенсивности межмолекулярных взаимодействий соприкасающихся фаз. Чем больше эти различия, тем больше σ. Для границы жидкость – воздух можно пренебречь межмолекулярными взаимодействиями в воздухе, и, значит, поверхностное натяжение характеризует интенсивность межмолекулярных сил в конденсированной фазе. В таблице 1 приведены значения σ некоторых веществ в жидком состоянии на границе с воздухом. Таблица 1 Поверхностное натяжение на границе с воздухом (t = 200С)
Поверхностное натяжение у различных жидкостей колеблется в значительных пределах (для полярных жидкостей σ больше, чем для неполярных) и зависит от температуры, давления, а для растворов и от концентрации растворенных веществ. Поверхностное натяжение биологических жидкостей используется в диагностических целях. Так, поверхностное натяжение плазмы крови подвержено значительным колебаниям при различных заболеваниях. С возрастом человека поверхностное натяжение сыворотки крови уменьшается. Поверхностное натяжение играет значительную роль в таких явлениях как деление клеток, фагоцитоз, пиноцитоз, изменение проницаемости клеточных мембран и др. В системах газ - твердое тело или жидкость - твердое тело поверхность раздела неподвижна. Удельную свободную поверхностную энергию (σг/тв, σж/тв) экспериментально определить трудно, но её значение можно оценить по способности твердой поверхности к смачиванию. Свободная поверхностная энергия при постоянном давлении совпадает с термодинамической функцией - энергией Гиббса, характеризующей состояние поверхности раздела фаз в гетерогенных системах. В соответствии со вторым законом термодинамики, все самопроизвольные процессы происходят в направлении, приводящем к уменьшению энергии Гиббса, поэтому и все поверхностные явления самопроизвольно протекают только в тех случаях, когда свободная поверхностная энергия системы уменьшается (∆G < 0). Поскольку свободная поверхностная энергия зависит от двух параметров - σ и S, то и все поверхностные явления совершаются самопроизвольно, если при этом снижается удельная свободная поверхностная энергия (∆σ < 0) или уменьшается площадь поверхности раздела фаз (∆S < 0), или происходит такое изменение этих величин, чтобы ∆G = ∆σ · ∆S < 0. К самопроизвольным поверхностным явлениям, которые сопровождаются уменьшением G за счет уменьшения площади поверхности, относятся: Коалесценция - слияние капель жидкости или пузырьков газа. Коагуляция - слипание частиц в дисперсных системах. К самопроизвольным поверхностным явлениям, сопровождающимся уменьшением G за счет снижения удельной свободной поверхностной энергии σ, относится сорбцияи её последствия: смачивание, эмульгирование и др. СОРБЦИЯ И ЕЁ ВИДЫ Процессы поглощения газов или растворенных веществ твердыми материалами или жидкостями носят общее название сорбции. Если сорбция идет только на поверхности, то её называют адсорбцией.Она приводит к увеличению концентрации вещества на границе раздела фаз. Если поглощаемое вещество диффундирует вглубь поглотителя, то явление называется абсорбцией. То вещество, на поверхности которого идет адсорбция, называется адсорбентом, а которое адсорбируется - адсорбатом (адсорбтивом). Адсорбцию Г обычно выражают соотношением количества адсорбата X, приходящегося на единицу площади адсорбента S (кмоль/м2) Г = X / S Если адсорбентом является твердое пористое тело, общую поверхность которого определить невозможно, то величину адсорбции Г относят к единице массы адсорбента m (кмоль/кг) Г = X / m Между адсорбентом и адсорбатом возникают адсорбционные силы. В зависимости от их природы рассматривают два крайних случая: физическуюи химическуюадсорбцию. Физическая адсорбциявозникает за счет Ван-дер-Ваальсовых взаимодействий. Она характеризуется
адсорбция ↔ десорбция, при котором скорости двух противоположных процессов становятся одинаковыми.
С физической адсорбцией связаны стабилизация дисперсных систем, стирка, ощущение вкуса, запаха и др. Химическая адсорбция (хемосорбция)является химическим процессом, поэтому
Примером является адсорбция кислорода на алюминии, приводящая к образованию поверхностной оксидной пленки. Уравнение адсорбции устанавливает функциональную связь величины адсорбции с равновесной концентрацией и температурой Г = f (С, Т), если адсорбция идет из растворов, и равновесным давлением и температурой Г = f (Р, Т), если адсорбируется газ. При постоянной температуре адсорбированное количество вещества есть функция равновесной концентрации Г = f (С)т или равновесного давления Г = f (Р)т. Графическая зависимость называется изотермой адсорбции и имеет вид кривой, на которой можно выделить три участка: I и III - прямолинейные, II - криволинейный.  Рис. 2 Изотерма мономолекулярной адсорбции ТЕОРИЯ МОНОМОЛЕКУЛЯРНОЙ АДСОРБЦИИ ЛЕНГМЮРА В настоящее время нет общей теории, которая достаточно корректно описывала бы все виды адсорбции на различных адсорбентах и разных поверхностях раздела фаз. Широкое применение нашла теория Ленгмюра о мономолекулярном слое. В основе её лежат следующие положения:
На основании приведенных положений было выведено уравнение изотермы локализованной адсорбции 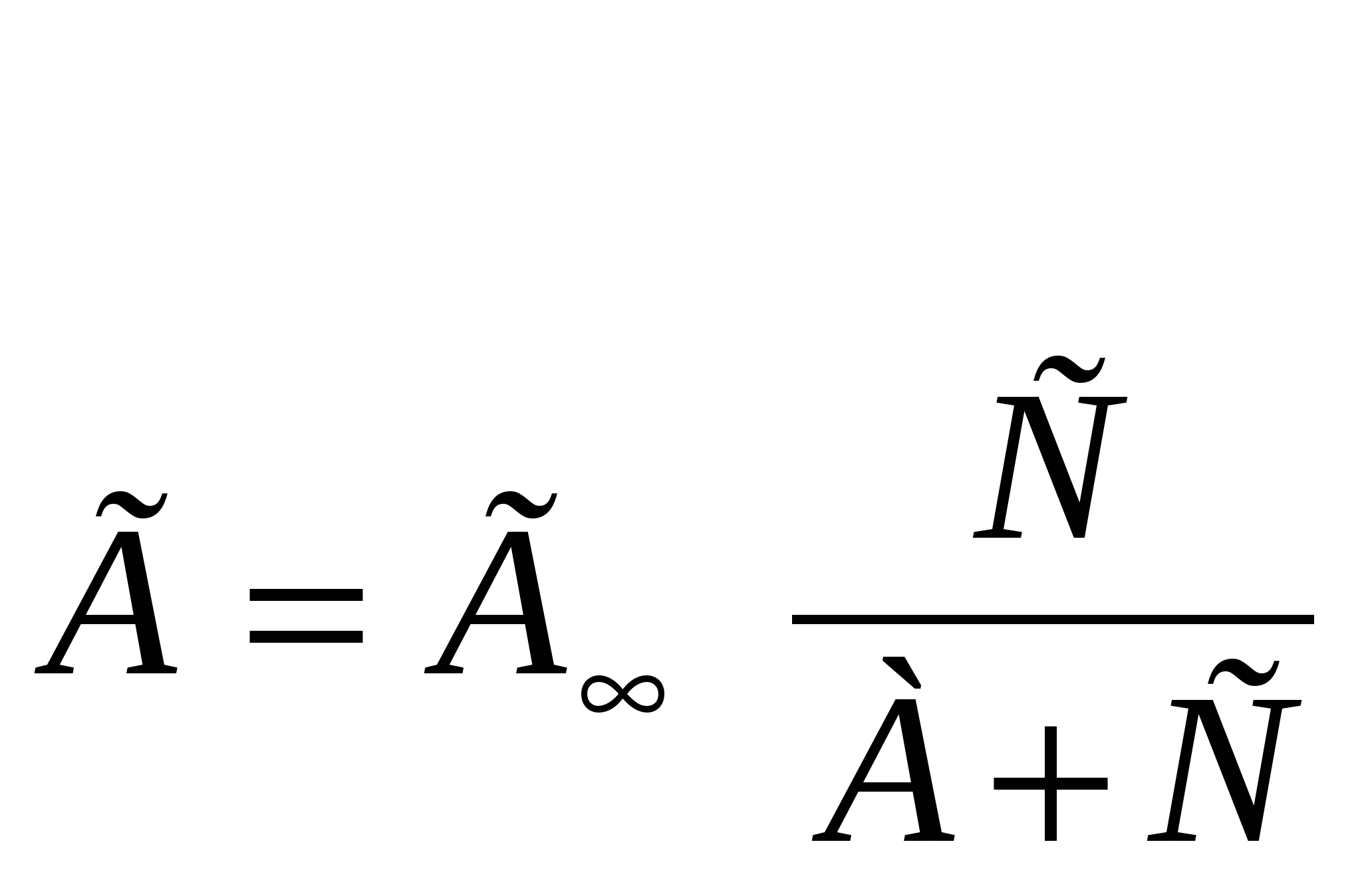 Где: С - равновесная концентрация, А - константа адсорбционного равновесия (отношение скоростей десорбции и адсорбции), Г∞- предельная адсорбция. Из уравнения следует, что:
что соответствует первому участку (I) изотермы адсорбции и отвечает относительно свободной поверхности адсорбента.
Константы в уравнении Ленгмюра находятся графическим методом, для чего исходное уравнение приводится к виду уравнения прямой:  Зависимость между 1/Г и 1/С (рис. 3) характеризуется прямой линией, тангенс угла наклона которой равен А/ Г∞, а отрезок, отсекаемый на оси ординат, равен 1/ Г∞. 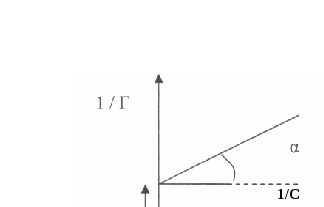 Рис. 3 Графическое определение коэффициентов А и Г∞ уравнения Ленгмюра Используя представления Ленгмюра о предельной величине адсорбции, можно рассчитать площадь поперечного сечения молекулы. Предельная адсорбция (Г∞) численно равна избыточному количеству вещества (моль), приходящемуся на единицу поверхности (м2). Произведение предельной адсорбции на постоянную Авогадро (Г∞ · Na) определяет число молекул, которое занимает единицу площади. Из этого следует, что площадь поперечного сечения молекулы в насыщенном адсорбционном слое можно рассчитать по уравнению Уравнение Ленгмюра пригодно как для описания адсорбции растворенных веществ, так и для адсорбции газов. В последнем случае концентрацию заменяют пропорциональной величиной - давлением газа. Наряду с мономолекулярной может наблюдаться полимолекулярная адсорбция, которая описывается теорией Поляни (1915 г). Брунауэр, Эммет и Теллер (1935 - 1940 г.) попытались обобщить представления Ленгмюра и Поляни и описать изотермы адсорбции различной формы с помощью одного уравнения (Теория БЭТ). ЗАКЛЮЧЕНИЕ Молекулы, находящиеся на поверхности раздела фаз, вследствие нескомпенсированности действующих на них сил, обладают повышенной энергией. Мерой поверхностной энергии является поверхностное натяжение (σ), равное термодинамически обратимой изотермической работе, которую необходимо совершить для увеличения площади межфазной поверхности на единицу. Чем сильней различаются межмолекулярные взаимодействия в граничащих фазах, тем больше поверхностное натяжение. Любые процессы протекают самопроизвольно, если они сопровождаются уменьшением свободной энергии. Это возможно либо за счет уменьшения величины межфазной поверхности, либо за счет уменьшения поверхностного натяжения. Стремление частиц принять сферическую форму, процессы коагуляции и коалесценции характерны для индивидуальных веществ, поверхностное натяжение которых постоянно. В тех случаях, когда постоянна площадь межфазной поверхности, самопроизвольно происходят процессы адсорбции – накопления в поверхностном слое частиц, понижающих поверхностное натяжение. |
