Экзамен эпу. экзамен эпу. 1 Гальванические элементы. Классификация. Назначение. Основные характеристики. Принцип работы
 Скачать 3.47 Mb. Скачать 3.47 Mb.
|
|
1 Гальванические элементы. Классификация. Назначение. Основные характеристики. Принцип работы . Гальванические элементы (ГЭ) – это первичные элементы, которые допускают лишь однократное использование заключенных в них активных элементов. Им свойственен только процесс разряда. Различают ГЭ сухие и с жидким электролитом. ГЭ любого типа состоит из двух разнородных электродов. Между этими электродами возникает разность потенциалов, которая зависит от материала электродов и состава электролита. Э  лемент Вольта состоит из сосуда с раствором Н2SO4 и двух электродов – цинкового и медного. Цинковый электрод в электролите растворяется. Под действием химических сил в электролит переходят ионы цинка. Эти ионы, соединяясь с отрицательным ионом SO4, образуют молекулы цинкового купороса ZnSO4. Электролит заряжается положительно. Свободные валентные электроны, остающиеся в цинке, заряжают цинковый электрод отрицательно. В области соприкосновения цинкового электрода с цинком образуется электрическое поле. Силы электрического поля направлены противоположно химическим силам, т.е. препятствуют растворению цинка. Если цепь разомкнута, то химические силы уравновешиваются силами электрического поля и процесс растворения цинка быстро прекращается. При этом между цинковым электродом и электролитом возникает определенная разность потенциалов, которая называется электродным потенциалом металла. Электродный потенциал цинка лемент Вольта состоит из сосуда с раствором Н2SO4 и двух электродов – цинкового и медного. Цинковый электрод в электролите растворяется. Под действием химических сил в электролит переходят ионы цинка. Эти ионы, соединяясь с отрицательным ионом SO4, образуют молекулы цинкового купороса ZnSO4. Электролит заряжается положительно. Свободные валентные электроны, остающиеся в цинке, заряжают цинковый электрод отрицательно. В области соприкосновения цинкового электрода с цинком образуется электрическое поле. Силы электрического поля направлены противоположно химическим силам, т.е. препятствуют растворению цинка. Если цепь разомкнута, то химические силы уравновешиваются силами электрического поля и процесс растворения цинка быстро прекращается. При этом между цинковым электродом и электролитом возникает определенная разность потенциалов, которая называется электродным потенциалом металла. Электродный потенциал цинка 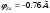 . Медный электрод нейтрализует часть ионов водорода электролита, отдавая им свободные электроны, поэтому получает положительный потенциал . Медный электрод нейтрализует часть ионов водорода электролита, отдавая им свободные электроны, поэтому получает положительный потенциал  . Следовательно, ЭДС элемента Вольта составляет: . Следовательно, ЭДС элемента Вольта составляет: . .ЭДС многих ГЭ находится в пределах 0,8÷1,6В. Поэтому для получения больших напряжений ГЭ соединяют последовательно. При замыкании внешней цепи валентные электроны цинка начинают перемещаться по проводнику r. При этом ослабляется электрическое поле между цинковым электродом и электролитом. Нарушается равновесие электрических и химических сил. В связи с этим под действием последних возобновляется процесс растворения цинка, перемещение ионов цинка и водорода к медному электроду, а ионы кислотного остатка – к цинковому электроду, т.е. осуществляется процесс разрядки ГЭ. Важной характеристикой качественной работы ГЭ является явления поляризации. Во время работы ГЭ происходит непрерывный процесс растворения отрицательного электрода, а к положительному электроду из электролита подходят ионы водорода, которые разряжаются на нем. При этом молекулы водорода на положительном электроде образуют непроводящий слой. Это явление называется поляризацией. В результате этого явления увеличивается внутреннее сопротивление элемента и снижается его напряжение. Для устранения поляризации в состав элемента вводят деполяризаторы, т.е. вещества, богатые кислородом, например, перекись марганца. Деполяризаторы превращают водород в воду и освобождают положительный электрод от непроводящего слоя водорода. Емкость и саморазряд ГЭ. Количество электричества, которое можно получить от элемента в течение разряда, называется емкостью первичного элемента:  где Ip – ток разряда (А); tp – время разряда (ч). где Ip – ток разряда (А); tp – время разряда (ч). Емкость первичного элемента зависит от количества заложенных в него активных веществ, разрядного тока, режима разряда, температуры электролита и времени хранения. Увеличение разрядности тока ухудшает процесс деполяризации. Активные вещества, заложенные в элемент, используются не полностью. В результате снижается емкость элементов. Для улучшения условий эксплуатации ГЭ рекомендуется производить перерывы разрядного тока, что будет улучшать процесс деполяризации и способствовать увеличению емкости ГЭ. С увеличением температуры электролита химические процессы в элементах протекают более интенсивно и емкость электролита возрастает. Однако при слишком высоких температурах происходит высыхание электролита и снижение емкости. Даже при отключенной нагрузке в ГЭ происходит процесс саморазряда, т.е. бесполезный расход его активных веществ. Саморазряд элемента вызывается несовершенством изоляции между электродами и образованием на отрицательном электроде местных гальванических пар в местах вкрапления в электрод посторонних примесей. Саморазряд увеличивается при установке элемента в сыром месте, при загрязнении его пылью и грязью. Номинальная или гарантированная емкость элемента. Номинальная емкость элемента – минимально допустимая емкость, которую должен отдавать элемент в режиме работы, указанном заводом-изготовителем. Фактическая емкость обычно превосходит на 10-20% его номинальную. Номинальная емкость марганцево-цинкового элемента определяется при непрерывном разряде на R=10 Ом и t=15÷30 ºC до напряжения 0,7 В и определяется выражением: 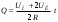 , где UН – начальное напряжение, измеренное на зажимах элемента в течение первых 10с после начала разряда; UК – конечное напряжение разряда (0,7 В); R – сопротивление разрядной цепи (10 Ом);T – время разряда. , где UН – начальное напряжение, измеренное на зажимах элемента в течение первых 10с после начала разряда; UК – конечное напряжение разряда (0,7 В); R – сопротивление разрядной цепи (10 Ом);T – время разряда.При повышении температуры внешней цепи интенсивность электрохимических процессов возрастает, что приводит к увеличению саморазрядов элементов, а это приводит к быстрому уменьшению их емкости. Зависимость емкости элемента от температуры определяется следующим выражением: 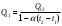 ,где t1 – начальная температура; t2 – конечная температура; α – темпера-турный коэффициент емкости. ,где t1 – начальная температура; t2 – конечная температура; α – темпера-турный коэффициент емкости.Электрическим аккумулятором называют химический источник тока, который обладает способностью накапливать (аккумулировать) электрическую энергию и отдавать ее по мере надобности. 2. Свинцовые аккумуляторы (Pb). Классификация. Назначение. Основные характеристики. Принцип работы . Реагентами в свинцовых аккумуляторах служат диоксид свинца (PbO2) и свинец (Pb), электролитом - раствор серной кислоты. Их разделяют на четыре основные группы; стартерные, стационарные, тяговые и портативные (герметизированные). Наиболее распространенные из свинцовых аккумуляторов - стартерные аккумуляторы, предназначены для запуска двигателей внутреннего сгорания и энергообеспечения устройств машин. Стационарные аккумуляторы используются в энергетике, на телефонных станциях, в телекоммуникационных системах, в качестве аварийного источника тока и т.д. Обычно они работают в режиме непрерывного подзаряда. Относятся к недорогим аккумуляторам. Тяговые аккумуляторы предназначены для электроснабжения подъемников, шахтных электровозов, электромобилей и других машин. Действуют в режимах глубокого разряда, имеют большой ресурс и низкую стоимость. Портативные (герметизированные) свинцовые аккумуляторы используются для питания приборов, инструмента, аварийного освещения. К их достоинствам относятся более низкая стоимость по сравнению со стоимостью других портативных аккумуляторов, широкий интервал рабочих температур. Недостатками кислотных аккумуляторов являются невозможность хранения в разряженном состоянии, трудность изготовления аккумуляторов малых размеров Принцип действия свинцового аккумулятора П  ростейший свинцовый аккумулятор имеет вид: состоит из двух свинцовый пластин, погруженных в водный раствор серной кислоты. Положительная пластина покрывается перекисью свинца PbO2, а отрицательная пластина состоит из губчатого свинца Pb. Перекись свинца и губчатый свинец являются активными веществами кислотного аккумулятора. Молекулы серной кислоты под действием растворителя распадаются на положительные ионы водорода и отрицательные ионы кислотного остатка SO4. Если к зажимам аккумулятора подсоединить нагрузку r, то аккумулятор начинает разряжаться. Положительные ионы водорода перемещаются к пластине с перекисью свинца и разряжаются на ней. Образующиеся при этом нейтральные молекулы водорода вступают в реакцию с активной массой перекиси свинца. ростейший свинцовый аккумулятор имеет вид: состоит из двух свинцовый пластин, погруженных в водный раствор серной кислоты. Положительная пластина покрывается перекисью свинца PbO2, а отрицательная пластина состоит из губчатого свинца Pb. Перекись свинца и губчатый свинец являются активными веществами кислотного аккумулятора. Молекулы серной кислоты под действием растворителя распадаются на положительные ионы водорода и отрицательные ионы кислотного остатка SO4. Если к зажимам аккумулятора подсоединить нагрузку r, то аккумулятор начинает разряжаться. Положительные ионы водорода перемещаются к пластине с перекисью свинца и разряжаются на ней. Образующиеся при этом нейтральные молекулы водорода вступают в реакцию с активной массой перекиси свинца. Таким образом, при разряде аккумулятора на положительной и отрицательной пластинах образуется серно-кислый свинец PbSO4. При образовании PbSO4 расходуется часть находящейся в электролите кислоты. Поэтому разряд аккумулятора сопровождается уменьшением плотности электролита. При глубоком разряде PbSO4 превращается в твердую крупно-кристаллическую соль, которая плохо восстанавливается в процессе заряда. Поэтому необходимо аккумуляторы разряжать до определенной плотности электролита. Заряд аккумуляторной батареи осуществляется постоянным током. При заряде аккумуляторной батареи постоянный ток от выпрямителя поступает на положительную пластину, и далее через электролит на отрицательную. На положительную пластину будут поступать отрицательные ионы SO2-, а к отрицательной пластине будут стремиться положительные ионы водорода 2Н+. После разряда ионы нейтрализуются и вступают в химическую реакцию с активной массой. Масса положительной и отрицательной пластин восстанавливается, а плотность электролита увеличивается. ЭДС и напряжение свинцового аккумулятора Активные вещества положительных и отрицательных пластин обладают определенными потенциалами относительно электролита. Разность этих потенциалов определяет ЭДС аккумулятора, которая не зависит от количества активного вещества в пластинах. ЭДС аккумулятора зависит в основном от плотности электролита, эта зависимость определяется эмпирической формулой: E = 0,85 + d, где d – плотность электролита в порах активной массы пластин. Напряжение аккумулятора при заряде больше, чем величина ЭДС, на величину внутреннего падения напряжения: UЗ = E + IЗ ∙ r0, где r0 – внутреннее сопротивление аккумулятора, а при разряде соответственно: UР = E – IР ∙ r0. ЭДС разряженного аккумулятора при отключенной нагрузке мало отличается от ЭДС заряженного аккумулятора. Емкость свинцового аккумулятора Номинальная емкость определяется при десятичасовом разряде до напряжения 1,8 В, при температуре электролита 25°С. Номинальная емкость свинцового аккумулятора составляет 36 А/ч. Этой емкости соответствует ток разряда IР = Q/10 = 3,6 А. Если изменить ток разряда IР и температуру электролита, то изменится и его емкость. Повышение температуры окружающей среды способствует повышению емкости, но при температуре 40°С происходит коробление положительных пластин и резко увеличивается саморазряд аккумулятора, поэтому для нормальной эксплуатации аккумулятора должна поддерживаться температура + 35°С – 15°С. Номинальная емкость при температуре 25°С и десятичасовом разряде определяется формулой: 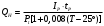 где Pt – коэффициент использования активной массы аккумулятора, %; Т – фактическая температура электролита при разряде. 3 Топливные элементы  ТЭ относятся к числу химических источников электрической энергии. В качестве активный веществ, вступающих в химическую реакцию в ТЭ, используется твердое, жидкое или газообразное топливо (древесный уголь, нефтепродукты, спирты, водород и т.д.) схематическое устройство ТЭ рассмотрим на основе водородно-кислотного ТЭ. ТЭ относятся к числу химических источников электрической энергии. В качестве активный веществ, вступающих в химическую реакцию в ТЭ, используется твердое, жидкое или газообразное топливо (древесный уголь, нефтепродукты, спирты, водород и т.д.) схематическое устройство ТЭ рассмотрим на основе водородно-кислотного ТЭ.Данный ТЭ состоит из положительного 1 и отрицательного 3 электродов, погруженных в щелочной электролит 2. Активным материалом положительного электрода является кислород O2, а отрицательного – водород Н2. Электроды ТЭ в реакциях активно не участвуют и в процессе работы не разрушаются, поэтому ТЭ обеспечивают непосредственное преобразование химической энергии в электрическую очень длительное время, пока идет активная подача веществ к его электродам. Расчеты показывают, что топливные элементы могут иметь очень высокие удельные характеристики, мощность и КПД. Принцип действия: Активные вещества подаются к электродам через пористые трубки. Водород вступает в соединение с ионами гидроксила электролита. В результате образуется вода и свободные электроны. С водородного электрода свободные электроны перемещаются к кислородному электроду через нагрузку r. В пористом положительном электроде 1 кислород вступает в реакцию с водой электролита, образуя ионы гидроксильного остатка. В результате в замкнутой цепи возникает электрический ток. Расход воды Н2О в элементы восполняет водород, а расход гидроксила ОН- восполняет кислород. Рассмотренный химический процесс противоположен процессу электролитического разложения воды, где при пропускании тока через электролит вновь образуется кислород и водород. Этим объясняется высокий уровень КПД при выработке электрической энергии. 4. Автономная система электропитания. Структурная схема. Назначение. Основные характеристики Систему питания от первичных элементов в основном используют для обеспечения работы переносной аппаратуры (радиостанций, измерительной аппаратуры и др.). Для питания стационарной аппаратуры автономную систему питания применяют в местах, где отсутствуют сети переменного тока. Система питания от аккумуляторов по способу «заряд-разряд» (рис. 2.2) предназначена для случаев, когда энергия от сетей переменного тока подается нерегулярно. Сущность этого способа питания заключается в том, что для каждой градации напряжения имеется отдельный выпрямитель  и две (или более) аккумуляторные батареи и две (или более) аккумуляторные батареи . От одной батареи питается аппаратура, а другая заряжается от выпрямителя или находится в резерве заряженной. Как только батарея разрядится до определенного состояния, ее отключают и подсоединяют к выпрямителю для заряда, а для питания аппаратуры подключают заряженную батарею. При работе по этому способу аккумуляторы чаще всего заряжаются в режиме неизменяющегося тока. Емкость аккумуляторов определяется исходя из продолжительности питания аппаратуры в течение 12 -24 ч, поэтому аккумуляторные батареи очень громоздкие и для их установки требуются специально оборудованные помещения больших размеров. Срок службы таких аккумуляторов 6-7 лет, так как глубокие и частые циклы заряда и разряда приводят к быстрому разрушению пластин. Необходимость постоянного наблюдения за процессами заряда и разряда приводит к большим эксплуатационным расходам. . От одной батареи питается аппаратура, а другая заряжается от выпрямителя или находится в резерве заряженной. Как только батарея разрядится до определенного состояния, ее отключают и подсоединяют к выпрямителю для заряда, а для питания аппаратуры подключают заряженную батарею. При работе по этому способу аккумуляторы чаще всего заряжаются в режиме неизменяющегося тока. Емкость аккумуляторов определяется исходя из продолжительности питания аппаратуры в течение 12 -24 ч, поэтому аккумуляторные батареи очень громоздкие и для их установки требуются специально оборудованные помещения больших размеров. Срок службы таких аккумуляторов 6-7 лет, так как глубокие и частые циклы заряда и разряда приводят к быстрому разрушению пластин. Необходимость постоянного наблюдения за процессами заряда и разряда приводит к большим эксплуатационным расходам.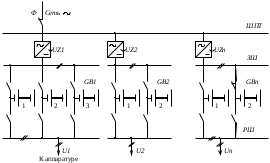 Рис.2.2. Схема системы питания от аккумуляторов по способу «заряд – разряд»:Ф – фидер; ШПТ – шина переменного тока; ЗШ – зарядные шины; РШ–рязрядные шины; 1, 2, 3 – группы аккумуляторов Перечисленные недостатки наряду с низким к. п. д. установки (30-45%) ограничивают использование этого режима. К достоинствам способа относятся отсутствие пульсации напряжения на нагрузке и возможность использования для заряда различных источников тока. 5. Буферная система электропитания. Режим среднего тока. Назначение. Основные характеристики. БСП - система питания, когда параллельно выпрямителю UZи нагрузке включена аккумуляторная батарея GB(рис. 2.3). В случае аварии в сети переменного тока или повреждения выпрямителя дальнейшее питание нагрузки обеспечивает батарея без перерыва в подаче энергии. Аккумуляторная батарея обеспечивает надежное резервирование источников электрической энергии, и, кроме того, она совместно с фильтром питания осуществляет необходимое сглаживание пульсации. При буферной системе питания различают три режима работы: среднего тока, импульсного и непрерывного подзаряда. 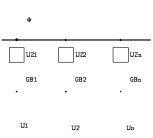 Рисунок 2.3 – Схема буферной системы питания Рисунок 2.3 – Схема буферной системы питанияПри режиме среднего тока (рис. 2.4) выпрямитель UZ, включенный параллельно с аккумуляторной батареей GВ, обеспечивает постоянный ток Iв независимо от изменения тока Iн в нагрузке Rн. Когда ток нагрузки Iн мал, выпрямитель питает нагрузку и заряжает аккумуляторную батарею током I3, а когда ток нагрузки велик, выпрямитель совместно с батареей, которая разряжается током Iр, питает нагрузку. Для осуществления данного режима могут быть использованы простейшие выпрямители без устройств автоматической регулировки. Ток выпрямителя рассчитывают исходя из количества электрической энергии (ампер-часы), затрачиваемой на питание нагрузки в течение суток. Это значение должно быть увеличено на 15-25% для компенсации потерь, которые всегда существуют при заряде и разряде аккумуляторов 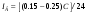 К недостаткам режима относятся: невозможность точно определить и установить необходимый ток выпрямителя, так как действительный характер изменения тока нагрузки никогда точно неизвестен, что приводит к недозаряду или перезаряду аккумуляторов; небольшой срок службы аккумуляторов (8-9 лет), вызываемый глубокими циклами заряда и разряда; значительные колебания напряжения на нагрузке, так как напряжение на каждом аккумуляторе может изменяться от 2 до 2,7 В.  Рисунок 2.4 – Режим среднего тока: а – схема; б – диаграмма токов; в – зависимости токов и напряжений от времени; IЗ и IР – соответственно токи заряда и разряда аккумуляторной батареи Рисунок 2.4 – Режим среднего тока: а – схема; б – диаграмма токов; в – зависимости токов и напряжений от времени; IЗ и IР – соответственно токи заряда и разряда аккумуляторной батареи6. Буферная система электропитания. Режим импульсного подзаряда. Назначение. Основные характеристики. При такой системе питания параллельно выпрямителю UZи нагрузке включена аккумуляторная батарея GB(рис. 2.3). В случае аварии в сети переменного тока или повреждения выпрямителя дальнейшее питание нагрузки обеспечивает батарея без перерыва в подаче энергии. Аккумуляторная батарея обеспечивает надежное резервирование источников электрической энергии, и, кроме того, она совместно с фильтром питания осуществляет необходимое сглаживание пульсации. При буферной системе питания различают три режима работы: среднего тока, импульсного и непрерывного подзаряда.  Рисунок 2.3 – Схема буферной системы питания Рисунок 2.3 – Схема буферной системы питания |
