Аминокислоты и Белки. 1. Какие вещества называют аминокислотами, а какие белками Что общего между этими классами органических соединений
 Скачать 250.3 Kb. Скачать 250.3 Kb.
|
|
1.Какие вещества называют аминокислотами, а какие белками? Что общего между этими классами органических соединений Аминокислоты – органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы. Белки – высокомолекулярные органические вещества, состоящие из альфа-аминокислот, соединенных в цепочку пептидной связью. Общее между классами данных веществ: качественный состав. Белки состоят из аминокислот. 2.Какими свойствами обладают аминокислоты? Напишите уравнения реакций, характеризующих химические свойства аланина С кислотами: NH2-CH2-COOH+HCL-HCL·NH2-CH2-COOH(хлороводородная соль глицина) Со щелчами: NH2-CH2-COOH+NaOH-H2O+NH2-CH2-COONa(натриевая соль глицина) Этерификация: NH2-CH2-COOH+CH3OH-H2O+NH2-CH2-COOCH3(метиловый эфир глицина) Реакция образования пептидов: HOOC-CH2-NH-H+HOOC-CH2-NH2-HOOC-CH2-NH-CO-CH2-NH2+H2O 3. Назовите области применения аминокислот? Производство нейлона, капрона, энанта.Аминокислоты входят в состав спортивного питания и комбикорма. Аминокислоты применяются в пищевой промышленности в качестве вкусовых добавок, например, натриевая соль глутаминовой кислоты. 4.Охарактеризуйте три структуры белка. 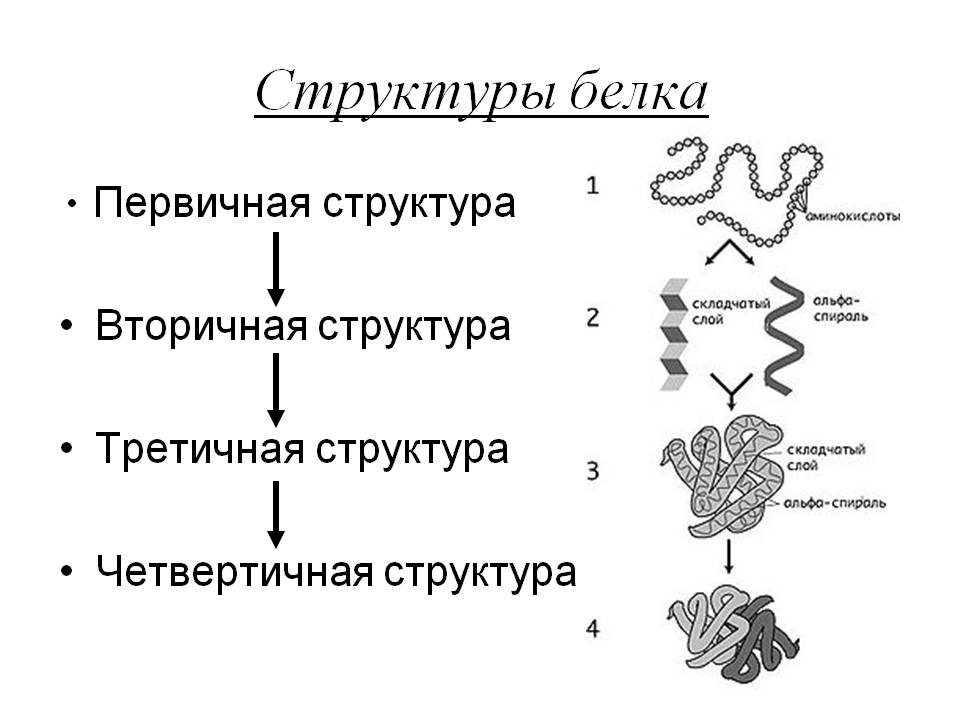 Первичная структура — последовательность аминокислот в полипептидной цепи. Важными особенностями первичной структуры являются консервативные мотивы — сочетания аминокислот, играющих ключевую роль в функциях белка. Консервативные мотивы сохраняются в процессе эволюции видов, по ним часто удаётся предсказать функцию неизвестного белка. Вторичная структура — локальное упорядочивание фрагмента полипептидной цепи, стабилизированное водородными связями меду атомами кислорода и водорода и пептидных групп одной полипептидной цепи. Третичная структура — пространственное строение полипептидной цепи (набор пространственных координат составляющих белок атомов). Структурно состоит из элементов вторичной структуры, стабилизированных различными типами взаимодействий, в которых гидрофобные взаимодействия играют важнейшую роль. В стабилизации третичной структуры принимают участие. Четвертичная структура (или субъединичная, доменная) — взаимное расположение нескольких полипептидных цепей в составе единого белкового комплекса. Белковые молекулы, входящие в состав белка с четвертичной структурой, образуются на рибосомах по отдельности и лишь после окончания синтеза образуют общую надмолекулярную структуру. В состав белка с четвертичной структурой могут входить как идентичные, так и различающиеся полипептидные цепочки. В стабилизации четвертичной структуры принимают участие те же типы взаимодействий, что и в стабилизации третичной. Надмолекулярные белковые комплексы могут состоять из десятков молекул. 5. Какие химические свойства характерны для белков Для белков наиболее характерны реакции гидролиз (разрушение полипептидной цепочки с образованием более простых фрагментов), денатурация (разрушение пространственной структуры белка), ксантопротеиновая и биуретова реакции. 6. Что такое денатурация? Какие внешние факторы могут вызвать ее Денатурация – это необратимое разрушение третичной и вторичной структуры белка. Практически любое заметное изменение внешних условий, например, нагревание или существенное изменение pH приводит к последовательному нарушению четвертичной, третичной и вторичной структур белка. Обычно денатурация вызывается повышением температуры, действием сильных кислот и щелочей, солей тяжелых металлов, некоторых растворителей (спирт), радиации и др. 7. Как с помощью одного и того же реактива распознать растворы трех веществ: белка, глюкозы и глицерина Гидроксид меди (II). При добавлении к белку дает фиолетовое окрашивание, при сдобавлении к глюкозе и глицерину – синее. Если пробирку с раствором глюкозы нагреть, то происходит обесцвечивание раствора и выпадение красного осадка. 8. Запишите уравнения реакций, с помощью которых можно осуществить следующие превращения: этан → этилен → этиловый спирт → уксусный альдегид → уксусная кислота → хлоруксусная кислота → аминоуксусная кислота → полипептид  |
