РК № 2-1. 1 Классификация углеводов
 Скачать 1.85 Mb. Скачать 1.85 Mb.
|
: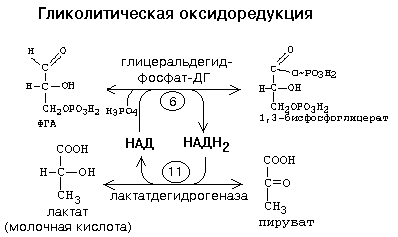 Реакции гликолитической оксидоредукции полностью обратимы. В отсутствие кислорода сколько НАДН2 образуется на 6-й стадии, столько же НАДН2 и отдаст свой водород на ПВК. Поэтому в анаэробных условиях конечным продуктом распада глюкозы является ЛАКТАТ. Процесс распада глюкозы до лактата в анаэробных условиях называется ГЛИКОЛИЗОМ, а гликогена - ГЛИКОГЕНОЛИЗОМ. Таким образом, ГЛИКОЛИТИЧЕСКАЯ ОКСИДОРЕДУКЦИЯ - это сопряжение между 6-й стадией (окисление ФГА) и 11-й стадией (восстановление ПВК до лактата) гликолиза. В состоянии покоя, наступающего после интенсивной мыщечной работы, в клетку начинает поступать кислород. Это приводит к запуску митохондриальных дыхательных цепей. Запускаются окислительное декарбоксилирование пирувата, ЦТК и челночный механизм переноса водорода в митохондрии, а, значит, и ГБФ-путь распада глюкозы (гликогена). При этом процесс гликолиза тормозится автоматически. Торможение гликолиза поступившим в клетку кислородом называется ЭФФЕКТОМ ПАСТЕРА по имени ученого, открывшего это явление. 2 ключевых ферментов — гликогенсинтазы и гликогенфосфорилазы - с помощью их фосфорилирования и дефосфорилирования. -7- Глюконегенез. Биологическое значение. Глюконеогенез — это процесс синтеза глюкозы из веществ неуглеводной природы. У млекопитающих эту функцию выполняет в основном печень, в меньшей мере - почки и клетки слизистой кишечника. Главными субстратами глюконеогенеза являются пируват, лактат, глицерин, аминокислоты Глюконеогенез обеспечивает потребности организма в глюкозе в тех случаях, когда диета содержит недостаточное количество углеводов (физическая нагрузка, голодание). Постоянное поступление глюкозы особенно необходимо для нервной системы и эритроцитов. При понижении концентрации глюкозы в крови ниже определенного критического уровня нарушается функционирование мозга; при тяжелой гипогликемии возникает коматозное состояние и может наступить летальный исход.Запасов гликогена в организме достаточно для удовлетворения потребностей в глюкозе в период между приемами пищи. При углеводном или полном голодании, а также в условиях длительной физической работы концентрация глюкозы в крови поддерживается за счет глюконеогенеза. В этот процесс могут быть вовлечены вещества, которые способны превратиться в пируват или любой другой метаболит глюконеогенеза.Семь реакций гликолиза легко обратимы и используются в глюконеогенезе. Но три киназные реакции необратимы и должны шунтироваться (рис. 12). Так, фруктозо-1,6-дифосфат и глюкозо-6-фосфат дефосфорилируются специфическими фосфатазами, а пируват фосфорилируется до образования фосфоенолпирувата посредством двух промежуточных стадий через оксалоацетат. Образование оксалоацетата катализируется пируваткарбоксилазой. Этот фермент содержит в качестве кофермента биотин. Оксалоацетат образуется в митохондриях, транспортируется в цитозоль и включается в глюконеогенез. Следует обратить внимание на то, что каждая из необратимых реакций гликолиза вместе с соответствующей ей необратимой реакцией глюконеогенеза составляют цикл, называемый субстратным:Таких циклов существует три - соответственно трем необратимым реакциям. Эти циклы служат точками приложения регуляторных механизмов, в результате чего изменяется поток метаболитов либо по пути распада глюкозы, либо по пути ее синтеза. -8- Окислетильный этап пентозофосфатный пути превращения глюкозы.Значение окислительного этапа ГМФ-пути. Протекает в цитоплазме. Состоит из 2-х этапов: 1. Окислительный. 2. Неокислительный . Весь пентозофосфатный путь заключается в том, что молекулы глюкозы превращаются в молекулы глюкозо-6-фосфата, каждая из которых два раза окисляется и дает молекулу рибозо-5-фосфата, 2 молекулы НАДФН2 и 1 молекулу СО2. (окислительный этап). Значение окислительного этапа пентозофосфатного пути 1.Один из главных источников НАДФН2 для клетки. Образуется этот НАДФН2 в цитоплазме, поэтому он не передает свой водород по системе митохондриального окисления на кислород и АТФ не образуется. Он отдает свой водород на синтез жирных кислот, холестерина и других стероидов, а также на монооксигеназные реакции. 2. Образуются пентозы - строительный материалом для синтеза нуклеотидов, коферментов и некоторых других веществ. 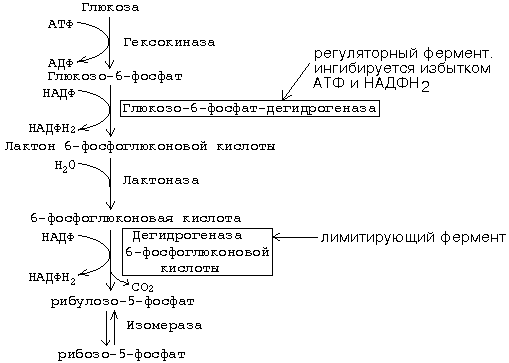 Скорость пентозофосфатного пути определяется либо 6-фосфоглюконат-дегидрогеназой, либо (когда много НАДФН2 и АТФ) - глюкозо-6-фосфат-дегидрогеназой. Реакции пентозофосфатного пути регулируются генетически на уровне биосинтеза этих ферментов. Пентозофосфатный путь существует не во всех типах клеток. Наиболее интенсивно пентозофосфатный путь протекает в печени, эритроцитах, надпочечниках, половых железах, жировой ткани и молочной железе. Но даже в этих тканях пентозофосфатный путь расщепляется не более 25-30% глюкозы. Почему в этих тканях пентозофосфатный путь имеет такое значение? Потому что клеткам этих тканей нужно много НАДФН2. -9- 10.Неокислительный этап пентозофосфатного пути превращения глюкозы.Значение неокислительного этапа ГМФ-пути. Протекает в цитоплазме. Состоит из 2-х этапов: 1. Окислительный. 2. Неокислительный . Неокислительный этап – это совокупность большого количества обратимых реакций. Каждая из них - это перенос 2-х или 3-х углеродного фрагмента с одного моносахарида на другой. Между моносахаридами происходит взаимный обмен частями своих молекул. При этом из пентозофосфатов, вступающих в реакцию, образуются моносахариды с разным числом углеродных атомов. Это триозы (например, фосфоглицериновый альдегид (ФГА)), тетрозы, гексозы, гептозы. Реакции неокислительного этапа катализируются ферментами трансальдолазами и транскетолазами. В состав кофермента транскетолаз входит витамин В1. В результате 6 молекул рибозо-5-фосфата превращаются в 5 молекул глюкозо-6-фосфата. Эти 5 молекул глюкозо-6-фосфата вместе с еще одной, поступающей дополнительно, опять вступают в пентозофосфатный путь. Получается цикл. На каждом его "обороте" происходит частичное окисление 6-ти молекул глюкозо-6-фосфата, то есть 5 молекул глюкозо-6-фосфата остаются нетронутыми, а одна молекула полностью расщепляется до СО2 и Н2О. Значение неокислительного этапа пентозофосфатного пути 1.Является источником моносахаридов с разным числом углеродных атомов. Это строительный материал для разных синтезов, в том числе для синтезов различных олигосахаридов, которые входят в состав различных клеточных рецепторов. 2 Образующийся фосфоглицериновый альдегид является точкой сопряжения между пентозофосфатным путем и некоторыми другими путями метаболизма. Например: он может восстанавливаться до фосфоглицерина, который нужен для синтеза жиров. 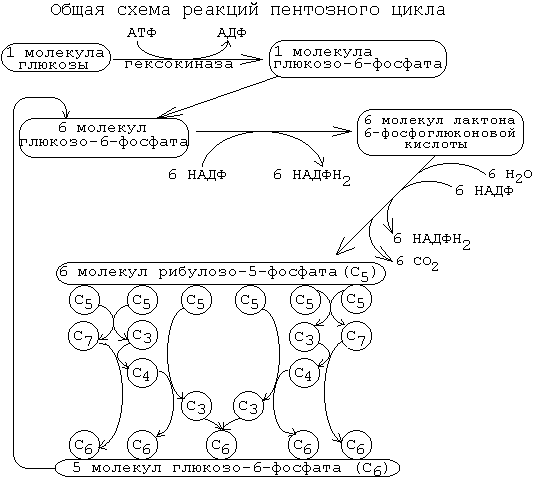 Пентозофосфатный путь существует не во всех типах клеток. Наиболее интенсивно пентозофосфатный путь протекает в печени, эритроцитах, надпочечниках, половых железах, жировой ткани и молочной железе. Но даже в этих тканях пентозофосфатный путь расщепляется не более 25-30% глюкозы. Почему в этих тканях пентозофосфатный путь имеет такое значение? Потому что клеткам этих тканей нужно много НАДФН2. -10- Синтез гликогена Гликоген синтезируется в период пищеварения (1—2 ч после приема углеводной пищи). Синтез гликогена требует энергии. Глюкоза, поступающая в клетку, фосфорилируется при участии АТФ.Затем глюкозо-6-фосфат в ходе обратимой реакции превращается в глюкозо-1-фосфат под действием фермента фосфоглюкомутазы. После изомеризации глюкозо-6-фосфата в глюкозо-1-фосфат протекает дополнительная активация глюкозного фрагмента. При этом расходуется 1 молекула УТФ, что эквивалентно расходованию 1-й молекулы АТФ. В результате образуется активированная форма - УДФ-глюкоза. Затем с УДФ глюкозный остаток переносится на молекулу гликогена. Удлинение цепи гликогена катализирует фермент гликогенсинтетаза. Таким образом, цепь гликогена становится на 1 глюкозный фрагмент длиннее. Гликоген, в отличие от растительного крахмала, более сильно разветвлен. Для формирования ответвлений существует специальный фермент, который называется "гликогенветвящий фермент" . Молекула гликогена синтезируется не с "нуля", а происходит постепенное удлинение уже имеющегося кусочка цепи: "затравки" или праймера. И при распаде гликогена никогда не происходит полного разрушения его молекул. Для включения одного остатка глюкозы в молекулу гликогена клетка расходует 2 молекулы АТФ. При распаде гликогена эта АТФ не регенерирует, а освобождается только Фн (неорганический фосфат). Ключевым ферментом синтеза гликогена является гликогенсинтаза. Это "пункт вторичного контроля" (рис. 5). Регуляция гликогенсинтазы: она активируется избытком глюкозо-6-фосфата. Поэтому если глюкозо-6-фосфат другими путями утилизируется медленно, то возрастание его концентрации приводит к увеличению скорости синтеза гликогена. Реакция, катализируемая гликогенсинтазой, необратима. -11- Распад гликогена Мобилизация гликогена происходит в основном в период между приемами пищи и ускоряется во врем физической работы. Этот процесс происходит путем последовательного отщепления остатков глюкозы в виде глюкозо-1-фосфата с помощью гликогенфосфорилазы. Этот фермент не расщепляет 1,6-гликозидные связи в местах разветвлений, поэтому необходимы еще 2 фермента, после действия которых глюкозный остаток в точке ветвления освобождается в форме свободной глюкозы. Гликоген распадается до глюкозо-6-фосфата без затрат АТР. Далее глюкозо-6-фосфат включается в процесс катаболизма или другие метаболические пути.В печени(но не в мышцах) глюкозо-6-фосфат может гидролизоваться с образованием глюкозы, которая выделяется в кровь.Эту реакцию катализирует фермент глюкозо-6-фосфатаза. Реакция протекает в просвете ЭР(эндоплазматический ретикулум), куда с помощью специального белка транспортируется глюкозо-6-фосфат.Фермент локализован на мембране ЭР таким образом, что его активный центр обращен в просвет ЭР.Продукты гидролиза (глюкоза и неорганический фосфат) возвращаются в цитоплазму также с помощью транспортных систем. 2 ключевых ферментов — гликогенсинтазы и гликогенфосфорилазы - с помощью их фосфорилирования и дефосфорилирования. -12- Обмен галактозы.Нарушение обмена галактозы. Галактоза образуется в кишечнике в результате гидролиза лактозы.Чтобы превратить галактозу в глюкозу, необходимо изменить оптическую конфигурацию Н и ОН групп С4 атома в галактозе,т.е. провести реакцию эпимеризации.  Обмен галактозы особенно интересен в связи с наследственным заболеванием галактоземией. Галактоземия — это результат нарушения обмена галактозы, обусловленное наследственным дефектом любого из трех ферментов, включающих галактозу в метаболизм. Галактоземия вследствие недостаточности галактозил-1-фосфат-уридилтрансферазы (ГАЛТ) известна наиболее хорошо. Заболевание проявляется очень рано, особенно тяжело протекает у детей, так как основным источником углеводов служит грудное молоко, содержащее лактозу. Ранними симптомами являются рвота, диарея, дегидратация, снижение массы тела, желтуха. В крови, моче и тканях повышается концентрация галактозы и галактозо-1-фосфата. В тканях глаза (в хрусталике) галактоза восстанавливается алдольредуктазой с образованием галактитола. В качестве донора водорода в этой реакции используется HADPH + Н+ Восстановление галактозы характерно и для нормального метаболизма, но протекает с небольшой скоростью. При галактоземии галактитол накапливается в стекловидном теле и связывает большое количество воды. (развитие катаракты) Серьезные изменения наблюдаются в печени в связи с накоплением галактозо-1-фосфата. Нарушается функция печени, отмечаются гепатомегалия, жировая дистрофия, околодольчатый некроз. В почках у таких больных повышена концентрация галактитола и галактозо-1-фосфата, что нарушает их функции. Выявляются нарушения в клетках полушарий большого мозга и мозжечка, в тяжелых случаях — отек мозга, задержка умственного развития; возможен летальный исход. -13- Обмен фруктозы. Нарушение обмена фруктозы. Значительное количество фруктозы,образующееся при расщеплении сахарозы,прежде чем поступить в систему воротной вены, превращается в глюкозу уже в клетках кишечника.Другая часть фруктозы всасывается с помощью белка переносчика, т.е. путем облегченной диффузии. Метаболизм фруктозы начинается с реакции фосфорилирования, катализируемой фруктокиназой с образованием фруктозо-1-фосфат.Фермент обнаружен  В печени имеется недостаточное количество специального фермента (фруктозо-1-фосфат-альдолазы), который преобразовывает фруктозу. В результате продукты обмена (фруктозо-1-фосфат) накапливаются в организме (печени, почках, слизистых оболочках кишечника) и оказывают повреждающее действие..СимптомыПризнаки заболевания появляются сразу же, как только в пищу добавляют сахар. Чаще всего это бывает в период прикорма, когда ребенку начинают давать фруктовые соки, пюре, или раньше, если в качестве продукта питания ребенок получает коровье молоко с добавлением сахара (при смешанном или искусственном питании). В случае раннего перехода на искусственное вскармливание коровьим молоком с сахаром заболевание протекает тяжело. У ребенка появляется упорная рвота, а затем он отказывается от приема пищи вообще. Это сказывается на его развитии: масса тела увеличивается очень медленно, и развивается гипотрофия (дефицит массы тела). В более тяжелых случаях снижается уровень сахара в крови, из-за чего дети становятся бледными и сонливыми. В раннем возрасте можно заподозрить непереносимость фруктозы уже потому, что рвота носит упорный характер и возникает после каждого кормления, увеличивается печень, а вслед за этим развивается желтуха. Печень увеличивается у 70% больных фруктоземией, особенно у детей первого года жизни. С возрастом плотность печени нарастает, легко определяется ее нижний край, плотный и болезненный -14- Инсулин зависимый сахарный диабет. Сахарный диабет возникает вследствие относительного или абсолютного дефицита инсулина. В соответствии с классификацией ВОЗ различают две основные формы заболевания: диабет I типа — инсулинзависимый (ИЗСД) и диабет II типа инсулиннезависимый (ИНСД). ИЗСД является следствием разрушения -клеток островков Лангерганса в результате аутоиммунных реакций. Фактором, провоцирующим возникновение диабета I типа, может быть вирусная инфекция, вызывающая деструкцию -клеток. Кроме того, ИЗСД может быть результатом частичного генетически обусловленного дефекта иммунной системы и сочетаться с другими аутоиммунными заболеваниями. При сахарном диабете происходит ослабление стимуляции процессов депонирования гликогена и жиров и усиление мобилизации запасов энергоно сителей. Печень, мышцы и жировая ткань даже после приема пищи функционируют в режиме постабсорбтивного состояния. Признаки поздних осложнений сахарного диабета наиболее часто появляются через 15—20 лет после вьывления гипергликемии. Вместе с тем у некоторых пациентов они могут или возникнуть раньше, или вообще не проявиться. В основе поздних осложнений СД лежат главным образом метаболические расстройства в тканях. -15- Инсулин независимый сахарный диабет. Сахарный диабет возникает вследствие относительного или абсолютного дефицита инсулина. В соответствии с классификацией ВОЗ различают две основные формы заболевания: диабет I типа — инсулинзависимый (ИЗСД) и диабет II типа инсулиннезависимый (ИНСД). ИНСД возникает в результате повреждения механизмов передачи инсулинового сигнала в клетки-мишени или нарушения секреции инсулина. Диабет II типа характеризуется высокой частотой семейных форм. Возможными причинами ИНСД могут быть: образование антител к рецепторам инсулина; генетический дефект пострецепторного аппарата инсулинзависимых тканей; нарушение регуляции секреции инсулина Мутации глюкокиназы приводят к развитию одной из форм сахарного диабета — диабета MODY. Основным провоцирующим фактором ИНСД является ожирение. Этот тип диабета часто сочетается с гиперинсулинемией, что способствует ожирению. Таким образом, ожирение, с одной стороны, является важнейшим фактором риска, а с другой — одним из ранних проявлений диабета. При сахарном диабете происходит ослабление стимуляции процессов депонирования гликогена и жиров и усиление мобилизации запасов энергоно сителей. Печень, мышцы и жировая ткань даже после приема пищи функционируют в режиме постабсорбтивного состояния. Признаки поздних осложнений сахарного диабета наиболее часто появляются через 15—20 лет после вьывления гипергликемии. Вместе с тем у некоторых пациентов они могут или возникнуть раньше, или вообще не проявиться. В основе поздних осложнений СД лежат главным образом метаболические расстройства в тканях. -16- Глицерофосфолипиды, сфингофосфолипиды 1. ГЛИЦЕРОФОСФОЛИПИДЫ (ГФЛ) - содержат спирт глицерин. Все они относятся к L-ряду. Есть асимметрический углеродный атом (на рисунке обозначен звездочкой). Полярная группировка может быть представлена аминокислотой серином (фосфатидилсерин), холином (фосфатидилхолин, другое название – лецитин), этаноламином (фосфатидилэтаноламин), инозитолом (фосфатидилинозитол), глицерином (полиглицерофосфатиды). 2. СФИНГОФОСФОЛИПИДЫ (СФЛ) - содержат спирт сфингозин: СФИНГОМИЕЛИНЫ. Сфингофосфолипиды бывают различными по строению, но имеют общие черты. Молекула сфингофосфолипида содержит сфингозин, жирную кислоту, фосфорную кислоту и полярную группировку. ОБЩАЯ ФОРМУЛА СФЛ представлена на рисунке.  Сфингозин - это 2-хатомный непредельный аминоспирт. Жирная кислота присоединена пептидной связью к аминогруппе сфингозина. Фосфолипиды - это амфифильные вещества. Расположение гидрофильных и гидрофобных участков особое. Гидрофильные участки (остаток фосфорной кислоты и полярная группировка) образуют "головку", а гидрофобные радикалы жирных кислот (R1 и R2) образуют "хвосты". -17- Гликолипиды. Стероиды, ЖК ГЛИКОЛИПИДЫ. Состоят из сфингозина, жирной кислоты и молекулы какого-либо углевода. Если в формулу СФЛ вместо фосфорной кислоты поставить какой-нибудь углевод, то получим формулу ГЛ. Гликолипиды тоже имеют гидрофильную "головку" и 2 гидрофобных "хвоста". Общая схема их строения представлена на рисунке:  Гликолипиды классифицируют в зависимости от строения углеводного компонента. Различают 2 группы гликолипидов: 1. ЦЕРЕБРОЗИДЫ. В качестве углеводного компонента содержат какой-либо моносахарид (глюкоза, галактоза), либо дисахарид, или нейтральный небольшой олигосахарид. 2. ГАНГЛИОЗИДЫ. Углеводным компонентом является олигосахарид, состоящий из разных мономеров, как самих моносахаридов, так и их производных. Этот олигосахарид обязательно кислый, в его состав обязательно входит сиаловая кислота. Благодаря определенной последовательности мономеров, олигосахариды в составе ганглиозида придают молекуле выраженные антигенные свойства. СТЕРОИДЫ. Делятся на 2 группы. 1. Стерины (в их составе полициклическая стуктура стерана). 2. Стериды (эфиры холестерина и высших жирных кислот). Свойства стероидов. Стерины содержат гидроксильную группу (-ОН), поэтому они немножко гидрофильны, но всётаки их молекулы в основном гидрофобны. К ним относится холестерин. Холестерин является полициклическим веществом. Преобладают гидрофобные свойства, но есть одна ОН-группа. Стериды являются полностью гидрофобными веществами. |
