|
|
Биохимия итоговая. Итоговая работа 2 по БХ (занятие 10). 1. Общая схема распада нуклеиновых кислот пищи, ферменты, субстраты, продукты
1. Общая схема распада нуклеиновых кислот пищи, ферменты, субстраты, продукты.
2. Общая схема синтеза и распада пиримидиновых нуклеотидов. Регуляция. Оротацидурия.
3. Общая схема синтеза и распада пуриновых нуклеотидов. Регуляция. Подагра.
4. Синтез дезоксирибонуклеотидов. Регуляция.
5. Первичная структура нуклеиновых кислот. ДНК и РНК – черты сходства и различия состава, локализации в клетке, функции.
6. Вторичная структура ДНК (модель Уотсона и Крика). Связи, стабилизирующие вторичную структуру ДНК. Комплементарность. Правило Чаргаффа. Полярность. Антипараллельность.
7. Гибридизация нуклеиновых кислот. Денатурация и ренативация ДНК. Гибридизация (ДНК-ДНК, ДНК-РНК). Методы лабораторной диагностики, основанные на гибридизации нуклеиновых кислот.
8. Третичная структура ДНК. Роль гистоновых и негистоновых белков в компактизации ДНК. Организация хроматина. Ковалентная модификация гистонов и ее роль в регуляции структуры и активности хроматина.
9. Репликация. Принципы репликации ДНК. Стадии репликации. Инициация. Белки и ферменты, принимающие участие в формировании репликативной вилки
10. Элонгация и терминация. Ферменты. Асимметричный синтез ДНК. Фрагменты Оказаки. Роль ДНК-лигазы в формировании непрерывной отстающей цепи.
11. Теломерная ДНК. Синтез теломерной ДНК.
12. Повреждения и репарация ДНК. Виды повреждений. Способы репарации. Дефекты репарационных систем и наследственные болезни.
13. Транскрипция у прокариот. Характеристика компонентов системы синтеза РНК. Структура ДНК-зависимой РНК-полимеразы: роль субъединиц (a2ВВ′d). Инициация процесса.
14. Элонгация, терминация транскрипции (ρ-независимая, ρ-зависимая терминация)
15. Особенности транскрипции у эукариот. Структура белков, регулирующих процесс транскипции.
16. Первичный транскрипт и его процессинг. Рибозимы как пример каталитической активности нуклеиновых кислот. Биороль.
17. Регуляция транскрипции у прокариот. Теория оперона, регуляция по типу индукции и репрессии (примеры).
18. Механизмы регуляции экспрессии генов у эукариот.
19. Постранскрипционная регуляция у эукариот, обеспечивающая разнообразие белков: альтернативный сплайсинг. Редактирование РНК.
20. Биосинтез белков (трансляция). Основные компоненты белоксинтезирующей системы: аминокислоты, т-РНК, рибосомы, источники энергии, белковые факторы, ферменты.
21. Строение и функции рибосом. Связывающие и каталитическик центры рибосом.
22. Активация аминокислот. Аминоацил-т-РНК синтетазы, субстратная специфичность.
23. Сборка полипептидной цепи на рибосоме. Образование инициаторного комплекса у прокариот. Особенности стадии инициации у эукариот.
24. Элонгация: образование пептидной связи (р-ция транспептидации). Транслокация. Терминация. Роль белковых факторов на каждой из стадий трансляции.
25. Регуляция биосинтеза белков на уровне трансляции. Изменение скорости трансляции.
26. Процессинг первичных полипептидных цепей после трансляции: частичный протеолиз, образование ковалентных связей, присоединение простетических групп, ковалентная модификация аминокислотных остатков (гликозилирование, метилирование, фосфорилирование, ацетилирование).
27. Фолдинг белков. Ферменты. Роль шаперонов в фолдинге белка. Фолдинг белковой молекулы с помощью шаперониновой системы. Болезни, связанные с нарушением фолдинга белка.
28. Особенности синтеза и процессинга секретируемых белков (на примере коллагена и инсулина).
29. Различия в продолжительности жизни белков. Убиквитинзависимая система протеолиза.
30. Лекарственные препараты – ингибиторы матричных биосинтезов. Вирусы и токсины ингибиторы матричных синтезов в эукариотических клетках. Интерфероны
---------------------------------------------------------------------------------
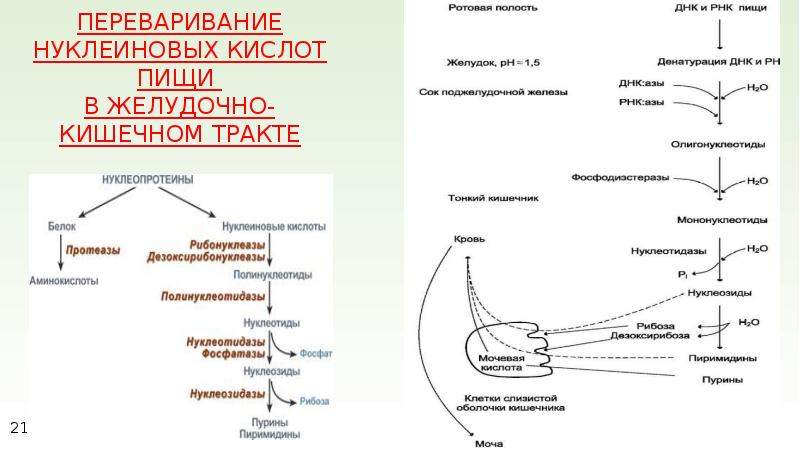
1. Общая схема распада нуклеиновых кислот пищи, ферменты, субстраты, продукты.

2. Общая схема синтеза и распада пиримидиновых нуклеотидов. Регуляция. Оротацидурия.
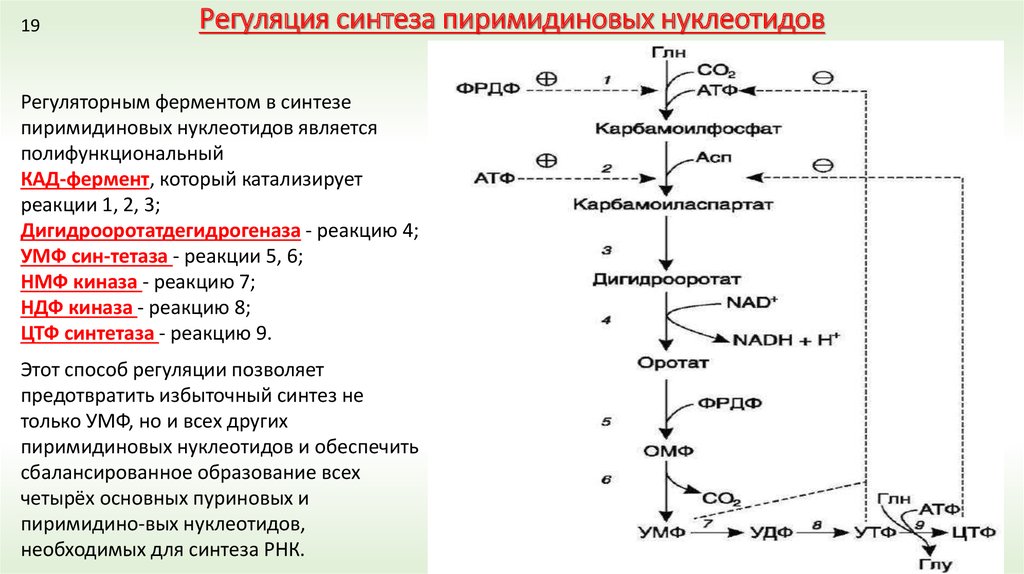
Оротацидурия
Это единственное нарушение синтеза пиримидинов de novo. Оно вызвано снижением активности УМФ-синтазы, которая катализирует образование и декарбоксилирование ОМФ. Поскольку в эмбриогенезе от образования пиримидинов de novo зависит обеспечение синтеза ДНК субстратами, то жизнь плода невозможна при полном отсутствии активности этого фермента. Действительно, у всех пациентов с оротацидурией отмечают заметную, хотя и очень низкую активность УМФ-синтазы. Установлено, что содержание оротовои кислоты в моче пациентов (1 г/сут и более) значительно превосходит количество оротата, которое ежедневно синтезируется в норме (около 600 мг/сут). Снижение синтеза пиримидиновых нуклеотидов, наблюдающееся при этой патологии, нарушает регуляцию КАД-фермента по механизму ретроингибирования, из-за чего возникает гиперпродукция оротата.
Клинически наиболее характерное следствие оротацидурии - мегалобластная анемия, вызванная неспособностью организма обеспечить нормальную скорость деления клеток эритроцитарного ряда. Её диагностируют у детей на том основании, что она не поддаётся лечению препаратами фолиевой кислоты.
Недостаточность синтеза пиримидиновых нуклеотидов сказывается на интеллектуальном развитии, двигательной способности и сопровождается нарушениями работы сердца и ЖКТ. Нарушается формирование иммунной системы, и наблюдается повышенная чувствительность к различным инфекциям.
Гиперэкскреция оротовои кислоты сопровождается нарушениями со стороны мочевыводящей системы и образованием камней. При отсутствии лечения больные обычно погибают в первые годы жизни. При этом оротовая кислота не оказывает токсического эффекта. Многочисленные нарушения в работе разных систем организма вызваны "пиримидиновым голодом".
Для лечения этой болезни применяют уридин (от 0,5 до 1 г/сут), который по "запасному" пути превращается в УМФ.
Уридин + АТФ → УМФ + АДФ.
Нагрузка уридином устраняет "пиримидиновый голод", а поскольку из УМФ могут синтезироваться все остальные нуклеотиды пиримидинового ряда, то снижается выделение оротовои кислоты из-за восстановления механизма ретроингибирования КАД-фермента. Для больных оротацидурией лечение уридином продолжается в течение всей жизни, и этот нуклеозид становится для них незаменимым пищевым фактором.
Кроме генетически обусловленных причин, оротацидурия может наблюдаться:
при гипераммониемии, вызванной дефектом любого из ферментов орнитинового цикла,
за исключением карбамоилфосфат- синтетазы I. В этом случае карбамоилфосфат, синтезированный в митохондриях, выходит в цитозоль клеток и начинает использоваться на образование пиримидиновых нуклеотидов. Концентрация всех метаболитов, в том числе и оротовой кислоты, повышается. Наиболее значительная экскреция оротата отмечается при недостаточности орнитинкарбамоилтрансферазы (второго фермента орнитинового цикла);
в процессе лечения подагры аллопуринолом, который превращается в оксипуринолмононуклеотид и становится сильным ингибитором УМФ-синтазы. Это приводит к накоплению оротовой кислоты в тканях и крови.
3. Общая схема синтеза и распада пуриновых нуклеотидов. Регуляция. Подагра.
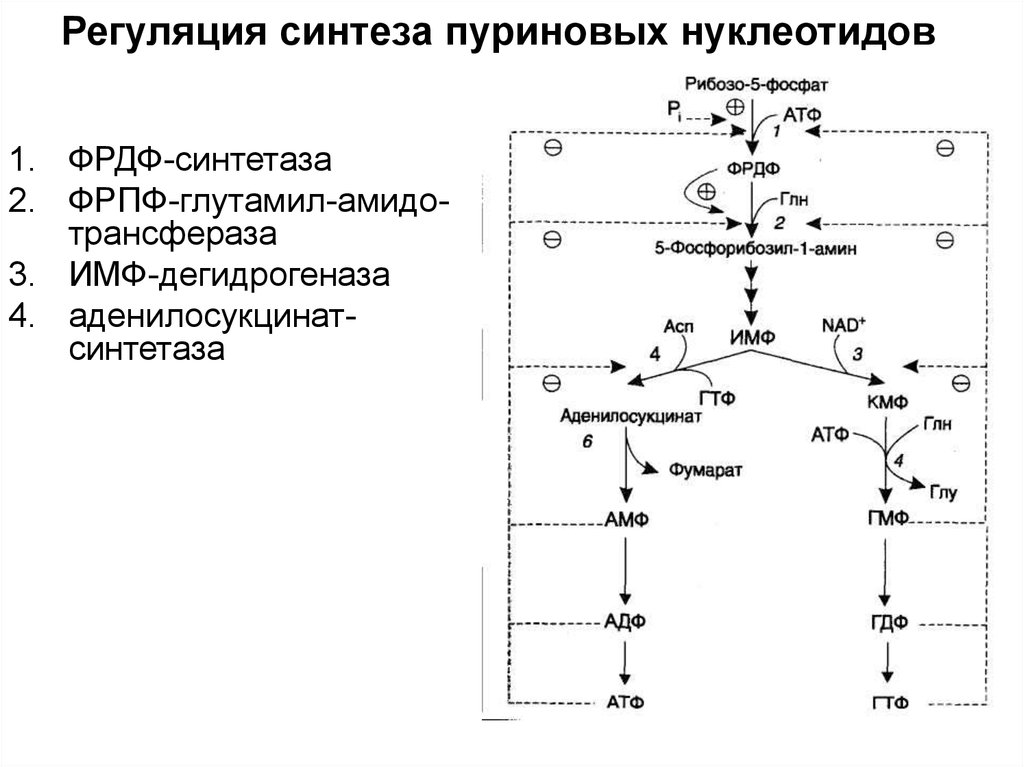
Гиперурикемия подагры
Когда в плазме крови концентрация мочевой кислоты превышает норму, то возникает гиперурикемия. Вследствие гиперурикемии может развиться подагра - заболевание, при котором кристаллы мочевой кислоты и уратов откладываются в суставных хрящах, синовиальной оболочке, подкожной клетчатке с образованием подагрических узлов, или тофусов. К характерным признакам подагры относят повторяющиеся приступы острого воспаления суставов (чаще всего мелких) - так называемого острого подагрического артрита. Заболевание может прогрессировать в хронический подагрический артрит.
Поскольку лейкоциты фагоцитируют кристаллы уратов, то причиной воспаления является разрушение лизосомальных мембран лейкоцитов кристаллами мочевой кислоты. Освободившиеся лизосомальные ферменты выходят в иитозоль и разрушают клетки, а продукты клеточного катаболизма вызывают воспаление.
Общий фонд сывороточных уратов в норме составляет 1,2 г у мужчин и 0,6 г у женщин. При подагре без образования тофусов (т.е. подагрических узлов, в которых накапливаются ураты натрия и мочевая кислота) количество уратов возрастает до 2-4 г, а у пациентов с тяжёлой формой болезни, сопровождающейся ростом тофусов, может достигать 30 г.
Подагра - распространённое заболевание, в разных странах ею страдают от 0,3 до 1,7% населения. А поскольку сывороточный фонд уратов у мужчин в 2 раза больше, чем у женщин, то они и болеют в 20 раз чаще, чем женщины.
Как правило, подагра генетически детерминирована и носит семейный характер. Она вызвана нарушениями в работе ФРДФ синтетазы или ферментов "запасного" пути: гипоксантин-гуанин- или аденинфосфорибозилтрансфераз.
К другим характерным проявлениям подагры относят нефропатию, при которой наблюдают образование уратных камней в мочевыводящих путях.
4. Синтез дезоксирибонуклеотидов. Регуляция.
Синтез дезоксирибонуклеотидов идёт с заметной скоростью только в тех клетках, которые вступают в S-фазу клеточного цикла и готовятся к синтезу ДНК и делению. В покоящихся клетках дезоксинуклеотиды практически отсутствуют. Все дезоксинуклеотиды, кроме тимидиловых, образуются из рибонуклеотидов путём прямого восстановления ОН-группы у второго углеродного атома рибозы в составе рибонуклеозиддифосфатов до дезоксирибозы. Тимидиловые нук-леотиды синтезируются из dУМФ особым путём с участием N5,N10-метилен-Н4-фолата.
А. Рибонуклеотидредуктазный комплекс
Реакцию восстановления НДФ в дезоксипроизводные катализирует рибонуклеотидредук-тазный комплекс, в состав которого входят: собственно рибонуклеотидредуктаза (РНР), белок тиоредоксин и фермент тиоредоксинредуктаза, обеспечивающий регенерацию восстановленной формы тиоредоксина (рис. 10-17).
Рибонуклеотидредуктаза - олигомерный белок, состоящий из двух В1- и двух В2-субъединиц, и содержит негеминовое железо в качестве кофактора.
Непосредственным донором водорода в реакции восстановления рибозы служит низкомолекулярный белок тиоредоксин. В рабочую часть этого белка входят 2 SH-группы, которые, отдавая водород, окисляются с образованием дисульфидного мостика. Второй фермент комплекса - тиоредоксинредуктаза - катализирует гидрирование окисленного тиоредоксина с использованием NADPH.
При участии комплекса РНР образуются: dАДФ, dГДФ, dУДФ и dЦДФ, которые с помощью НДФ-киназ превращаются в дНТФ, 3 из которых (кроме дУДФ) непосредственно используются в синтезе ДНК.
дНДФ + АТФ → дНТФ + АДФ.
Б. Биосинтез тимидиловых нуклеотидов
Тимидин-5'-монофосфат (дТМФ) образуется из дУМФ в реакции, катализируемой тимиди-латсинтазой (рис. 10-18). Донором метильной группы, появляющейся в 5-положении пиримидинового кольца в молекуле дТМФ, служит кофермент тимидилатсинтазы - N5,N10-метилен-Н4-фолат. С помощью этого кофермента в молекулу дУМФ включается метиленовая группа и восстанавливается в метальную, используя 2 атома водорода от Н4-фолата.

Рис. 10-17. Восстановление рибонуклеозиддифосфатов в 2'-дезоксирибонуклеозиддифосфаты.1 - рибонуклеотидредуктаза (РНР); 2 - тиоредоксинредуктаза.
Образование субстрата тимидилатсинтазной реакции - дУМФ осуществляется двумя путями (рис. 10-19):
дефосфорилированием дУДФ;
гидролитическим дезаминированием дЦМФ с помощью дЦМФ дезаминазы. дЦМФ получается при дефосфорилировании дЦДФ - одного из продуктов рибонуклеотидредуктаз-ной реакции. В организме человека это основной путь образования дУМФ.
Скорость синтеза дТМФ зависит также от количества второго субстрата тимидилатсинтазной реакции - N5,N10-метилен-Н4-фолата, пополнение запасов которого осуществляется при участии 2 ферментов: дигидрофолатредуктазы, которая с участием NADPH восстанавливает Н2-фолат в Н4-фолат, и серии гидроксиметилтрансферазы, осуществляющей перенос β-гидроксиметиленовой группы серина на Н4-фолат (см. раздел 9). У человека дТМФ образуется, главным образом, из дЦДФ.
В. "Запасные" пути синтеза дезоксирибонуклеотидов
В быстроделящихся клетках наряду с синтезом дезоксинуклеотидов с помощью рибонуклеотид-редуктазного комплекса и тимидилатсинтазы активируются реакции, обеспечивающие повторное использование тимина и дезоксицитидина в реакциях, катализируемых ферментами "запасных" путей и обратимых реакций катаболизма. Под влиянием тимидинфосфорилазы протекает следующая реакция:
Тимин + Дезоксирибоза-1-фосфат → Тимидин + Н3Р04.
Рис. 10-18. Синтез дТМФ из дУМФ.
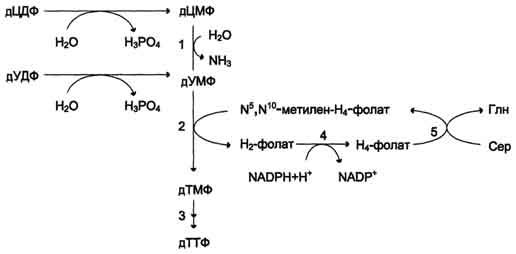
Рис. 10-19. Образование ТТФ из дЦДФ и дУДФ.1 - дЦМФ дезаминаза; 2 -тимидилатсинтаза; 3 - дНМФ- и дНДФ 4 - дигидрофолатредуктаза; 5 - серингидроксиметилтрансфераза.
Тимидинкиназа катализирует следующую реакцию:
Тимидин + АТФ → дТМФ + АДФ.
Дезоксицитидинкиназа катализирует следующую реакцию:
Дезоксицитидин + АТФ → дЦМФ + АДФ.
Г. Регуляция синтеза дезоксирибонуклеотидов
Рибонуклеотидредуктаза, тимидилатсинтаза и тимидинкиназа - индуцируемые ферменты, их количество в клетке регулируется на генетическом уровне по механизму индукции и репрессии. Синтез этих белков начинает нарастать в G1-периоде, достигает максимума во время активного синтеза ДНК, снижаясь практически до нуля в G2- и М-периоды клеточного цикла.
В то же время активность РНР подвержена сложной аллостерической регуляции, с помощью которой достигается сбалансированное образование всех дНДФ.
РНР осуществляет последовательное восстановление всех рибонуклеозиддифосфатов. Первыми восстанавливаются шфимидиновые нуклеотиды, а последним - дАДФ. дАДФ фосфорилируется в дАТФ, накопление которого полностью прекращает восстановление всех остальных рибонуклеозиддифосфатов.
Д. Нарушения в работе РНР, вызванные недостаточностью ферментов катаболизма пуриннуклеотидов
Аденозиндезаминаза (АДА) и пуриннуклеозидфосфорилаза (ПНФ) участвуют в превращении пуриновых нуклеозидов в азотистые основания. Их недостаточность сопровождается развитием тяжёлых форм иммунодефицита.
Недостаточность аденозиндезаминазы. АДА катализирует гидролитическое дезаминирование аденозина и дезоксиаденозина:
Аденозин + Н2О → Инозин + NH3,
Дезоксиаденозин + Н2О → Дезоксиинозин + NH3.
Фермент АДА обнаружен во многих органах и тканях, однако его недостаточность имеет наиболее тяжёлые последствия для клеток лимфоци-тарного ряда. Низкая активность этого фермента нарушает пролиферацию и созревание Т- и В-лимфоцитов и сопровождается тяжёлыми формами клеточного и гуморального иммунодефицита. Дети, страдающие этой патологией, как правило, погибают в раннем возрасте от бактериальных, вирусных или грибковых инфекций.
Столь тяжёлые последствия недостаточности АДА для клеток лимфоцитарного ряда объясняют тем, что при снижении скорости дезаминирования адениловых и дезоксиадениловых нук-леотидов в клетках увеличивается концентрация дАТФ, который ингибирует РНР. Это нарушает синтез всех дНТФ и лишает клетки субстратов для синтеза ДНК. Для нелимфоцитарных клеток недостаточность АДА не сопровождается нарушениями метаболизма в связи с тем, что в них активно работает фосфатаза дАТФ, которая предотвращает накопление основного ингибитора РНР - дАТФ.
Фермент обладает групповой субстратной специфичностью и использует в качестве субстратов некоторые производные аденозина, которые применяются в терапии онкологических и противовирусных заболеваний (аденозинарабинозид, формицин).
Недостаточность пуриннуклеозидфосфорилазы (ПНФ). ПНФ катализирует фосфоролиз пуриновых рибо- и дезоксирибонуклеозидов с освобождением азотистых оснований и рибозо- или дезоксирибозо-1-фосфата. Субстратами служат гуанозин, дезоксигуанозин и инозин.
Нуклеозид + Н3РО4→ Азотистое основание + Рибозо-1-фосфат.
Фермент обнаружен во многих органах и тканях, но особенно активен в клетках-предшественниках Т-лимфоцитов в процессе их созревания в тимусе. При наследственной недостаточности пуриннуклеозидфосфорилазы, вызванной генными мутациями, в крови снижается образование и количество зрелых Т-лимфоцитов. Нарушение созревания Т-лимфоцитов вызвано тем, что в этих клетках высокой активностью обладает дезоксигуанозинкиназа, а это приводит к накоплению дГТФ в концентрациях, которые, подобно дАТФ, ингибируют РНР.
У детей снижен клеточный иммунитет, хотя гуморальный иммунитет не страдает, так как в В-лимфоцитах дезоксигуанозинкиназа малоактивна и накопления дГТФ в токсических концентрациях не отмечают.
Болезнь, вызванная недостаточностью ПНФ, характеризуется более лёгким течением, чем болезнь, обусловленная дефицитом АДА.
5. Первичная структура нуклеиновых кислот. ДНК и РНК – черты сходства и различия состава, локализации в клетке, функции.
|
|
|
 Скачать 1.5 Mb.
Скачать 1.5 Mb.





