Вопросы по пищевой химии. 1. Предмет и задачи пищевой химии. Понятия о пищевой и биологической ценности продуктов
 Скачать 1.85 Mb. Скачать 1.85 Mb.
|
|
Ф  ерменты и белковые ингибиторы зерна ерменты и белковые ингибиторы зернаПри переработке пищевого сырья, в т.ч. зерна, его клеточная структура разрушается и в нём начитают интенсивно протекать окислительные и гидролитические процессы. Поэтому технологи, перерабатывающие биологическое сырьё, основное внимание уделяют ферментам двух классов — оксидоредуктаз и гидролаз. Оксидоредуктазы Наибольшее значение имеют три фермента класса оксидоредуктаз — тирозиназа, липоксигеназа и глюкозооксидаза. Тирозиназа — катализирует реакцию окисления тирозина кислородом с образованием меланинов. С действием тирозиназы связано потемнение срезов картофеля, яблок, грибов, персиков и других растительных тканей. С целью предотвращения ферментативного потемнения плодов и овощей при их сушке, а также макаронных изделий в ходе их производства проводят тепловую инактивацию фермента путём бланшировки. Липоксигеназа — катализирует окисление кислородом полиненасыщенных высокомолекулярных жирных кислот (линолевой, линоленовой) с образованием гидроперекисей, обладающих свойствами сильных окислителей. Этот фермент широко распространён в растительном мире. Его выделили из зерна пшеницы, семян бобовых и масличных культур, клубней картофеля, плодов баклажана. Самым богатым источником липоксигеназы является мука соевых бобов. Липоксигеназе принадлежит важная роль в процессах созревания пшеничной муки, связанных с улучшением её хлебопекарных достоинств. Образующиеся под воздействием липоксигеназы продукты окисления жирных кислот способны вызывать сопряжённое окисление ряда других компонентов муки — пигментов, SН-групп клейковинных белков, ферментов. При этом происходит осветление муки, укрепление клейковины, снижение активности протеолитических ферментов (схема выше) В разных странах разработаны способы улучшения качества хлеба, основанные на использовании препаратов липоксигеназы (главным образом липоксигеназы соевой муки). Однако все эти способы требуют очень точного дозирования фермента, т.к. даже небольшая его передозировка приводит к отрицательному эффекту и вместо улучшения качества хлеба происходит его ухудшение. Чтобы избежать передозировки фермента, используют методы активации собственной липоксигеназы пшеничной муки. Использование липоксигеназы для улучшения качества хлеба требует определённой осторожности, т.к. при интенсивном окислении этим ферментом свободных жирных кислот происходит образование различных веществ с неприятным вкусом и запахом, характерным для прогорклого продукта. Следует также помнить, что переокисленные жиры токсичны. 57. Основные гидролитические ферменты биологического сырья (липаза, гликозидазы, протеазы). Гидролазы Эти ферменты расщепляют липиды, полисахариды, белки. До разрушения клетки гидролазы содержатся в лизосомах, а после её разрушения — осуществляют процесс автолиза. Наибольшее значение среди ферментов этого класса имеют эстеразы, гликозидазы и протеазы. Эстеразы. К эстеразам относится фермент липаза, катализирующий реакцию расщепления жиров с образованием глицерина и свободных жирных кислот. Накопление свободных жирных кислот является причиной роста кислотного числа жира. Эти кислоты легко подвергаются окислению под воздействием различных факторов. Таким образом, липаза инициирует процесс прогоркания, что ограничивает сроки хранения пищевых продуктов. Липаза также вызывает переэтерификацию триацилглицеринов, т.е. изменение их жирнокислотного состава, что можно использовать для получения новых форм жировых продуктов. Так, например, можно получать аналог дорогого масла какао из дешёвого исходного сырья. Гликозидазы — расщепляют полисахариды. Основной формой запасания углеводов является крахмал. Его ферментативные превращения лежат в основе многих пищевых технологий. Интенсивность гидролиза крахмала в перерабатываемом сырье определяется взаимодействием многих факторов: 1) активностью амилаз, т.е. возможностью перехода связанной формы амилаз в свободную; 2) доступностью крахмала действию ферментов (атакуемостью субстрата), которая зависит от фракционного состава крахмальных гранул, т.е. соотношения мелких и крупных крахмальных зёрен, а также от содержания повреждённых гранул крахмала, которые легче поддаются действию ферментов; 3) высвобождением амилаз из связанного состояния под действием протеаз; 4) гидролизом той части запасных белков, которая прочно связана с поверхностью крахмальных зёрен, что облегчает доступ фермента к субстрату; 5) активностью системы белковых ингибиторов амилаз и протеаз, которые регулируют расщепление крахмала. Они образуют неактивные комплексы: Белковый ингибитор • Амилаза, Белковый ингибитор • Протеаза В зерне пшеницы содержится двуцентровой ингибитор, который ингибирует активность и амилаз, и протеаз: Протеаза • Белковый ингибитор • Амилаза Протеазы — расщепляют запасные белки до аминокислот при прорастании семян. Выделяют несколько типов протеаз, различающихся по оптимуму рН среды, в которой они проявляют свою каталитическую активность: 1) кислые протеиназы — рН opt 3,7–4,0; 2) нейтральные протеиназы — рН opt 6,5–7,0; 3) щелочные протеиназы — рН opt > 8,0. Наиболее интересны нейтральные протеиназы. Они существенно более активны, чем прочие и эффективно расщепляют белки клейковины в тесте. В созревших семенах пшеницы нейтральные протеиназы находятся в неактивном комплексе с белковыми ингибиторами. Это определяет стабильность белкового комплекса в водных суспензиях. Поэтому автолитические процессы в тесте выражены слабо. При прорастании зерна происходит распад комплекса Белковый ингибитор • Протеаза и начинается интенсивный протеолиз запасных белков. Н 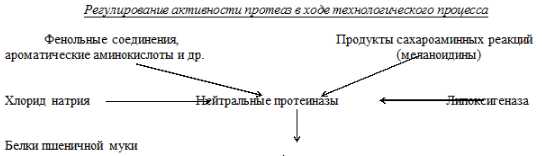 ейтральные протеиназы ингибируются фенольными соединениями, ароматическими аминокислотами, меланоидинами и др. ейтральные протеиназы ингибируются фенольными соединениями, ароматическими аминокислотами, меланоидинами и др.Хлорид натрия является обязательным компонентом рецептуры и снижает интенсивность автолиза на 60–70 %. В зависимости от качества муки и состояния клейковины можно, варьируя время внесения соли, регулировать интенсивность протеолиза. Если мука слабая, то NaCl нужно вносить как можно раньше, а если клейковина чрезмерно крепкая, то следует активизировать протеолиз и вносить NaCl на более поздних стадиях. 58. Применение ферментов в пищевых технологиях. Ферментные препараты в отличие от ферментов содержат помимо активного фермента множество балластных веществ, в том числе и других белков. Кроме того, большинство ферментных препаратов являются комплексными, т. е. кроме основного фермента, имеющего наибольшую активность, в его состав входят другие сопутствующие ферменты. Однако существуют препараты и индивидуальных ферментов. Название ферментного препарата включает название основного фермента и название микроорганизма-продуцента, с окончанием "-ин". Например: амилоризин — основной фермент — амилаза, продуцент Aspergillus oryzae; протосубтилин — основной фермент — протеаза, продуцент Bacillus subtilis. Помимо этого, в названии обязательно отражается способ культивирования микроорганизма: Г — глубинное; П — поверхностное, а также степень очистки — X (2Х; ЗХ; 10Х; 15Х; 20Х). Применение ферментных препаратов в отраслях пищевой промышленности позволяет интенсифицировать технологические процессы, улучшать качество готовой продукции, увеличивать ее выход, а также сэкономить ценное пищевое сырье. Ферментные препараты должны удовлетворять требованиям, предъявляемым конкретными технологиями не только по типу катализируемой реакции, но и в отношении условий их действия: рН, температуры, стабильности, присутствия активаторов и ингибиторов, т. е. тех факторов, которые обуславливают эффективность действия препарата в данной среде и позволяют правильно определить технологические режимы его применения. В зависимости от цели применения к ферментным препаратам предъявляются определенные требования не только в отношении состава ферментов и оптимальных условий их действия, но и в отношении степени очистки, применяемых наполнителей, стоимости и ряда других параметров. Очень важным моментом является оценка безопасности ферментных препаратов, и в первую очередь это касается микробных ферментных препаратов, которые требуют тщательного химического, микробиологического и токсикологического контроля. Особое место занимают ферментные препараты, получаемые из генетически модифицированных микроорганизмов. Основными ферментными препаратами, полученными методами генной инженерии и разрешенными к применению в пищевой промышленности, являются: α-амилаза из В. stearothermophilys, экспрессированная в В. subtilis; α-амилаза из В. megaterium, экспрессированная в В. subtilis; химозин А, полученный из штамма Е. coli К-12, содержащего ген телячьего прохимозина А. В настоящее время в мире производится большое количество ферментных препаратов для разных отраслей пищевой промышленности, применяемых на различных стадиях технологического процесса. Различные фирмы выпускают ферментные препараты под разными коммерческими (торговыми) названиями. Однако работа по поиску новых продуцентов, созданию новых препаратов пролонгированного действия, очистке ферментных препаратов, повышению их стабильности и т. п. ведется весьма интенсивно. 59. Вода, её роль в организме человека и функции в пищевых продуктах. Свободная и связанная влага. В  ода входит в состав всех пищевых продуктов, но содержание их различно. Количество воды в пищевых продуктах влияет на их качество и сохраняемость. Скоропортящиеся продукты с повышенным содержанием влаги без консервирования длительное время не сохраняются. Вода, содержащаяся в продуктах, способствует ускорению в них химических, биохимических и других процессов. Продукты с малым содержанием воды лучше сохраняются. ода входит в состав всех пищевых продуктов, но содержание их различно. Количество воды в пищевых продуктах влияет на их качество и сохраняемость. Скоропортящиеся продукты с повышенным содержанием влаги без консервирования длительное время не сохраняются. Вода, содержащаяся в продуктах, способствует ускорению в них химических, биохимических и других процессов. Продукты с малым содержанием воды лучше сохраняются.Количество воды во многих продуктах, как правило, нормируется стандартами с указанием верхнего предела ее содержания, так как от этого зависят не только качество и сохраняемость, но и пищевая ценность продуктов. 6  0. Активность воды и стабильность пищевых продуктов. Влияние активности воды на скорость реакций в пищевых продуктах и рост микроорганизмов. 0. Активность воды и стабильность пищевых продуктов. Влияние активности воды на скорость реакций в пищевых продуктах и рост микроорганизмов. Активность воды (аw) – это отношение давления паров воды над данным продуктом к давлению паров над чистой водой при той же температуре. Это отношение входит в основную термодинамическую формулу определения энергии связи с материалом (уравнение Ребиндера). Активность воды характеризует состояние воды в пищевых продуктах, ее причастность к химическим и биохимическим изменениям. По величине аw различают: продукты с высокой влажностью (аw =1,0-0,9), продукты с промежуточной влажностью (аw=0,9=0,6), продукты с низкой влажностью (аw=06-0,0). 61. Пищевые продукты с высокой, промежуточной и низкой влажностью. Влияние воды на ферментативные процессы при хранении пищевого сырья и готовых продуктов. В продуктах с низкой влажностью могут происходить окисление жиров, неферментативное потемнение, потеря водорастворимых веществ (витаминов), порча, вызванная ферментами. Активность микроорганизмов здесь подавлена. В продуктах с промежуточной влажностью могут протекать разные процессы, в том числе с участием микроорганизмов. В процессах, протекающих при высокой влажности, микроорганизмам принадлежит решающая роль. Эффективным средством для предупреждения микробиологической порчи и целого ряда химических реакций, снижающих качество пищевых продуктов при хранении, является снижение активности воды в пищевых продуктах. Для снижения активности воды используют такие технологические приемы, как сушка, вяление, добавление различных веществ (сахар, соль и др.), замораживание. С целью достижения той или иной активности воды в продукте можно применять такие технологические приемы, как: Адсорбция — продукт высушивают, а затем увлажняют до определенного уровня влажности Сушка посредством осмоса — пищевые продукты погружают в растворы, активность воды в которых меньше активности воды пищевых продуктов. 62. Методы определения свободной и связанной влаги. Дифференциальная сканирующая калориметрия. Если образец охладить до температуры меньше 0°С, то свободная влага замерзнет, связанная — нет. При нагревании замороженного образца в калориметре можно измерить тепло, потребляемое при таянии льда. Незамерзающая вода определяется как разница между общей и замерзающей водой. Термогравиметрический метод. Метод основан на определении скорости высушивания. В контролируемых условиях граница между областью постоянной скорости высушивания и областью, где эта скорость снижается, характеризует связанную влагу. Диэлектрические измерения. Метод основан на том, что при 0°С значения диэлектрической проницаемости воды и льда примерно равны. Но если часть влаги связана, то ее диэлектрические свойства должны сильно отличаться от диэлектрических свойств объемной воды и льда. Измерение теплоемкости. Теплоемкость воды больше, чем теплоемкость льда, т.к. с повышением температуры в воде происходит разрыв водородных связей. Это свойство используют для изучения подвижности молекул воды. Значение теплоемкости воды в зависимости от ее содержания в полимерах дает сведения о количестве связанной воды. Если при низких концентрациях вода специфически связана, то ее вклад в теплоемкость мал. В области высоких значений влажности ее в основном определяет свободная влага, вклад которой в теплоемкость примерно в 2 раза больше, чем льда. ЯМР. Метод заключается в изучении подвижности воды в неподвижной матрице. При наличии свободной и связанной влаги получают две линии в спектре ЯМР вместо одной для объемной воды. 63. Особенности физиолого-биохимических процессов в биологическом сырье с неразрушенной клеточной структурой. Биохимические основы хранения растительного сырья Растительное сырьё может быть представлено либо жизнеспособными объектами — зерном, семенами, овощами, фруктами, либо объектами с разрушенной (перемолотой) клеточной структурой, например мукой. То, в каком состоянии следует хранить растительное сырьё, в жизнеспособном или в перемолотом, определяется интенсивностью и характером протекания происходящих в нём процессов. Процессы, происходящие в сырье с неразрушенной клеточной структурой. В растительном сырье с неразрушенной клеточной структурой — зерне, картофеле, сахарной свёкле, овощах, фруктах и т.п. протекают обменные процессы, оказывающие негативное влияние на качество сырья. Интегральным показателем, определяющим интенсивность протекания обменных процессов в жизнеспособном сырье, является интенсивность дыхания, которую чаще всего выражают в миллиграммах СО2, выделенного 100 граммами сухих веществ сырья за 24 часа. Баланс биохимических превращений, происходящих при дыхании, выражается суммарным уравнением: C6H12O6 + 6O2 6CO2 + 6H2O + 686 ккал/моль Как следует из суммарного уравнения дыхания, при хранении жизнеспособного растительного сырья в нём может происходить ряд существенных изменений. Во-первых, дыхание сопровождается биологическими потерями — уменьшением массы растительного сырья вследствие того, что в этом процессе расходуются углеводы, которые превращаются в CO2 и H2O. Следовательно, хранить растительное сырьё без потерь невозможно, и уменьшение его массы может достигать очень больших величин, в особенности у сочного сырья (именно поэтому сахарная промышленность работает сезонно) и у проросшего зерна — солода. Таким образом, очевидно, что необходимо хранить сырьё так, чтобы потери, происходящие вследствие дыхания, были минимальными. Во-вторых, дыхание сопровождается изменением состава воздушной среды, окружающей растительное сырьё, вследствие поглощения O2 и выделения CO2. Причём, изменение состава воздуха в хранилище может быть довольно значительным. Известны случаи, когда в хранилищах зерна концентрация CO2 изменялась от 0,03 % (обычное содержание углекислого газа в атмосфере) до 13 %. Прежде всего, это опасно для обслуживающего персонала. Кроме этого, при отсутствии O2 в зерне начинается процесс спиртового брожения, в результате чего накапливается этиловый спирт. Он оказывает отравляющее воздействие на зародыш, который быстро погибает, а это значит, что теряется жизнеспособность зерна. Его уже нельзя использовать как семенной материал. Также, увеличивается расход сырья на получение энергии, за счёт того, что процесс диссимиляции начинает протекать менее эффективно. В-третьих, при дыхании выделяется влага. С повышением влажности создаются благоприятные условия на поверхности сырья для жизнедеятельности микроорганизмов, например плесневых грибов, которые тоже дышат, и таким образом способствуют ещё большему возрастанию интенсивности дыхания. В-четвёртых, при дыхании происходит выделение тепла, т.к. не вся освобождающаяся при аэробном распаде углеводов энергия аккумулируется в виде молекул АТФ, часть её рассеивается в виде тепла. Если зерно, например, плохо проветривать, то тепло может накапливаться, т.е. будет идти процесс его самосогревания, причём температура зерновой массы может достигать большой величины — 70–75 °C. В таких условиях зерно буквально обугливается, а зерновая масса теряет сыпучесть и превращается в тёмный монолит. Такое зерно нельзя использовать ни в качестве семенного материала, ни для пищевых целей. Чтобы предупредить или прервать процесс самосогревания, нужно снизить температуру и влажность зерновой массы, для чего проводят её интенсивную вентиляцию, перелопачивание и т.п. Выделение влаги и тепла, вызываемое дыханием растительного сырья, может являться причиной дальнейшего усиления дыхания. Температура и влажность — важнейшие факторы, от которых зависит интенсивность дыхания. Например, зерно пшеницы с влажностью 15,5 % дышит в 2–4 раза интенсивнее, чем сухое (с влажностью меньше 14 %), а с влажностью, превышающей 17 % — в 20–30 раз интенсивнее. Сухое зерно, по сравнению с влажным, имеет ничтожную интенсивность дыхания (рис. 12). Интенсивность дыхания растительного сырья резко возрастает при появлении в нём свободной влаги, т.к. это вызывает увеличение активности гидролитических и дыхательных ферментов, а следовательно, и увеличение расходования сухих веществ. Влажность, при которой в сырье появляется свободная влага и резко возрастает интенсивность его дыхания, называют критической. Для каждого вида сырья величина критической влажности устанавливается соответствующим ГОСТом. При повышении температуры до определённого уровня (50 °C) интенсивность дыхания растительного сырья возрастает (рис. 13). Однако дальнейшее повышение температуры приводит к резкому снижению интенсивности дыхания, что связано с нарушением нормального строения и функционирования протоплазмы клеток сырья, с инактивированием ферментов и, в конечном счёте, с отмиранием тканей. w = 22 % w = 18 % w = 16 % w = 14 % 5 10 15 20 w, % 50 t, °C Рис. 12. Влияние влажности на Рис. 13. Влияние температуры на дыхание зерна пшеницы дыхание зерна пшеницы при различной влажности Чтобы при хранении растительного сырья не происходило усиление процесса дыхания, необходимо хранить его в сухом состоянии при влажности ниже критической и при низкой температуре (2–4 °C), хорошо проветривать помещение для удаления накапливающихся в нём водяных паров и понижения его температуры, а также по возможности перемешивать хранящееся сырьё 64. Интенсивность дыхания как интегральный показатель физиологического состояния биологического сырья. Интегральным показателем, определяющим интенсивность протекания обменных процессов в жизнеспособном сырье, является интенсивность дыхания, которую чаще всего выражают в миллиграммах СО2, выделенного 100 граммами сухих веществ сырья за 24 часа. Баланс биохимических превращений, происходящих при дыхании, выражается суммарным уравнением: C6H12O6 + 6O2 6CO2 + 6H2O + 686 ккал/моль Как следует из суммарного уравнения дыхания, при хранении жизнеспособного растительного сырья в нём может происходить ряд существенных изменений. 65. Функции клеточного компартмента. Особенности биохимических процессов, протекающих в биологическом сырье с разрушенной клеточной структурой. |
