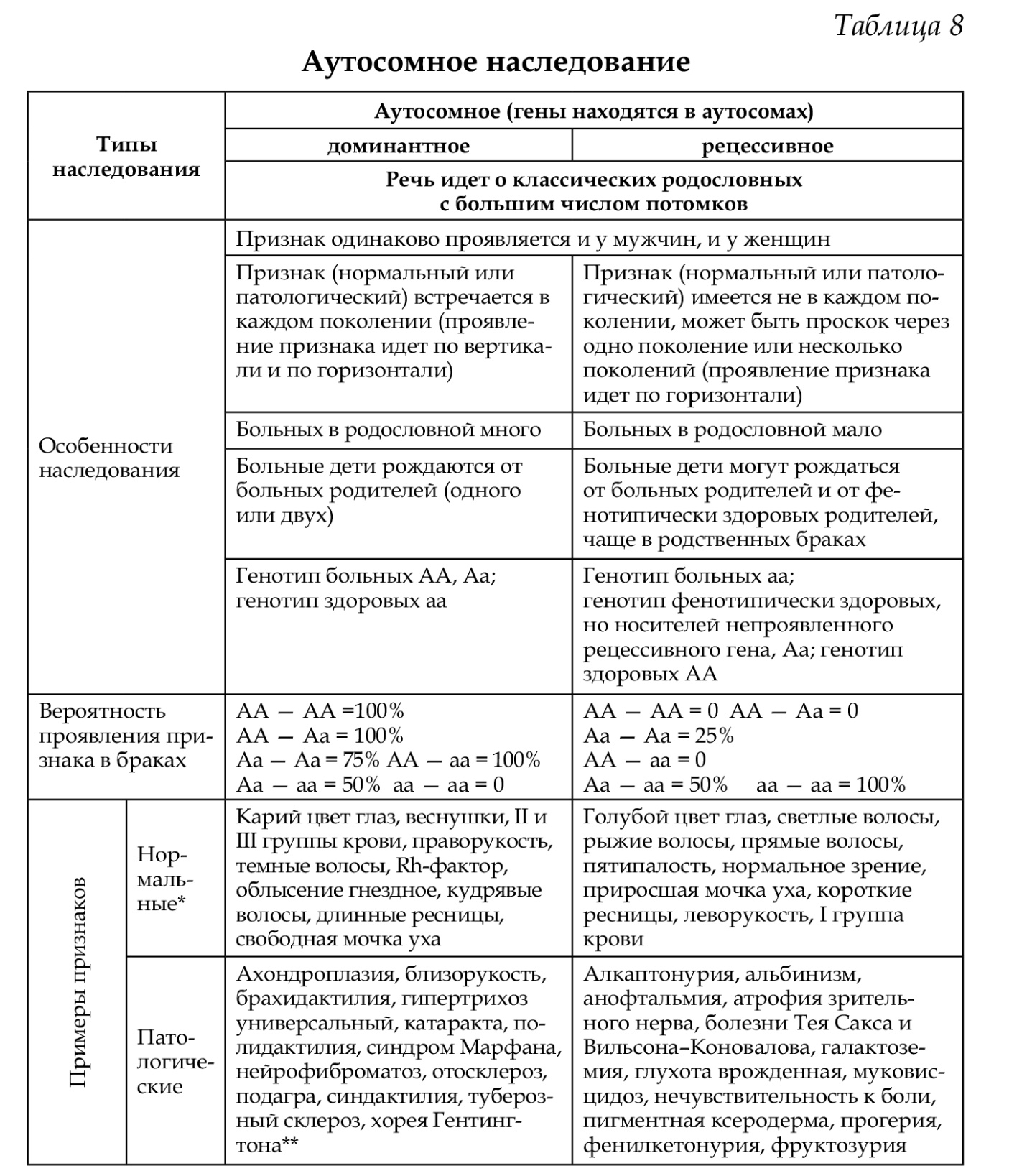
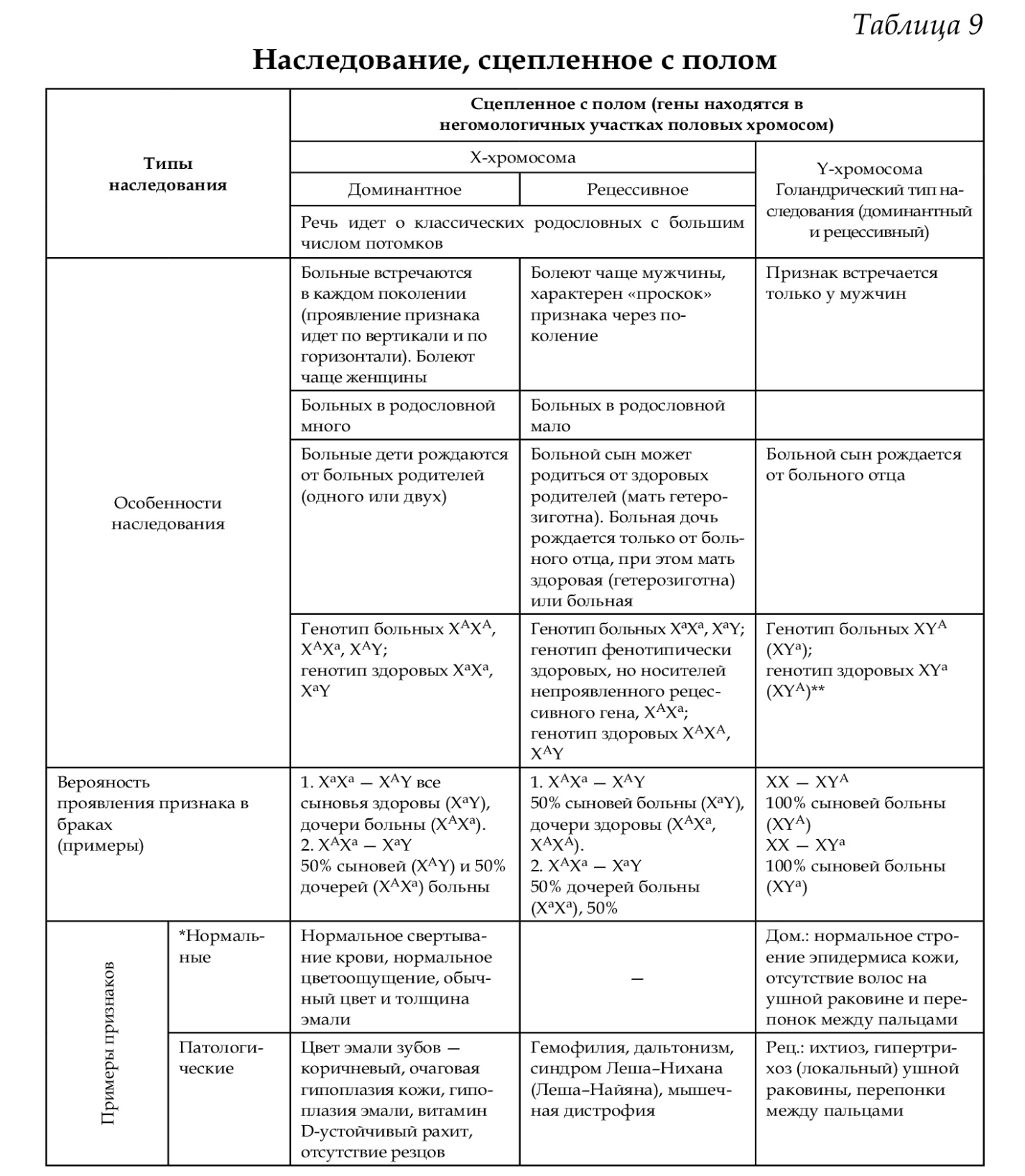
Генетика. 34. Ген как структурная и функциональная единица наследственности. Классификация и свойства генов. Регуляторные гены и регуляторные последовательности
 Скачать 3.46 Mb. Скачать 3.46 Mb.
|
48. Генные и хромосомные мутации. Классификация, механизм возникновения. Примеры проявления мутаций.1% от всех родившихся (1 на 89 родов). Среди них различают монозиготных, или однояйцевых ,и дизиготных, или разнояйцевых близнецов. Близнецовый метод заключается в изучении наследования признаков в парах монозиготных и дизиготных близнецов. Он базируется на трех положениях:— свойства и признаки организма определяются взаимодействием генотипа и среды; — монозиготные близнецы имеют идентичные (одинаковые) генотипы, а дизиготные — неидентичные (различные); — среда (условия жизни), в которой развиваются близнецы и под действием которой формируются признаки, может быть одинаковой и различной для одной и той же пары. Монозиготными называются близнецы, которые образовались из одной зиготы (полиэмбриония). Они генетически идентичны, одного пола. Среда жизни для М3 близнецов может быть одинаковой или различной. • М3 близнецы имеют одинаковые условия жизни. Признак имеется у обоих близнецов одной пары — пара конкордантна. • М3 близнецы имеют разные условия жизни. Близнецы могут быть сходны фенотипически или различны по фенотипу. В данной ситуации все различия в проявлении признаков у одной пары близнецов обусловлены средой. Дизиготные близнецы возникают из разных зигот (полиовуляция), могут быть однополые или разнополые. Они генетически сходны между собой не более, чем обычные сибсы, рожденные в разное время. Различия между ними могут быть обусловлены как генотипом, так и факторами среды. При совместном воспитании ДЗ имеют общую среду жизни; в таком случае различия между близнецами внутри одной пары, в основном, связаны с неидентичными генотипами. О причинах образования близнецов нет четких данных, но предполагают, что образование монозиготных близнецов связано с цитоплазматической наследственностью, так как их рождение наблюдается в определенных семьях и наследуется по женской линии. На частоту рождения дизиготных близнецов влияет возраст матери, что связано с увеличением уровня гонадотропина и частоты полиовуляций. Близнецовый метод генетики используется для выяснения: • соотносительной роли генотипа и среды в развитии фенотипических особенностей человека, его морфологических, физиологических, биохимических признаков и психологических свойств личности; • целесообразности того или иного медицинского (применение лекарственных препаратов при лечении, трансплантации) или психологического (использование системы тестов, методов воспитания) воздействия на человека; • нормы реакции отдельных признаков, т. е. модификационной изменчивости. Для идентификации монозиготных близнецов необходимо: • подобрать пары близнецов; • определить зиготность близнецов; • сравнить пары близнецов по анализируемым признакам (качественным или количественным). Для определения роли наследственности и среды в развитии признаков исследуют отдельно группы М3 и ДЗ близнецов и определяют процент конкордатных пар по отдельным признакам, а затем вычисляют коэффициент наследуемости Н (в % или долях единицы) по формуле, предложенной немецким генетиком Хольцингером. 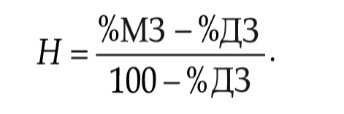 При Н > 0,7 — преобладает действие наследственных факторов. При Н = 0,5-0,7 — равноценное действие среды и генотипа. При Н < 0,5 — преобладает средовой фактор. 58. Цитогенетические методы изучения наследственности человека, возможности методов. Пренатальная диагностика. С помощью данного метода можно изучать наследственный материал клетки: совокупность хромосом в целом (кариотипирование) или наличие и количество Х-хромосом (определение полового хроматина — число глыбок полового хроматина или телец Барра). Исследование проводится с помощью светового микроскопа (изготовление и изучение микропрепаратов). Пренатальная диагностика проводится до 22 недели беременности и является одним из методов первичной профилактики наследственных болезней. Методы делятся на три группы: просеивающие, неинвазивные, инвазивные (с последующей лабораторной диагностикой). Для каждого метода есть свои показания и противопоказания, разрешающие возможности, осложнения после проведения процедур. Выбор метода строго индивидуализирован в соответствии с конкретной ситуацией в семье и состоянием здоровья беременной женщины. Просеивающие методы позволяют выявить женщин, имеющих повышенный риск рождения ребенка с наследственной патологией (возраст матери — 35 лет и старше, повторные спонтанные прерывания беременности и др.). К этим методам относятся: определение концентрации альфа-фетопротеина (АФП) в сыворотке крови беременной (выявляют врожденные дефекты нервной трубки); уровня хорионического гонадотропина (повышен при синдроме Дауна) и несвязанного эстриола (уменьшен при синдроме Дауна); ультразвуковое обследование (УЗИ). Неинвазивные методы: обследование плода без оперативного вмешательства с помощью ультразвукового обследования (УЗИ). Проводится с 6 до 23 недели с целью выявления врожденных пороков развития (редукция конечностей, отставание в росте, анэнцефалия и др.). Инвазивные методы: хорион- и плацентобиопсия (получение небольших кусочков ворсин хориона и кусочков плаценты с 7 по 16 неделю беременности трансабдоминально или трансцервикально под контролем УЗИ), получение амниотической жидкости и клеток плода на 15-18 неделе беременности (рис. 57), биопсия кожи плода, кордоцентез (взятие крови из пуповины под контролем УЗИ с 18-22 недели беременности). Полученный материал подвергается цитогенетическому, биохимическому, молекулярно-генетическому исследованию. Результаты используются в пренатальной диагностике хромосомных и генных болезней, определении пола, выявлении пороков развития. 59. Кариотип человека, методы получения и изучения. Типы классификации хромосом человека. Кариограмма. Возможности картирования генов. Хромосомный набор (кариотип) соматической клетки характеризуется формой хромосом, их количеством, размерами, характерными для каждого вида. Классификация и номенклатура равномерно окрашенных хромосом (стандартное окрашивание) была разработана на международных совещаниях в Денвере (1960), Лондоне (1963) и Чикаго (1966). Согласно рекомендациям этих конференций, хромосомы располагаются в порядке уменьшения их длины от 1 до 23 хромосомы. Они разделены на 7 групп, которые обозначены буквами английского алфавита от А до G. Все пары хромосом предложено нумеровать арабскими цифрами: группа А 1-3, В 4-5, С 6-12 и Х-хромосома, D 13-15, Е 16-18, F 19- 20, G 21-22, Y-хромосома. При этом хромосомы различных групп хорошо отличаются друг от друга (критерии: размер и форма — метацентрические, субметацентрические, акроцентрические), в то время как внутри группы их сложно различить, за исключением хромосом группы А. Важным параметром является центромерный индекс, который отражает в процентах длину короткого плеча к длине всей хромосомы, например, хромосома № 1 — 48,3%, хромосома № 22 — 22,1%. Парижская классификация хромосом В начале 70-х годов XX века был разработан метод дифференциальной окраски хромосом, выявляющий характерную сегментацию, который позволил индивидуализировать каждую хромосому. Каждая хромосома человека содержит свойственную только ей последовательность полос, что позволяет идентифицировать каждую хромосому. Хромосомы спирализованы максимально в метафазе, менее спирализованы в профазе и прометафазе, что позволяет выделить большее число сегментов, чем в метафазе. На метафазной хромосоме приводятся символы, которыми принято обозначать короткое и длинное плечо, а также расположение районов и сегментов. При описании кариотипа: • указывается общее число хромосом и набор половых хромосом, между ними ставится запятая (46, XX; 46, XY); • отмечается какая хромосома лишняя или какой не хватает (это указывается ее номером 5, 6 и др., или буквами данной группы А, В и др.); знаком «+» указывают на увеличение количества хромосом, знаком «-» указывают на отсутствие данной хромосомы 47, XY,+ 21; • плечо хромосомы, в котором произошло изменение (удлинение короткого плеча указывается символом (р+); укорочение (р-); удлинение длинного плеча указывается символом (q+); укорочение (q-); • символы перестроек (транслокация обозначается t, а делеция — del) помещают перед номерами вовлеченных хромосом, а перестроечные хромосомы заключают в скобки. Наличие двух структурно-аномальных хромосом обозначается точкой с запятой (;) или нормальной дробью (15/21). Система записи кариотипов 46, XX — нормальный кариотип (женщина) 46, XY — нормальный кариотип (мужчина) 45, X — синдром Шерешевского-Тернера 47 XXY 1 4g' xxxY I — синдром Клайнфельтера 47, XXX — синдром «трисомии по Х-хромосоме» 47, XYY — синдром Вай-Вай 47, XX, + 21 — синдром Дауна (женщина) 47, XY, + 21 — синдром Дауна (мужчина) 47, XX, + 18 — синдром Эдвардса (женщина) 47, XY, + 18 — синдром Эдвардса (мужчина) 47, XX, + 13 — синдром Патау (женщина) 47, XY, + 13 — синдром Патау (мужчина) 46, XX, t (9/22) — хронический миелолейкоз (женщина) 46, XY, t (9/22) — хронический миелолейкоз (мужчина) 46, XX, t (15/21) — транслокационный Даун (женщина) 46, XY, t (15/21) — транслокационный Даун (мужчина) 46, XX, del (5p-) — синдром кошачьего крика (женщина) 46, XY, del (5р-) — синдром кошачьего крика (мужчина) 46, XX, del (13q-) — синдром Орбели (женщина) 46, XY, del (13q-) — синдром Орбели (мужчина) Сегменты и районы метафазной хромосомы обозначаются цифрами, центромера служит исходной точкой для цифровой схемы. При определении локализации гена используют 4 критерия: номер хромосомы, символ плеча, номер района и номер сегмента в пределах этого района. Например, запись 1р32 означает, что речь идет о хромосоме первой пары, коротком плече, районе 3, сегменте 2. Для гена Rh формула локализации: 1р35. |