Алкалоиды 2019. Алкалоиды классификация Алкалоиды, происходящие из орнитина
 Скачать 1.45 Mb. Скачать 1.45 Mb.
|
|
Физико-химические свойства Большинство алкалоидов, кроме атомов углерода, водорода и азота, содержат и атом кислорода. Есть алкалоиды, которые содержат еще и атом серы. По агрегатному состоянию отличаются алкалоиды содержащие кислород и не содержащие кислород. Кислородсодержащие алкалоиды – кристаллические вещества с определенной температурой плавления, большинство бесцветные, реже окрашенные в желтый (берберин), оранжевый (сангвинарин) или красный (беталаины) цвета. Бескислородные алкалоиды – маслянистые жидкости, легко перегоняются с водяным паром. К этой группе относятся никотин, конин, пахикарпин. Алкалоиды имеют горький вкус, почти все не обладают запахом (исключение оставляют бескислородные алкалоиды, например, никотин). Многие алкалоиды обладают оптической активностью, как правило, один из изомеров имеет более высокую фармакологическую активность. Некоторые алкалоиды флюоресцируют в УФ-свете. Например, цитизин имеет фиолетовую флюоресценцию, а берберин – желто-зеленую. Алкалоиды основания мало растворяются в воде и легко растворяются в органических растворителях. Здесь есть исключения, например, цитизин, кофеин и кодеин хорошо растворимы в воде. Основные (щелочные) свойства алкалоидов выражены в различной степени. Благодаря основному характеру алкалоиды образуют соли с кислотами разной степени прочности. Соли алкалоидов хорошо растворимы в воде и этиловом спирте (особенно в разбавленном), плохо или совсем не растворимы в органических растворителях (хлороформ, этиловый эфир и др.). Правда существуют отдельные исключения из общего правила, например, сульфат хинина плохо растворим в воде, а гидробромидскополамина растворяется в хлороформе. В растениях алкалоиды находятся чаще всего в виде солей и растворены в клеточном соке вакуолей. Соли образованы с широко распространенными органическими кислотами – яблочной, лимонной, щавелевой, винной. Некоторые алкалоиды представляют собой сложные эфиры (атропин, скополамин) и подвергаются гидролизу кислотами и щелочами. Методы выделения В основу принципиальной схемы выделения алкалоидов положены следующие этапы: 1. Экстракция растительного сырья 2. Отделение суммы алкалоидов от других экстрактивных веществ 3. Разделение алкалоидов и очистка индивидуальных веществ Экстракция алкалоидов Выбор растворителя зависит от типа алкалоидов, их физико-химических свойств типа растительного материала и поставленной задачи. При необходимости извлечения из растения кроме алкалоидов соединений других классов с целью комплексного использования сырья применяют полярные растворители, например, спирты, с последующей отгонкой растворителя и переводом алкалоидов в виде их солей в водную фазу, а соединений других классов в органическую. Чаще использую целевую экстракцию алкалоидов, извлекая их в виде оснований из подщелоченного растительного материала малополярными органическими растворителями. Из органических растворителей в промышленности для экстракции алкалоидов чаще всего используют дихлорэтан, который дешев и обладает универсальными свойствами. Одним из лучших растворителей для алкалоидов красавки является диэтиловый эфир, однако в промышленности его в настоящее время почти не применяют из-за взрыво- и пожароопастнисти. Иногда удается подобрать экстрагент, преимущественно извлекающий целевое соединение. Например, хлороформ экстрагирует соли некоторых алкалоидов. Это свойство использовано в технологии получения глауцина из мачка желтого: гидрохлорид глауцина экстрагируют хлороформом из водного раствора суммы гидрохлоридов алкалоидов. Экстракции органическим растворителем предшествует подщелачивание растительного материала NaOH или NH4OH для перевода алкалоидов из солевых форм, в которых они находятся в растительном сырье в форму свободных оснований. При экстракции алкалоидов органическими растворителями в виде оснований, экстракт содержит меньшее количество сопутствующих веществ, нежели при экстракции их водными растворами в виде солей. Метод водной экстракции алкалоидов в форме солей кажется наиболее простым и экономичным. Однако в ряде случаев водная экстракция в производственных условиях сопряжена с существенными технологическими трудностями. В частности она непригодна для извлечения действующих веществ из клубней растений, содержащих большое количество крахмала, вызывающего набухание сырья и затрудняющего фильтрование. Здесь целесообразнее отжимать сок растения, как поступают в случае стефании гладкой, либо использовать органические растворители. Аналогичные трудности возникают при обработке растительного материала, содержащего водорастворимые белковые вещества, способствующие образованию эмульсий при дальнейшей обработке водного раствора органическими растворителями. Обычно для экстракции алкалоидов в виде солей используют не воду, а водные растворы неорганических (HCl, H2SO4) или органических (CH3COOH) кислот, чтобы получить более прочные соли алкалоидов с сильными кислотами. В последние годы показано, чтоN-окиси алкалоидовдовольно широко распространены в растениях. N-окиси гораздо менее основны, чем третичные основания, но гораздо более полярны и лучше растворимы в воде. Как правило, N-окиси выделяются с трудом из-за плохой растворимости в органических растворителях. Поэтому их часто превращают в третичные основания восстановлением бисульфитом натрия, цинковой пылью и др. Получение суммы алкалоидов и разделение по фракциям Концентрирование суммы алкалоидов Отделение суммы алкалоидов или индивидуальных алкалоидов от соединений других классов достигается: 1) обработкой экстракта органического растворителя, водным раствором органической или минеральной кислоты, с последующим подщелачиванием и извлечением выделившихся оснований подходящим органическим растворителем; 2) подщелачиванием водного извлечения и экстракции алкалоидов в форме оснований органическим растворителем; 3) сорбцией водно-кислотного экстракта на катионите с последующей десорбцией подходящим методом (кислотой, солями, спиртовым раствором аммиака и др.) и регенерацией суммы оснований обычными методами; В ряде производств из экстрактов растительного сырья сумму алкалоидов удается выделить в виде труднорастворимых соединений. Четвертичные алкалоиды сангвинарин и хелеритрин можно выделить в виде труднорастворимых бисульфатов при обработке дихлорэтановых экстрактов серной кислотой. В производстве гликоалкалоидов используют осаждение алкалоидов, например, α-томатидина, из метанольного раствора холестерином, образующего с α-томатидином молекулярное соединение в соотношении 1:1. Полученные комплексы разрушают горячим диметилсульфоксидом или кислотой. Для выделения низкомолекулярных алкалоидов может быть использована перегонка в вакууме. Например, перегонкой суммы алкалоидов из семян анабазиса в вакууме (3-4 мм рт. ст.) получен жидкий алкалоид анабазин и кристаллический лупинин. Методы разделения алкалоидов 1.Разделение алкалоидов разгонкой в вакууме Разделение жидких алкалоидов или отделение жидких алкалоидов от кристаллических можно осуществить разгонкой в вакууме. Если жидкие алкалоиды существенно различаются температурами кипения их довольно легко можно отделить друг от друга фракционной вакуум-перегонкой. В качестве примера отделения жидкого алкалоида от кристаллических можно привести промышленный способ получения алкалоида пахикарпина (жидкий) из травы софоры толстоплодной, когда выделенную сумму алкалоидов нагревают в вакууме до 160-210 ◦С (Рост.=15-20 мм рт. ст.) и отгоняют пахикарпин. В методике количественного определения пахикарпина в траве софоры толстоплодной выделенную смесь алкалоидов нагревают с водой и отгоняют пахикарпин согласно закону Дальтона о парциальных давлениях. К отгону добавляют избыток раствора серной кислотой и оттитровывают его NaOH. 2. Разделение алкалоидов на основе разной растворимости 2.1. Кристаллизация.Метод основан на различной растворимости алкалоидов оснований или их солей в некоторых растворителях. Примером такого разделения может быть разделение двух основных алкалоидов крестовника плосколистного платифиллина и сенецифиллина, путем образования их виннокаменной соли, которая у платифиллина плохо растворима в спирте и выпадает в осадок, а у сенецифиллина хорошо растворяется в спирте. Другим похожим примером является отделение алкалоида берберина от других алкалоидов барбариса (пальматина, ятроризина) в виде бисульфата, который плохо растворяется в спирте и воде, в отличие от сульфатных солей указанных алкалоидов. 2.2.Избирательная жидкость-жидкостная экстракция. Если в предыдущем случае использовалась плохая растворимость алкалоидов в определенных растворителях, в данном варианте напротив хорошая селективная растворимостьотдельных алкалоидов. Например, соли отдельных алкалоидов могут растворяться в органических растворителях, что позволяет их избирательно экстрагировать из водных растворов. В качестве примера можно привести избирательную экстракцию глауцина гидрохлорида из водного раствора насыщенного хлоридом натрия хлороформом, в методике его получения из травы мачка желтого. 3. Разделение алкалоидов по основности Важный критерий при разделении алкалоидов константа кислотности (ионизации)рКА, позволяющая определить область рН в которой алкалоид менее всего ионизирован и переходит в органическую фазу из водных растворов. Алкалоиды могут иметь различную основность в зависимости от радикалов у атомов азота и в общей структуре алкалоидов. Чем больше алифатических радикалов у атома азота, тем более сильными основаниями являются алкалоиды, а ароматические радикалы уменьшают основность алкалоидов. Например, возрастание основности происходит в ряду NH2CH3→NH(CH3)2→ NH(CH3)3, и напротив уменьшение основности происходит в ряду NH2(C6H5) ←NH2(C6H5)2 ←NH2(C6H5)3. Подобное влияние радикалов на основность алкалоидов связано с тем, что алифатические группировки электродонорные и, следовательно, усиливают электроотрицательность азота и увеличивают у него плотность электронов, а ароматические, карбонильные, карбоксильные и другие – акцепторные, они оттягивает электроны и уменьшают основность. Международной ассоциацией химиков принято основность всех соединений выражать черезрКА (отрицательный логарифм константы кислотности). При этом исходят из того, что каждому основанию соответствует в растворе сопряженная кислота. Вода как растворитель обладает как кислотными, таки и основными свойствами: Н2О + Н2О = Н3О+ + ОН– Алкалоид, проявляя себя основанием в воде, взаимодействует с протоном по следующему уравнению: R3N + Н2О=R3NH++ ОН– Приведенная реакция обратима, одновременно протекает следующий процесс: R3NH+ + Н2О=R3N+ Н3О+ Приведенные уравнения демонстрируют, что вода ведет себя как кислота и как основание. В чистой воде и в любом водном растворе (при постоянной температуре) произведение концентраций ионов водорода и гидроксила постоянно и равно 1∙10-14 (-lg KW=14). Исходя из изложенного, силу основности соединений можно выражать константой кислотности сопряженной кислоты, обратно пропорциональной константе основности: KА = 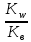 , pKА = 14 – pKВ , pKА = 14 – pKВКонстанты кислотности и основности некоторых алкалоидов
С кислотами алкалоиды образуют соли. Механизм солеобразованиия – действие протона на неподеленную пару электронов азота с образованием координационной и ионной связи, т.е. возникновение семиполярной (полуполярной) связи. Происходит полное присоединение молекулы кислоты с образованием соли и последующей диссоциацией на катион и анион. H2O R3N: + НCl = R3N:+HCl–↔ [R3NH]++ Cl– Чем выше основность алкалоидов, тем легче они образуют соли. Слабые основания солей не образуют, например кофеин. Поскольку в одном растении находятся алкалоиды с разной основностью, их можно предварительно разделить на фракции, проводя экстракцию при разных значениях рН растворов. Слабоосновные алкалоиды извлекаются при низких значениях рН, сильноосновные – при высоких. В качестве одного из примеров можно привести технологию получения алкалоида аймалина из альтернативного сырья – биомассы раувольфии змеиной. Высушенная биомасса содержит сумму алкалоидов (более 2%), в том числе аймалин, резерпин, серпентин. Константы кислотности и основности некоторых алкалоидов раувольфии
Аймалин – основание средней силы основности, т.к. содержит метильную группу у атома азота в положении 2 и отсутствует в положении 2-3 двойная связь. Сначала биомассу экстрагируют 50% этиловым спиртом, затем спирт отгоняют и извлекают алкалоиды из водного остатка хлороформом предварительно подщелочив ее аммиаком до рН=9,5-10. Аймалин избирательно экстрагируют из хлороформного раствора лимонно-фосфорным буферным водным раствором (рН=5,5-5,6). Аймалин переходит в буферный раствор, а более слабые основания остаются в хлороформе. Аналогичный подход использован в методик количественного определения гиндарина в клубнях с корнями стефании гладкой. Клубни с корнями стефании гладкой содержат наряду с гиндарином и другие алкалоиды – стефаглабрин, циклеанин, ротундин и др., среди которых гиндарин является наиболее слабым основанием. По методике измельченное сырье стефании гладкой экстрагируют хлороформом, предварительно смочив его аммиаком. Из полученного хлороформного раствора алкалоиды извлекают 10% раствором серной кислоты. Объединённые кислотные извлечения доводят раствором аммиака до pН=5, и обрабатывают хлороформом, взбалтывая каждый раз в течение 5 минут. Как наиболее слабое основание гидарин окажется в хлороформном растворе и будет отделен от других алкалоидов. 4. Разделение алкалоидов хроматографическими методами Чаще других для разделения алкалоидов используют окись алюминия и силикагель. Разделение основано на разном сродстве к сорбенту и элюирующим растворителям разделяемых соединений. Хроматография на окиси алюминия применена в технологической схеме получения глауцина из травы мачка желтого. В технологии получения алкалоидов спорыньи, разработанной вВИЛАРе также используется колоночная хроматография на окиси алюминия. Сначала с колонки вымывается эрготамин, обладающий более слабыми основными свойствами, затем при элюировании более полярным растворителем вымывается эргометрин с более сильными основными свойствами. В аналитических методиках чаще используется хроматографическое разделение алкалоидов на тонкослойных пластинах с силикагелем, в качестве примеров можно привести методику количественного определения глауцина в траве мачка желтого и методику определения алкалоидов хелеретнина и сангвинарина в траве маклеи. В последние годы для аналитических определений алкалоидов широко используется метод ВЭЖХ. Качественный анализ алкалоидов Для обнаружения алкалоидов в растительном сырье чаще всего используют общие (осадочные), специфические (цветные) реакции и хроматографию. Реакции осаждения позволяют установить наличие алкалоидов даже при незначительном содержании их в сырье. Они основаны на том, что алкалоиды при взаимодействии с некоторыми веществами образуют нерастворимые в воде соединения. Это главным образом соли тяжелых металлов, комплексные иодиды, комплексные неорганические кислоты и некоторые органические соединения кислотного характера. Для проведения качественных реакций из растительного сырья готовят водно-кислотное извлечение. Наиболее часто используют следующие реактивы: 1. Йод и его растворы. 1. Реактивы Вагнера (1 г I2 и 2г KI в 50 мл Н2О) и Бушарда (2 г I2 и 5г KI в 100 мл Н2О) с алкалоидами образуют бурые осадки. |
