Билеты по микре. BILET_PO_MIKRE_ответы. Билет 1 Микробиология как фундаментальная наука. Ее задачи
 Скачать 0.54 Mb. Скачать 0.54 Mb.
|
|
2. Реакция агглютинации. Реакция агглютинации — простая по постановке реакция, при которой происходит связывание антителами корпускулярных антигенов (бактерий, эритроцитов или других клеток, нерастворимых частиц с адсорбированными на них антигенами, а также макромолекулярных агрегатов). Она протекает при наличии электролитов, например при добавлении изотонического раствора натрия хлорида. Применяются различные варианты реакции агглютинации: развернутая, ориентировочная, непрямая и др. Реакция агглютинации проявляется образованием хлопьев или осадка (клетки, «склеенные» антителами, име ющими два или более антигенсвязывающих центра — рис. 13.1). РА используют для: 1) определения антител в сыворотке крови больных, например, при бруцеллезе (реакции Райта, Хеддельсона), брюшном тифе и паратифах (реакция Видаля) и других инфекционных болезнях; 2) определения возбудителя, выделенного от больного; 3) определения групп крови с использованием моноклональных антител против алло-антигенов эритроцитов. Для определения у больного антител ставят развернутую реакцию агглютинации: к разведениям сыворотки крови больного добавляют диагностикум (взвесь убитых микробов,) и через несколько часов инкубации при 37 ˚С отмечают наибольшее разведение сыворотки (титр сыворотки), при котором произошла агглютинация, т. е. образовался осадок. Характер и скорость агглютинации зависят от вида антигена и антител. Примером являются особенности взаимодействия диагностикумов (О- и H-антигенов) со специфическими антителами. Реакция агглютинации с О-диагностикумом (бактерии, убитые нагреванием, сохранившие термостабильный О-антиген) происходит в виде мелкозернистой агглютинации. Реакция агглютинации с Н-диагностикумом (бактерии, убитые формалином, сохранившие термолабильный жгутиковый Н-антиген) — крупнохлопчатая и протекает быстрее. Если необходимо определить возбудитель, выделенный от больного, ставят ориентировочную реакцию агглютинации, применяя диагностические антитела (агглютинирующую сыворотку), т. е. проводят серотипирование возбудителя. Ориентировочную реакцию проводят на предметном стекле. К капле диагностической агглютинирующей сыворотки в разведении 1:10 или 1:20 добавляют чистую культуру возбудителя, выделенного от больного. Рядом ставят контроль: вместо сыворотки наносят каплю раствора натрия хлорида. При появлении в капле с сывороткой и микробами хлопьевидного осадка ставят развернутую реакцию агглютинации в пробирках с увеличивающимися разведениями агглютинирующей сыворотки, к которым добавляют по 2—3 капли взвеси возбудителя. Агглютинацию учитывают по количеству осадка и степени просветления жидкости. Реакцию считают положительной, если агглютинация отмечается в разведении, близком к титру диагностической сыворотки. Одновременно учитывают контроли: сыворотка, разведенная изотоническим раствором натрия хлорида, должна быть прозрачной, взвесь микробов в том же растворе — равномерно мутной, без осадка. Разные родственные бактерии могут агглютинироваться одной и той же диагностической агглютинирующей сывороткой, что затрудняет их идентификацию. Поэтому пользуются адсорбированными агглютинирующими сыворотками, из которых удалены перекрестно реагирующие антитела путем адсорбции их родственными бактериями. В таких сыворотках сохраняются антитела, специфичные только к данной бактерии. 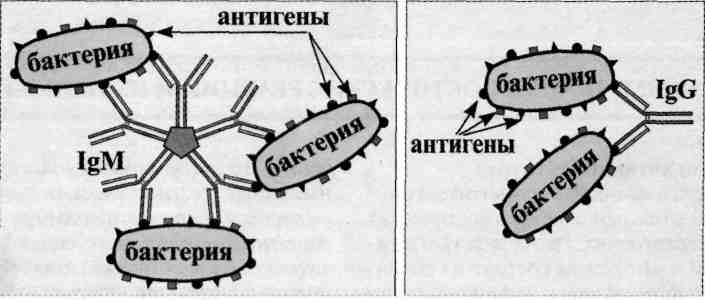 Реакция непрямой (пассивной) гемагглютинации (РНГА, РПГА) основана на использовании эритроцитов (или латекса) с адсорбированными на их поверхности антигенами или антителами, взаимодействие которых с соответствующими антителами или антигенами сыворотки крови больных вызывает склеивание и выпадение эритроцитов на дно пробирки или ячейки в виде фестончатого осадка. Компоненты. Для постановки РНГА могут быть использованы эритроциты барана, лошади, кролика, курицы, мыши, человека и другие, которые заготавливают впрок, обрабатывая формалином или глютаральдегидом. Адсорбционная емкость эритроцитов увеличивается при обработке их растворами танина или хлорида хрома. Антигенами в РНГА могут служить полисахаридные АГ микроорганизмов, экстракты бактериальных вакцин, АГ вирусов и риккетсий, а также другие вещества. Эритроциты, сенсибилизированные АГ, называются эритроцитарными диагностикумами. Для приготовления эритроцитарного диагностикума чаще всего используют эритроциты барана, обладающие высокой адсорбирующей активностью. Применение. РНГА применяют для диагностики инфекционных болезней, определения гонадотропного гормона в моче при установлении беременности, для выявления повышенной чувствительности к лекарственным препаратам, гормонам и в некоторых других случаях. Механизм. Реакция непрямой гемагглютинации (РНГА) отличается значительно более высокой чувствительностью и специфичностью, чем реакция агглютинации. Ее используют для идентификации возбудителя по его антигенной структуре или для индикации и идентификации бактериальных продуктов — токсинов в исследуемом патологическом материале. Соответственно используют стандартные (коммерческие) эритроцитарные антительные диагностикумы, полученные путем адсорбции специфических антител на поверхности танизированных (обработанных танином) эритроцитов. В лунках пластмассовых пластин готовят последовательные разведения исследуемого материала. Затем в каждую лунку вносят одинаковый объем 3 % суспензии нагруженных антителами эритроцитов. При необходимости реакцию ставят параллельно в нескольких рядах лунок с эритроцитами, нагруженными антителами разной групповой специфичности. Через 2 ч инкубации при 37 °С учитывают результаты, оценивая внешний вид осадка эритроцитов (без встряхивания): при отрицательной реакции появляется осадок в виде компактного.диска или кольца на дне лунки, при положительной реакции — характерный кружевной осадок эритроцитов, тонкая пленка с неровными краями. 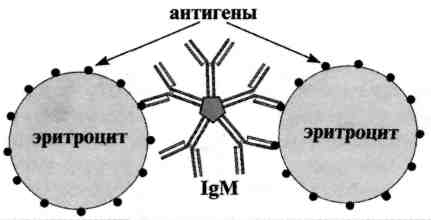 Реакцию коагглютинации применяют для определения антигенов с помощью антител, адсорбированных на белке А клеток стафилококка (антительный диагностикум). Белок А имеет сродство к Fc-фрагменту иммуноглобулинов, поэтому такие бактерии, обработанные иммунной диагностической сывороткой неспецифически адсорбируют антитела сыворотки, которые затем взаимодействуют активными центрами с соответствующими микробами, выделенными от больных. В результате коагглютинации образуются хлопья, состоящие из стафилококков, антител диагностической сыворотки и определяемого микроба. Механизм. Основан на том, что находящийся на поверхности золотистого стафилококка белок А селективно реагирует с Fc-фрагментом IgGl, G2, G4, оставляя свободными антидетерминанты Ат, которые, взаимодействуя с гомологичным Аг, вызывают агглютинацию стафилококков. Для постановки КОА применяют коммерческие стафилококковые реагенты, содержащиеся в ампулах или высушенные в лунках полистироловых пластин или предметных стекол. К реагенту добавляют 0,01-0,1 мл исследуемой культуры или растворимого Аг, инкубируют при комнатной температуре 10-30 мин (в условиях постановки реакции на стекле) или 18 -20 ч (в условиях постановки реакции в капиллярах). Учет проводят так же, как при обычной РА. Агглютинацию учитывают по количеству осадка и степени просветления жидкости. Реакцию считают положительной, если агглютинация отмечается в разведении, близком к титру диагностической сыворотки. Одновременно учитывают контроли: сыворотка, разведенная изотоническим раствором натрия хлорида, должна быть прозрачной, взвесь микробов в том же растворе — равномерно мутной, без осадка. 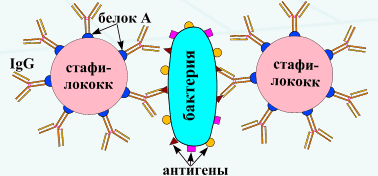 Реакция торможения гемагглютинации (РТГА) - метод идентификации вируса или выявления противовирусных антител в сыворотке крови больного, основанный на феномене отсутствия агглютинации эритроцитов препаратом, содержащим вирус, в присутствии иммунной к нему сыворотки крови. Реакция торможения гемагглютинации (РТГА) основана на блокаде, подавлении антигенов вирусов антителами иммунной сыворотки, в результате чего вирусы теряют свойство агглютинировать эритроциты. РТГА применяют для диагностики многих вирусных болезней, возбудители которых (вирусы гриппа, кори, краснухи, клещевого энцефалита и др.) могут агглютинировать эритроциты различных животных. Механизм. Типирование вируса проводят в реакции торможения гемаг-глютинации (РТГА) с набором типоспецифических сывороток. Результаты реакции учитывают по отсутствию гемагглютинации. Подтипы вируса А с антигенами H0N1, H1N1, Н2N2, H3N2 и др. могут быть дифференцированы в РТГА с набором гомологичных типоспецифических сывороток. 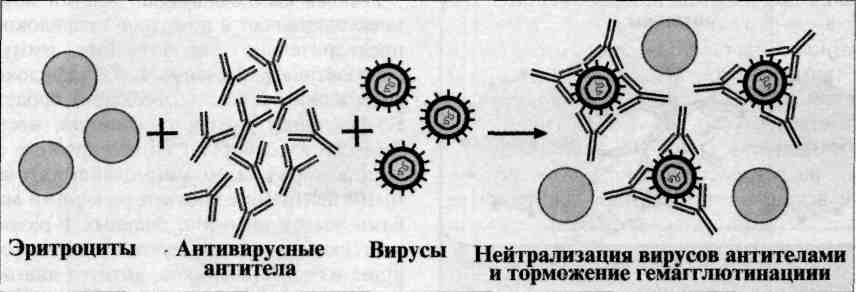 3. Лептоспиры и боррелии. Свойства, патогенез, заболевания, иммунитет, лабораторная диагностика, профилактика. Лептоспиры являются возбудителями зоонозной бактериальной инфекции, характеризующейся волнообразной лихорадкой, интоксикацией, поражением капилляров печени, почек, ЦНС. Возбудитель L. interrhogansотносится к семейству Leptospiraceae, poд Leptospira. Морфология. Лептоспиры представляют собой тонкие спирохеты, с изогнутыми концами. Двигательный аппарат - фибриллы. Легко различимы при микроскопии в темном поле и фазово-контрасте. Цист не образуют. Культуральные и биохимические свойства. Аэробы. Источником углерода и энергии служат липиды. Каталаза-и оксидазаположительны. Культивируются на питательных средах, содержащих сыворотку или сывороточный альбумин, при температуре 30С. Особенность роста на жидкой питательной среде — отсутствие помутнения. Делятся поперечным делением. Растут медленно. Цист не образуют. Антигенная структура. Содержат общеродовой антиген белковой природы, выявляемый в PCК, а также вариантоспецифический поверхностный антиген липополисахаридной природы, выявляемый в реакции агглютинации. Таксономическим критерием для лептоспир служит антигенный состав. Основным таксоном является серовар.Серовары объединены в серогруппы (насчитывается более 25 серогрупп). Резистентность. L. interrhogansчувствительна к высыханию, нагреванию, низким значениям рН, дезинфицирующим веществам. При нагревании до 56С погибает в течение 25—30 мин. Кипячение убивает микроб мгновенно. Эпидемиология. Лептоспироз относится к природно-очаговым зоонозам, с преимущественно фекально-оральным механизмом передачи возбудителя. Основным резервуаром и источником инфекции служат домовые и полевые грызуны, дополнительными — домашние животные. У диких животных инфекция имеет хроническое течение без клинических проявлений, при этом возбудитель выделяется с мочой, загрязняя водоемы и почву. Каждый из сероваров циркулирует в популяции определенного вида животного и является самостоятельным возбудителем заболевания. Восприимчивость людей к лептоспирозу высокая, но больной человек, хотя и выделяет лептоспиры в окружающую среду не имеет практического значения в распространении заболевания. Основные пути передачи: водный, алиментарный, контактный. Факторы патогенности. Некоторые серовары характеризуются гемолитической и липазной активностью, продуцируют плазмокоагулазу, фибринолизин, цитотоксины. Патогенез и клиника заболевания. острая инфекционная болезнь, которая вызывается различными сероварами. Инкубационный период составляет 7—10 дней. Входные ворота — слизистые оболочки пищеварительного тракта, поврежденная кожа. Проникнув в организм, микроб с кровью разносится к органам ретикулоэндотелиальной системы (печень, почки), где размножается и вторично поступает в кровь, что совпадает с началом болезни. Возбудитель поражает капилляры печени, почек, ЦНС, что приводит к развитию геморрагии в этих органах. Болезнь протекает остро, с явлениями волнообразной лихорадки, интоксикации, с желтухой, развитием почечной недостаточности, асептического менингита. Иммунитет: Стойкий, гуморальный, серовароспецифический иммунитет. Микробиологическая диагностика. Материалом для исследования служат кровь, спинномозговая жидкость, моча, сыворотка крови в зависимости от стадии заболевания. Для диагностики используют бактериоскопический (обнаружение лептоспир в темнопольном микроскопе), бактериологический и серологические методы (РА, РСК), а также применяют ПЦР. Биопробу на кроликах. Профилактика и лечение. Специфическая профилактика проводится вакцинацией по эпидемическим показаниям убитой нагреванием, корпускулярной вакциной, содержащей 4 основных серогруппы возбудителя. Для лечения используют антибиотики (пенициллин, тетрациклин) в сочетании с лептоспирозным гетерологичным иммуноглобулином. Спирохеты рода Borreliaвызывают антропонозные (возвратный тиф), зоонозные (болезни Лайма) инфекционные болезни с трансмиссивным механизмом передачи возбудителей (клещи, вши). Морфологические свойства: тонкие спирохеты с крупными завитками. Двигательный аппарат представлен фибриллами. Они хорошо воспринимают анилиновые красители, по Романовскому—Гимзе окрашиваются в сине-фиолетовый цвет. Боррелии обладают генетическим аппаратом, который состоит из небольших размеров линейной хромосомы и набора циркулярных и линейных плазмид. Культуральные свойства: культивируются на сложных питательных средах, содержащих сыворотку, тканевые экстракты, а также в куриных эмбрионах. Чувствительны к высыханию и нагреванию. Устойчивы к низким t-рам. Болезнь Лайма - возбудитель В. burgdorferi. Хроническая инфекция с поражением кожи, сердечной и нервной систем, суставов. Морфология и культуральные свойства: типичные боррелии. Антигенная структура: Сложная. Белковые антигены фибриллярного аппарата и цитоплазматического цилиндра, антитела к которым появляются на ранних этапах инфекции. Протективную активность имеют антигены, представленные липидмодифицированными интегральными белками наружной мембраны А, В, С, D, E, F. Факторы патогенности. Липидмодифицированные белки наружной мембраны обеспечивают способность боррелий прикрепляться и проникать в клетки хозяина. В результате взаимодействия боррелий с макрофагами происходит выделение ИЛ-1, который индуцирует воспалительный процесс. Патогенез: На месте укуса клеща образуется красная папула. Возбудитель распространяется из места укуса через окружающую кожу с последующей диссеминацией с током крови к различным органам, особенно сердцу, ЦНС, суставам. Клиника подразделяется на 3 стадии: 1.Мигрирующая эритема, которая сопровождается развитием гриппоподобного симптомокомплекса. 2.Развитие доброкачественных поражений сердца и ЦНС 3.Развитие артритов крупных суставов Иммунитет. Гуморальный, видоспецифический к антигенам клеточной стенки. Микробиологическая диагностика. Используются бактериоскопический, серологический методы и ПЦР в зависимости от стадии заболевания. Материалом для исследования служат биоптаты кожи, синовиальная жидкость суставов, ликвор, сыворотка крови. На 1-й стадии заболевания проводится бактериологическое исследование биоптатов кожи из эритемы. Начиная со 2-й стадии заболевания осуществляется серологическое исследование определением IgM или нарастания титра IgG ИФА или РИФ. ПЦР используется для определения наличия боррелий в ликворе, суставной жидкости. Лечение: антибиотики тетрациклинового ряда. Профилактика. Неспецифическая. Возвратные тифы — группа острых инфекционных заболеваний, вызываемых боррелиями, характеризующихся острым началом, приступообразной лихорадкой, общей интоксикацией. Различают эпидемический и эндемический возвратные тифы. Возбудителем эпидемического возвратного тифа является В. recurrentis. Эпидемический возвратный тиф - антропоноз. Специфические переносчики - платяная, головная вши. Человек заражается возвратным тифом при втирании гемолимфы раздавленных вшей в кожу при расчесывания места укуса. Эндемический возвратный тиф— зооноз. Возбудители - В. duttoniи В. persica. Резервуар - грызуны, клещи. Человек заражается через укусы клещей. Патогенез: Попав во внутреннюю среду организма, боррелии внедряются в клетки лимфоидно-макрофагальной системы, где размножаются и поступают в кровь, вызывая лихорадку, головную боль, озноб. Взаимодействуя с АТ, боррелии образуют агрегаты, которые нагружаются тромбоцитами, вызывая закупорку капилляров, следствием чего является нарушение кровообращения в органах. Иммунитет: к эпидемическому возвратному тифу гуморальный, непродолжительный. Микробиологическая диагностика. Бактериоскопический метод — обнаружение возбудителя в крови, окрашенной по Романовскому—Гимзе. Биопробу ставят для дифференциации В. recurrentisот возбудителей эндемического возвратного тифа.В качестве вспомогательного используют серологический метод с постановкой РСК. Лечение: антибиотики тетрациклинового ряда, левомицетин, ампициллин. Профилактика. Неспецифическая. Билет 21 1. Основные методы и принципы культивирования бактерий. Питательные среды, классификация. Основные методы создания анаэробных условий для культивирования микроорганизмов. 1.Физический- откачивание воздуха, введение специальной газовой безкислородной смеси (чаще- N2- 85%, CO2- 10%, H2- 5%). 2.Химический- применяют химические поглотители кислорода. 3.Биологический- совместное культивирование строгих аэробов и анаэробов (аэробы поглощают кислород и создают условия для размножения анаэробов). 4.Смешанный- используют несколько разных подходов. Необходимо отметить, что создание оптимальных условий для строгих анаэробов- очень сложная задача. Очень непросто обеспечить постоянное поддержание безкислородных условий культивирования, необходимы специальные среды без содержания растворенного кислорода, поддержание необходимого окислительно- восстановительного потенциала питательных сред, взятие и доставка, посев материала в анаэробных условиях. Существует ряд приемов, обеспечивающих более подходящие условия для анаэробов- предварительное кипячение питательных сред, посев в глубокий столбик агара, заливка сред вазелиновым маслом для сокращения доступа кислорода, использование герметически закрывающихся флаконов и пробирок, шприцев и лабораторной посуды с инертным газом, использование плотно закрывающихся эксикаторов с горящей свечой. Используются специальные приборы для создания анаэробных условий- анаэростаты. Однако в настоящее время наиболее простым и эффективным оборудованием для создания анаэробных и микроаэрофильных условий является система “Газпак” со специальными газорегенерирующими пакетами, действующими по принципу вытеснения атмосферного воздуха газовыми смесями в герметически закрытых емкостях. Основные принципы культивирования микроорганизмов на питательных средах. 1.Использование всех необходимых для соответствующих микробов питательных компонентов. 2.Оптимальные температура, рН, rH2, концентрация ионов, степень насыщения кислородом, газовый состав и давление. Микроорганизмы культивируют на питательных средах при оптимальной температуре в термостатах, обеспечивающих условия инкубации. По температурному оптимуму роста выделяют три основные группы микроорганизмов. 1.Психрофилы- растут при температурах ниже +20 градусов Цельсия. 2.Мезофилы- растут в диапозоне температур от 20 до 45 градусов (часто оптимум- при 37 градусах С). 3.Термофилы- растут при температурах выше плюс 45 градусов. Краткая характеристика питательных сред. По консистенции выделяют жидкие, плотные (1,5- 3% агара) и полужидкие (0,3- 0,7 % агара) среды. Агар- полисахарид сложного состава из морских водорослей, основной отвердитель для плотных (твердых) сред. В качестве универсального источника углерода и азота применяют пептоны- продукты ферментации белков пепсином, различные гидролизаты- мясной, рыбный, казеиновый, дрожжевой и др. По назначению среды разделяют на ряд групп: - универсальные (простые), пригодные для различных нетребовательных микроорганизмов (мясо- пептонный бульон- МПБ, мясо- пептонный агар- МПА); - специальные- среды для микроорганизмов, не растущих на универсальных средах (среда Мак- Коя на туляремию, среда Левенштейна- Иенсена для возбудителя туберкулеза); - дифференциально- диагностические- для дифференциации микроорганизмов по ферментативной активности и культуральным свойствам ( среды Эндо, Плоскирева, Левина, Гисса); - селективные (элективные)- для выделения определенных видов микроорганизмов и подавления роста сопутствующих- пептонная вода, селенитовая среда, среда Мюллера. По происхождению среды делят на естественные, полусинтетические и синтетические. |
