|
|
Ответы на дополнительные задачи. Дополнительный список 2006 год
№ 28 После предшествующего 5-часового перерыва в приеме пищи, студентка выпила сладкий чай с пирожным. Как изменится обмен углеводов в печени в этой ситуации? При ответе представьте схемы, объясняющие как гормоны «переключают» обмен углеводов в печени при переходе от постабсорбтивного состояния к абсорбтивному.
Углеводы пойдут на синтез жиров и произойдёт их депонирование, также произойдёт активация аэробного гликолиза и синтез гликогена.
Синтез жирных кислот Синтез гликогена (ниже)
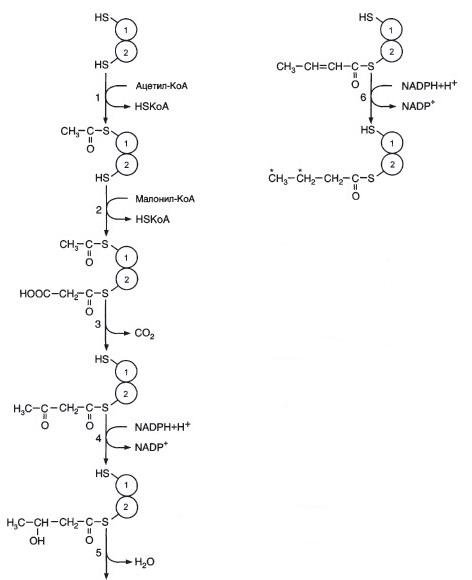 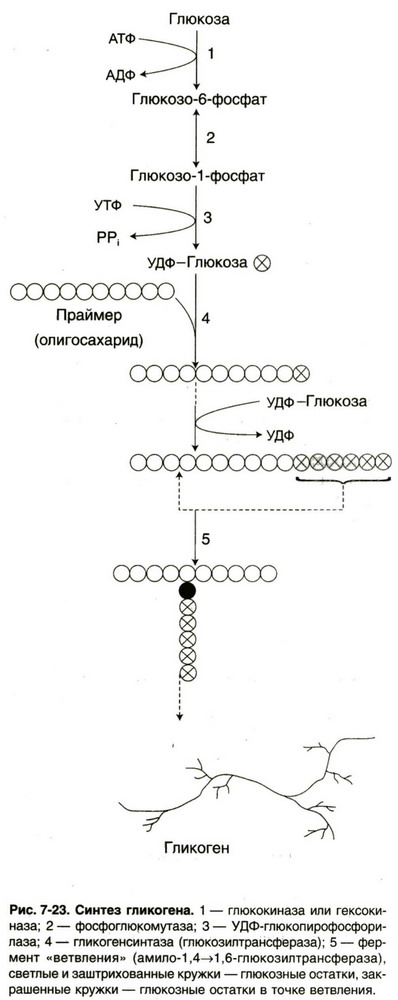
Аэробный распад глюкозы
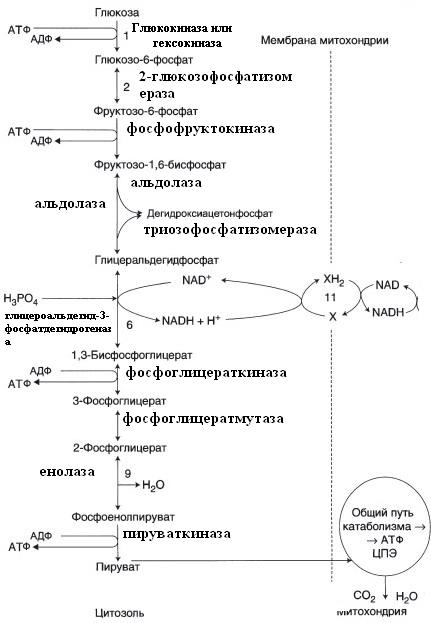
|
№ 29 Спортсмен совершает 5-километровую пробежку. Укажите, поток каких метаболитов увеличивается из мышц в печень к концу дистанции. Напишите краткие схемы возможных превращений этих веществ в печени в данной ситуации. Объясните значение этих процессов.
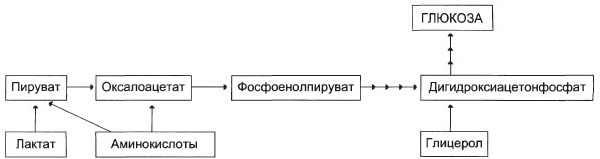
У спортсмена совершающего пробежку в интенсивно работающих мышцах происходят процессы гликолиза, при этом в результате анаэробного гликолиза (в первые минуты - при нехватке кислорода (затем идет аэробный), и при длительной работе) образуется лактат. Он вступает в "глюкозо-лактатный цикл", или цикл "Кори".
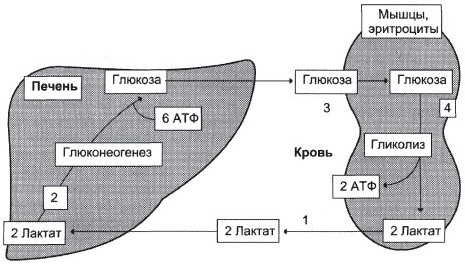
В печени отношение NADH\NAD+ ниже, чем в сокращающейся мышце, поэтому лактатдегидрогеназная реакция протекает в сторону образования пирувата из лактата. Далее пируват включается в глюкогенез, а образовавшаяся глюкоза поступает в кровь и поглощается скелетными мышцами.
Значение.
1) утилизация лактата - предотвращение лактоацидоза;
2) синтез глюкозы
При длительной мышечной работе могут образовываться аминокислоты, в результате распада мышечных белков, которые при катаболизме превращаются в пируват или метаболиты цитратного цикла (гликогенный аминокислоты) и способны включаться в глюконеогенез.
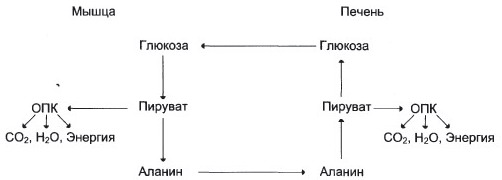
Значение: транспорт аминного азота из мышц в печень и предотвращение лактоацидоза.
|
№ 30 При длительной физической работе в крови повышается концентрация лактата. Объясните, как лактат может использоваться в этой ситуации в миокарде, напишите схему соответствующего метаболического пути.
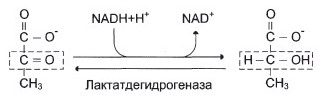
Пируват потом переходит в ЦТК.
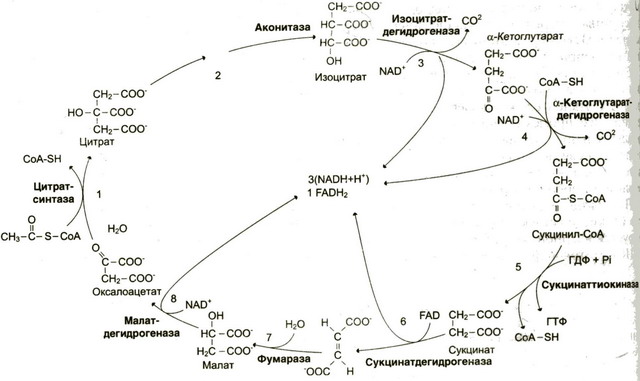
|
№ 33 Основное значение регуляции скоростей синтеза и распада гликогена в печени заключается в поддержании постоянной концентрации глюкозы в крови. Укажите концентрацию глюкозы в крови в норме. Объясните роль гормонов в регуляции активности ключевых ферментов обмена гликогена. Ответ проиллюстрируйте соответствующими схемами.
Концентрация глюкозы в норме: 3,3-5,5 ммоль/л (60-100 мг/дл).
Гормоны, регулирующие метаболизм гликогена: инсулин и глюкагон. Первичный сигнал для их синтеза - изменение концентрации глюкозы в крови. При повышении инсулин/глюкагонового индекса идет синтез гликогена, при понижении - распад.
Механизм действия глюкагона:
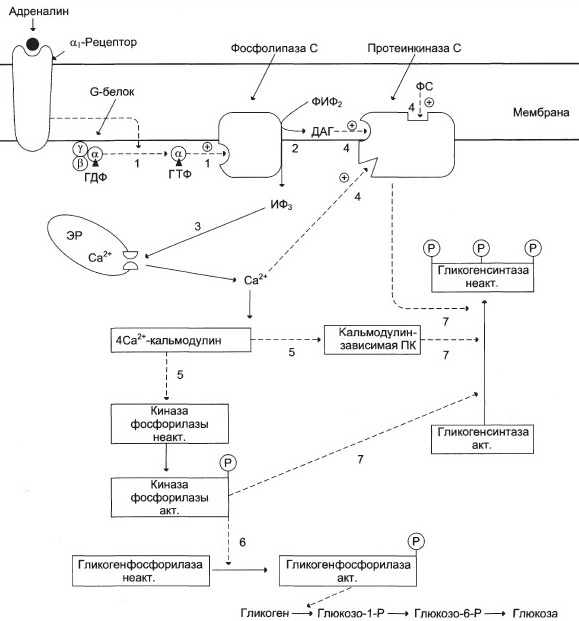
Влияние инсулина:
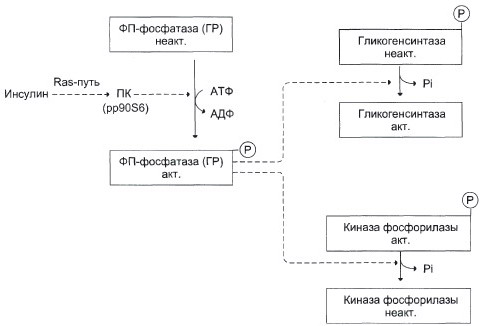
Так же на обмен гликогена может влиять адреналин в экстремальной ситуации.
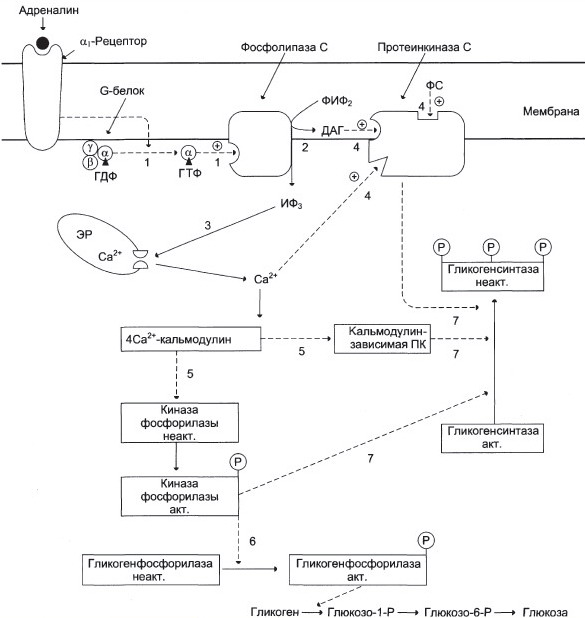
Какая система передачи сигнала в клетку будет использована, зависит от рецепторов, с которыми взаимодействует адреналин.
|
№ 32 Из клеток печени двух крыс был выделен бифункциональный фермент (БИФ), в фосфорилированной и дефосфорилированной формах, имеющих разную ферментативную активность. Объясните особенности функционирования этого фермента. Какую роль играет БИФ в регуляции обмена углеводов в печени животных?
Б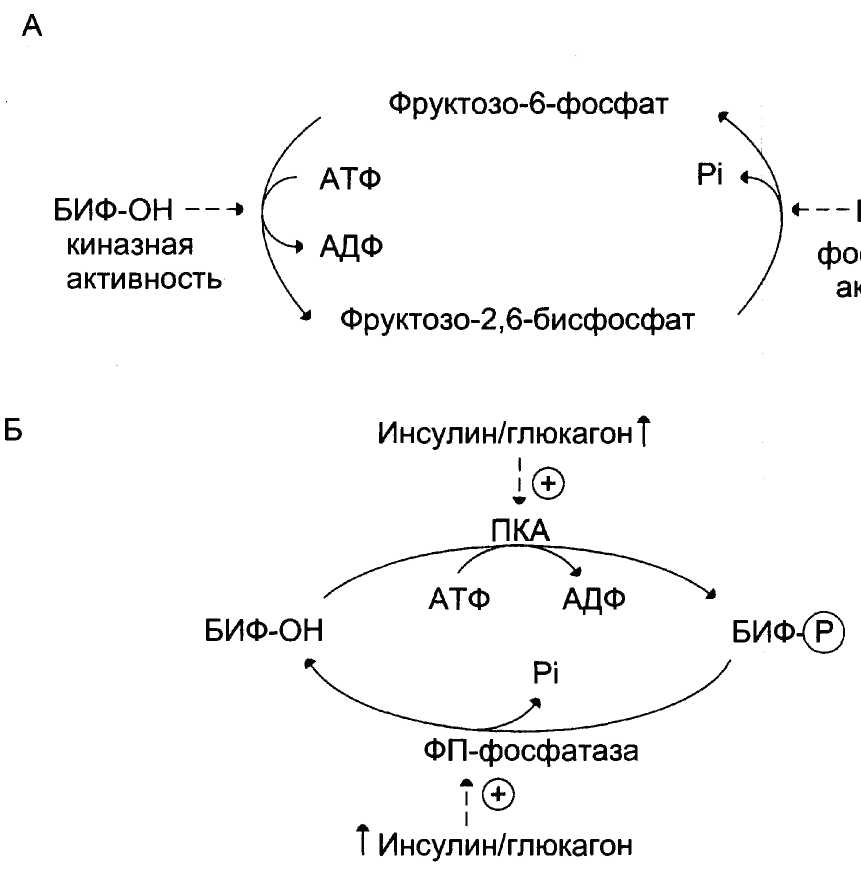 ифункциональный фермент (БИФ) катализирует прямую и обратную реакции образования фруктозо-2,6-бисфосфата путём фосфорилирования фруктозо-6-фосфата. Однако превращение фруктозо-2,6-бисфосфата в фрук-тозо-6-фосфат не является обратимым процессом. Образование фруктозо-2,6-бисфосфата требует затрат АТФ, а при образовании фруктозо-6-фосфата из фруктозо-2,6-бисфосфата гидролитически отщепляется неорганический фосфат. ифункциональный фермент (БИФ) катализирует прямую и обратную реакции образования фруктозо-2,6-бисфосфата путём фосфорилирования фруктозо-6-фосфата. Однако превращение фруктозо-2,6-бисфосфата в фрук-тозо-6-фосфат не является обратимым процессом. Образование фруктозо-2,6-бисфосфата требует затрат АТФ, а при образовании фруктозо-6-фосфата из фруктозо-2,6-бисфосфата гидролитически отщепляется неорганический фосфат.
В реакции фосфорилирования фруктозо-6-фосфата фермент проявляет киназную активность, а при дефосфорилировании образованного фруктозо-2,6-бисфосфата — фосфатазную. Это обстоятельство и определило название фермента «бифункциональный».
Киназная активность БИФ проявляется, когда фермент находится в дефосфорилированной форме (БИФ-ОН). Дефосфорилированная форма БИФ характерна для абсорбтивного периода, когда инсулин/глюкагоновый индекс высокий. В этот период количество фруктозо-2,6-бисфос-фата увеличивается.
При низком инсулин-глюкагоновом индексе, характерном для периода длительного голодания, происходит фосфорилирование БИФ, и он функционирует как фосфатаза. Результат — снижение количества фруктозо-2,6-бисфосфата.
Киназную и фосфатазную реакции катализируют разные активные центры БИФ, но в каждом из двух состояний фермента (фосфорили-рованном и дефосфорилированном) один из активных центров ингибирован. Регуляторное влияние фруктозо-2,6-бисфосфата заключается в том, что он аллостерически активирует фосфофруктокиназу (фермент гликолиза). При этом фруктозо-2,6-бисфосфат снижает ингибирующее действие АТФ на этот фермент в абсорбтивном периоде и повышает его сродство к фруктозо-6-фосфату. В то же время фруктозо-2,6-бисфос-фат ингибирует фруктозо-1,6-бисфосфатазу (фермент глюконеогенеза). Итак, в абсорбтивном периоде уровень фруктозо-2,6-бисфосфата повышается, что приводит к активации фосфофруктокиназы и ускорению гликолиза. Результатом уменьшения количества фруктозо-2,6-бисфосфата в постабсорбтивном периоде будет снижение активности фосфофруктокиназы, замедление гликолиза и переключение гликолиза на глюконеогенез.
|
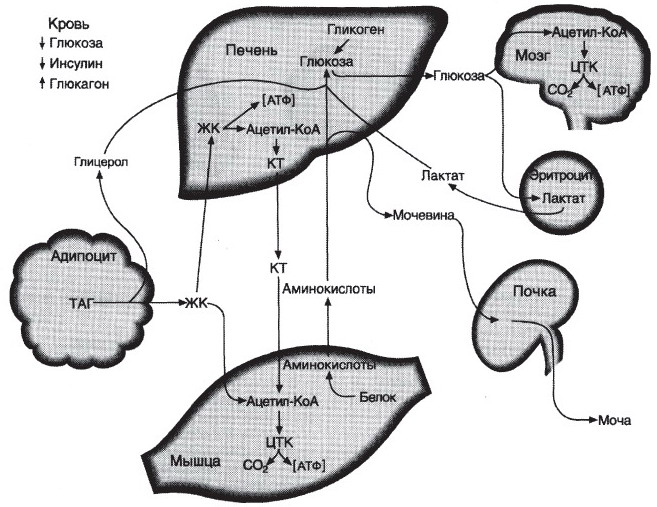
№ 31 При смене абсорбтивного состояния на постабсорбтивное в печени происходит переключение гликолиза на глюконеогенез. Каким образом изменение секреции гормонов и метаболитов регулирует этот процесс? Ответ аргументируйте соответствующими схемами.
Количество инсулина падает, а глюкагона возрастает. В печени скорость синтеза жирных кислот уменьшается, а скорость β-окисления и синтеза кетоновых тел увеличивается. В жировой ткани скорость синтеза ТАГ уменьшается.
Происходит изменение активности и количества ферментов гликолиза и глюконеогенеза.
|
|
№ 34 На дистанции два бегуна: спринтер завершает стометровку, стайер бежит десятый километр. Укажите различия в энергетическом обеспечении работы мышц у этих бегунов. Приведите схемы метаболических путей в обмене углеводов и липидов, которые являются источником энергии у стайера и спринтера.
У спринтера происходит анаэробный гликолиз, так как невозможно так быстро обеспечить мышцы необходимым количеством кислорода. У стайера функционирует β-окисление жирных кислот и аэробный гликолиз.
У стайера – β-окисление жирных кислот и аэробный гликолиз
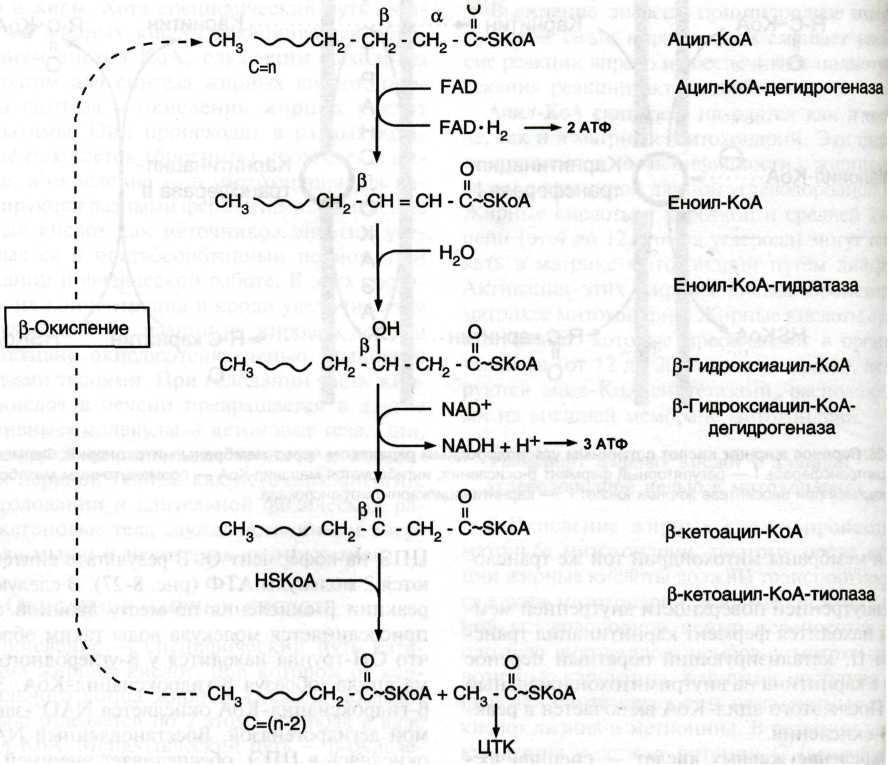

Аэробное окисление глюкозы до CO2 и воды
Глюкоза → 2 пирувата.
Выход АТФ: -1 -1+2(3 + 1+ 1)+15*2=38 АТФ
АТФ АТФ NADH АТФ АТФ ЦТК
У спринтера – анаэробный гликолиз.
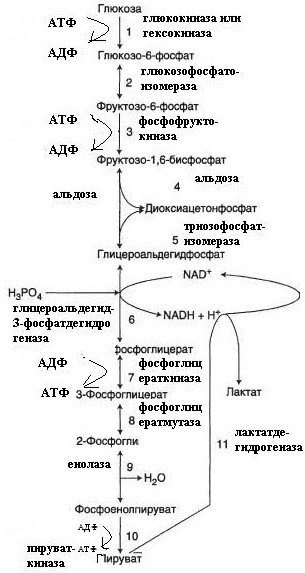
Выход АТФ: -1 -1+2( 1 + 1)=2 АТФ
АТФ АТФ АТФ АТФ
|
№ 35 Использование скелетными мышцами жирных кислот в качестве источника энергии зависит от их концентрации в крови. Укажите ситуации, при которых концентрация жирных кислот в крови может увеличиваться и напишите схему, описывающую использование жирных кислот в качестве источника энергии.
Концентрация жирных кислот в крови увеличивается в при голодании и длительной физической работе за счёт мобилизации из жировых депо.

|
№ 36 Студент А. получил в составе пищи только 200г углеводов, а студент В. - только 60г жиров. Через 2 часа у обоих студентов концентрация триацилглицеролов в крови увеличилась. Составьте схемы, объясняющие разницу в составе липопротеинов в крови у этих студентов после еды.
В данной задаче инсулин-глюкагоновый индекс повышается.
У первого студента в печени и жировой ткани идет синтез жиров из глюкозы , при этом, за счет синтеза жиров в печени, в крови увеличивается фракиця ЛПОНП, транспортирующая триациглиролы в жировую ткань (активируются и индуцируются ключевые ферменты синтеза жирных кислот).
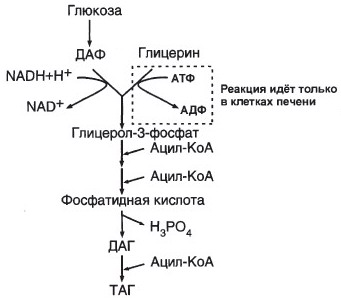
В составе ЛПОНП
У второго студента происходит транспорт триациглицеролов из кишечника в составе хиломикронов. В крови на ХМ и ЛПОНП действует ЛП-липаза,. В результате гидролиза триацилглицеролов жирные кислоты поступают в адипоциты и используются для синтеза жиров.
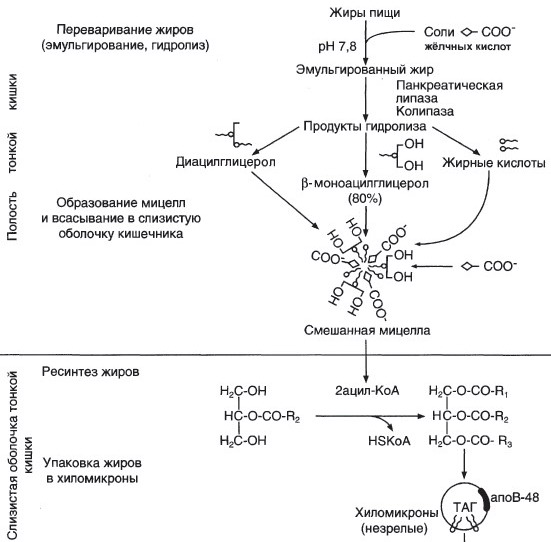
Далее хиломикроны идут в кровь
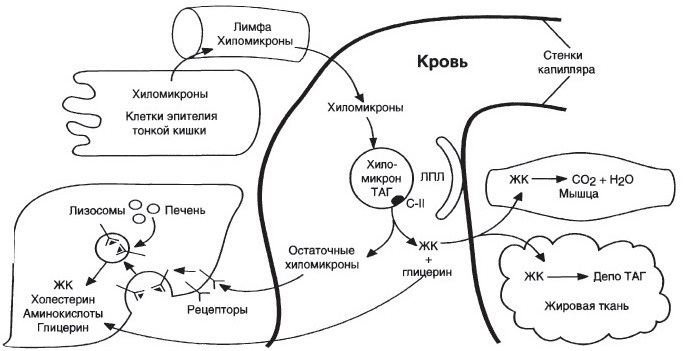
|
№ 38 После введения животным в течение нескольких дней глюкозы, содержащей меченые атомы углерода (С14), обнаружили, что метка появляется в изопентенилпирофосфате, а затем в структуре желчных кислот. Как это происходит? Для ответа на вопрос:
а) Объясните, в каком процессе изопентенилпирофосфат является промежуточным метаболитом и будет ли сохраняться радиоактивная
метка в конечном продукте процесса;
б) Напишите схему включения С14 в состав желчных кислот и укажите орган, в котором это происходит;
в) Укажите, будет ли сохраняться в организме животных меченые по С14 желчные кислоты, после прекращения введения меченой глюкозы.
а) Синтез холестерола в цитозоле клеток печени. Метка будет сохраняться.
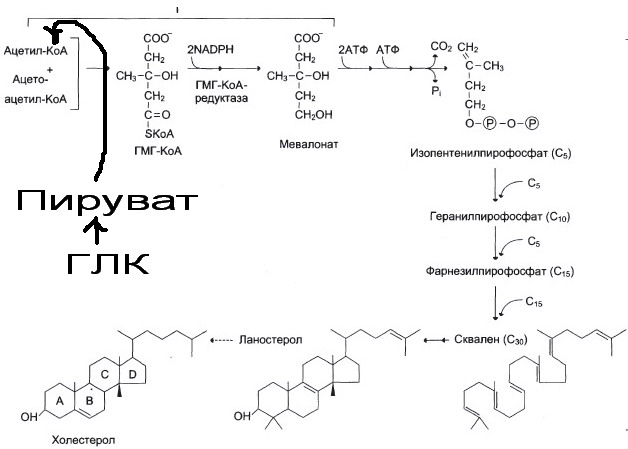
б) Орган – Печень.
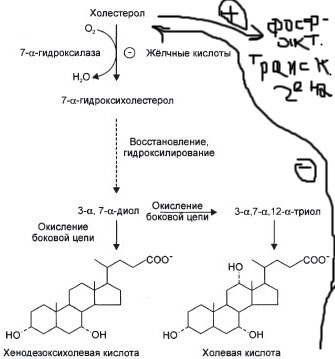
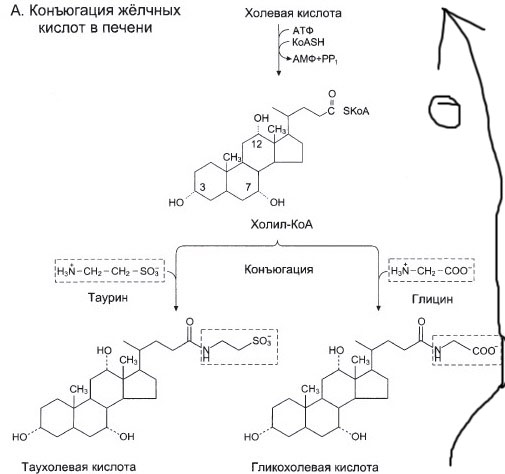
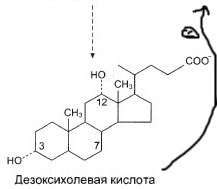
Стрелками показана регуляция. От дезоксихолевой стрелка идёт к холестеролу
в) Не будут сохраняться, а будут медленно выводиться с фекалиеми в виде чистого хоестерола и в виде желчных кислот,а также с кожным салом.
|
|
№ 37 При обследовании пациента с атеросклерозом коэффициент атерогенности оказался равным 5,3. Напишите формулу для расчета коэффициента, укажите возможные причины его увеличения. Объясните функции различных липопротеинов в транспорте холестерола.
Xc общ – Хс(ЛВП)
K = Хс(ЛВП) ИЛИ
Xc (ЛНП) – Хс(ЛОНП)
K = Хс(ЛВП)
Причины:
1. Потребление высококалорийной пищи, а такжн пищи, содержащей много холестерола
следовательно гиперхиломикронемия
2. Генетический дефект любого из Б., участвующих в метаболизме Хм.
3. Мутация гена ЛПП, Апо-с-II
Функции:
1. Хм – транспорт липидов из клеток кишечника.
2. ЛОНП – транспорт липидов, синтезируемых в печени.
3. ЛППП – промежуточная форма превращения ЛОНП → KYG под действием ЛП-липазы.
4. ЛПНП – транспорт холестерола вткани
5. ЛПВП – удаление избыточного холестерола из клеток и других липопротеинов, донор апопротеинов А, C-II.
|
№ 39 При одинаковом питании у одних людей ожирение развивается быстрее, чем у других. Для объяснения этого:
а) Изобразите схемы метаболических путей, активация которых приводит к увеличению веса;
б) Назовите гормон, под влиянием которого это происходит, и объясните механизм его действия;
в) Укажите возможные причины (кроме гиперкалорийного питания) ожирения.
а) Депонирование жира в адипоцитах
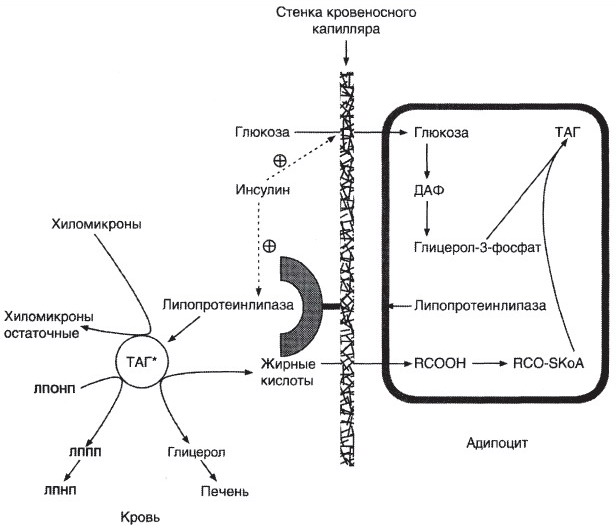
После еды при повышении концентрации глюкозы в крови увеличивается секреция инсулина. Инсулин активирует транспорт глюкозы внутрь адипоцитов, действуя на ГЛЮТ-4, и синтез ЛП-липазы в адипоцитах и её экспонирование на поверхности стенки капилляров. ЛП-липаза, связанная с эндотелием сосудов, гидролизует жиры в составе ХМ и ЛПОНП. АпоС-П на поверхности ХМ и ЛПОНП активирует ЛП-липазу. Жирные кислоты проникают в адипоцит, а глицерол транспортируется в печень. Так как в адипоцитах нет фермента глицеролкиназы, то свободный глицерол не может использоваться для синтеза ТАГ в этой ткани. Активированные жирные кислоты взаимодействуют с глицерол-3-фосфатом, образующимся из дигидроксиацетонфосфата, и через фосфатидную кислоту превращаются в ТАГ, которые депонируются в адипоцитах. Сокращения: ТАГ* — триацилглицеролы в составе ХМ и ЛПОНП; ДАФ — дигидроксиацетонфосфат.
 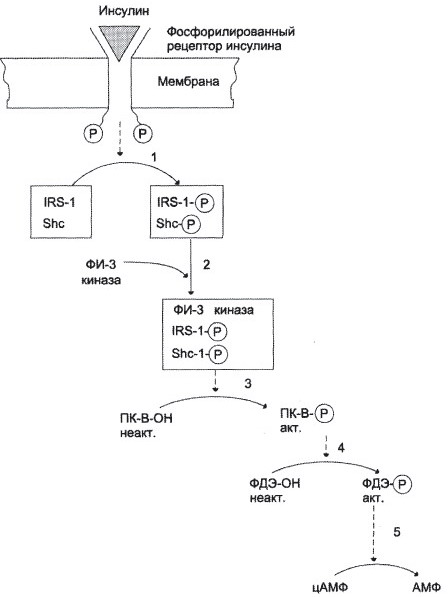
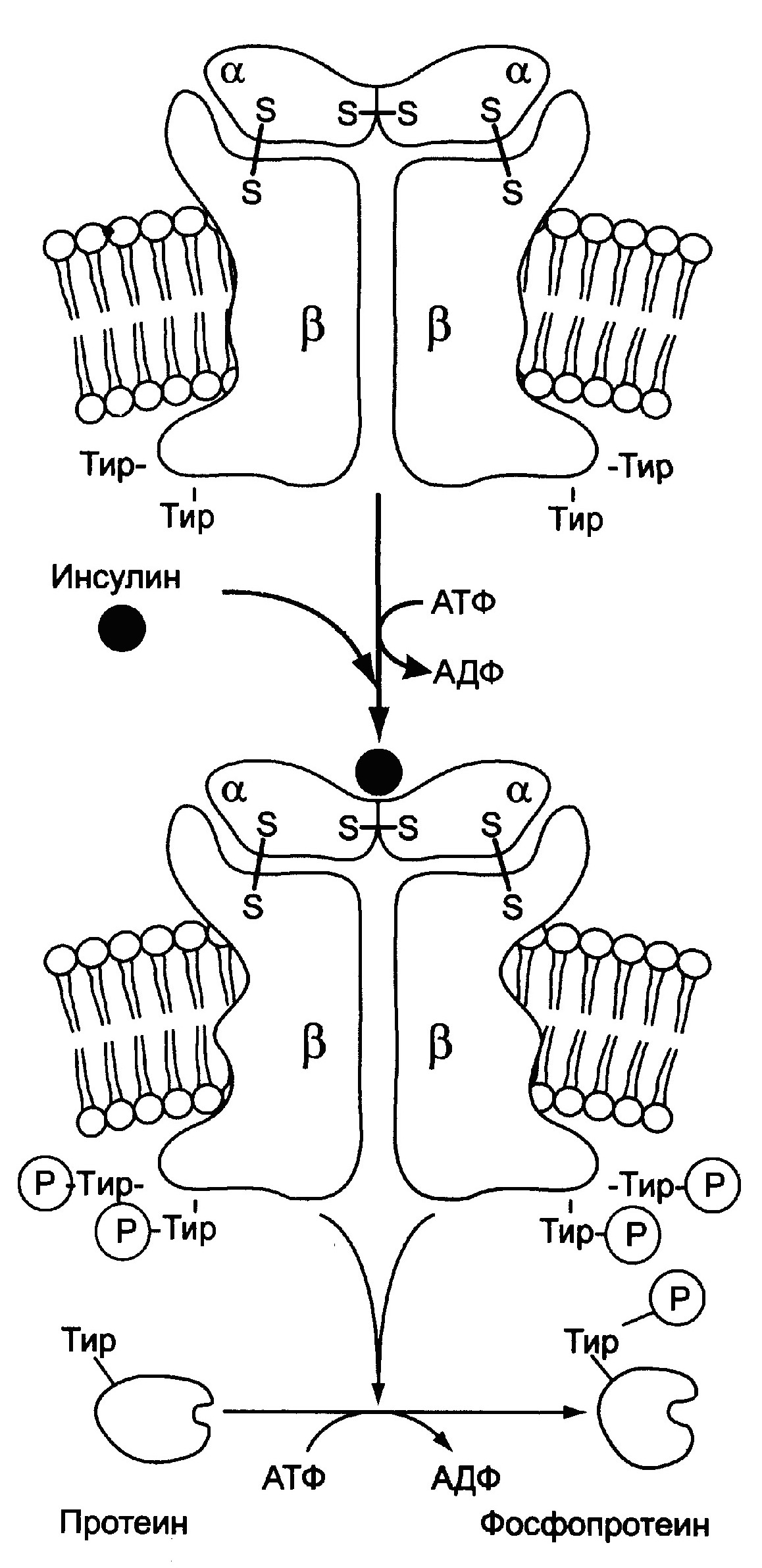
б) Схемы показаны сверху.
1 – фосфорилированный рецептор инсулина фосфорилирует субстраты инсулинового рецептора. 2 – образование комплекса Фосфоинозитол-3-киназы с активированными субстратами инсулинового рецептора. 3 – активация протеинкиназы В 4 – протеинкиназа В активирует фосфодиэстеразу путём фосфорилирование. 5 – фосфодиэстераза Катализирует реакцию превращения цАМФ в АМФ.
в) Избыточное потребление жиров и углеводов, низкий уровень физической активности, психологические факторы, генетические нарушения (более прочное сопряжение дыхания и фосфорилирования, малая доля анаэробного гликолиза, дефект рецепторов лептина), ожирение вследствие другой патологии (гипотиреоз).
|
№ 40 Для установления риска развития атеросклероза, помимо определения общего холестерола в крови, дополнительно рассчитывают коэффициент атерогенности. Напишите схему синтеза холестерола, формулу для расчета коэффициента и объясните:
а) Почему в расчете коэффициента необходимо учитывать уровень ЛПВП в крови:
б) Метаболизм ЛПВП (формирование, взаимодействие с другими липопротеинами т.д.).
Синтез холестерола в цитозоле клеток печени.
Xc общ – Хс(ЛВП)
K = Хс(ЛВП) ИЛИ
Xc (ЛНП) – Хс(ЛОНП)
K = Хс(ЛВП)

а) ЛВП освобождают ткани от Хс и транспортируют его в печень.
Функции ЛВП:
1. Поставляют апопротеины другим ЛП в крови
2. Участвуют в так называемом «обратном транспорте холестерола»
Синтезируются ЛВП в печени и токном кишечнике.
б)
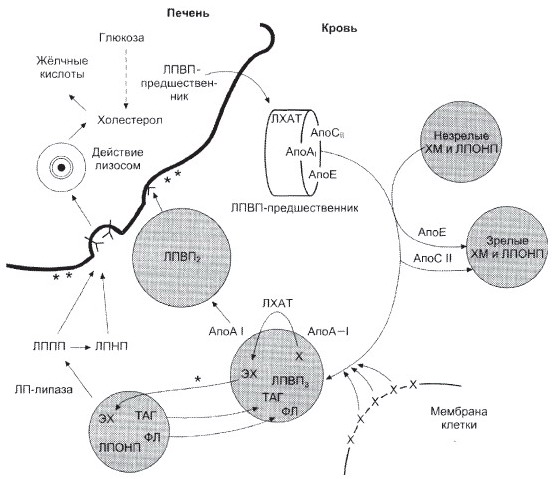
Незрелые ЛПВП-предшественники обогащаются хопестеролом, который поступает в ЛПВП при участии фермента ЛХАТ с поверхности клеток и других липопротеинов, содержащих холестерол. Незрелые ЛПВП, обогащаясь холестеролом, превращаются в ЛПВП3 — частицы сферической формы и большего размера. ЛПВП3обменивают эфиры холестерола на триацилглицеролы, содержащиеся в ЛПОНП, ЛППП при участии «белка, переносящего эфиры холестерола»*. ЛПВП3 превращается в ЛПВП2, размер которых увеличивается за счёт накопления триа-цилглицеролов. ЛПОНП и ЛППП под действием ЛП-липазы превращаются в ЛПНП, которые доставляют холестерол в печень. Часть ЛПВП захватывается клетками печени, взаимодействуя со специфическими для ЛПВП рецепторами к апоА-1. На поверхности клеток печени фосфолипиды и триацилглицеролы ЛППП, ЛПВП2 гидролизуются печёночной ЛП-липазой**, что дестабилизирует структуру поверхности ЛП и способствует диффузии холестерола в гепатоциты. ЛПВП2 в результате этого опять превращаются в ЛПВП3 и возвращаются в кровоток. X — холестерол, ЭХ — эфиры холестерола, ФЛ — фосфолипиды, ЛХАТ — лецитин-холестеролацилтрансфераза, А-1 — апопротеин, активатор ЛХАТ.
|
№ 41 Каковы особенности метаболизма жиров у человека, получающего высококалорийную пищу с повышенным содержанием легко усвояемых углеводов? Для ответа на вопрос:
а) Напишите регуляторную реакцию синтеза жирных кислот и схему синтеза жиров из углеводов;
б) Объясните особенности гормональной регуляции этих процессов при избыточном углеводном питании.
а) Регуляторная реакция - Образование малонил-КоА.
Регуляторный фермент – ацетил-КоА-карбоксилаза
CH3 – CO-SKoA + CO2 + АТФ → HOOC-CH2-CO-SKoA + АДФ + H3PO4
ацетил-КоА малонил-КоА
Схема синтеза жиров из углеводов.
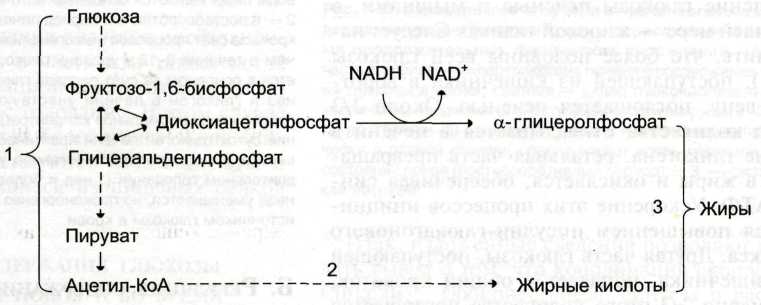
1 – окисление глюкозы до пирувата и окислительное декарбоксилирование пирувата приводят к образованию ацетил-КоА; 2 – ацетил-КоА является строительным белком для синтеза жирных кислот; 3 – жирные кислоты и α-глицеролфосфат, образующися в реакции восстановления дигидроксиацетонфосфата, участвует в синтезе триацилглицеролов.
б) Длительное потребление богатой углеводами и бедной жирами пищи приводит к увеличению секреции инсулина, который стимулирует индукцию синтеза ферментов: ацетил-КоА-карбоксилазы, синтазы жирных кислот, цитратлиазы, изоцитратдегидрогеназы. Следовательно, избыточное потребление углеводов приводит к ускорению превращения продуктов катаболизма глюкозы в жиры. Голодание или богатая жирами пища приводит к снижению синтеза ферментов и, соответственно, жиров.
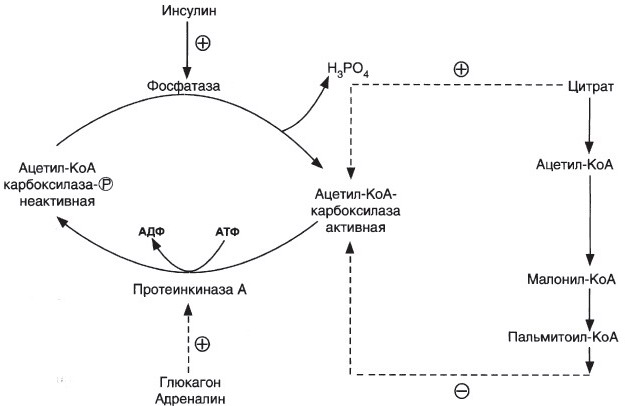
В постабсорбтивном состоянии или при физической работе глюкагон или адреналин через аденилатциклазную систему активируют протеинкиназу А и стимулируют фосфорилирование субъединиц ацетил-КоА карбоксилазы. Фосфорилированный фермент неактивен, и синтез жирных кислот останавливается. В абсорб-тивный период инсулин активирует фосфатазу, и ацетил-КоА карбоксилаза переходит в дефосфорилированное состояние. Затем под действием цитрата происходит полимеризация протомеров фермента, и он становится активным. Кроме активации фермента, цитрат выполняет и другую функцию в синтезе жирных кислот. В абсорбтивный период в митохондриях клеток печени накапливается цитрат, в составе которого остаток ацетила транспортируется в цитозоль.
|
|
|
№ 42 Человек получил с пищей 250 грамм углеводов и в течение 2-х часов не совершал физической работы. Опишите изменения жирового обмена, происходящие в организме человека в течение этого времени с помощью соответствующих схем, объясните роль гормонов в регуляции этих процессов.
В данной задаче инсулин-глюкагоновый индекс повышается.
В печени и жировой ткани идет синтез жиров из глюкозы, при этом, за счет синтеза жиров в печени, в крови увеличивается фракиця ЛПОНП, транспортирующая триациглиролы в жировую ткань (активируются и индуцируются ключевые ферменты синтеза жирных кислот).

В составе ЛПОНП
Синтез жирных кислот

Далее жир депонируется в адипоцитах в абсорбтивный период

Роль инсулина.
Инсулин активирует ацетил-КоА-карбоксилазу, регуляторный фермент в биосинтезе жирных кислот. К тому же инсулин может индуцировать синтез ферментов биосинтеза ЖК за счет усиления транскрипции с соответствующих генов (ген ацетил-КоА-карбоксилазы, синтазы жирных кислот, цитратлиазы, изоцитратдегидрогеназы). Плюс ко всему, инсулин вызывает усиление гликолиза, а продукты гликолиза (ацетил-КоА, НАДФН, ДАФ) являются исходными компонентами для синтеза жирных кислот и жиров.

|
№ 43 В крови голодающего человека возрастает концентрация кетоновых тел. Объясните причины и механизмы, приводящие к усилению синтеза кетоновых тел. Для этого:
а) Укажите уровень каких гормонов повышен в крови этого человека;
б) Напишите схемы метаболических путей, которые активируют эти гормоны в печени, укажите ключевые реакции и механизмы их регуляции.
в) Назовите причину, объясняющую более высокую концентрацию в крови β-гидроксибутирата по сравнению с ацетоацетатом.
а) Глюкагон и кортизол
б) β-окисление жирных кислот

Синтез кетоновых тел
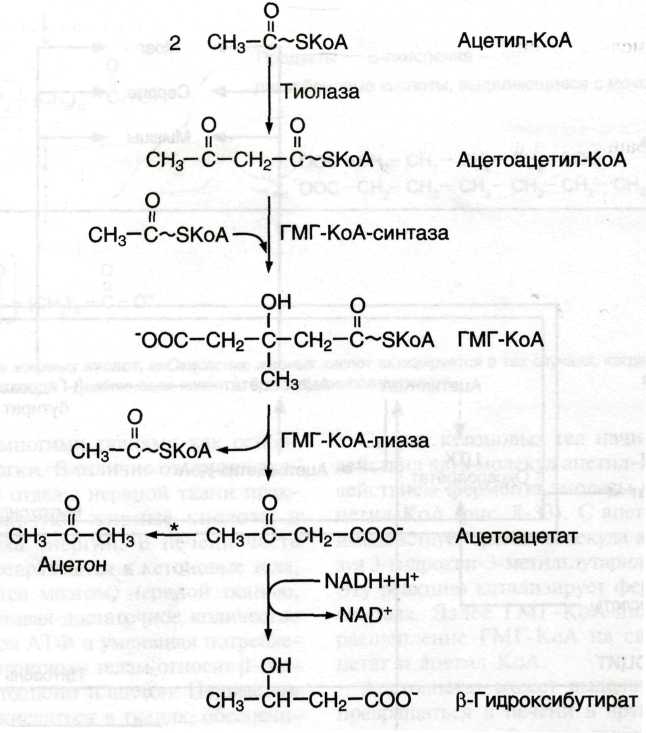
Мобилизация жира
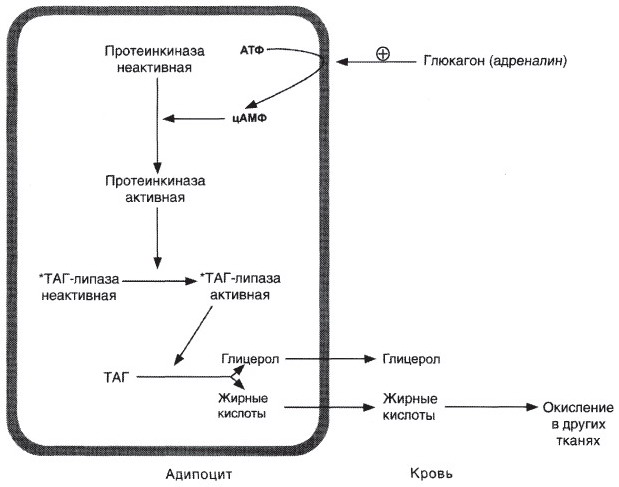
Глюконеогенез (снизу-вверх) Распад гликогена
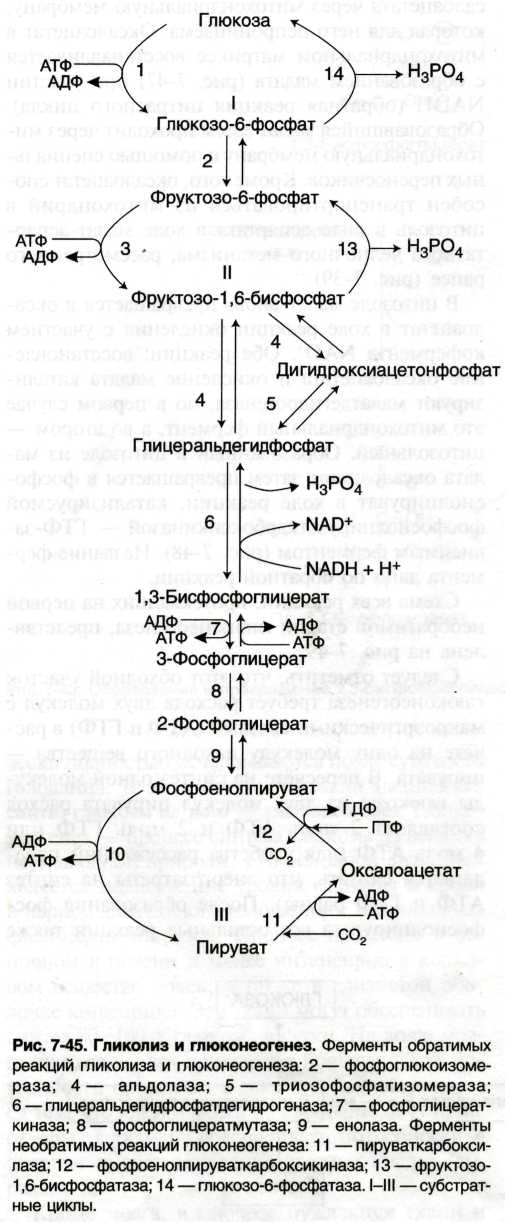 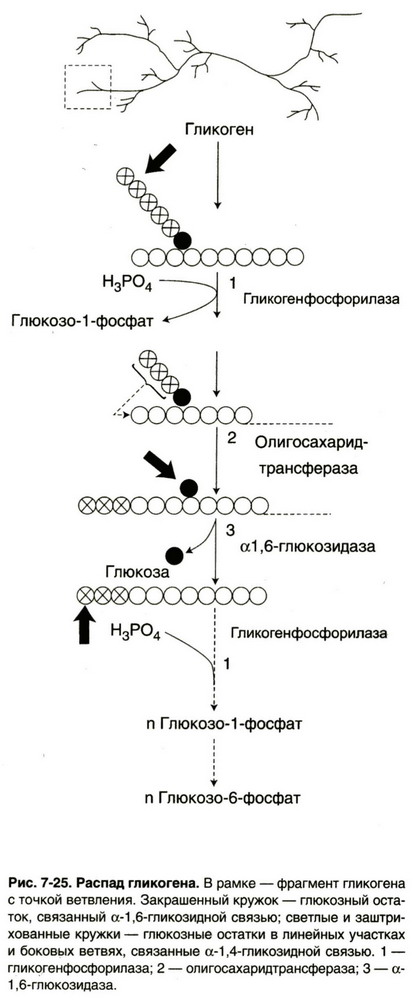
Также в механизме можно упомянуть о распаде гликоегна в течение 24 часов, расщеплении жира и ЦТК.
в) Ацетоацетат может выделяться в кровь или превращаться в печени в другое кетоновое тело - β-гидроксибутират путём восстановления. В клетках печени при активном β-окислении создаётся высокая концентрация NADH. Это способствует превращению большей части ацетоацетата в β-гидроксибутират, поэтому основное кетоновое тело в крови – именно β-гидроксибутират.
|
№ 44 Человек получил 250 г углеводов за один прием пищи и в течение 2 часов не совершал физической работы. Какой процесс обмена жирных кислот будет активироваться в печени через 2 ч после еды? Изобразите схему метаболического пути жирных кислот выбранного вами и укажите, какой гормон и каким образом может стимулировать данный метаболический путь.
В данной задаче инсулин-глюкагоновый индекс повышается.
В печени и жировой ткани идет синтез жиров из глюкозы , при этом, за счет синтеза жиров в печени, в крови увеличивается фракция ЛПОНП, транспортирующая триациглицеролы в жировую ткань (активируются и индуцируются ключевые ферменты синтеза жирных кислот).

В составе ЛПОНП
Далее происходит транспорт триациглицеролов из кишечника в составе хиломикронов. В крови на ХМ и ЛПОНП действует ЛП-липаза,. В результате гидролиза триацилглицеролов жирные кислоты поступают в адипоциты и используются для синтеза жиров.

Далее хиломикроны идут в кровь

Далее жир депонируется в адипоцитах в абсорбтивный период

Инсулин активирует ацетил-КоА-карбоксилазу, регуляторный фермент в биосинтезе жирных кислот. К тому же инсулин может индуцировать синтез ферментов биосинтеза ЖК за счет усиления транскрипции с соответствующих генов (ген ацетил-КоА-карбоксилазы, синтазы жирных кислот, цитратлиазы, изоцитратдегидрогеназы). Плюс ко всему, инсулин вызывает усиление гликолиза, а продукты гликолиза (ацетил-КоА, НАДФН, ДАФ) являются исходными компонентами для синтеза жирных кислот и жиров.

|
|
| |
|
|
 Скачать 7.65 Mb.
Скачать 7.65 Mb.