Ответы на вопросы по фармакологии. Фармакология. Фармакология Литературный обзор
 Скачать 0.7 Mb. Скачать 0.7 Mb.
|
|
Фармакология Литературный обзор препарат Артрозан действующее вещество Мелоксикам лит обзор требуется по препарату Артрозан, производства Фармстандарт. Артрозан, производства Фармстандарт. Препарат отпускается по рецепту Артрозан® Р-р д/в/м введения 6 мг/1 мл: амп. 2.5 мл 3, 5 или 10 шт. рег. №: ЛСР-004856/10 от 28.05.10 Дата перерегистрации: 11.08.20 ФАРМСТАНДАРТ-УфаВИТА (Россия) контакты: ФАРМСТАНДАРТ АО (Россия) Препарат отпускается по рецепту Артрозан® Таб. 7.5 мг: 20 шт. рег. №: ЛС-001013 от 31.05.10 Дата перерегистрации: 23.08.18 Таб. 15 мг: 10 или 20 шт. рег. №: ЛС-001013 от 31.05.10 Дата перерегистрации: 23.08.18 ФАРМСТАНДАРТ-ЛЕКСРЕДСТВА (Россия) контакты: ФАРМСТАНДАРТ АО (Россия) Содержание Литературный обзор 3 Фармакокинетика 3 Общая информация 9 Стадии заболевания 9 Виды 10 Причины развития 10 Симптомы 11 Анализы и диагностика 13 Лечение артроза суставов 14 Медикаментозное лечение 14 Немедикаментозное лечение 15 Хирургическое лечение 15 Артроз у детей 15 Диета 16 Профилактика 16 Последствия и осложнения 17 Прогноз 17 Лечение в клинике «Энергия здоровья» 17 Преимущества клиники 17 Врачи отделения 19 Список использованных источников 50 Литературный обзорРезюме Препарат Артрозан, производства Фармстандарт, Россия. Механизм действия связан с ингибированием синтеза простагландинов в результате избирательного торможения ферментативной активности циклооксигеназы второго типа (ЦОГ-2), участвующей в биосинтезе простагландинов в области воспаления. При назначении в высоких дозах, длительном применении и индивидуальных особенностях организма избирательность в отношении ЦОГ-2 снижается. В меньшей степени действует на циклооксигеназу первого типа (ЦОГ-1), участвующую в синтезе простагландинов, защищающих слизистую оболочку ЖКТ и принимающих участие в регуляции кровотока в почках. За счет указанной селективности подавления активности ЦОГ-2 препарат реже вызывает эрозивно-язвенные поражения ЖКТ. ФармакокинетикаХорошо всасывается из ЖКТ, абсолютная биодоступность - 89%. Одновременный прием пищи не изменяет всасывание препарата. При приеме препарата внутрь в дозах 7.5 и 15 мг его концентрации пропорциональны дозам. Css достигаются в течение 3-5 дней лечения. При длительном применении препарата (более 1 года) концентрации сходны с таковыми, которые отмечаются после первого достижения устойчивого состояния фармакокинетики. Связывание с белками плазмы составляет 99%. При применении дозы 7.5 мг Cmin составляет 0.4 мкг/мл, Сmax - 1.0 мкг/мл; при использовании дозы 15 мг Cmin - 0.8 мкг/мл, Сmax - 2.0 мкг/мл. Почти полностью метаболизируется в печени с образованием четырех неактивных в фармакологическом отношении производных. Основной метаболит, 5'-карбоксимелоксикам (60% от величины дозы), образуется путем окисления промежуточного метаболита, 5'-гидроксиметилмелоксикама, который также экскретируется, но в меньшей степени (9% от величины дозы). Исследования in vitro показали, что в данном метаболическом превращении важную роль играет изофермент CYP2С9, дополнительное значение имеет изофермент CYP3А4. В образовании двух других метаболитов, (составляющих, соответственно, 16% и 4% от величины дозы препарата), принимает участие пероксидаза, активность которой, вероятно, варьирует. Препарат проникает через гистогематические барьеры, концентрация в синовиальной жидкости составляет 50% Сmax в плазме. Плазменный клиренс составляет в среднем 8 мл/мин. У лиц пожилого возраста клиренс препарата снижается. Vd небольшой и составляет в среднем 11 л. Печеночная или почечная недостаточность средней степени тяжести существенного влияния на фармакокинетику мелоксикама не оказывает. Выводится в равной пропорции с калом и мочой, преимущественно в виде метаболитов. Через кишечник в неизмененном виде выводится менее 5% суточной дозы, в моче в неизмененном виде препарат обнаруживается только в следовых количествах. T1/2 мелоксикама составляет 15-20 часов. Симптоматическое лечение воспалительных и дегенеративных заболеваний мышечно-суставной системы, сопровождающихся болевым синдромом, в т.ч.: остеоартроза; ревматоидного артрита; анкилозирующего спондилита (болезнь Бехтерева); остеохондроза. Обзор медицинских литературных источников должен включать наименование лекарственного препарата, краткое описание информации по безопасности лекарственных средств (резюме), название проанализированных медицинских литературных источников. Резюме должно включать следующее: эпидемиология и происхождение заболевания в рамках показаний к применению препарата (может включать, но не ограничиваться): Боль – одна из наиболее частых причин, которая побуждает пациентов обращаться за специализированной помощью. Более половины жалоб вызваны хронической болью, которая определяется как: боль, персистирующая по меньшей мере 3–6 месяцев; боль, сохраняющаяся свыше 1 месяца после окончания острого заболевания или заживления повреждения; боль, ассоциированная с хроническим патологическим процессом или рекуррентным патологическим процессом с относительно короткими интервалами между экзацербациями. По результатам большинства исследований, хроническая боль представляет значительные трудности для диагностики и плохо поддается лечению [1]. Согласно данным Американского общества по изучению боли, приблизительно половина больных, имеющих хроническую боль, меняют врача как минимум однократно по следующим причинам: боль персистирует (42%), врач недостаточно осведомлен о причинах боли (31%), врач недостаточно серьезно оценивает боль пациента (29%), врач не склонен проводить более активное лечение боли (27%) [2]. Пациенты с хронической болью нуждаются в комплексном обезболивании, что требует значительных временных затрат и часто консультации нескольких специалистов. Многие процессы потенциально могут быть причиной пролонгирования хронической боли. Боль подразделяется на острую или хроническую; ноцицептивную (соматическую или висцеральную (органную)), невропатическую или мультифакториальную/смешанную, включая ноцицептивный тип боли, эволюционировавший в невропатический тип. Крайне важно корректно категоризировать боль, поскольку именно знание базовых механизмов, поддерживающих боль, в каждом конкретном случае позволяет выбрать оптимальное лечение. Патогенез ноцицептивной и невропатической боли Ноцицептивная боль (острая или хроническая) опосредована активацией болевых рецепторов в коже, мышечно-скелетной системе, связочных тканях и висцеральных органов. Традиционно ноцицептивная боль рассматривается как последствие активации нейрональных сенсорных (ноцицептивных) путей в ответ на стимулы от поврежденной ткани. В процессе, известном как трансдукция, повреждающий стимул конвертируется в потенциал действия периферических ноцицепторных, сенсорных волокон. Сигнал передается через периферические нервы и спинной мозг в головной мозг, где формируется чувство боли. Болевой опыт невозможен без трансмиссии повреждающего сигнала в мозг. Ноцицептивная боль может возникнуть в результате травмы (повреждение, ожог), инфекционного воспаления и при различных заболеваниях, включая артриты, онкологические процессы, постоперационные боли, мышечно-скелетные боли в спине и др. Пациенты обычно описывают соматическую боль как хорошо локализуемую, постоянную, ноющую или пульсирующую, сдавливающую или острую (вонзающуюся). Висцеральная боль часто описывается как плохо локализуемая, схваткообразная или сверлящая. В большинстве случаев нервная система возвращается в обычное состояние после излечения воспалительного процесса, и боль редуцируется. Ноцицептивная боль обеспечивается вовлечением различных нейрохимических агентов и медиаторов, включая эндорфины, разнообразные биогенные амины, гамма-аминомасляную кислоту (ГАМК), нейрокинины, интерлейкины, простагландины и др. Все эти субстанции могут рассматриваться как целевые мишени для анальгетического воздействия. В 1971 г. впервые была установлена связь между фармакологической активностью нестероидных противовоспалительных средств (НПВС) и продукцией простагландинов [3]. Последующие исследования позволили понять центральную роль ингибиции фермента циклооксигеназы (ЦОГ) в редукции биосинтеза простагландинов и, соответственно, в клинической эффективности и токсичности НПВС. Простагландины являются важнейшим медиатором периферической сенситизации (активация болевых рецепторов), но в последнее время также активно обсуждается их роль в центральной сенситизации. Переход от острой к хронической ноцицептивной боли происходит, когда неболевые стимулы воспринимаются как болевые в результате периферической и центральной сенситизации. Блокирование продукции простагландинов (ингибиция фермента ЦОГ-2) приводит к редукции боли. Основным механизмом анальгетического и противовоспалительного эффектов НПВС является ингибиция ЦОГ. По этой причине НПВС рассматриваются как золотой стандарт для лечения ноцицептивного компонента боли. К основным модуляторам боли относятся эндорфины, однако воздействие на эту медиаторную систему ограничивают побочные эффекты наркотических анальгетиков. Помимо эндорфинов, биологические амины (серотонин и норадреналин) модулируют болевые ощущения, являясь важной составляющей антиноцицептивной системы. Нисходящие системы ингибируют болевую чувствительность на спинальном уровне. Ослабление ингибирующей функции антиноцицептивных систем приводит к снижению порога болевой чувствительности. К целевым препаратам, активирующим ингибирующие боль системы, относятся антидепрессанты. Наиболее высоким анальгетическим рейтингом обладают трициклические антидепрессанты и антидепрессанты двойного действия, которые одновременно усиливают серотониновую и норадреналиновую медиацию. С целью десенсибилизации ноцицепторов могут быть использованы местные анестетики, в том числе в форме трансдермальных систем. В отличие от ноцицептивной боли невропатическая боль инициируется поврежденной нервной системой при интактном состоянии периферических рецепторов и может поддерживаться различными механизмами. В случае невропатической боли сигнал спонтанно генерируется поврежденной нервной системой, чрезмерно стимулируя структуры нервной системы, отвечающие за боль, что влечет за собой появление боли при отсутствии периферического повреждающего фактора и, соответственно, инактивных периферических болевых рецепторах. В формировании как невропатической боли, так и ноцицептивной боли участвуют одни и те же сенсорные системы и нейротрансмиттеры. Но в отличие от ноцицептивной боли невропатическая боль не несет адаптивной (сигнальной) функции. Невропатическая боль плохо откликается на лечение традиционными анальгетиками, включая НПВС и опиоиды. В то же время антидепрессанты, антиконвульсанты более эффективны в отношении невропатической боли. Очень часто хроническая боль может быть обусловлена вовлечением как ноцицептивных, так и невропатических механизмов, то есть иметь смешанный характер, что, безусловно, является показанием для комбинированного лечения. Лечение хронической боли Фармакологическое лечение хронической боли включает использование антидепрессантов, противоэпилептических препаратов, опиоидных ненаркотических анальгетиков или их комбинацию. Дополнительные препараты, такие как ингибиторы ЦОГ, мышечные релаксанты, бензодиазепины и другие ГАМКергические препараты, местные анестетики, могут быть использованы при специфических типах хронической боли. Поскольку не все лекарства эффективны в отношении и ноцицептивного, и невропатического компонента боли, при определении стратегии лечения в первую очередь следует оценить ведущий компонент боли, чтобы воздействовать на него. Среди локализованных болевых синдромов классификация хронической боли в спине наименее разработана, что, безусловно, затрудняет разработку целевых методов лечения. Дегенеративные структурные изменения позвоночного столба традиционно рассматриваются как базис для формирования боли в спине, хотя прямой зависимости между степенью морфологических изменений и болевой симптоматикой не прослеживается. Структурные и функциональные нарушения двигательного сегмента не всегда возникают одновременно, выраженные морфологические нарушения не у всех индивидуумов приводят к развитию клинических симптомов. В этой связи целевая терапия боли в спине в большей мере основывается на выделении ведущих патогенетических механизмов формирования боли. Ноцицептивный компонент всегда представлен в болевых синдромах, локализованных в области спины [4], и доминирует при фасеталгиях, дискалгии, миофасциальных болевых синдромах. К смешанным болевым синдромам (относительно равнозначно представлены ноцицептивный и невропатический компоненты) относятся радикулярная боль и боли, ассоциированные с позвоночным стенозом. Именно поэтому основными базисными препаратами для лечения любых болевых синдромов, локализованных в области спины, является НПВС. Эффективность НПВС в лечении боли в спине неоднократно подтверждалась систематическими обзорами независимого Кохрейновского общества врачей [5], что позволяет рассматривать НПВС как «золотой стандарт» лечения боли в спине. НПВС – это самый популярный класс анальгетиков, который содержит более двадцати различных по химической структуре подклассов. Об успешности НПВС свидетельствует огромное количество дженериковых препаратов и лидирующее положение класса по продажам во всем мире. В начале 1990-х гг. после открытия двух форм ЦОГ (ЦОГ-1 и ЦОГ-2) стал понятен механизм НПВС-индуцированной гастропатии, появилась возможность ранжировать препараты по степени ингибирования ЦОГ-1 (по степени нарушения синтеза физиологического пула простагландинов) и, соответственно, прогнозировать безопасность НПВС. ЦОГ-1 катализирует продукцию простагландинов, повышающих защитные свойства слизистой желудочно-кишечного тракта, в то время как ЦОГ-2 ответственна за продукцию простагландинов, связанных с воспалением и болью. Ярким представителем препаратов, преимущественно ингибирующих ЦОГ-2, является мелоксикам. Мелоксикам в течение уже нескольких лет одобрен и успешно применяется более чем в 100 странах мира, а во многих европейских странах устойчиво удерживает статус самого выписываемого препарата из класса НПВС. Наиболее часто мелоксикам используется для купирования боли, ассоциированной с остеоартритом, ревматоидным артритом, мышечно-скелетными болями в спине. Остеоартроз (ОА) представляет собой гетерогенную группу заболеваний различной этиологии со сходными биологическими, морфологическими, клиническими проявлениями и исходом [1]. Поражение хряща, субхондральной кости, синовиальной оболочки, капсулы, связок и периартикулярных мышц является основой данной патологии [2]. В англоязычной литературе обычно используется название заболевания «остеоартрит» (osteoarthritis), которое подчеркивает роль воспаления в развитии заболевания [3]. ОА является наиболее частым заболеванием суставов. На долю ОА приходится 60–70% всех заболеваний суставов, артрозом болеют 10–20% населения [4]. При этом доля пациентов с ОА неуклонно растет, предполагается, что к 2020 г. ОА станет четвертой причиной инвалидности [5]. ОА представляет серьезную социально-экономическую проблему, так как значительно ухудшает качество жизни больных. ОА является одной из основных причин преждевременной потери трудоспособности, уступая в этом только ишемической болезни сердца. - определение медицинской и социально-экономической значимости болезни, её места в структуре патологии населения; - распространение болезни по территории и среди различных групп населения (возрастных, половых, профессиональных и т. д.). ртроз – это заболевание, характеризующееся постепенным разрушением сустава вследствие развития дистрофических изменений в тканях. Согласно данным ВОЗ, с этой проблемой сталкивается каждый десятый житель планеты. После 50 лет риск появления заболевания составляет около 30%, а к 70 годам достигает 80-90%. 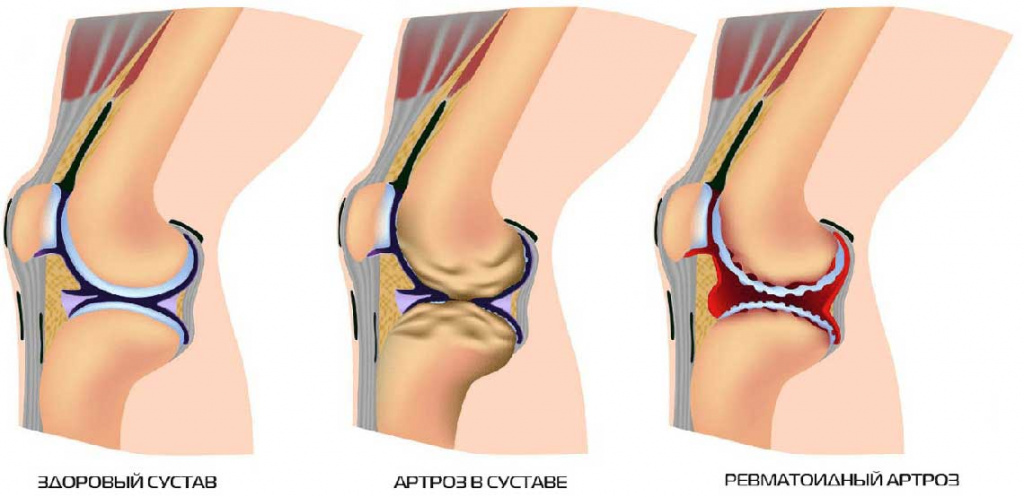 |
