Обмен липидов. Функции липидов жестко связаны с их строением
 Скачать 1.24 Mb. Скачать 1.24 Mb.
|
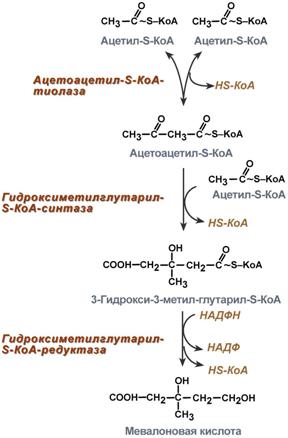
Синтез холестерола должен быть согласован с его выведениемСинтез холестерола в организме составляет примерно 0,5-0,8 г/сут, примерно 50% образуется в печени, около 15% в кишечнике. Все клетки организма способны синтезировать холестерол. Поступление с пищей составляет около 0,4 г/сут. Единственным реальным способом выведения холестерола является желчь – до 1 г/сут. Биосинтез холестеролаБиосинтез холестерола происходит в эндоплазматическом ретикулуме. Источником всех атомов углерода в молекуле является ацетил-SКоА, поступающий сюда из митохондрий в составе цитрата, также как при синтезе жирных кислот. При биосинтезе холестерола затрачивается 18 молекул АТФ и 13 молекул НАДФН. Образование холестерола идет более чем в 30 реакциях, которые можно сгруппировать в несколько этапов. 1. Синтез мевалоновой кислоты. Первые две реакции синтеза совпадают с реакциями кетогенеза, но после синтеза 3-гидрокси-3-метилглутарил-SКоА вступает в действие фермент гидроксиметил-глутарил-SКоА-редуктаза (ГМГ-SКоА-редуктаза), образующая мевалоновую кислоту.
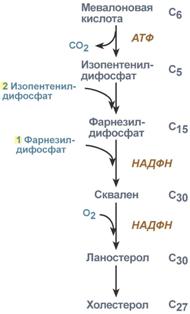
2. Синтез изопентенилдифосфата. На этом этапе три остатка фосфат присоединяются к мевалоновой кислоте, затем она декарбоксилируется и дегидрируется. 3. После объединения трех молекул изопентенилдифосфата синтезируется фарнезилдифосфат. 4. Синтез сквалена происходит при связывания двух остатков фарнезилдифосфата. 5. После сложных реакций линейный сквален циклизуется в ланостерол. 6. Удаление лишних метильных групп, восстановление и изомеризация молекулы приводит к появлению холестерола. Регуляция синтезаРегуляторным ферментом является гидроксиметилглутарил-SКоА-редуктаза, активность которой может изменяться в 100 и более раз. 1. Метаболическая регуляция – по принципу обратной отрицательной связи фермент ингибируется конечным продуктом реакции – холестеролом. Это помогает поддерживать внутриклеточное содержание холестерола постоянным. 2. Ковалентная модификация при гормональной регуляции: инсулин, активируя протеин-фосфатазу, способствует переходу фермента в активное состояние. Важным следствием такой регуляции является активация кетогенеза при отсутствии инсулина. Глюкагон и адреналин посредством аденилатциклазного механизма активируют протеинкиназу А, которая фосфорилирует фермент и переводит его в неактивную форму. 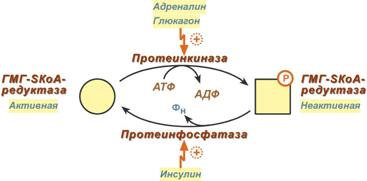 Регуляция активности гидроксиметилглутарил-S-КоА-редуктазы3. Скорость биосинтеза холестерола также зависит от концентрации специфического белка-переносчика, обеспечивающего связывание и транспорт гидрофобных промежуточных метаболитов синтеза. Холестерол используется как переносчик полиненасыщенных жирных кислотТранспорт холестерола и его эфиров осуществляется липопротеинами низкой и высокой плотности. Липопротеины высокой плотностиОбщая характеристика
Функция
Метаболизм1. Синтезированный в печени ЛПВП (насцентный или первичный) содержит в основном фосфолипиды и апобелки. Остальные липидные компоненты накапливаются в нем по мере метаболизма в плазме крови. 2. В ЛПВП активно протекает реакция при участии лецитин:холестерол-ацилтрансферазы (ЛХАТ-реакция). В этой реакции остаток полиненасыщенной жирной кислоты переносится от ФХ на свободный ХС с образованием лизофосфатидилхолина (лФХ) и эфиров ХС. 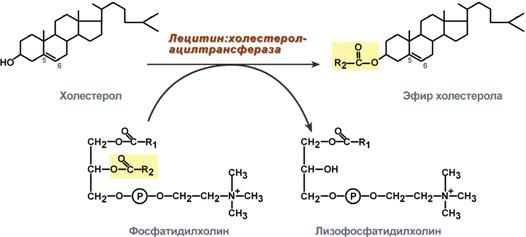 Реакция лецитин:холестерол-ацилтрансферазы3. Взаимодействует с ЛПНП и ЛПОНП, которые являются источником свободного ХС для ЛХАТ-реакции, в обмен ЛПВП отдают эфиры ХС. 4. Взаимодействуя с ЛПОНП и ХМ, получают ТАГ и отдают им апоЕ- и апоСII-белки. 5. При посредстве специфических транспортных белков получают свободный ХС из клеточных мембран. 6. Взаимодействует с мембранами клеток, отдает часть фосфолипидной оболочки, доставляя таким образом полиеновые жирные кислоты в клетки. 7. Накопление свободного ХС, ТАГ, лизоФХ и утрата фосфолипидной оболочки преобразует ЛПВП3 (условно его можно назвать "зрелый") в ЛПВП2 ("остаточный"). Последний захватывается гепатоцитами при помощи апоА-1-рецептора. 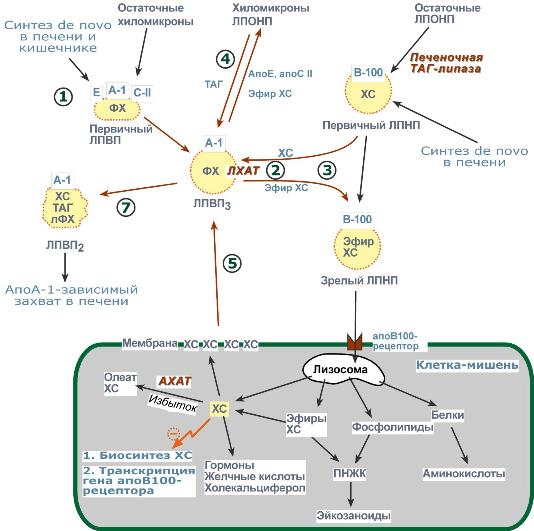 Транспорт холестерола и его эфиров в организмеЛипопротеины низкой плотностиОбщая характеристика
Функция1. Транспорт холестерола в клетки, использующие его для реакций синтеза половых гормонов (половые железы), глюко- и минералокортикоидов (кора надпочечников), холекальциферола (кожа), утилизирующие ХС в виде желчных кислот (печень). 2. Транспорт полиеновых жирных кислот в виде эфиров ХС в некоторые клетки рыхлой соединительной ткани (фибробласты, тромбоциты, эндотелий, гладкомышечные клетки), в эпителий гломерулярной мембраны почек, в клетки костного мозга, в клетки роговицы глаз, в нейроциты, в базофилы аденогипофиза. Клетки рыхлой соединительной ткани активно синтезируют эйкозаноиды. Поэтому им необходим постоянный приток полиненасыщенных жирных кислот (ПНЖК), что осуществляется либо переходом фосфолипидов от оболочки ЛПВП в мембраны клеток либо поглощением ЛПНП, которые несут ПНЖК в виде эфиров холестерола. Особенностью всех этих клеток является наличие лизосомальных кислых гидролаз, расщепляющих эфиры ХС. У других клеток таких ферментов нет. Обмен1. В крови первичные ЛПНП взаимодействуют с ЛПВП, отдавая свободный ХС и получая этерифицированный. В результате в них происходит накопление эфиров ХС, увеличение гидрофобного ядра и "выталкивание" белка апоВ-100 на поверхность частицы. Таким образом, первичный ЛПНП переходит в зрелый. 2. На всех клетках, использующих ЛПНП, имеется высокоафинный рецептор, специфичный к ЛПНП – апоВ-100-рецептор. При взаимодействии ЛПНП с рецептором происходит эндоцитоз липопротеина и его лизосомальный распад на составные части – фосфолипиды, белки (и далее до аминокислот), глицерол, жирные кислоты, холестерол и его эфиры.
Около 50% ЛПНП взаимодействуют с апоВ-100-рецепторами гепатоцитов и примерно столько же поглощаются клетками других тканей. |