Иммунка. Иммунная система
 Скачать 1.62 Mb. Скачать 1.62 Mb.
|
|
IgM. Молекула IgM представляет пентамерный комплекс, образованный из пяти мономеров-иммуноглобулинов кдассического строения, соединенных Fс-фрагментами с помощью дисульфидных связей и J-цепи. Такой комплекс имеет большую молекулярную массу (970 кДа), поэтому он плохо проникает в ткани. В процессе иммунного ответа первыми вырабатываются IgM антитела. IgM, связавшись с антигеном, претерпевает конформационные изменения, посде чего приобретает наибольшую способность, связывать и активировать белки системы комплемента. Благодаря форме пентамера, IgM обладает высокой авидностью, поэтому основная физиологическая функция IgM - нейтрализация патогенов в кровяном русле, помимо пентамера, IgM в мономерной форме присутствует, на мембране В-лимфоцитов, выполняя роль антигенраспознающего рецептора (BCR) IgG. Иммуноглобупины этого изотипа имеют классическую мономерную форму и составляют большинство антител при вторичном иммунном ответе. Благодаря низкой молекулярной массе IgG свободно проникает в ткани, а также является единственным иммуноглобулином, способным проходить через плацентарный барьер. Существует четыре подкласса IgG: IgG1, IgG2, IgG3, IgG4; IgG1 и IgG3 способны активировать систему комплемента, усиливать фагоцитарную активность и активировать клетки-киллеры. IgG2 и IgG4 участвуют в прямой нейтрализации патогенов. IgA присутствует в крови в виде мономера и участвует в нейтрализации антигенов, попавших в кровоток. Но главная функция IgA - это обеспечение специфической защиты на уровне слизистых оболочек. В больших количествах IgA присутствует во внешних секретах (слюна, слезы, пищеварительные соки) и в секретах слизистых оболочек. Секреторный IgA (sIgA) продуцируется плазматическими клетками лимфоидных фолликулов слизистых оболочек. Здесь он представляет собой димер, состоящий из двух молекул иммуноглобулинов, соединенных между собой J-цепью. Димеры sIgA путём эндоцитоза захватываются клетками эпителия, в специальной везикуле этот комплекс транспортируется через клетку и выделяется в составе слизи. В состав молекулы sIgA входит так называемый секреторный компонент, который защищает ее от действия протеолитических ферментов, присутствующих в секрете слизистых. SIgA участвует в формировании первой линии защиты слизистых. Он не способен активировать комплемент, не обладает бактерицидной активностью, но играет важную роль в нейтрализации бактериальных токсинов, а также препятствуют проникновению бактерий и вирусов через слизистые. IgE имеет мономерную форму, способен связываются через Fс-ε рецепторы с базофилами, тучными клетками и эозинофилами, вызывая их дегрануляцию. Биологическая роль IgE состоит в реализации иммунного ответа против гельминтов и других паразитов. Связывание IgE с эозинофилами через Fс-ε рецептор II типа индуцирует образование и секрецию биоцидных веществ, убивающих гельминтов. Повышенная продукция IgE в ответ на аллергены приводит к развитию аллергических реакций. IgD присутствует на мембране В-лимфоцитов, незначительное количество содержится в растворенном виде в крови и лимфе, функции его до конца не известны. 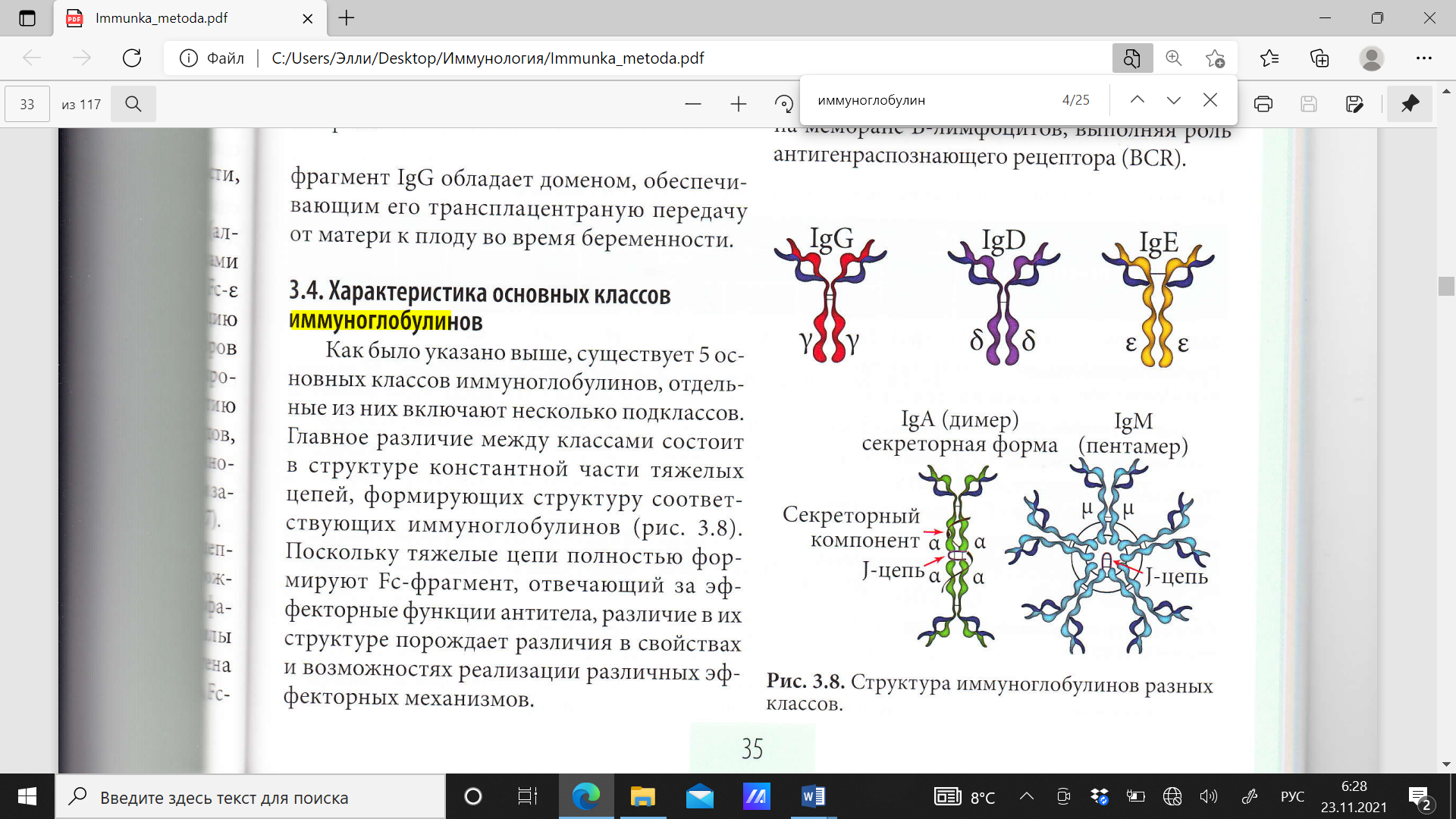 46. Расскажите о функциях иммуноглобулинов разных классов См. предыдущий вопрос 47. В чем особенности синтеза, строения и функций секреторного иммуноглобулина А (sIgA) IgA синтезируется в димерной форме в клетках собственной пластинки и после связывания с иммуноглобулиновым рецептором, синтезированным в эпителиальных клетках, транспортируется на поверхность слизистой оболочки. В момент выхода IgA в просвет кишечника рецептор частично расщепляется, в результате чего в составе IgA остается фрагмент рецептора, который называют секреторным компонентом. Таким образом, секреторный IgA является продуктом кооперации двух типов клеток – плазматических и эпителиальных. Секреторный IgA образуется не только в димерной, но и в тетрамерной форме, что усиливает его вируснейтрализирующую способность. Секреторный компонент предохраняет IgA от расщепления протеолитическими ферментами, что обуславливает его значительные преимущества перед антителами других классов. Секреторный IgA нейтрализует вирус не только в просвете кишечника, но и при транспортировке его внутрь клетки. Димер IgA может нейтрализовать вирус в подслизистой оболочке кишечника, а затем, связавшись с рецептором, транспортировать его в просвет кишечника. 48. Расскажите о различиях первичного и вторичного иммунного ответа гуморального типа При первичном попадании антигена в организм человека для развития иммунного ответа обычно требуется около 10 дней. Этот период обозначают терминами «время lag» или «лаг-фаза». Лимфоидные клетки встречаются с антигеном, размножаются с образованием клона клеток со сходной активностью, дифференцируются и начинают синтезировать антитела. Процесс образования антител при первой (первичной) встрече с антигеном отличается от такового после второго (повторного) контакта. При первичном ответе лаг-фаза имеет большую продолжительность, максимальный уровень антител ниже, а падение титров антител происходит быстрее, чем при вторичном иммунном ответе. Существенным компонентом первичного иммунного ответа являются иммуноглобулины класса М, тогда как при вторичном иммунном ответе иммуноглобулины представлены в основном IgG. Различия между первичным и вторичным иммунным ответом выражены в наибольшей степени в тех случаях, когда антиген стимулирует как В-лимфоциты, так и Т-лимфоциты, т.е. когда речь идет о Т-зависимых антигенах. 49. Дайте определение идиотипа, изотипа и аллотипа молекул антител Изотипы – детерминанты, определяющие структурные особенности константных областей тяжелых цепей иммуноглобулинов, т.е. изотоп определяется типом тяжелых цепей. Изотипы одинаковы у всех особей одного вида. В зависимости от изотипа выделяют классы и субклассы иммуноглобулинов. Аллотипы - индивидуальные аллельные варианты иммунглобулинов в пределах одного изотипа, обусловленные внутривидовой вариабельностью константных доменов или каркасных участков вариабельных доменов. Идиотипы - детерминанты, локализованные в вариабельных доменах, определяющие специфичность, молекулы иммуноглобулина. В зависимости от идиотипа иммуноглобулины отличаются по антигенной специфичности, то есть имеют различное строение вариабельных доменов. 50. Расскажите о механизмах взаимодействия антигенов и антител. Понятие об аффиности и авидности антител Аффинность, или аффинитет - прочность взаимодействия антигена и антитела. Это показатель силы связи между эпитопом и паратопом. Авидность - функциональная аффинность целой молекулы антитела, определяемая числом антигенсвязывающих участков и их способностью взаимодействовать с эпитопами. Чем больше антитело связывает эпитопов, тем выше его авидность. Основной задачей антител является специфическое связывание с молекулами антигенов. Оно обеспечивается пространственной коплементарностью между паратопом антитела (антигенсвязывающим участком, образованным вариабельными доменами тяжелой и легкой цепей FаЬ-фраrмента) и эпитопом антигена, в этом случае между молекулами антигена и антитела возникают многочисленные нековалентные связи: электростатические взаимодействия, силы Ван-дер-Ваальса, водородные связи и гидрофобные взаимодействия. Электростатические взаимодействия образуются между противоположено заряженными группами атомов антигенов и антител. Сиды Ван-дер-Ваальса являются силами притяжения, возникающими только на очень близких расстояниях, при перекрывании электронных облаков сблизившихся атомов. Они обусловлены электростатическим притяжением отрицательно заряженных электронов одного атома с положительно заряженным ядром другого атома. Гидрофобные взаимодействия возникают в результате стремления гидрофобных групп к взаимной ассоциации, что ослабляет их связь, с молекулами воды и приводит к возникновению сил притяжения между ними. 51. Расскажите о механизмах развития Т-клеточной цитотоксичности Цитолиз инфицированных клеток может происходить посредством следующих механизмов: Перфорин-гранзимовый механизм цитотоксичности; Fas-опосредованный апоптоз; Цитокиновый механизм цитотоксичности. Перфорин-гранзимовый механизм цитотоксичности: Цитотоксическое действие ЦТЛ включает следующие этапы: Распознавание клетки-мишени; Формирование контакта ЦТЛ и клетки-мишени с их поляризацией; Экзоцитоз гранул (программирование лизиса); Индукция гибели клетки-мишени. Т-цитотоксический лимфоцит распознает молекулы МНСI класса в комплексе с антигеном на мишенях с формированием цитотоксического иммунного синапса. Эти взаимодействия приводят к активации ЦТЛ и экзоцитозу содержимого гранул (перфорин и гранзимы) в зону контакта между клетками. Перфорин представляет собой гидрофобный белок, который встраивается в мембрану клетки-мишени (в присутствии ионов Са2+) и образует канал. Через эти каналы в клетку проникают гранзимы В-протеазы, индуцирующие каскад реакций с участием сериновых протеаз, ведущих к запуску апоптоза клетки-мишени. Fas-опосредованный апоптоз: При действии ЦТЛ апоптоз может происходить с участиемFas-лиганда, экспрессируемого Т-клеткой, и Fas-рецептора клетки-мишени. Экспрессии Fas-рецептора на клетки-мишени способствует инфицирование её вирусом. При взаимодействии лиганд-рецептор активируются внутриклеточные каспазы, приводящие клетку к апоптозу. Цитокиновый механизм цитотоксичности: В этом случае цитолиз обеспечивается посредством взаимодействия ФНО-α, синтезируемого ЦТЛ, с соответствующими рецепторами на клетках-мишенях. Сигнал передается через домены смерти и приводит к развитию апоптоза по механизму, схожему с таковым при Fas-цитолизе. Спустя 7-10 дней после распознавания антигена ЦТЛ подвергается апоптозу. Через 2 недели после этого формируется популяция Т-клеток памяти. 52. Охарактеризуйте основные субпопуляции регуляторных Т-клеток, их роль в иммунном ответе и патологии Регуляторные Т-клетки (Treg, Tr1, Тh3). Регуляторные Т-лимфоциты (Treg) подразделяются на природные (естественные), развивающиеся в тимусе, и индуцированные на периферии из Тh-клеток. Основные функции природных Тrеg-клеток - подавление (супрессия) аутоагрессивных клонов Т-лимфоцитов и формирование толерантности к пищевым антигенам и комменсалам, Тr1 и Th3 подавляют ответ эффекторных клеток адаптивного иммунитета, регулируя развитие иммунных реакций. Помимо Th3- и Tr1-клеток к ним относят адаптивный вариант CD4+CD25hi регуляторных Т-лимфоцитов. Th3-клетки представляют разновидность Т-хелперов, индуцируемую при иммунном ответе. Эти клетки секретируют исключительно или преимущественно TGFβ (трансформирующий фактор роста β), который и играет роль их основного эффекторного фактора. Tr1-клетки описаны в барьерных тканях, как клетки, секретирующие IL10 и вовлеченные в формирование неотвечаемости на антигены пищи и симбиотических микроорганизмов. Допускается возможность выработки этими клетками TGFβ, а также из родства или идентичность с Th3-клетками. 53. Дайте сравнительную характеристику Th1 и Th2 Главным подходом при разграничении Th1- и Th2-клеток служит оценка спектра секретируемых ими цитокинов. При дифференцировке Т-хелперов происходит супрессия одних и усиление экспрессии других цитокиновых генов, прежде слабо экспрессированных в Th0-клетках. Th1-лимфоциты продуцируют INFγ, IL2, TNFα, TNFβ, IL3, GM-CSF. Th2-лимфоциты продуцируют IL4, IL13, IL5, IL6, IL9, IL11, IL21, IL25, IL10, IL3 GM-CSF. В этих спектрах есть цитокины, общие для двух линий(например, GM-CSF). Другие цитокины более специфичны для субпопуляций. Среди них есть ключевые: для Th1 – INFγ; для Th2 - IL4. Через цитокины Th1- и Th2-лимфоциты способны ингибировать развитие и функционирование друг друга. Помимо свойств цитокинов, вырабатываемых Th1 и Th2, их функция зависит от прямых контактных взаимодействий с клетками-мишенями, выступающих в качестве эффекторных клеток при иммунном ответе. Для Th1 – это макрофаги, а для Th2 – В-лимфоциты. Развитию Th1-клеток способствуют крайние (очень высокие и очень низкие) дозы антигена и его высокое сродство к рецептору, а развитию Th2-клеток – промежуточные дозы антигена и более низкое сродство к рецептору. 54. Перечислите стадии и фазы иммунного ответа Фазы иммунного ответа: Индуктивная: реализуется в течение 5-7 суток после внедрения антигена, заключается в формировании эффекторных лимфоцитарных клеток и клеток памяти. В индуктивную фазу входят следующие процессы: Переработка и презентация антигена АПК; Распознавание антигена при взаимодействии АПК и Т-лимфоцитами; Активация и пролиферация специфического клона лимфоцитов; Дифференцировка лимфоцитов, направленная на формирование эффекторных клеток и клеток памяти. Эффекторная: длится в среднем около 2-х недель, заключается в реализации механизмов, направленных на непосредственное удаление чужеродного агента и формирование иммунологической памяти. 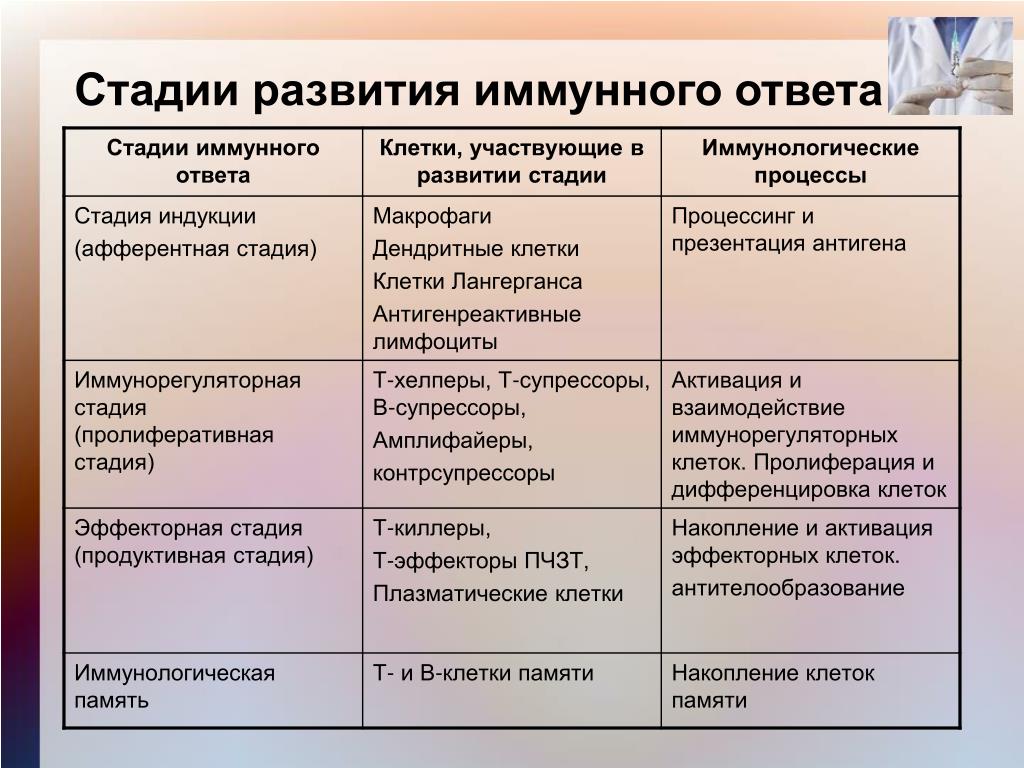 55. Расскажите об антигенпрезентирующих клетках и процессинге Антигенпрезентирующая клетка (АПК) - клетка, обладающая способностью представлять Т-лимфоцитам фрагменты белковых антигенов в иммуногенной форме (в комплексе с МНС). Процессинг антигенов – это частичный протеолиз белковых антигенов (до 5-20 аминокислотных остатков), упаковывание таких фрагментов антигена в молекулы главного комплекса гистосовместимости 1 и 2 классов. 56. Опишите свойства NK-клеток, их функции, рецепторы и маркеры Естественные киллеры (NK-клетки) – особая субпопуляция лимфоцитов, дифференцируются из общей лимфоидной клетки-предшественницы, способны осуществлять цитолиз некоторых опухолевых, а также инфицированных вирусами клеток. По эффекторным функциям NK-клетки близки к Т-лимфоцитам: они проявляют цитотоксическую активность в отношении клеток-мишеней (по тому же перфорин-гранзимовому механизму, что и Т-цитотоксические лимфоциты) и продуцируют цитокины (ИФНγ, ФНО, GMCSF, ИЛ5, ИЛ8). Однако у NK-клеток отсутствует Т-клеточный рецептор. NK-клетки не формируют клеток иммунологической памяти. 57. Противомикробные пептиды: классификация, механизм действия, клетки-продуценты Бактерицидные пептиды – это обширная группа катионных белков, способных поражать многие вирусы, бактерии, грибы и простейшие. Они осуществляют «мгновенный иммунитет». Противомикробные пептиды называют также естественными эндогенными антибиотиками. Бактерицидные пептиды синтезируются нейтрофилами и эпителиальными клетками слизистых оболочек и выделяются в межклеточное пространство при взаимодействии антигена с TLR этих клеток. Различают два семейства противомикробных пептидов: дефенсины и кателицидины. Противомикробные пептиды разрушают наружные мембраны микроорганизмов за счет прямого цитолитического действия, которое связано с тем, что мембраны бактериальных клеток заряжены отрицательно, а пептиды – положительно. Разность зарядов обеспечивает их взаимодействие. Таким образом, катионные белки встраиваются в мембрану клетки и проходят сквозь нее, в результате нарушается целостность мембраны бактерий и образуются поры. Через образовавшиеся поры бактериальная клетка теряет необходимые вещества (ионы калия, аминокислоты и т.д), а внутрь клетки поступает вода, в результате клетка погибает. 58. Что такое главный комплекс гистосовместимости? Расскажите о его функциях На цитоплазматических мембранах практически всех клеток макроорганизма обнаруживаются антигены гистосовместимости. Большая часть из них относится к системе главного комплекса гистосовместимости, или MHC. Гены МНС локализованы в нескольких локусах короткого плеча 6 хромосомы и содержат гены 3 классов: I, II, III класса. Антигены гистосовместимости представляют собой гликопротеины, прочно связанные с цитоплазматической мембраной клеток. Продукты генов МНС I экспрессируются на всех клетках организма, за исключением эритроцитов и клеток ворсинчатого трофобласта. Распознаются СD8+ Т-лимфоцитами. На каждой клетке обычно содержится около 7000 молекул MHC-I. Плотность их экспрессии может изменяться под влиянием различных факторов, в частности, цитокинов. Продукты генов МНС II экспрессируются на профессиональных антигенпрезентирующих клетках (макрофаги, дендритные клетки, В-лимфоциты). Распознаются СD4+ Т-клетками. Содержание молекул на поверхности этих клеток сильно варьирует. На одной дендритной клетке обычно содержится порядка 100 000 молекул MHC-II. При определенных условиях (например, при воспалении) они могут появляться на поверхности других активированных клеток — эпителиальных, эндотелиальных и т.д. Классический индуктор молекул MHC-II — IFNγ. Гены MHC III контролируют некоторые компоненты комплемента, цитокины семейства фактора некроза опухоли, белки теплового шока. 59. Классификация генов ИНС и кодируемые ими молекулы См. предыдущий вопрос 60. Опишите строение молекул HLAI класса. Какие функции они выполняют В молекулах МНС класса I полипептидные цепи сильно отличаются друг от друга. Цепь α состоит из трех внеклеточных доменов, из которых 3-й (прилегающий к мембране) принадлежит супер-семейству иммуноглобулинов, а 2 других имеют иное строение. α-Цепь заякорена в мембране; помимо трансмембранного, она имеет короткий цитоплазматический участок (30 остатков), не обладающий ферментативной активностью и не связанный с ферментами. β-цепь, называемая также β2-микроглобулином, относится к супер-семейству иммуноглобулинов. Она нековалентно связана с α-доменом α-цепи и не имеет трансмембранного участка. β2микроглобулин кодируется геном, расположенным вне комплекса MHC (в хромосоме 15). Функции: 1)обслуживает зону цитозоля (внутренняя среда клетки), сообщающуюся через ядерные поры с содержимым ядра; 2)вирусы и пептиды связываются с молекулами HLA I. |
