ответы на вопросы по иммунологии. Исторические этапы взаимодействия человека с инфекцией
 Скачать 445.09 Kb. Скачать 445.09 Kb.
|
|
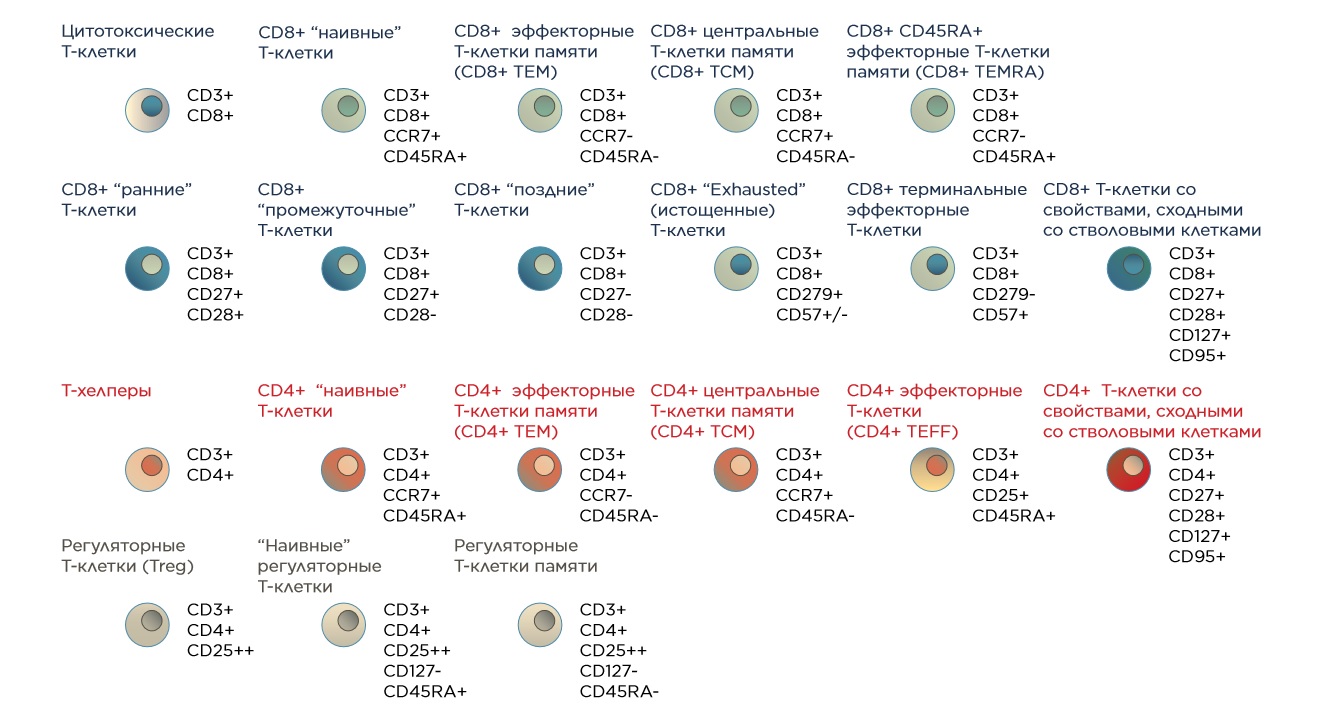
Селезенка, как и другие периферические органы иммунной системы, принимает участие в обеспечении неспецифической резистентности, играя роль фильтра, удаляющего из циркуляции чужеродные частицы и собственные поврежденные или отжившие свой срок клетки крови. Вместе с тем селезенка входит в число основных органов иммуногенеза и образования антител, особенно выраженного в тех случаях, когда антиген поступает с током крови непосредственно в селезенку, которая по строению сходна с лимфатическими узлами. От покрывающей орган капсулы отходят трабекулы, составляющие каркас органа. Селезенка содержит белую пульпу - аналог коры лимфоузлов, заполненную в основном лимфоидными клетками, и красную пульпу, где преобладают эритроциты и макрофаги. В белой пульпе и пограничной зоне между белой и красной пульпой имеются Т-зависимые зоны, где сосредоточены преимущественно Т-лимфоциты, и Т-независимые зоны или зародышевые центры, содержащие преимущественно В-лимфоциты. Удаление селезенки (травма, лечение анемий) снижает способность организма к продукции антител, но не влияет на Т-зависимые формы иммунного ответа, продукцию иммуноглобулинов, процессы фагоцитоза. Функции селезенки дублируются другими органами иммунной системы Гематотимический барьер В корковом веществе тимуса происходит антигеннезависимая дифференцировка Т-лимфоцитов, и действие антигенов на этом этапе может нарушить нормальный лимфопоэз. Поэтому развивающиеся Т-лимфоциты коркового вещества отделены от крови и находящихся в ней антигенов гематотимическим барьером. В его состав входят следующие структуры: эндотелий капилляра непрерывного типа; непрерывная базальная мембрана эндотелия; перикапиллярное пространство, в соединительной ткани которого присутствуют макрофаги, расщепляющие антигены; базальная мембрана периваскулярных ретикулоэпителиоцитов; ретикулоэпителиоциты, которые имеют отростчатую форму и при помощи своих отростков охватывают гемокапилляры. 5) Периферические органы иммунной системы. Селезенка. Строение. Функции. В селезенке различают две поверхности: диафрагмальную, facies diaphragmatica, и висцеральную, facies visceralis, два конца: задний и передний, extremitas posterior et anterior, и два края: верхний и нижний, margo superior et inferior. Диафрагмальная поверхность выпуклая, гладкая, на висцеральной – различают щелеобразные ворота, hilus lienis, через которые в селезенку входят 6-8 ветвей селезеночной артерии и покидают ее вены. В адвентиции артерий находятся вегетативные нервные сплетения. Венозная система селезенки имеет многочисленные расширения, синусы, где скапливаются эритроциты. Брюшина покрывает селезенку со всех сторон, интраперитонеально, за исключением ворот. От ворот селезенки начинаются связки, образованные брюшиной. Связки от селезенки направляются к своду желудка, lig. gastrolienale, к диафрагме, lig. phrenicolienale, к левому изгибу толстой кишки, lig. phrenicocolicum Селезенка покрыта фиброзной капсулой, состоящей из коллагеновых, эластических и гладких мышечных волокон. Селезенка имеет серозную оболочку. От капсулы в направлении паренхимы отходят соединительнотканные перекладины, трабекулы, разделяющие белую и красную пульпу селезенки на отдельные участки. Белая пульпа построена из лимфатической ткани, собранной вокруг артерий в виде шаров. В белой пульпе имеются более светлые узелки лимфатической ткани, которые называются реактивными центрами и являются местами размножения лимфоцитов. Внутренняя архитектура пульпы во многом зависит от кровеносных сосудов Селезенка – кроветворный орган, где образуются лимфоциты. Кроме того, в ее кровеносной системе происходит разрушение старых эритроцитов, «кладбище» эритроцитов, депонирующая функция селезенки заключается в накоплении крови в сосудах, которая по мере необходимости поступает в селезеночную вену. Поэтому селезенка изменяет свою величину в зависимости от кровенаполнения. В среднем ее длина колеблется от 10 до 15 см, ширина составляет 7-9 см, толщина 4-6 см, масса около 200 г. При застое крови в воротной вене, цирроз печени, порок сердца селезенка может значительно увеличиваться и уплотняться. Возрастные изменения. В старческом возрасте в селезенке происходит атрофия белой и красной пульпы, вследствие чего ее трабекулярный аппарат вырисовывается более четко. Количество лимфатических узелков в селезенке и размеры их центров постепенно уменьшаются. Ретикулярные волокна белой и красной пульпы грубеют и становятся более извилистыми. У лиц старческого возраста наблюдаются узловатые утолщения волокон. Количество макрофагов и лимфоцитов в пульпе уменьшается, а число зернистых лейкоцитов и тучных клеток возрастает. У детей и лиц старческого возраста в селезенке обнаруживаются гигантские многоядерные клетки — мегакариоциты. Количество железосодержащего пигмента, отражающее процесс гибели эритроцитов, с возрастом в пульпе увеличивается, но располагается он главным образом внеклеточно. 6) Методы выделения клеток иммунной системы.(будет ссылка на презентацию) 7) Клеточные основы иммунной системы. Этапы развития лимфоцитов как клеток иммунной системы. Основные популяции. Места созревания. Основные мембранные маркеры. Основные функции. Т-клеточный рецептор, молекулярные компоненты, функции. Т- лимфоциты. Локализация. Обычно локализуются в так называемых Т- зависимых зонах периферических лимфоидных органов (периартикулярно в белой пульпе селезенки и паракортикальных зонах лимфоузлов). Функции. Т- лимфоциты распознают процессированный и представленный на поверхности антиген- представляющих ( А ) клеток антиген. Они отвечают за клеточный иммунитет, иммунные реакции клеточного типа. Отдельные субпопуляции помогают В- лимфоцитам реагировать на Т- зависимые антигены выработкой антител. Происхождение и созревание. Родоначальницей всех клеток крови, в том числе лимфоцитов, является единая стволовая клетка костного мозга. Она генерирует два типа клеток- предшественников- лимфоидную стволовую клетку и предшественника клеток красной крови, от которой происходят и клетки- предшественники лейкоцитов и макрофагов. Образование и созревание иммунокомпетентных клеток осуществляется в центральных органах иммунитета (для Т- лимфоцитов - в тимусе). Клетки- предшественники Т- лимфоцитов попадают в тимус, где пре- Т- клетки (тимоциты) созревают, пролиферируют и проходят дифференцировку на отдельные субклассы в результате взаимодействия с эпителиальными и дендритными клетками стромы и воздействия гормоноподобных полипептидных факторов, секретируемых эпителиальными клетками тимуса (альфа1- тимозин, тимопоэтин, тимулин и др.). При дифференцировке Т- лимфоциты приобретают определенный набор мембранных CD- маркеров. Т-клетки разделяют на субпопуляции в соответствии с их функцией и профилем CD- маркеров. Т- лимфоциты распознают антигены с помощью двух типов мембранных гликопротеинов- Т- клеточных рецепторов (семейство Ig- подобных молекул) и CD3, нековалентно связанных между собой. Их рецепторы, в отличие от антител и рецепторов В- лимфоцитов, не распознают свободно циркулирующие антигены. Они распознают пептидные фрагменты, представляемые им А- клетками через комплекс чужеродных веществ с соответствующим белком главной системы гистосовместимости 1 и 2 класса. Выделяют три основные группы Т- лимфоцитов - помощники (активаторы), эффекторы, регуляторы. Первая группа- помощники (активаторы), в состав которых входят Т- хелперы1, Т- хелперы2, индукторы Т- хелперов, индукторы Т- супрессоров. 1. Т- хелперы1 несут рецепторы CD4 (как и Т- хелперы2) и CD44, отвечают за созревание Т- цитотоксических лимфоцитов (Т- киллеров), активируют Т- хелперы2 и цитотоксическую функцию макрофагов, секретируют ИЛ-2, ИЛ-3 и другие цитокины. 2. Т- хелперы2 имеют общий для хелперов CD4 и специфический CD28 рецепторы, обеспечивают пролиферацию и дифференцировку В- лимфоцитов в антителпродуцирующие (плазматические) клетки, синтез антител, тормозят функцию Т- хелперов1, секретируют ИЛ-4, ИЛ-5 и ИЛ-6. 3. Индукторы Т- хелперов несут CD29, отвечают за экспрессию антигенов HLA класса 2 на макрофагах и других А - клетках. 4. Индукторы Т- супрессоров несут CD45 специфический рецептор, отвечают за секрецию ИЛ-1 макрофагами, активацию дифференцировки предшественников Т- супрессоров. Вторая группа- Т- эффекторы. В нее входит только одна субпопуляция. 5. Т- цитотоксические лимфоциты (Т- киллеры). Имеют специфический рецептор CD8, лизируют клетки- мишени, несущие чужеродные антигены или измененные аутоантигены (трансплантант, опухоль, вирус и др.). ЦТЛ распознают чужеродный эпитоп вирусного или опухолевого антигена в комплексе с молекулой класса 1 HLA в плазматической мембране клетки- мишени. Третья группа- Т-клетки- регуляторы. Представлена двумя основными субпопуляциями. 6. Т- супрессоры имеют важное значение в регуляции иммунитета, обеспечивая подавление функций Т- хелперов 1 и 2, В- лимфоцитов. Имеют рецепторы CD11, CD8. Группа функционально разнородна. Их активация происходит в результате непосредственной стимуляции антигеном без существенного участия главной системы гистосовместимости. 7. Т- контсупрессоры. Не имеют CD4, CD8, имеют рецептор к особому лейкину. Способствуют подавлению функций Т- супрессоров, вырабатывают резистентность Т- хелперов к эффекту Т- супрессоров. В- лимфоциты. Существует несколько подтипов В- лимфоцитов. Основная функция В- клеток- эффекторное участие в гуморальных иммунных реакциях, дифференциация в результате антигенной стимуляции в плазматические клетки, продуцирующие антитела. Образование В- клеток у плода происходит в печени, в дальнейшем- в костном мозге. Процесс созревания В- клеток осуществляется в две стадии- антиген - независимую и антиген - зависимую. Антиген - независимая фаза. В- лимфоцит в процессе созревания проходит стадию пре- В- лимфоцита - активно пролиферирующей клетки, имеющей цитоплазменные H- цепи типа C мю (т.е. IgM). Следующая стадия- незрелый В- лимфоцит характеризуется появлением мембранного (рецепторного) IgM на поверхности. Конечная стадия антигеннезависимой дифференцировки- образование зрелого В- лимфоцита, который может иметь два мембранных рецептора с одинаковой антигенной специфичностью (изотипа) - IgM и IgD. Зрелые В- лимфоциты покидают костный мозг и заселяют селезенку, лимфоузлы и другие скопления лимфоидной ткани, где их развитие задерживается до встречи со “своим” антигеном, т.е. до осуществления антиген- зависимой дифференцировки. Антиген- зависимая дифференцировка включает активацию, пролиферацию и дифференцировку В- клеток в плазматические клетки и В- клетки памяти. Активация осуществляется различными путями, что зависит от свойств антигенов и участия других клеток (макрофагов, Т- хелперов). Большинство антигенов, индуцирующих синтез антител, для индукции иммунного ответа требуют участия Т- клеток - тимус- зависимые антигены. Тимус - независимые антигены (ЛПС, высокомолекулярные синтетические полимеры) способны стимулировать синтез антител без помощи Т- лимфоцитов. В- лимфоцит с помощью своих иммуноглобулиновых рецепторов распознает и связывает антиген. Одновременно с В- клеткой антиген по представлению макрофага распознается Т- хелпером (Т- хелпером 2), который активируется и начинает синтезировать факторы роста и дифференцировки. Активированный этими факторами В- лимфоцит претерпевает ряд делений и одновременно дифференцируется в плазматические клетки, продуцирующие антитела. Пути активации В- клеток и кооперации клеток в иммунном ответе на различные антигены и с участием популяций имеющих и не имеющих антиген Lyb5 популяций В- клеток отличаются. Активация В- лимфоцитов может осуществляться: - Т- зависимым антигеном при участии белков МНС класса 2 Т- хелпера; - Т- независимым антигеном, имеющим в составе митогенные компоненты; - поликлональным активатором (ЛПС); - анти- мю иммуноглобулинами; - Т- независимым антигеном, не имеющим митогенного компонента 8) Метод проточной цитофлюориметрии. Принцип метода. Использование в иммунологических исследованиях. Принципы проточной цитометрии По-научному, проточная цитометрия, или flow cytometry – это метод регистрации оптических параметров находящихся в потоке клеток или частиц по сигналам светорассеяния и флуоресценции в режиме поштучного анализа. Для фокусировки клеток в потоке жидкости используется гидродинамическое или акустическое фокусирование, с помощью которого клетки выстраиваются в потоке в ряд, одна за другой. В проточной ячейке клетки облучаются лазером, оптика цитометра собирает световой сигнал от клеток, а электроника преобразует и оцифровывает сигнал для дальнейшего анализа. В проточной цитометрии измеряются следующие параметры: прямое светорассеяние (рассеяние света под малым углом, FSC) для определения относительного размера клеток или частиц; боковое светорассеяние (рассеяние света под прямым углом, SSC) для оценки неоднородности внутриклеточного содержимого клетки (например, размеры ядра и гранулярность цитоплазмы); флюоресценция – для изучения клеточных маркеров с помощью меченных флюорохромными красителями антител к поверхностным и внутриклеточным компонентам клеток. При этом по интенсивности флюоресценции можно судить об экспрессии антигенов (количестве рецепторов) на клетках. Проточная цитометрия в иммунологии активно используется для иммунофенотипирования клеток крови, позволяет идентифицировать внутриклеточные белки, оценить степень цитотоксичности, и многое другое. Субпопуляции Т-клеток периферической крови и поверхностные антигены, применяемые для их выявления * только для научных исследований, не для клинической диагностики
В тимусе происходит дифференцировка Т-лимфоцитов (тимусзависимых), образующихся из поступивших в этот орган стволовых клеток костного мозга. В дальнейшем обе эти популяции лимфоцитов с током крови поступают в периферические органы иммунной системы, к которым относят миндалины, лимфоидные узелки, расположенные в стенках полых органов пищеварительной и дыхательной систем, мочевыводящих путей, лимфатические узлы и селезенку. Функции периферических органов иммунной системы находятся под влиянием центральных органов иммуногенеза. Т-лимфоциты заселяют тимусзависимую зону лимфатических узлов (паракортикальная зона), селезенки (периартериальные лимфоидные муфты и периартериальная часть лимфоидных узелков) и обеспечивают осуществление клеточного иммунитета путем накопления и ввода в действие сенсибилизированных (с повышенной чувствительностью) лимфоцитов, а также гуморального иммунитета (путем синтеза специфических антител). В-лимфоциты являются предшественниками антителообразующих клеток—плазмоцитов и лимфоцитов с повышенной активностью. Они поступают в бурсазависимые зоны лимфатических узлов (лимфоидные узелки, мякотные тяжи) и селезенки (лимфоидные узелки, кроме их периартериальной части). В-лимфоциты выполняют функции гуморального иммунитета, в котором основная роль принадлежит крови, лимфе, секрету желез, содержащему вещества (антитела), участвующие в иммунных реакциях. Т- и В-лимфоциты в световом микроскопе отличить друг от друга невозможно. Лимфоциты на своей поверхности несут рецепторы (чувствительные аппараты), распознающие антигены— сложные вещества, вызывающие в организме иммунную реакцию. Эта реакция заключается в образовании антител клетками лимфоидной ткани. Количество (плотность расположения) таких рецепторов на поверхности В-лимфоцитов в 100—200 раз больше, чем на поверхности Т-лимфоцитов. Клетки, выполняющие иммунные реакции, получили также название иммунокомпетентных клеток (иммуноциты). Органы иммунной системы локализуются в теле человека не беспорядочно, а в определенных местах. Центральные органы расположены в хорошо защищенных местах: костный мозг— в костномозговых полостях, тимус — в грудной полости позади рукоятки грудины. Периферические органы иммунной системы находятся на границах сред обитания микрофлоры, в участках возможного внедрения в организм чужеродных образований. Здесь формируются как бы пограничные, охранные зоны -«сторожевые посты», «фильтры», содержащие лимфоидную ткань. Миндалины залегают в стенках начального отдела пищеварительной трубки и дыхательных путей, образуя так называемое глоточное лимфоидное кольцо (кольцо Пирогова — Валь-дейера). Лимфоидная ткань миндалин имеется на границе полости рта, полости носа, с одной стороны, и полости глотки и гортани — с другой. Лимфоидные (пейеровы) бляшки располагаются в стенках тонкой кишки, главным образом подвздошной, вблизи места впадения ее в слепую, возле границы двух различных отделов пищеварительной трубки: тонкой и толстой кишки. По другую сторону илеоцекального клапана многочисленные плотно лежащие друг возле друга лимфоидные узелки находятся в стенках червеобразного отростка. Одиночные лимфо-идные узелки как бы рассеяны в толще слизистой оболочки органов пищеварения, дыхательных и мочевыводящих путей для осуществления иммунного надзора на границе организма и внешней среды, представленной воздухом, содержимым пищеварительного тракта, выводимой из организма мочой. Многочисленные лимфатические узлы лежат на путях следования лимфы от органов и тканей в венозную систему. Чужеродный агент, попадающий в ток лимфы, задерживается в них и обезвреживается. На пути тока крови из артериальной системы (из аорты) в систему воротной вены, разветвляющейся в печени, лежит селезенка, функцией которой является иммунный контроль крови. Характерным морфологическим признаком органов иммунной системы являются ранняя закладка (в эмбриогенезе) и состояние зрелости их уже у новорожденных, а также значительное развитие их в детском и подростковом возрасте, т. е. в период становления и созревания организма и формирования его защитных систем. В дальнейшем постепенно происходит возрастная инволюция как центральных, так и периферических органов иммунной системы. В них довольно рано (начиная с подросткового и юношеского возраста) уменьшается количество лимфоидной ткани, а на ее месте разрастается соединительная (жировая) ткань. Для лимфоидной ткани органов иммунной системы свойственно наличие лимфоидных узелков как без центра размножения, так и с таким центром (центр деления клеток и образования новых лимфоцитов). Общая масса органов иммунной системы в теле человека составляет (без костного мозга) около 1,5—2 кг (примерно 10'2 лимфоидных клеток). | ||||||||||||||||||||