Лекция фрш. лекции ФРШ. Кафедра биологии лекционный комплекс по дисциплине физиологическое развитие школьников
 Скачать 1.66 Mb. Скачать 1.66 Mb.
|
|
Женская эндокринная система  3D МОДЕЛЬ Эндокринная система мужчин  3D МОДЕЛЬ Гипоталамо-гипофизарная система Функции периферических эндокринных органов в той или иной степени контролируются гормонами гипофиза. Некоторые функции (например, секреция инсулина поджелудочной железой, зависящая главным образом от уровня глюкозы в крови) контролируются гипофизом в минимальной степени, тогда как другие (например, секреция тиреоидных или половых гормонов) практически целиком подчинены гипофизарным гормонам. Секреция самих гипофизарных гормонов контролируется гипоталамусом. Взаимоотношения между гипоталамусом и гипофизом (называемые гипоталамо-гипофизарной системой) представляют собой систему с обратной связью. Гипоталамус получает сигналы практически из всех областей центральной нервной системы и использует их для формирования сигналов, направляемых в гипофиз. Гипофиз в ответ выделяет различные гормоны, которые стимулируют многие эндокринные железы организма. Изменения в крови уровней гормонов, продуцируемых этими эндокринными железами, воспринимаются гипоталамусом, который соответственно усиливает или ослабляет стимуляцию гипофиза, поддерживая таким образом гомеостаз. Гипоталамус модулирует активность передней и задней долей гипофиза разными способами. Синтезируемые в гипоталамусе нейрогормоны достигают передней доли гипофиза (аденогипофиза) через особую портальную систему сосудов и регулируют синтез и секрецию 6 основных пептидных гормонов передней доли (см. рисунок Гипофиз и его органы-мишени). Последние регулируют функции периферических эндокринных желез (щитовидной железы, надпочечников и гонад), а также рост и лактацию. Прямые нервные контакты между гипоталамусом и передней долей гипофиза отсутствуют. В отличие от этого задняя доля гипофиза (нейрогипофиз) состоит из аксонов, нейронные тела которых расположены в гипоталамусе. Эти аксоны служат в качестве депо для 2 пептидных гормонов: вазопрессина (антидиуретического гормона) и окситоцина, синтезируемых в гипоталамусе; на периферии эти гормоны регулируют водный баланс, выработку молока и маточное сокращение. Практически все гормоны, продуцируемые гипоталамусом и гипофизом, выделяются в кровь импульсами; периоды секреции сменяются периодами покоя. Секреция некоторых гормонов [например, адренокортикотропного гормона (АКТГ), гормона роста, пролактина] обладает четким циркадным ритмом; секреция других (например, лютеинизирующего и фолликулостимулирующего гормонов в ходе менструального цикла) подчиняется месячному ритму, на который накладывается циркадный. ТАБЛИЦА Нейрогормоны Гипоталамуса Гипоталамическая регуляция На сегодняшний день выделяют (см. таблицу Нейрогормоны гипоталамуса) 7 физиологически значимых гипоталамических нейрогормонов. За исключением биогенного амина дофамина, все они являются небольшими пептидами. Некоторые из них вырабатываются не только в гипоталамусе, но и на периферии, особенно в желудочно-кишечном тракте, и функционируют как местные паракринные факторы. Одним из них является вазоактивный интестинальный пептид, который стимулирует также секрецию пролактина. Нейрогормоны контролируют секрецию многих гормонов гипофиза. Секреция большинства из них зависит от стимулирующих сигналов гипоталамуса. Исключение составляет пролактин, секреция которого контролируется ингибирующим стимулом. После перерезки ножки гипофиза (соединяющей гипофиз с гипоталамусом) секреция пролактина усиливается, тогда как секреция других гормонов передней доли гипофиза ослабевает. Большинство патологических процессов в гипоталамусе (включая опухоли и воспалительные поражения) сопровождается изменением секреции гипоталамических нейрогормонов. Поскольку нейрогормоны синтезируются в разных центрах гипоталамуса, некоторые патологические процессы изменяют продукцию только одного нейропептида, тогда как другие влияют на выработку нескольких из них. При этом может иметь место как гипо-, так и гиперсекреция нейрогормонов, что соответственно ослабляет или усиливает секрецию гормонов гипофиза. Клинические синдромы, которые возникают в результате дисфункции гипофизарных гормонов (например, несахарный диабет, акромегалия и гипопитуитаризм), обсуждаются в других разделах. Функции передней доли гипофиза Клетки передней доли гипофиза (которая составляет 80% веса всего гипофиза) синтезируют и выделяют ряд гормонов, необходимых для нормального роста и развития, а также стимулирующих активность нескольких желез-мишеней. Адренокортикотропный гормон (АКТГ) АКТГ называют также кортикотропином. Основным стимулятором секреции АКТГ является кортикотропин-рилизинг-гормон (КРГ), но при стрессе принимает участие и вазопрессин. Под влиянием АКТГ кора надпочечников секретирует кортизол и слабые андрогены, такие как дегидроэпиандростерон (ДГЭА). Попадая в кровь, кортизол и другие кортикостероиды (включая экзогенные кортикостероиды) ингибируют секрецию КРГ и АКТГ. Изменения в системе КРГ-АКТГ-кортизол являются основным компонентом реакции на стресс. В отсутствие АКТГ кора надпочечников атрофируется и практически перестает секретировать кортизол. Тиреотропный гормон (ТТГ) ТТГ регулирует структуру и функцию щитовидной железы, стимулируя синтез и секрецию тиреоидных гормонов. Синтез и секреция самого ТТГ стимулируется гипоталамическим тиреотропин-рилизинг гормоном (ТРГ) и тормозится (по принципу отрицательной обратной связи) присутствующими в крови тиреоидными гормонами. Лютеинизирующий и фолликулостимулирующий гормоны (ЛГ и ФСГ) ЛГ и ФСГ контролируют продукцию половых гормонов. Синтез и секреция самих ЛГ и ФСГ стимулируются в основном гонадотропин-высвобождающим гормоном (ГнВГ) и блокируются эстрогенами и тестостероном. Одним из факторов, контролирующим высвобождение ГнВГ, является кисспептин, гипоталамусный пептид, который активизируется за счет увеличения уровней лептина в период полового созревания. Два половых гормона, активин и ингибин, влияют только на ФСГ; активин является стимулирующим, а ингибин - подавляющим. У женщин ЛГ и ФСГ стимулируют развитие фолликулов яичников и овуляцию. У мужчин же ФСГ действует на клетки Сертоли и необходим для сперматогенеза, а ЛГ – на клетки Лейдига в яичках, стимулируя биосинтез тестостерона. Гормон роста (ГР) ГР стимулирует соматический рост и регулирует обмен веществ. Главным стимулятором синтеза и секреции ГР является рилизинг гормон гормона роста (РГГР), а ингибитором этих процессов – соматостатин. ГР контролирует синтез инсулиноподобного фактора роста 1 (ИФР-1), называемого также соматомедином-С, от которого в основном и зависит рост тканей. ИФР-1 продуцируется многими тканями, но главным его источником является печень. Одна из разновидностей ИФР-1 присутствует в мышцах, где играет роль в увеличении их силы. Этот вариант белка слабее регулируется ГР, чем печеночный его вариант. Метаболические эффекты ГР развиваются двухфазно. Вначале ГР действует подобно инсулину, увеличивая поглощение глюкозы мышцами и жировой тканью, стимулируя захват аминокислот и синтез белка в печени и мышцах и угнетая липолиз в жировой ткани. Через несколько часов развиваются более выраженные антиинсулиновые метаболические эффекты. К ним относится торможение захвата и утилизации глюкозы, что сопровождается повышением уровня глюкозы в крови и усилением липолиза с возрастанием уровня свободных жирных кислот в плазме. Повышение уровня ГР при голодании поддерживает содержание глюкозы в крови и мобилизует жир, являющийся альтернативным источником энергии. Продукция ГР с возрастом снижается. Грелин (гормон, вырабатываемый клетками дна желудка) способствует выделению ГР из гипофиза, увеличивает потребление пищи и улучшает память. Пролактин Пролактин продуцируется клетками, которые называются лактотрофами; на их долю приходится около 30% всех клеток аденогипофиза. Во время беременности размеры гипофиза удваиваются в основном вследствие гиперплазии и гипертрофии лактотрофов. Главная функция пролактина у человека – стимуляция продукции молока. Пролактин выделяется также во время полового акта и при стрессе. Уровень пролактина – чувствительный показатель дисфункции гипофиза; именно этот гормон чаще всего продуцируется опухолями гипофиза, а при инфильтративных процессах или опухолях, сдавливающих гипофиз, его содержание, как и уровень других гормонов, снижается. Другие гормоны Передняя доля гипофиза вырабатывает и ряд других гормонов. К ним относятся проопиомеланокортин (ПОМК, который способствует образованию АКТГ), альфа- и бета-меланоцитстимулирующие гормоны (МСГ), бета-липотропин (β-липотропин), энкефалины и эндорфины. ПОМК и МСГ могут вызывать гиперпигментацию кожи, что приобретает клиническое значение только при расстройствах, сопровождающихся резким повышением уровня АКТГ (например, при аддисоновой болезни или синдроме Нельсона). Функция β-ЛПГ неизвестна. Энкефалины и эндорфины представляют собой эндогенные опиоиды, которые связываются с опиатными рецепторами в ЦНС и активируют их. Функции задней доли гипофиза Задняя доля гипофиза секретирует вазопрессин (называемый также аргинин-вазопрессином или антидиуретическим гормоном [АДГ]) и окситоцин. Оба этих гормона выделяются в ответ на нервные импульсы, и их период полужизни в крови составляет примерно 10 минут. Вазопрессин (антидиуретический гормон, АДГ) Основная функция вазопрессина заключается в сохранении воды в теле почками путем повышения водной проницаемости эпителия дистальных труб. Высокие концентрации вазопрессина также вызывают сужение сосудов. Как и альдостерон, вазопресин играет важную роль в поддержании гомеостаза жидкости, а также гидратации сосудов и клеток. Основным стимулятором секреции вазопрессина является повышение осмотического давления воды в организме, которое «ощущается» осморецепторами гипоталамуса. Другой важный стимул – снижение объема жидкости, «ощущаемое» барорецепторами левого предсердия, легочных вен, каротидного синуса и дуги аорты; сигналы от барорецепторов по блуждающему и языкоглоточным нервам передаются в центральную нервную систему. К другим стимуляторам секреции вазопрессина относятся боль, стресс, рвота, гипоксия, физическая нагрузка, гипогликемия, холинергические агонисты, бета-блокаторы, ангиотензин и простагландины. Ингибиторами секреции вазопрессина являются алкоголь, альфа-блокаторы и глюкокортикоиды. Нехватка вазопрессина вызывает центральный несахарный диабет. Неспособность почек нормально реагировать на вазопрессин является причиной нефрогенного несахарного диабета. Удаление гипофиза обычно не приводит к постоянному несахарному диабету, поскольку некоторые сохранившиеся гипоталамические нейроны продолжают продуцировать небольшое количество вазопрессина. Копептин одновременно вырабатывается с вазопрессином в задней доле гипофиза. Измерение его уровня может помочь выяснению причины гипонатриемии. Окситоцин Окситоцин имеет 2 основных объекта воздействия: Миоэпителиальные клетки лактирующей груди, которые окружают альвеолы молочной железы Гладкая мускулатура матки Выработка окситоцина стимулируется при грудном кормлении, что вызывает сокращение миоэпителиальных клеток. Это сокращение помогает молоку проходить от альвеол к большим протокам, откуда оно и выделяется (так называемый рефлекс выброса молока кормящих матерей). Окситоцин вызывает сокращение гладкомышечных клеток матки, и при беременности чувствительность матки к окситоцину увеличивается. Однако во время родов резкого повышения уровня окситоцина в плазме не происходит и роль окситоцина в индукции родов остается неясной. Стимулы к секреции окситоцина у мужчин неизвестны; его концентрация в плазме мужчин крайне низка. ВЫДЕЛИТЕЛЬНАЯ СИСТЕМА. Мочевыделительная система выполняет в организме важные функции. За счет ее функционирования поддерживается гомеостаз в организме. Благодаря мочевыделительной системе регулируется ионный и кислотно-щелочной баланс в организме, происходит выведение из организма продуктов метаболизма, происходит обмен и синтез некоторых биологически активных веществ. Органы мочевыделения Почки к моменту рождения морфологическое и функциональное созревание почки еще не закончено. Масса, размеры и форма почек. Масса и размеры почек у детей раннего возраста относительно больше, чем у детей старшего возраста и взрослых. У новорожденного масса почек составляет 1:100, а у взрослых 1:200 по отношению к массе тела. У детей до 1 года верхний и нижний полюсы каждой почки сближены, и каждая почка имеет округлую форму, а в дальнейшем приобретает бобовидную форму. Топография почек. Относительно большие размеры почек и более короткий поясничный отдел позвоночника обусловливают низкое топографическое расположение почек у детей первых лет жизни. У них верхний полюс находится на уровне XI–XII грудного позвонка, а нижний – на уровне верхнего края IV поясничного позвонка, т.е. ниже гребешка подвздошной кости. Эта особенность исчезает к 7 годам. Разница в положении контралатеральных почек в норме не превышает высоты тела одного поясничного позвонка. Почки у детей раннего возраста расположены почти параллельно, в старшем возрасте их верхние полюсы сближаются. Околопочечная клетчатка. У детей младшего возраста почки более подвижны, чем у взрослых. Это связано со слабым развитием у них околопочечной клетчатки, предпочечной и позадипочечной фасций. Формирование фиксационных механизмов заканчивается к 5–8 годам. С этого времени смещаемость почек в норме на вдохе не превышает 1,8% от длины тела ребенка. Структура почки. В первые годы жизни почки имеют дольчатое строение (исчезающее к 2–5 годам), толщина мозгового слоя преобладает над толщиной коркового (1:4, в то время как у взрослых 1:2). Анатомические особенности почки: - масса и размеры относительно больше; - полюсы сближены (округлый орган); - более подвижны, чем у взрослых; - дольчатое строение; - мозговой слой преобладает над корковым; - большее число клубочков в единице объема почечной ткани. Физиологические особенности почки: - низкая клубочковая фильтрация; - ограничена реабсорбционная функция; - ограничена секреторная функция; - снижена концентрационная способность. Лоханки почек - относительно шире; - располагаются преимущественно внутрипочечно. Мочеточники - более извитые, имеют перегибы; - гипотоничные, относительно большего диаметра; - короткий дистальный отдел. Мочевой пузырь - мышечные волокна в области устьев мочеточников выражены слабо; - слизистая оболочка толстая, рыхлая, хорошо кровоснабжается. Количество нефронов такое же, как у взрослых (около 2 млн.), и только у глубоко недоношенных детей их новообразование идет еще некоторое время после рождения. Количество клубочков в единице объема ткани у новорожденных и грудных детей больше, чем у взрослых. Диаметр их значительно меньше. У детей до двухлетнего возраста нефрон недостаточно дифференцирован. Морфологическое созревание коркового вещества заканчивается к 3–5 годам, а почки в целом – к школьному возрасту. Функциональные особенности почек С момента рождения почки начинают выполнять гомеостатическую функцию, в основе которой лежит фильтрационная функция почек (рис. 1). Фильтрационная способность почек новорожденного низкая. Это обусловлено: - особенностями гистологического строения висцерального листка капсулы клубочков (кубический эпителий); - небольшими размерами клубочков (общая фильтрующая поверхность клубочков в 5 раз меньше, чем у взрослых); - низким гидростатическим давлением (объем крови, протекающей ежеминутно через почку, у взрослого человека составляет 25% сердечного выброса, у новорожденного – только 5%). По мере роста ребенка объем клубочковой фильтрации увеличивается и приближается к уровню взрослого человека к концу 1-го года жизни. 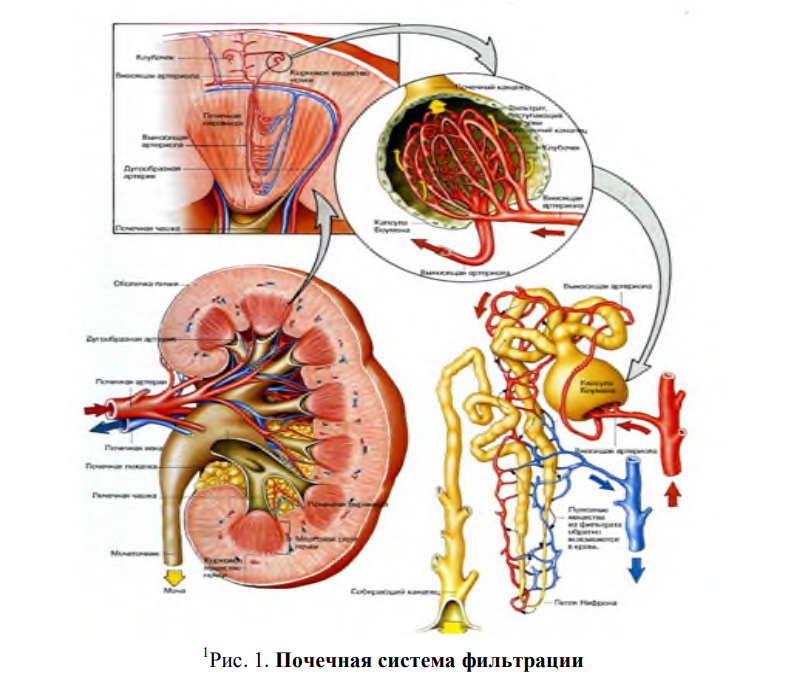 Процессы канальцевой реабсорбции и секреции различных веществ формируются постепенно, у новорожденных они имеют ряд отличий: - канальцевая реабсорбция электролитов и низкомолекулярных веществ снижена, поэтому в этом возрасте отмечают более высокую экскрецию с мочой аминокислот, фосфатов и бикарбонатов; - реабсорбция глюкозы уже в первые недели жизни равна таковой у взрослого или даже превышает ее, что способствует сохранению энергетически необходимого вещества для растущего организма; - реабсорбция ионов натрия происходит интенсивно, при нагрузке натрия хлоридом почки новорожденных продолжают реабсорбировать ионы натрия, в то время как у взрослых происходит угнетение их всасывания; - новорожденные не способны к адекватной экскреции воды и натрия хлорида; их почки могут выводить жидкость дробно на протяжении суток, а одномоментная нагрузка может сопровождаться отсутствием диуретического эффекта; - снижена способность к экскреции ионов калия, кальция, магния и др.; - процессы регуляции кислотно-основного состояния к моменту рождения не созревают: почки ребенка в единицу времени выделяют в 2 раза меньше кислотных радикалов; - из-за незрелости канальцев, низкой активности ферментов ограничена продукция и секреция ионов водорода и аммония, механизм экономии оснований практически не функционирует. Концентрационная функция почек у детей раннего возраста низкая, что Обусловлено недостаточным образованием антидиуретического гормона (АДГ), несовершенством регуляторных механизмов, малой длиной петли нефрона, функциональной неполноценностью эпителия дистальных канальцев, низкой клубочковой фильтрацией (и соответственно низким канальцевым наполнением) и др. В связи с этим для новорожденных характерен низкий удельный вес мочи. Концентрационной способности, аналогичной взрослым, почки детей достигают к 9–12 мес. Почки новорожденного способны обеспечивать гомеостаз только в условиях, когда к организму не предъявляется чрезмерная нагрузка. Оптимальная гомеостатическая функция почки устанавливается к возрасту 10–11 лет. Мочевыводящие пути у детей младших возрастных групп отличаются недостаточным развитием в их стенках мышечной и эластической ткани (рис. 2) 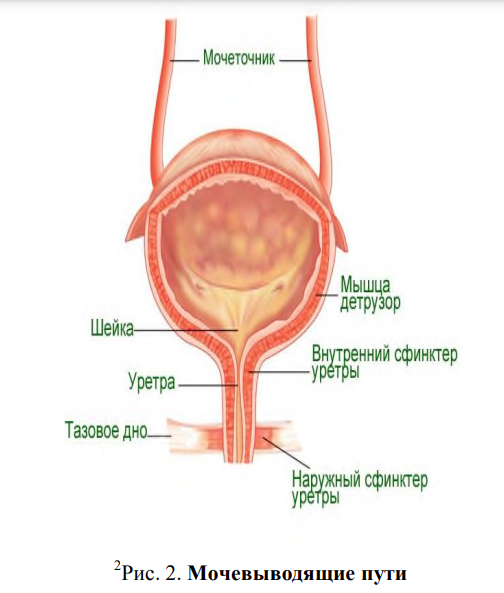 Лоханки почек относительно шире, чем у взрослых, и располагаются у детей до 5 лет преимущественно внутрипочечно, так как почечный синус выражен слабо. Мочеточники отходят от них под прямым углом. Мочеточники относительно длиннее, шире, гипотоничные, обладают относительно низкой сократительной способностью, более извитые, имеют перегибы. Дистальный отдел мочеточника (лежащий непосредственно в стенке и в подслизистом слое мочевого пузыря) очень короткий, с возрастом он удлиняется, достигая максимума к 10–12 годам. Мочевой пузырь у детей грудного возраста расположен выше, чем у взрослых (над симфизом), с возрастом он постепенно спускается в малый таз. Передняя его стенка не покрыта брюшиной, предлежит к передней стенке брюшной полости. Мочевой пузырь имеет овальную форму, слизистая оболочка его толстая, нежная, рыхлая, хорошо кровоснабжается. Мышечные волокна в области отверстий мочеточников развиты слабо, поэтому устья мочеточников зияют. Физиологическая емкость мочевого пузыря у новорожденного составляет около 50 мл, в возрасте 1 года – 100 мл, в 5–9 лет – 150–200 мл, в 12–14 лет–300– 400 мл. Мочеиспускательный канал (уретра) у девочек во все возрастные периоды короче и шире, чем у мальчиков. Его кривизна у детей грудного возраста выражена сильнее, чем у взрослых. Это необходимо учитывать при проведении катетеризации мочевого пузыря и цистоскопии. Анатомические особенности мочевыводящих путей у детей раннего возраста (относительно широкие, гипотоничные лоханки, извитые, гипотоничные мочеточники, отхождение последних от лоханок почти под прямым углом, большая, чем у взрослых, подвижность почек) предрасполагают к нарушению уродинамики, что может способствовать последующему присоединению микробно-воспалительного процесса. Короткий внутрипузырный сегмент мочеточника, слабое развитие мышечных волокон в области устьев мочеточников предрасполагают к развитию пузырно-мочеточникового рефлюкса. Особенности строения уретры у девочек, близость последней к заднему проходу создают условия для проникновения инфекции из периуретеральной области в мочевые пути. ОБЩАЯ ФИЗИОЛОГИЯ НЕРВНОЙ СИСТЕМЫ. Нервная система координирует и регулирует деятельность всех органов и систем, обеспечивая функционирование организма как единого целого; осуществляет адаптацию организма к изменениям окружающей обстановки, поддерживает постоянство его внутренней среды. Топографически нервную систему человека подразделяют на центральную и периферическую. К центральной нервной системе относят спинной и головной мозг. Периферическую нервную систему составляют спинномозговые и черепные нервы, их корешки, ветви, нервные окончания, сплетения и узлы, лежащие во всех отделах тела человека. Согласно анатомо-функциональной классификации, нервную систему условно подразделяют на соматическую и вегетативную. Соматическая нервная система обеспечивает иннервацию тела – кожи, скелетных мышц. Вегетативная нервная система регулирует обменные процессы во всех органах и тканях, а также рост и размножение, иннервирует все внутренние органы, железы, гладкую мускулатуру органов, сердце. Нервная система развивается из эктодермы, через стадии нервной полоски и мозгового желобка с последующим образованием нервной трубки. Из ее каудальной части развивается спинной мозг, из ростральной части формируется сначала 3-х, а затем 5-ти мозговых пузырей, из которых в дальнейшем развиваются конечный, промежуточный, средний, задний и продолговатый мозг. Такая дифференцировка центральной нервной системы происходит на третьей-четвертой неделе эмбрионального развития. В дальнейшем объем головного мозга увеличивается более интенсивно, чем спинного, и к моменту рождения составляет в среднем 400 г. Причем у девочек масса головного мозга несколько ниже, чем у мальчиков. Количество нейронов к моменту рождения соответствует уровню взрослого человека, но количество ветвлений аксонов, дендритов и синаптических контактов значительно возрастает после рождения. Наиболее интенсивно масса головного мозга увеличивается первые 2 года после рождения. Затем темпы его развития немного снижаются, но продолжают оставаться высокими до 6-7 лет. Окончательное созревание головного мозга заканчивается к 17-20 годам. К этому возрасту, его масса у мужчин в среднем составляет 1400 г, а у женщин – 1250 г. Развитие головного мозга идет гетерохронно. Прежде всего, созревают те нервные структуры, от которых зависит нормальная жизнедеятельность организма на данном возрастном этапе. Функциональной полноценности достигают, прежде всего, стволовые, подкорковые и корковые структуры, регулирующие вегетативные функции организма. Эти отделы приближаются по своему развитию к мозгу взрослого человека уже в возрасте 2-4 лет. Спинной мозг. В течение первых трех месяцев внутриутробной жизни спинной мозг занимает позвоночный канал на всю его длину. В дальнейшем позвоночник растет быстрее, чем спинной мозг. Поэтому нижний конец спинного мозга поднимается в позвоночном канале. У новорожденного ребенка нижний конец спинного мозга находится на уровне III поясничного позвонка, у взрослого человека – на уровне II поясничного позвонка. Спинной мозг новорожденного имеет длину 14 см. К 2 годам длина спинного мозга достигает 20 см, а к 10 годам, по сравнению с периодом новорожденности, удваивается. Быстрее всего растут грудные сегменты спинного мозга. Масса спинного мозга у новорожденного составляет около 5,5 г, у детей 1-го года – около 10 г. К 3 годам масса спинного мозга превышает 13 г, к 7 годам равна примерно 19 г. У новорожденного центральный канал шире, чем у взрослого. Уменьшение его просвета происходит главным образом в течение 1-2 годов, а также в более поздние возрастные периоды, когда наблюдается увеличение массы серого и белого вещества. Объем белого вещества спинного мозга возрастает быстро, особенно за счет собственных пучков сегментарного аппарата, формирование которого происходит в более ранние сроки по сравнению со сроками формирования проводящих путей. Продолговатый мозг. К моменту рождения он вполне развит как в анатомическом, так и функциональном отношении. Его масса достигает 8 г у новорожденного. Продолговатый мозг занимает более горизонтальное, чем у взрослых, положение и отличается степенью миелинизации ядер и путей, размерами клеток и их расположением. По мере развития плода размеры нервных клеток продолговатого мозга увеличиваются, а размеры ядра с ростом клетки относительно уменьшаются. Нервные клетки новорожденного имеют длинные отростки, в их цитоплазме содержится тигроидное вещество. Ядра продолговатого мозга формируются рано. С их развитием связано становление в онтогенезе регуляторных механизмов дыхания, сердечно-сосудистой, пищеварительной и др. систем. Мозжечок. В эмбриональном периоде развития сначала формируется древняя часть мозжечка – червь, а затем – его полушария. На 4-5-м месяце внутриутробного развития разрастаются поверхностные отделы мозжечка, образуются борозды и извилины. Наиболее интенсивно мозжечок растет в первый год жизни, особенно с 5-го по 11-й месяц, когда ребенок учится сидеть и ходить. У годовалого ребенка масса мозжечка увеличивается в 4 раза и в среднем составляет 95 г. После этого наступает период медленного роста мозжечка, к 3 годам размеры мозжечка приближаются к его размерам у взрослого. У 15-летнего ребенка масса мозжечка – 150 г. Кроме того, быстрое развитие мозжечка происходит и в период полового созревания. Серое и белое вещество мозжечка развивается неодинаково. У ребенка рост серого вещества осуществляется относительно медленнее, чем белого. Так, от периода новорожденности до 7 лет количество серого вещества увеличивается приблизительно в 2 раза, а белого – почти в 5 раз. Из ядер мозжечка раньше других формируется зубчатое ядро. Начиная от периода внутриутробного развития и до первых лет жизни детей, ядерные образования выражены лучше, чем нервные волокна. Клеточное строение коры мозжечка у новорожденного значительно отличается от взрослого. Ее клетки во всех слоях отличаются по форме, размерам и количеству отростков. У новорожденного еще не полностью сформированы клетки Пуркинье, в них не развито тигроидное вещество, ядро почти полностью занимает клетку, ядрышко имеет неправильную форму, дендриты клеток слаборазвиты. Формирование этих клеток идет бурно после рождения и заканчивается к 3-5 неделям жизни. Клеточные слои коры мозжечка у новорожденного значительно тоньше, чем у взрослого. К концу 2-го года жизни их размеры достигают нижней границы величины у взрослого. Полное формирование клеточных структур мозжечка осуществляется к 7-8 годам. Мост. У новорожденного расположен выше, чем у взрослого, а к 5 годам располагается на том же уровне, что и у зрелого организма. Развитие моста связано с формированием ножек мозжечка и установлением связей мозжечка с другими отделами центральной нервной системы. Внутреннее строение моста у ребенка не имеет отличительных особенностей по сравнению с взрослым человеком. Ядра расположенных в нем нервов к периоду рождения уже сформированы. Средний мозг. Его форма и строение почти не отличаются от взрослого. Ядро глазодвигательного нерва хорошо развито. Хорошо развито красное ядро, его крупноклеточная часть, обеспечивающая передачу импульсов из мозжечка к мотонейронам спинного мозга, развивается раньше, чем мелкоклеточная, через которую передается возбуждение от мозжечка к подкорковым образованиям мозга и к коре больших полушарий. У новорожденного черная субстанция представляет собой хорошо выраженное образование, клетки которого дифференцированы. Но значительная часть клеток черной субстанции не имеет характерного пигмента (меланина), который появляется с 6 месяцев жизни и максимального развития достигает к 16 годам. Развитие пигментации находится в прямой связи с совершенствованием функций черной субстанции. Промежуточный мозг. Отдельные формации промежуточного мозга имеют свои темпы развития. Закладка зрительного бугра осуществляется к 2 месяцам внутриутробного развития. На 3-м месяце разграничивается таламус и гипоталамус. На 4- 5-м месяце между ядрами таламуса проявляются светлые прослойки развивающихся нервных волокон. В это время клетки еще слабо дифференцированы. В 6 месяцев становятся хорошо видными клетки ретикулярной формации зрительного бугра. Другие ядра зрительного бугра начинают формироваться с 6 месяцев внутриутробной жизни, к 9 месяцам они хорошо выражены. С возрастом происходит их дальнейшая дифференциация. Усиленный рост зрительного бугра осуществляется в 4-летнем возрасте, а размеров взрослого он достигает к 13 годам жизни. В эмбриональном периоде развития закладывается подбугорная область, но в первые месяцы внутриутробного развития ядра гипоталамуса не дифференцированы. Только на 4-5-м месяце происходит накопление клеточных элементов будущих ядер, на 8- м месяце они хорошо выражены. Ядра гипоталамуса созревают в разное время, в основном к 2-3 годам. К моменту рождения структуры серого бугра еще полностью не дифференцированы, что приводит к несовершенству теплорегуляции у новорожденных и детей первого года жизни. Дифференциация клеточных элементов серого бугра заканчивается позднее всего – к 13- 17 годам. Кора больших полушарий. До 4-го месяца развития плода поверхность больших полушарий гладкая и на ней отмечается лишь вдавливание будущей боковой борозды, которая окончательно формируется только ко времени рождения. Наружный корковый слой растет быстрее внутреннего, что приводит к образованию складок и борозд. К 5 месяцам внутриутробного развития образуются основные борозды: боковая, центральная, мозолистая, теменно-затылочная и шпорная. Вторичные борозды появляются после 6 месяцев. К моменту рождения первичные и вторичные борозды хорошо выражены, и кора больших полушарий имеет такой же тип строения, как и у взрослого. Но развитие формы и величины борозд и извилин, формирование мелких новых борозд и извилин продолжается и после рождения. К моменту рождения кора больших полушарий имеет такое же количество нервных клеток (14-16 млрд.), как и у взрослого. Но нервные клетки новорожденного незрелы по строению, имеют простую веретенообразную форму и очень небольшое количество отростков. Серое вещество коры больших полушарий плохо дифференцировано от белого. Кора больших полушарий относительно тоньше, корковые слои слабо дифференцированы, а корковые центры недостаточно сформированы. После рождения кора больших полушарий развивается быстро. Соотношение серого и белого вещества к 4 месяцам приближается к соотношению у взрослого. К 9 месяцам становятся более отчетливыми первые три слоя коры, а к году общая структура мозга приближается к зрелому состоянию. Расположение слоев коры, дифференцирование нервных клеток в основном завершается к 3 годам. В младшем школьном возрасте и в период полового созревания продолжающееся развитие головного мозга характеризуется увеличением количества ассоциативных волокон и образованием новых нервных связей. В этот период масса мозга увеличивается незначительно. В развитии коры больших полушарий сохраняется общий принцип: сначала формируются филогенетически более старые структуры, а затем более молодые. На 5-м месяце, раньше других появляются ядра, регулирующие двигательную активность. На 6-м месяце появляется ядро кожного и зрительного анализатора. Позже других развиваются филогенетически новые области: лобная и нижнетеменная (на 7-м месяце), затем височно-теменная и теменно-затылочная. Причем филогенетически более молодые отделы коры больших полушарий с возрастом относительно увеличиваются, а более старые, наоборот, уменьшаются. 2. Основные этапы развития высшей нервной деятельности Низшая и высшая нервная деятельность ребенка формируются в результате морфофункционального созревания всего нервного аппарата. Нервная система, а вместе с ней и высшая нервная деятельность у детей и подростков достигают уровня взрослого человека примерно к 20 годам. Весь сложный процесс развития ВНД человека определяется как наследственно, так и многими другими биологическими и социальными факторами внешней среды. Последние приобретают ведущее значение в постнатальном периоде, поэтому на семью и учебные заведения ложится основная ответственность за развитие интеллектуальных возможностей человека. ВНД ребенка от рождения до 7 лет. Ребенок рождается с набором безусловных рефлексов, рефлекторные дуги которых начинают формироваться на 3-м месяце внутриутробного развития. Тогда у плода появляются первые сосательные и дыхательные движения, а активное движение плода наблюдается на 4-5-м месяце. К моменту рождения у ребенка формируется большинство врожденных рефлексов, которые обеспечивают ему нормальное функционирование вегетативной сферы. Возможность простых пищевых условных реакций возникает уже на 1-2-е сутки, а к концу первого месяца развития образуются условные рефлексы с двигательного анализатора и вестибулярного аппарата. Со 2-го месяца жизни образуются слуховые, зрительные и тактильные рефлексы, а к 5-му месяцу развития у ребенка вырабатываются все основные виды условного торможения. Большое значение в совершенствовании условно-рефлекторной деятельности имеет обучение ребенка. Чем раньше начато обучение, т. е. выработка условных рефлексов, тем быстрее идет их формирование впоследствии. К концу 1-го года развития ребенок относительно хорошо различает вкус пищи, запахи, форму и цвет предметов, различает голоса и лица. Значительно совершенствуются движения, некоторые дети начинают ходить. Ребенок пытается произносить отдельные слова, и у него формируются условные рефлексы на словесные раздражители. Следовательно, уже в конце первого года полным ходом идет развитие второй сигнальной системы и формируется ее совместная деятельность с первой. На 2-м году развития ребенка совершенствуются все виды условно-рефлекторной деятельности, и продолжается формирование второй сигнальной системы, значительно увеличивается словарный запас; раздражители или их комплексы начинают вызывать словесные реакции. Уже у двухгодовалого ребенка слова приобретают сигнальное значение. 2-й и 3-й год жизни отличаются живой ориентировочной и исследовательской деятельностью. Этот возраст ребенка характеризуется «предметным» характером мышления, т. е. решающим значением мышечных ощущений. Эта особенность в значительной степени связана с морфологическим созреванием мозга, так как многие моторные корковые зоны и зоны кожно-мышечной чувствительности уже к 1-2 годам достигают достаточно высокой функциональной полноценности. Основным фактором, стимулирующим созревание этих корковых зон, являются мышечные сокращения и высокая двигательная активность ребенка. Период до 3-х лет характеризуется также легкостью образования условных рефлексов на самые различные раздражители. Примечательной особенностью 2-3-летнего ребенка является легкость выработки динамических стереотипов – последовательных цепей условно-рефлекторных актов, осуществляющихся в строго определенном, закрепленном во времени порядке. Динамический стереотип это следствие сложной системной реакции организма на комплекс условных раздражителей (условный рефлекс на время – прием пищи, время сна и др.). Возраст от 3-х до 5-ти лет характеризуется дальнейшим развитием речи и совершенствованием нервных процессов (увеличивается их сила, подвижность и уравновешенность), процессы внутреннего торможения приобретают доминирующее значение, но запаздывательное торможение и условный тормоз вырабатываются с трудом. К 5-7 годам еще более повышается роль сигнальной системы слов и дети начинают свободно говорить. Это обусловлено тем, что только к семи годам постнатального развития функционально созревает материальный субстрат второй сигнальной системы – кора больших полушариев. ВНД детей от 7 до 18 лет. Младший школьный возраст (с 7 до 12 лет) – период относительно «спокойного» развития ВНД. Сила процессов торможения и возбуждения, их подвижность, уравновешенность и взаимная индукция, а также уменьшение силы внешнего торможения обеспечивают возможности широкого обучения ребенка. Но только при обучении письму и чтению слово становится предметом сознания ребенка, все, более отдаляясь от связанных с ним образов, предметов и действий. Незначительное ухудшение процессов ВНД наблюдается только в 1-м классе в связи с процессами адаптации к школе. Особое значение для педагогов имеет подростковый (с 11-12 до 15-17 лет) период. В это время нарушается уравновешенность нервных процессов, большую силу приобретает возбуждение, замедляется прирост подвижности нервных процессов, значительно ухудшается дифференцировка условных раздражителей. Ослабляется деятельность коры, а вместе с тем и второй сигнальной системы. Все функциональные изменения приводят к психической неуравновешенности и конфликтности подростка. Старший школьный возраст (15-18 лет) совпадает с окончательным морфофункциональным созреванием всех систем организма. Повышается роль корковых процессов в регуляции психической деятельности и функций второй сигнальной системы. Все свойства нервных процессов достигают уровня взрослого человека, т. е. ВНД старших школьников становится упорядоченной и гармоничной. Таким образом, для нормального развития ВНД на каждом отдельном этапе онтогенеза необходимо создание оптимальных условий. ЧАСТНАЯ ФИЗИОЛОГИЯ НЕРВНОЙ СИСТЕМЫ. Нервная система регулирует все системы организма, все рефлексы, и особенно важна для человека, так как обеспечивает умственную деятельность человека. Спинной мозг является частью центральной нервной системы. Его основная функция заключается в передаче нервных импульсов, поступающих от головного мозга в конечности, туловище и органы. Спинной мозг состоит из спинномозговых нервов. Они отвечают за двигательную и чувствительную функции конечностей, сфинктеров и органов таза. Каждый спинномозговой нерв объединяет в себе два спинномозговых корешка: задний - чувствительный и передний - двигательный. Поэтому изучение развития спинного мозга особенно важна в медицине с целью предупреждения и лечения поражений и повреждений спинного мозга, которые могут приводить к потере способности получать нервные импульсы, передаваемые головным мозгом, тем самым влеча за собой в большей или меньшей степени значительную потерю подвижности и чувствительности. Спинной мозг представляет собой длинный тяж длиной около 45 см у взрослого человека. Спинной мозг находится в полости позвоночного канала, которая образуется телами и отростками позвонков. Начало его исходит из головного мозга в большом затылочном отверстии (у нижней его границы). Окончание этого образования приходится на область I—II поясничных позвонков. В этом месте он сужается в мозговой конус, от которого вниз ответвляется терминальная нить. В верхних отделах нити находятся элементы нервной ткани. У зародыша человека нервная система развивается из широкой полосы наружного зародышевого листа , эктодермы, лежащей на средней линии, непосредственно над chorda dorsalis. Наружный зародышевый лист разделяется на два отдела: на тонкий роговой листок и более толстую, лежащую срединно-нервную, или мозговую пластинку. Мозговая пластинка вскоре превращается в мозговую трубку. В мозговой трубке, заключающей наполненный зародышевой лимфой щелевидный центральный канал – canalis centralis , различают головной и спинной отделы; из первого образуется головной мозг, а из второго спинной. К 10-й неделе эмбрионального развития формируется дефинитивная внутренняя структура спинного мозга. К 12-й неделе – начинается дифференцировка клеток нейроглии. В спинном мозге видны шейное и поясничное утолщения, появляются конский хвост и конечная нить спинного мозга. К 20-й неделе – начинается миелинизация спинного мозга: аксонов клеток передних и задних рогов спинного мозга, восходящих афферентных систем боковых, передних и задних канатиков, нисходящих эфферентных систем боковых канатиков (проводники экстрапирамидной системы). Миелинизация волокон пирамидной системы начинается на последнем месяце внутриутробного развития и продолжается в течение первого года жизни. В постнатальном периоде спинной мозг претерпевает изменения. Спинной мозг новорожденного относительно длиннее, чем у взрослых, и доходит до нижнего края III поясничного позвонка. Шейное и поясничное утолщение начинают значительно формироваться в первые годы жизни ребенка. Спинной мозг новорожденного имеет длину 14 см. Нижняя граница находится на уровне II поясничного позвонка. К 2 годам длина спинного мозга увеличивается до 20 см, а к 10 годам — до 28 см. Наиболее быстро растут грудные сегменты. Рост спинного мозга продолжается до 20 лет. Масса его увеличивается примерно в 8 раз по сравнению с периодом новорожденности. К 5 - 6 годам соотношение спинного мозга и позвоночного канала становится таким же, как у взрослых. Масса спинного мозга у новорожденного составляет 5 г, в год — 10 г, в 3 года — 13 г, в 7 лет — 19 г, в 14 лет — 22 г. В дальнейшем рост спинного мозга отстает от роста позвоночника, в связи с чем, нижний конец его перемещается кверху. Спинной мозг имеет твердую, паутинную и мягкую соединительнотканные оболочки, продолжающиеся в такие же оболочки головного мозга. Твердая (наружная) мозговая оболочка обтекает его снаружи в виде мешка. Между надкостницей и твердой оболочкой находится эпидуральное пространство. Вверху твердая оболочка срастается с краями большого отверстия затылочной кости, внизу на уровне II—III крестцовых позвонков суживается в виде нити и прикрепляется к копчику. Твердая оболочка мозга у новорожденного тонкая, сращена с костями, отростки оболочки развиты слабо. Паутинная (средняя) мозговая оболочка в виде тонкого прозрачного бессосудистого листка прилегает изнутри к твердой оболочке. Между паутинной и внутренней оболочкой находится подпаутинное пространство, в котором мозг и корешки лежат свободно и окружены большим количеством спинномозговой жидкости. Жидкость подпаутинного пространства спинного мозга непрерывно сообщается с жидкостью подпаутинных пространств головного мозга и мозговых желудочков. У детей подпаутинное пространство относительно большое. Его вместимость у новорожденного составляет около 20 см3, а затем быстро увеличивается: к концу первого года жизни — 30 см3, к 8 годам — 140 см3, у взрослого человека — 200 см3. Спинной мозг участвует в осуществлении сложных двигательных реакций организма. В этом заключается рефлекторная функция спинного мозга. Спинной мозг иннервирует всю скелетную мускулатуру, кроме мышц головы, которые иннервируются черепными нервами. В спинном мозге расположены рефлекторные центры мускулатуры туловища, конечностей и шеи, а также многие центры вегетативной нервной системы. Кора больших полушарий головного мозга Кора больших полушарий головного мозга представляет собой наиболее молодое образование центральной нервной системы.Деятельность коры больших полушарий основана на принципе условного рефлекса, поэтому ее называют условно-рефлекторной. Она осуществляет быструю связь с внешней средой и приспособление организма к изменяющимся условиям внешней среды. Глубокие борозды делят каждое полушарие большого мозга на лобную, височную, теменную, затылочную доли и островок. Островок расположен в глубине сильвиевой борозды и закрыт сверху частями лобной и теменной долей мозга. Кора большого мозга делится на древнюю (архиокортекс), старую (палеокортекс) и новую (неокортекс). Древняя кора, наряду с другими функциями, имеет отношение к обонянию и обеспечению взаимодействия систем мозга. Старая кора включает поясную извилину, гиппокамп. У новой коры наибольшее развитие величины, дифференциации функций отмечается у человека. Толщина новой коры 3-4 мм. Общая площадь коры взрослого человека 1700-2000 см2, а число нейронов — 14 млрд (если их расположить в ряд, то образуется цепь протяженностью 1000 км) — постепенно истощается и к старости составляет 10 млрд (более 700 км). В составе коры имеются пирамидные, звездчатые и веретенообразные нейроны. |
