Раздел 2. Клетка как биологическая система
 Скачать 22.74 Mb. Скачать 22.74 Mb.
|
|
2.3.2. Органические вещества клетки. Углеводы, липиды. Органические вещества Общая характеристика органических веществ клетки Органические вещества клетки могут быть представлены как относительно простыми моле кулами, так и более сложными. В тех случаях, когда сложная молекула (макромолекула) обра зована значительным числом повторяющихся более простых молекул, ее называют полимером, а структурные единицы — мономерами. В зависимости от того, по вторяются или нет звенья полимеров, их относят к регулярным или нерегулярным (рис. 2.6). Полимеры составляют до 90% массы сухого вещества клетки. Они относятся к трем основным классам органиче ских соединений — углеводам (полисахариды), белкам и нуклеиновым кислотам. Регулярными полимерами являются полисахариды, а белки и нуклеиновые кислоты — нерегулярными. В белках и нуклеиновых кислотах последовательность мономеров крайне важна, так как они выполняют информационную функцию. Углеводы Углеводы — это органические соединения, в состав которых входят в основном три химиче ских элемента — углерод, водород и кислород, хотя целый ряд углеводов содержит также азот или серу. Общая формула углеводов — Сm(Н20)n. Их делят на простые и сложные углеводы. Простые углеводы (моносахариды) содержат единственную молекулу сахара, которую невоз можно расщепить на более простые. Это кристаллические вещества, сладкие на вкус и хоро шо растворимые в воде. Моносахариды принимают активное участие в обмене веществ в клетке и входят в состав сложных углеводов — олигосахаридов и полисахаридов. Моносахариды классифицируют по количеству углеродных атомов (С3-С9), например, пентозы (С5) и гексозы (С6). К пентозам относятся рибоза и дезоксирибоза. Рибоза входит в состав РНК и АТФ. Дезоксирибоза является компонентом ДНК. Гексозы (С6Н1206) — это глюкоза, фруктоза, галактоза и др. Глюкоза (виноградный сахар) (рис. 2.7) встре чается во всех организмах, в том числе в крови человека, по скольку является энергетическим резервом. Она входит в со став многих сложных Сахаров: сахарозы, лактозы, мальтозы, крахмала, целлюлозы и др. Фруктоза (плодовый сахар) в наи больших концентрациях содержится в плодах, меде, корнепло дах сахарной свеклы. Она не только принимает активное уча стие в процессах обмена веществ, но и входит в состав сахарозы и некоторых полисахаридов, например инсулина. Большинство моносахаридов способно давать реакцию «се ребряного зеркала» и восстанавливать медь при добавлении фелинговой жидкости (смесь растворов сульфата меди (II) и ка лий-натрий виннокислого) и кипячении. 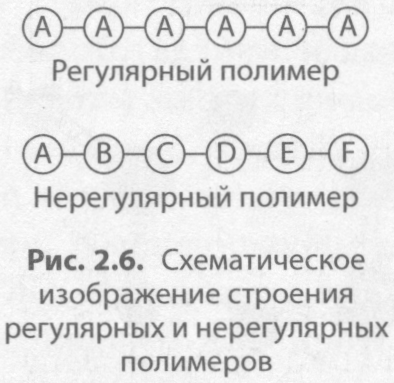 К олигосахаридам относят углеводы, образованные несколь кими остатками моносахаридов. Они в основном также хоро шо растворимы в воде и сладки на вкус. В зависимости от количества этих остатков различают дисахариды (два остатка),   Рис. 2.7. Строение молекулы глюкозы трисахариды (три) и др. К дисахаридам относятся сахароза, лактоза, мальтоза и др. Сахароза (свекловичный или тростниковый сахар) состоит из остатков глюкозы и фруктозы (рис. 2.8), она встречается в запасающих органах некоторых растений. Особенно много сахарозы в корнеплодах сахарной свеклы и сахарного тростника, откуда их получают промышленным способом. Она слу жит эталоном сладости углеводов. Лактоза, или молочный сахар, образована остатками глюкозы и галактозы, содержится в материнском и коровьем молоке. Мальтоза (солодовый сахар) состоит из двух остатков глюкозы. Она образуется в процессе расщепления полисахаридов в семенах рас тений и в пищеварительной системе человека, используется при производстве пива.  Полисахариды — это биополимеры, мономерами которых являются остатки моно- или ди- сахаридов. Большинство полисахаридов нерастворимы в воде и несладкие на вкус. К ним от носятся крахмал, гликоген, целлюлоза и хитин. Крахмал — это белое порошкообразное веще ство, не смачиваемое водой, но образующее при заваривании горячей водой взвесь — клейстер. В действительности крахмал состоит из двух полимеров — менее разветвленной амилозы и более разветвленного амилопектина (рис. 2.9). Мономером как амилозы, так и амилопектина является глюкоза. Крахмал — основное запасное вещество растений, которое в огромных количествах на капливается в семенах, плодах, клубнях, корневищах и других запасающих органах растений. Качественной реакцией на крахмал является реакция с йодом, при которой крахмал окрашива ется в сине-фиолетовый цвет. Гликоген (животный крахмал) — это запасной полисахарид животных и грибов, который у человека в наибольших количествах накапливается в мышцах и печени. Он также нерастворим в воде и несладок на вкус. Мономером гликогена является глюкоза. По сравнению с молекулами крахмала, молекулы гликогена еще более разветвлены. Целлюлоза, или клетчатка, — основной опорный полисахарид растений. Мономером целлю лозы является глюкоза (рис. 2.10). Неразветвленные молекулы целлюлозы образуют пучки, кото рые входят в состав клеточных стенок растений и некоторых грибов. Целлюлоза является основой древесины, она используется в строительстве, при производстве тканей, бумаги, спирта и многих органических веществ. Целлюлоза химически инертна и не растворяется ни в кислотах, ни в ще лочах. Она также не расщепляется ферментами пищеварительной системы человека, однако ее перевариванию способствуют бактерии толстого кишечника. Кроме того, клетчатка стимулирует сокращения стенок желудочно-кишечного тракта, способствуя улучшению его работы.  Хитин — это полисахарид, мономером которого является азотсодержащий моносахарид. Он входит в состав клеточных стенок грибов и панцирей членистоногих. В пищеварительной системе человека также отсутствует фермент переваривания хитина, его имеют лишь некоторые бактерии. Функции углеводов. Углеводы выполняют в клетке пластическую (строительную), энергети ческую, запасающую и опорную функции. Они образуют клеточные стенки растений и грибов. Энергетическая ценность расщепления 1 г углеводов составляет 17,2 кДж. Глюкоза, фруктоза, сахароза, крахмал и гликоген являются запасными веществами. Углеводы могут также входить в состав сложных липидов и белков, образуя гликолипиды и гликопротеины, в частности в кле точных мембранах. Не менее важной представляется роль углеводов в межклеточном узнава нии и восприятии сигналов внешней среды, поскольку они в составе гликопротеинов выполняют функции рецепторов. Липиды — это разнородная в химическом отношении группа низкомолекулярных веществ с гидрофобными свойствами. Данные вещества нерастворимы в воде, образуют в ней эмульсии, но при этом хорошо растворяются в органических растворителях. Липиды маслянисты на ощупь, многие из них оставляют на бумаге характерные невысыхающие следы. Вместе с белками и угле водами они являются одними из основных компонентов клеток. Содержание липидов в различ ных клетках неодинаково, особенно много их в семенах и плодах некоторых растений, в печени, сердце, крови. В зависимости от строения молекулы липиды делят на простые и сложные. К простым липидам относятся нейтральные липиды (жиры), воски, стерины и стероиды. Сложные липиды содержат и другой, нелипидный компонент. Наиболее важными из них являются фосфолипиды, гликолипиды и др. Жиры являются производными трехатомного спирта глицерина и высших жирных кислот (рис. 2.11). Большинство жирных кислот содержит 14-22 углеродных атома. Среди них есть как насыщенные, так и ненасыщенные, то есть содержащие двойные связи. Из насыщенных жирных кислот чаще всего встречаются пальмитиновая и стеариновая, а из ненасыщенных — олеиновая. Некоторые ненасыщенные жирные кислоты не синтезируются в организме человека или синте зируются в недостаточном количестве, и поэтому являются незаменимыми. Остатки глицерина образуют гидрофильные «головки», а остатки жирных кислот — «хвосты».  Жиры выполняют в клетках в основном запасающую функцию и служат источником энергии. Ими богата подкожная жировая клетчатка, выполняющая амортизационную и термоизоляционную функции, а у водных животных — еще и повышающая плавучесть. Жиры растений большей частью содержат ненасыщенные жирные кислоты, вследствие чего они являются жидкими и называются маслами. Масла содержатся в семенах многих растений, таких как подсолнечник, соя, рапс и др. Воски — это сложные смеси жирных кислот и жирных спиртов. У растений они образуют пленку на поверхности листа, которая защищает от испарения, проникновения патогенов и т. п. У ряда животных они покрывают тело или служат для построения сот. К стеринам относится такой липид, как холестерол — обязательный компонент клеточных мембран, а к стероидам — половые гормоны эстрадиол, тестостерон и др. Фосфолипиды, помимо остатков глицерина и жирных кислот, содержат остаток ортофосфор- ной кислоты. Они входят в состав клеточных мембран и обеспечивают их барьерные свойства. Гликолипиды также являются компонентами мембран, но их содержание там невелико. Не- липидной частью гликолипидов являются углеводы. Функции липидов. Липиды выполняют в клетке пластическую (строительную), энергетиче скую, запасающую, защитную и регуляторную функции, кроме того, они являются растворите лями для ряда витаминов. Это обязательный компонент клеточных мембран. При расщеплении 1 г липидов выделяется 38,9 кДж энергии. Они откладываются в запас в различных органах растений и животных. К тому же подкожная жировая клетчатка защищает внутренние органы от переохлаждения или перегревания, а также ударов. Регуляторная функция липидов связана с тем, что некоторые из них являются гормонами. 2.3.3. Белки, их строение и функции. Белки — это высокомолекулярные соединения, биополимеры, мономерами которых являются аминокислоты, связанные пептидными связями. Аминокислотой называют органическое соединение, имеющее аминогруппу, карбоксильную группу и радикал (рис. 2.12). Всего в природе встречается около 200 аминокислот, которые раз личаются радикалами и взаимным расположением функциональных групп, но только 20 из них могут входить в состав белков. Такие аминокислоты называютпротеиногенными. К сожалению, не все протеиногенные аминокислоты могут синтезироваться в организме че ловека, поэтому их делят на заменимые и незаменимые. Заменимые аминокислоты образуются в организме человека в необходимом количестве, а незаменимые — нет. Они должны поступать с пищей, но могут и частично синтезироваться микроорганизмами кишечника. Полностью не заменимых аминокислот насчитывается 8. К ним относятся валин, изолейцин, лейцин, лизин, метионин, треонин, триптофан и фенилаланин. Несмотря на то, что в растениях синтезируются абсолютно все протеиногенные аминокислоты, растительные белки являются неполноценными, поскольку не содержат полного набора аминокислот, к тому же наличие белка в вегетативных частях растений редко превышает 1-2% массы. Поэтому необходимо употреблять в пищу белки не только растительного, но и животного происхождения.  Последовательность из двух аминокислот, связанных пептидными связями (рис. 2.13), назы вается дипептидом, из трех — трипептидом и т. д. Среди пептидов встречаются такие важные соединения, как гормоны (окситоцин, вазопрессин), антибиотики и др. Цепочка из более чем десяти аминокислот называется полипептидом, а полипептиды, содержащие более 50 аминокис лотных остатков, — это белки. Уровни структурной организации белка. Белки могут иметь первичную, вторичную, третич ную и четвертичную структуры. Первичная структура белка — это последовательность аминокислот, соединенных пептидной связью (рис. 2.14). Первичная структура в конечном итоге определяет специфичность белка и его уникальность, поскольку, если даже предположить, что в среднем белок содержит 500 амино кислотных остатков, то число их возможных комбинаций составляет 20 500. Поэтому изменение расположения хотя бы одной аминокислоты в первичной структуре влечет за собой изменение вторичной и более высоких структур, а также свойств белка в целом.  Особенности строения белка обусловливают его пространственную укладку — возникновение вторичной и третичной структур. Вторичная структура представляет собой пространственную укладку белковой молекулы в виде спирали или складок, удерживаемой водородными связями между атомами кислорода и водорода пептидных группировок разных витков спирали или складок (рис. 2.15). Многие бел ки содержат более-менее длинные участки со вторичной структурой. Это, например, кератины волос и ногтей, фиброин шелка. Третичная структура белка также является формой пространственной укладки полипептид ной цепи, удерживаемой гидрофобными, водородными, дисульфидными (S—S) и другими связями (рис. 2.16). Она характерна для большинства белков организма, например миоглобина мышц. Четвертичная структура — наиболее сложная, образованная несколькими полипептидными цепями, соединенными в основном теми же связями, что и в третичной (гидрофобными, ионными и водородными), а также иными слабыми взаимодействиями (рис. 2.17). Четвертичная структура характерна для немногих белков, таких как гемоглобин, хлорофилл и др. По форме молекулы различают фибриллярные и глобулярные белки. Первые из них вытянуты, как, например, коллаген соединительной ткани или кератины волос и ногтей. Глобулярные же белки имеют форму клубка (глобулы), как миоглобин мышц. Простые и сложные белки. Белки могут быть простыми и сложными. Простые белки состоят только из аминокислот, тогда как сложные белки (липопротеины, хромопротеины, гликопротины, нуклеопротеины и др.) содержат белковую и небел ковую части. Хромопротеины содержат окрашенную небелковую часть. К ним относятся гемоглобин, миоглобин, хлорофилл, цитохромы и др.   Так, в составе гемоглобина каждая из четырех полипептид ных цепей белка глобина связана с небелковой частью — гемом, в центре которого находится ион железа, придающий гемоглобину красную окраску. Небелковой частью липопротеинов является липид, а гликопротеинов — углевод. Как липопротеины, так и гликопротеины входят в состав клеточных мембран. Нуклеопротеины представляют собой комплексы белков и нуклеиновых кислот (ДНК и РНК). Они выполняют важнейшие функции в процессах хранения и передачи на следственной информации. Свойства белков. Многие белки хорошо растворимы в воде, од нако есть среди них и такие, которые растворяются только в рас творах солей, щелочей, кислот или органических растворителях. Структура молекулы белка и его функциональная активность за висят от условий окружающей среды. Утрата белковой молекулой своей структуры, вплоть до первичной, называется денатурацией (рис. 2.18). Денатурация происходит вследствие изменения температуры, рН, атмосферного давления, под действием кислот, щелочей, солей тяжелых металлов, органических растворителей и т. п. Обратный процесс восстановления вторичной и более высоких структур называется ренатурацией, однако он не всегда возможен. Полное раз рушение белковой молекулы называется деструкцией. Белки выполняют в клетке ряд функций: пластическую (строительную), каталитическую (ферментативную), энергетическую, сигнальную (рецепторную), сократительную (двигательную), транспортную, защитную, регуляторную и запасающую. Строительная функция белков связана с их наличием в клеточных мембранах и структурных компонентах клетки. Энергетическая — обусловлена тем, что при расщеплении 1 г белка высво бождается 17,2 кДж энергии. Белки-рецепторы мембран принимают активное участие в восприя тии сигналов окружающей среды и их передаче по клетке, а также в межклеточном узнавании. Без белков невозможно движение клеток и организмов в целом, так как они составляют основу жгутиков и ресничек, а также обеспечивают сокращение мышц и перемещение внутриклеточных компонентов. В крови человека и многих животных белок гемоглобин переносит кислород и часть углекислого газа, другие белки транспортируют ионы и электроны. Защитная роль белков связа на, в первую очередь, с иммунитетом, поскольку белок интерферон способен уничтожать многие вирусы, а белки-антитела подавляют развитие бактерий и иных чужеродных агентов. Среди бел ков и пептидов немало гормонов, например, гормон поджелудочной железы, инсулин, регули рующий концентрацию глюкозы в крови. У некоторых организмов белки могут откладываться в запас, как у бобовых в семенах, или белки куриного яйца.  2.3.4. Нуклеиновые кислоты. Нуклеиновые кислоты — это биополи меры, мономерами которых являются нуклеотиды. В настоящее время известно два типа нуклеиновых кислот: рибонуклеиновая (РНК) и дезоксирибонуклеиновая (ДНК). Нуклеотид образован азотистым основа нием, остатком сахара-пентозы и остатком ортофосфорной кислоты (рис. 2.19). Особен ности нуклеотидов в основном определяются азотистыми основаниями, входящими в их состав, поэтому даже условно нуклеотиды обозначаются по первым буквам их назва ний.  В состав нуклеотидов могут входить пять азотистых оснований: аденин (А), гуа нин (Г), тимин (Т), урацил (У) и цитозин (Ц). Пентозы нуклеотидов — рибоза и дезоксирибоза — определяют, какой нуклеотид будет образован — рибонуклеотид или дезоксирибонуклеотид. Рибонуклеотиды являются мономерами РНК, могут выступать в качестве сигнальных молекул (цАМФ) и входить в состав макроэргических соединений, например АТФ, и коферментов, таких как НАДФН + Н+, НАДН + Н+, ФАДН2 и др., а дезоксирибонуклеотиды входят в состав ДНК. |
