Практикум Доказательная медицина. Конспект по противопоказаниям к применению следующих препаратов Для этого надо найти в интернете инструкцию по применению, в ней найти противопоказания и записать их
 Скачать 144.05 Kb. Скачать 144.05 Kb.
|
|
Развитие контролируемых исследований в медицине. В 1898 г. И. Фибигер (1867–1928) опубликовал результаты клинического испытания, в ходе которого сравнивались результаты терапии больных дифтерией, распределенных на группы получавших и не получавших сыворотку для лечения [36]. Однако исследование осталось незамеченным. Лишь в 1948 г. были опубликованы результаты изучения эффекта стрептомицина при лечении больных туберкулезом. Именно данное испытание считается первым контролируемым исследованием, соответствующим современным методологическим стандартам рандомизации (случайного распределения) и проведения статистического анализа После Второй мировой войны по мере экономического подъема в различных странах появился целый ряд новых методов лечения заболеваний. Обычно сторонники нового метода аргументировали свою точку зрения только тем, что эффективность его использования вытекает из существующих знаний о механизмах развития болезни, однако впоследствии было показано, что некоторые из этих методов лечения бесполезны. Примером может служить использование антикоагулянтов при инфаркте миокарда. В 50-х годах ХХ в. механизмы свертывания крови привлекли пристальное внимание ученых-медиков, и применение недавно открытых антагонистов витамина К при тромбозе коронарных артерий было признано теоретически оправданным. Более того, данную точку зрения подтверждали результаты клинических исследований, опубликованные в разных странах и свидетельствовавшие об улучшении выживаемости больных, получавших эти препараты. Однако после проведения рандомизированных испытаний стало ясно, что использование антагонистов витамина К при данном заболевании не вызывает положительный эффект Эти и другие подобные наблюдения убедили здравомыслящих медиков, что научный подход необходим не только в экспериментальных исследованиях, но и в клинической практике. Рандомизированные контролируемые испытания приобрели статус «золотого стандарта» исследований, посвященных оценке эффективности лечебных вмешательств. Нельзя преувеличивать значение теорий, пусть даже они выглядят убедительно и научно обоснованно. Необходимо помнить, что человеческий организм необычайно сложен и наши знания о механизмах заболеваний остаются неполными. Поэтому практически никогда нельзя с уверенностью предсказать, каким будет эффект от рационального, казалось бы, лечебного вмешательства Появление концепции доказательной медицины (ДМ) около 10 лет назад стало закономерным в связи с начавшимся лавинно-образным ростом числа научных медицинских публикации. Одновременно медицина стала областью применения высоких технологии, дорогостоящего оборудования и препаратов. Поэтому основной причиной доказательной медицины был сформулирован как добросовестное, точное и осмысленное использование лучших результатов клинических исследований для принятия решений в оказании помощи конкретному пациенту ( Sackett et. Al 1997). Доказательная медицина основывается на трех компонентах: - клиническая экспертиза - результаты исследовании - предпочтение пациента. Работа в ДМ имеет свои специфические стадии: - формулировка четкого клинического вопроса, исходя из специфики пациента. - поиск литературы по проблеме - оценка (критический подход) исследовании на предмет их валидности и полезности. - применение полезных находок в клинической практике. Четыре шага в ДМ: Шаг 1: сформулируйте правильный клинический вопрос Шаг2: найдите самые надежные и актуальные исследования Шаг 3: оцените достоверность и полезность найденной информации. Шаг 4: примените результаты в клинической практике. Понятие о клинической эпидемиологии и медицине, основанной на доказательствах. Главная цель клинической эпидемиологии. Клинические явления, представляющие интерес для клинической эпидемиологии (заболевания, инвалидизация, смерть, неудовлетворенность и т.д.) На рубеже 80-90-х годов ХХ века в англоязычной медицине сформировалась новая область знаний – клиническая эпидемиология. Наибольшую известность получили работы группы Канадских ученых из университета Мак Мастера, Онтарно, которые впервые попытались рассмотреть врачебное искусство с точки зрения строгих научных принципов. К сожалению до последнего времени наши доктора не были знакомы с новой концепцией. Вот почему только сейчас в учебный процесс медицинских ВУЗов вводится курс доказательной медицины для врачей общей практики. Клиническая эпидемиология разрабатывает научные основы врачебной практики – свод правил для принятия клинических решений. Главный постулат клинической эпидемиологии таков: каждое клиническое решение должно базироваться на строго доказательных научных фактах. Этот постулат получил название «evidence – based medicine», что в переводе означает «медицина основанная на фактах» или научно-доказательная медицина. Главная цель клинической эпидемиологии – внедрять практику клинического наблюдения и анализа данных, обеспечивающих принятие верных решений. Клинические явления, представляющие интерес для клинической эпидемиологии – это исходы, имеющие наибольшее значение для больных и для медицинского персонала: - смерть - заболевание - дискомфорт - инвалидизация - неудовлетворенность При внедрении ДМ для оценки эффективности лечения, риска, диагностики и прогноза ставится следующие типы вопросов: 1. Зачем авторы проводили это исследование и какую гипотезу они проверяли? 2. Какого типа проведенное исследование? 3. Адекватен ли лечение изучаемому явлению? Лечение - проверка эффективности лекарственных препаратов, хирургических вмешательств и других видов лечения. Диагностика – выяснение таких параметров нового диагностического метода как достоверность и надежность. Прогноз – определение того, что может вероятно произойти с пациентом у которого болезнь диагностировали на ранних стадиях. Риск – получение возможных осложнении при лечении новым методом. Оценка уровня доказательности является основным рабочим инструментом в доказательной медицине Поэтому важнейшим механизмом, позволяющим врачу ориентироваться в огромном количестве публикуемых медицинских данных, является рейтинговая система оценки научных исследований. Практические рекомендации по диагностике и лечению могут опираться как на данные исследований, так и на их экстраполяцию. С учетом этого обстоятельства рекомендации подразделяют на 3-5 уровней, которые принято обозначать латинскими буквами - A, B, C, D, E. А - доказательства убедительны: есть веские доказательства в пользу применения данного метода; В - относительная убедительность доказательств: есть достаточно доказательств в пользу того, чтобы рекомендовать данное предложение; С - достаточных доказательств нет: имеющихся доказательств недостаточно для вынесения рекомендации, но рекомендации могут быть даны с учетом иных обстоятельств; D - достаточно отрицательных доказательств: имеется достаточно доказательств, чтобы рекомендовать отказаться от применения данного метода в определенной ситуации; Е - веские отрицательные доказательства: имеются достаточно убедительные доказательства, чтобы исключить данный метод из рекомендаций. В большинстве стран Западной Европы и Канаде выделяют три уровня доказательности - A, B, C. Для практических врачей, имеющих самые элементарные представления о клинической эпидемиологии и статистике, вполне приемлемой может быть оценка достоверности доказательств из различных источников по рекомендациям Шведского совета по методологии оценки в здравоохранении, Согласно им достоверность убывает в следующем порядке: • рандомизированное контролируемое клиническое исследование; • нерандомизированное клиническое исследование с одновременным контролем; • нерандомизированное клиническое исследование с историческим контролем; • когортное исследование; • «случай-контроль»; • перекрестное клиническое исследование; • результаты наблюдений. Систематизированные обзоры Рост количества и повышение качества результатов клинических исследований в последние 10 лет играют важную роль в принятии практических решений в повседневной клинической деятельности. Практикующему врачу разобраться в беспрерывном и нарастающем информационном потоке достаточно сложно, существенную помощь в этом ему оказывают систематизированные обзоры по разным проблемам профилактики, диагностики и лечения широкого круга заболеваний. Главное достоинство обзора - объединение информации о нескольких исследованиях, что позволяет получить объективное представление о клиническом эффекте анализируемого вмешательства по сравнению с отдельно взятым клиническим исследованием. Систематизированные обзоры являются одной из наиболее важных составляющих доказательной медицины. Прежде всего для систематизированного обзора отбираются исследования в соответствии с конкретным клиническим вопросом. Главной целью систематизированного обзора является получение ответа на следующие вопросы в доступной для понимания практического врача форме. 1. Действительно ли эффективно анализируемое вмешательство? 2. Насколько эффективнее анализируемое вмешательство по сравнению с плацебо, «традиционной» терапией или по сравнению с другими схожими вмешательствами, применяемыми при конкретной патологии в настоящее время? 3. Насколько безопасно анализируемое вмешательство, в том числе и при сравнении с уже применяющимися вмешательствами? 4. Оправдано ли применение анализируемого вмешательства у конкретного больного с учетом соотношения польза (эффективность)/ риск (безопасность)? 5. Возможна ли замена анализируемого вмешательства на уже применяющееся вмешательство и какие последствия будет иметь такая замена? Результаты систематизированных обзоров, как правило, изобилуют не только цифрами, но специальной терминологией и сокращениями, которые трудно понять и правильно интерпретировать практикующему врачу. Наиболее употребительные в доказательной медицине термины и сокращения приведены в приложении, в настоящее время большинство из них используется уже не только в специальной медицинской литературе, но и во время презентаций на национальных конгрессах и симпозиумах. Одним из наиболее важных понятий является показатель NNT (the number needed to treat; русская аббревиатура ЧБНЛБИ или ЧБНЛ - число больных, которых необходимо лечить определенным методом в течение определенного времени, чтобы достичь определенного эффекта или предотвратить неблагоприятный исход у одного больного). Достоинством этого показателя является возможность его применения в условиях реальной клинической практики обычного врача. Кроме этого, при различных вмешательствах, приводящих к одинаковому результату при одном заболевании, знание величины ЧБНЛ позволяет выбрать оптимальную тактику лечения конкретного пациента ПРИМЕР статистической таблицы с пояснением. таблица. Влияние ИАПФ на смертность в РКИ по профилактике и лечению ХСН 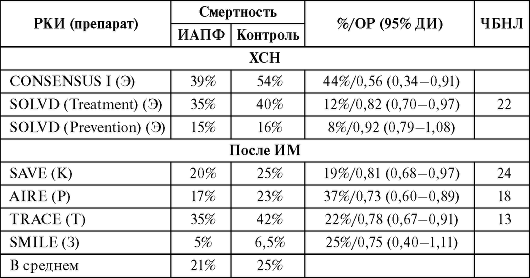 Примечание. Э - эналаприл; К - каптоприл; Р - рамиприл; Т - трандалоприл; З - зофеноприл Примечание. Э - эналаприл; К - каптоприл; Р - рамиприл; Т - трандалоприл; З - зофеноприлПоказатель ЧБНЛ всегда предполагает существование группы сравнения (референтной группы), в которой больные получают плацебо или какое-то другое лечение или вообще не получают его. Показатель ЧБНЛ может быть различным в рамках одного исследования в зависимости от выбранного критерия оценки эффективности вмешательства (чаще всего это «суррогатные» конечные точки, принятые для конкретного заболевания). Противоположным по смыслу является показатель «число больных, которых необходимо лечить определенным методом в течение определенного времени, чтобы вмешательство могло нанести вред одному больному». Особую важность этот показатель приобретает при оценке целесообразности профилактического вмешательства. Знание этого показателя и ЧБНЛБИ позволяет оценить степень риска вмешательства у конкретного пациента. ЧБНЛ для определенного вида вмешательства (чаще всего лечения) является величиной, обратной снижению абсолютного риска при этом вмешательстве. Рассмотрим это на конкретном примере. В результате проведенного исследования было показано, что в результате лечения препаратом Х риск развития одного из характерных осложнений для анализируемого заболевания снизился с 0,5 до 0,3, относительный риск составил 0,20, снижение относительного риска - 0,80, а снижение абсолютного риска - 0,20. Следовательно ЧБНЛ равно 1 : 0,20 = 5. С практической точки зрения это означает, что врачу надо лечить препаратом Х 5 больных, чтобы предотвратить развитие одного осложнения у одного больного. На величину показателя ЧБНЛ существенное влияние оказывает степень снижения абсолютного риска. Простота расчета показателя ЧБНЛ позволяет широко использовать его в качестве основного цифрового показателя эффективности (или потенциального вреда) анализируемого вида вмешательства. Главное преимущество ЧБНЛ состоит в том, что его может использовать любой врач применительно к условиям своей практики. В этой связи становится очень важным понять возможности и пределы использования показателя ЧБНЛ в условиях реальной клинической практики. Особенности показателя: • строго специфичен для определенного вида вмешательства и у конкретной категории пациентов; • описывает различие по клинически важным исходам между группой вмешательства и контрольной группой; • низкий показатель (около 1) означает, что благоприятный исход наблюдается почти у каждого больного, получающего лечение, и лишь у небольшой части больных в группе сравнения; • на практике показатель, равный единице, встречается крайне редко даже при исследовании антибиотиков; • абсолютное значение показателя не является критерием для принятия решения о целесообразности вмешательства, а отражает вероятность достижения положительного эффекта. Так, при сердечной недостаточности эффективность различных, в том числе и официально рекомендованных лечебных вмешательств, колеблется от 20 до более чем 100, но при этом все они используются у этой категории пациентов, потому что считаются эффективными, причем часто одновременно (например, комбинация ИАПФ с β-адреноблокаторами и спиронолактоном). Мета-анализ Одной из разновидностей систематизированных обзоров является мета-анализ. Часто мета-анализ рассматривается как высшая ступень доказательности и становится основой для выбора наиболее эффективных лечебно-профилактических и диагностических вмешательств. Мета-анализ, появившийся в конце 1980-х годов, сегодня относится к одной из самых популярных и быстро развивающихся методик системной интеграции результатов отдельных научных исследований. Например, в Великобритании до 50% всех используемых сегодня методов лечения заболеваний внутренних органов основаны на результатах рандомизированных контролируемых испытаний (РКИ), а также соответствующих мета-анализов. Сегодня мета-анализ - это «объединение результатов различных исследований, складывающееся из качественного компонента (например, использование таких заранее определенных критериев включения в анализ, как полнота данных, отсутствие явных недостатков в организации исследования и т.д.) и количественного компонента (статистическая обработка имеющихся данных)». Целью мета-анализа является оценка эффективности изучаемого вмешательства, а также выявление, изучение и объяснение неоднородности или гетерогенности в результатах исследований и подгруппах пациентов. Он должен представить точечные и интервальные (95% доверительный интервал) оценки обобщенного эффекта вмешательства. Как указывалось выше, в мире ежегодно публикуется более 2,5 миллиона медицинских статей, не считая материалов многочисленных национальных и международных конференций, книг. Естественно, в этой ситуации велика потребность в анализе и синтезе имеющейся информации. Примеров расхождения результатов описательного обзора литературы и ее метаанализа очень много (публикация вывода лауреата Нобелевской премии профессора Л. Полинга о снижении заболеваемости простудой в результате применения аскорбиновой кислоты, эффективность антиоксидантов в профилактике сердечно-сосудистой патологии, целесообразность профилактики нарушений ритма с использованием лидокаина в остром периоде инфаркта миокарда, возможность снижения риска сердечно-сосудистой патологии у женщин на фоне заместительной гормональной терапии). Ни один из этих выводов впоследствии не был подтвержден результатами соответствующих мета-анализов. В то же время кумулятивный мета-анализ 33 клинических исследований мог еще в 1973 г. (почти за 20 лет до широкого внедрения в практику внутривенного тромболизиса) сделать рутинной практику введения стрептокиназы при остром инфаркте миокарда. Однако существуют и противоположные примеры. В качестве одного из них можно привести дискуссию середины 1990-х годов прошлого века о целесообразности и безопасности применения антагонистов кальция при артериальной гипертензии. По данным двух мета-анализов было показано их негативное влияние на риск развития инфаркта миокарда, но последующие крупные исследования ALLHAT и ASCOT полностью опровергли эти опасения, также как и новый мета-анализ BPTLC. В целом мета-анализ позволяет более точно, чем результаты отдельно взятого клинического исследования, определить категории больных, у которых применимы полученные результаты. На основании результатов мета-анализа часто принимаются не только лечебно-диагностические, но и управленческие решения (например, развертывание специализированных инсультных отделений, снижающих риск смертности и тяжелой инвалидизации более чем на треть). Интересно, что ни в одном из более чем 10 рандомизированных клинических исследований преимущества специализированных отделений не были доказаны. Постоянно обновляемые мета-анализы позволяют существенно сократить время между научным открытием и широким внедрением его результатов в практику здравоохранения. В качестве примера можно привести результаты мета-анализа по применению β-адреноблокаторов при артериальной гипертензии, которые существенно сузили показания для их назначения у этой категории пациентов. |
