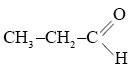конспект. Конспект урока по теме. Конспект урока по теме Альдегиды и кетоны
 Скачать 183.5 Kb. Скачать 183.5 Kb.
|
|
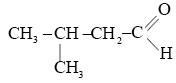
Конспект урока по теме: Альдегиды и кетоны» к учебнику О.С. Габриеляна Химия 10 класс Тип урока: изучение нового материала Цели: образовательные: учащиеся должны рассмотреть строение молекул альдегидов и кетонов, их номенклатуру и виды изомерии. Изучить особенности строения карбонильной группы Изучить химические свойства альдегидов. Рассмотреть способы получения альдегидов и кетонов развивающие: учащиеся должны сформировать умения использовать химическую терминологию совершенствовать умения обобщать, делать выводы, анализировать, сравнивать, устанавливать причинно-следственную зависимость между составом, строением и свойствами веществ. воспитательные: учащиеся должны убедиться на примере генетической связи органических веществ разных гомологических рядов о единстве материального мира совершенствовать информационно- познавательную компетенцию Методы и методические приемы: объяснение нового материала с демонстрацией опытов Знать: строение молекул альдегидов и кетонов, их функциональные группы; сходство и различие в свойствах альдегидов и кетонов; о токсичности действия альдегидов и кетонов на живые организмы. Уметь: составлять структурные формулы альдегидов и кетонов; называть альдегиды по рациональной и систематической номенклатуре; составлять уравнения реакций, характеризующих свойства альдегидов. Межпредметные и внутрипредметные связи: биология химия (О.С. Габриелян Тема: Спирты §17 стр. 138). Оборудование и реактивы: Карточки «Алгоритм составления названий кетонов / альдегидов», «Химические свойства альдегидов и кетонов» О.С. Габриелян учебник по химии 10 класс Для ДО: раствор AgNO3, раствор NaOH, раствор NH4OH, формальдегид, спиртовка, раствор CuSO4, штатив с пробирками Впервые с альдегидами вы познакомились в 9 классе и упоминали их пр изучении спиртов, когда при окислении первичного спирта вы получили альдегид. C2 Изучать данный класс соединений мы будем по следующему плану: Определение Классификация Номенклатура и изомерия Физические свойства Химические свойства Способы получения Альдегиды Кетоны В соответствии с номенклатурой названия предельных альдегидов образуются из названия алкана с тем же числом атомов углерода в молекуле с помощью суффикса – аль. Перед вами алгоритм составления названий, для альдегидов и кетонов. Алгоритм составления названий альдегидов Найдите главную углеродную цепь - это самая длинная цепь атомов углерода, включающая атом углерода альдегидной группы. Пронумеруйте атомы углерода в главной цепи, начиная с атома углерода альдегидной группы. Назовите соединение по алгоритму для углеводородов. В конце названия допишите суффикс -аль. Алгоритм составления названий кетонов 1. Пронумеровать самую длинную углеродную цепь, начиная с того конца, где ближе карбонильная группа. 2. Указать положение радикала и его название. 3. Назвать углеводород. 4. Принадлежность к классу кетоны указать суффиксом он . 5. Указать положение функциональной группы Кроме систематического названия у альдегидов и кетонов также есть тривиальные названия. Запишем самые основные: HCHO метаналь (формальдегид, муравьиный альдегид) CH3CHO этаналь (ацетальдегид, уксусный альдегид) CH3CH2CHO пропаналь (пропионовый альдегид) CH3CH2CH2CHO бутаналь (масляный альдегид) CH3—CO—CH3 пропанон (ацетон) CH3—CO—CH2CH3 бутанон (метилэтилкетон) Для альдегидов характерна только изомерия углеродного скелета, которая возможно с бутаналя. Кетоны: - изомерия углеродного скелета - изомерия положения карбонильной группы - межклассовая изомерия (пропаналь и пропанон) Физические свойства На них мы останавливаться не будем, скажу лишь, что между молекулами у альдегидов не возникают водородные связи, метаналь – газ (далее жидкости, высшие альдегиды – твердые). Температура кипения у альдегидов ниже, чем у спиртов. Низшие альдегиды хорошо растворяются в воде, так как образуются водородные связи между «Н» воды и «О» альдегида. Химические свойства Реакции присоединения Гидрирование (восстановление) HCHO + H2 CH3—CO—CH3 + H2 Альдегид – первичный спирт Кетон – вторичный спирт Присоединение циановодорода CH3COH + HCN = CH3CHC(OH)N Присоединение NaHSO3 – эта реакция позволяет не только обнаружить альдегиды, но и выделить их из смеси с другими веществами. CH3COH + NaHSO3 = CH3CH(OH)SO3Na Реакцииокисления реакция «серебряного зеркала» Прежде чем записать данную реакцию, давайте проведем опыт и получим сами зеркало. Для этого нам понадобится 4-5 мл AgNO3, 2-3 капли NaOH, 5-8 капель NH4OH, формальдегид, нагреем немного данную смесь. Что мы заметили? Запишем уравнение реакции CH3CHO + Ag2O реакция взаимодействия с Cu(OH)2, качественная реакиця на альдегиды. Проведем опыт, взяв 2-3 капли CuSO4, 2- 3 капли NaOH и формальдегид, подогреем данную смесь. Что можно наблюдать? (осадок кирпично – красного цвета, медь восстанавливается в одноокись меди) Запишем реакцию HCHO + 2Cu(OH)2 Реакция полимеризации и поликонденсации 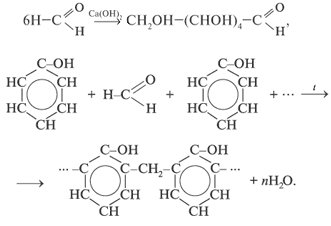 Получение Окисление спиртов Первичных CH3OH + CuO Вторичных CH3—CH(OH)—CH3 + [O] Дегидрирование спиртов (отщепление водорода) Первичных CH3CH2OH Вторичных CH3—CH(OH)—CH3 реакция Кучерова (гидратация ацителена) C2H2 + H2O гидролиз дигалогенпроизводных CH3CHCl2 + 2NaOH = CH3COH + NaCl + H2O На этом наша лекция окончена. А теперь я предлагаю вам выполнить ряд заданий: №1
№2 Какой объем формальдегда необходимо подвергнуть гидрированию для получения 16 г метилового спирта? №3 Напишите структурные формулы следующих соединений: 2- хлорпропаналь 4 – метилпентаналь 2,3 – диметилбутаналь 3 – гидрокси – 4 – метилгексаналь Домашнее задание: §11 упр. 6,7 + сообщение на тему: Применение альдегидов в быту», «Интересные факты из истории альдегидов». Список литературы: В.Г. Денисов Химия для учащихся 11 классов и поступающих в вузы. Тренажеры и тесты - Волгоград, 2007 Егоров А.С. Химия: современный курс для подготовки к ЕГЭ – изд.8-е, Ростов: Феникс, 2009 – 711 с. Химия для любознательных 2-е издание – Л.: Химия, 1985 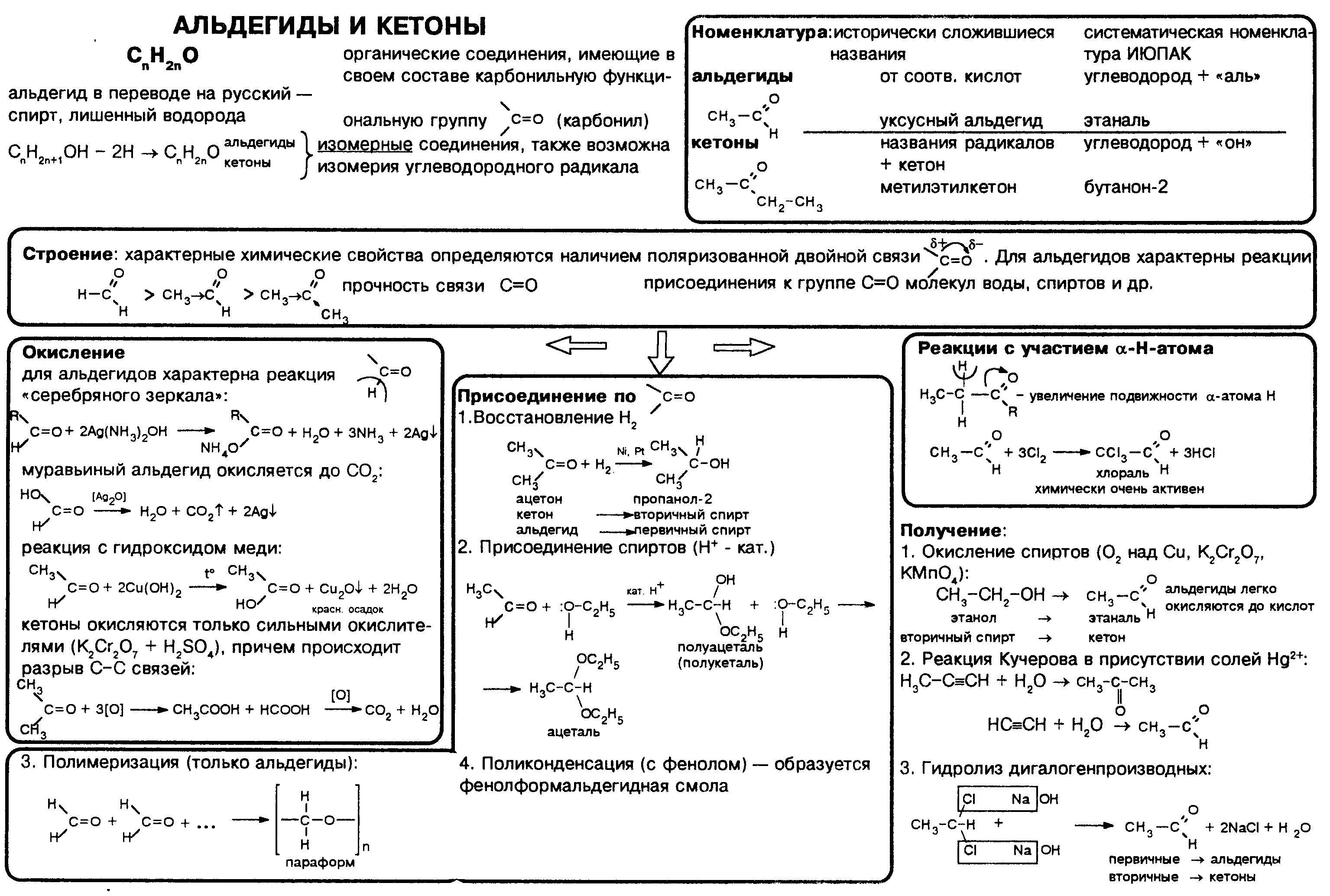 |