Исследование диода. Контрольная работа 1 Вариант 86 Содержание Вопрос 4
 Скачать 329.57 Kb. Скачать 329.57 Kb.
|
|
Контрольная работа №1 Вариант 86 Содержание: Вопрос: 4 Идеальная кристаллическая решетка представляет собой многократное повторение элементарных кристаллических ячеек. Для реального металла характерно наличие большого количества дефектов строения, нарушающих периодичность расположения атомов в кристаллической решетке. Эти дефекты оказывают существенное влияние на свойства материала. 4 Различают три типа дефектов кристаллического строения: точечные, линейные и поверхностные. 4 Точечные дефекты 4 Точечные дефекты характеризуются малыми размерами во всех трех измерениях. Величина их не превышает нескольких атомных диаметров. К точечным дефектам относятся: а) свободные места в узлах кристаллической решетки — вакансии (дефекты Шоттки); б) атомы, сместившиеся из узлов кристаллической решетки в межузельные промежутки — дислоцированные атомы (дефекты Френкеля); в) атомы других элементов, находящиеся как в узлах, так и в междоузлиях кристаллической решетки — примесные атомы. 4 Точечные дефекты образуются в процессе кристаллизации под воздействием тепловых, механических, электрических воздействий, а также при облучении нейтронами, электронами, рентгеновскими лучами. 4 Вакансии и дислоцированные атомы могут появляться вследствие тепловых движений атомов. В характерных для металлов решетках энергия образования дислоцированных атомов значительно больше энергии образования тепловых вакансий. Поэтому основными точечными дефектами в металлах являются тепловые вакансии. При комнатной температуре концентрация вакансий сравнительно невелика и составляет около 1 на 1018 атомов, но резко повышается при нагреве, особенно вблизи температуры плавления. Точечные дефекты не закреплены в определенных объемах металла, они непрерывно перемещаются в кристаллической решетке в результате диффузии. 4 Присутствие вакансий объясняет возможность диффузии — перемещения атомов на расстояния, превышающие средние межатомные расстояния для данного металла. Перемещение атомов осуществляется путем обмена местами с вакансиями. Различают самодиффузию и гетеродиффузию. В первом случае перемещения атомов не изменяют их концентрацию в отдельных объемах, во втором — сопровождаются изменением концентрации. Гетеродиффузия характерна для сплавов с повышенным содержанием примесей. 4 Точечные дефекты приводят к локальным изменениям межатомных расстояний и, следовательно, к искажениям кристаллической решетки. При этом увеличивается сопротивление решетки дальнейшему смещению атомов, что способствует некоторому упрочнению кристаллов и повышает их электросопротивление. 5 Вакансии, дислоцированные атомы и другие точечные дефекты обнаружены при исследовании металлов с помощью автоионного микроскопа, дающего увеличение свыше 106 раз. 5 Задача 6 Литература: 9 Вопрос:Какие дефекты строения кристаллов относятся к точечным? Опишите их сущность Ответ: Идеальная кристаллическая решетка представляет собой многократное повторение элементарных кристаллических ячеек. Для реального металла характерно наличие большого количества дефектов строения, нарушающих периодичность расположения атомов в кристаллической решетке. Эти дефекты оказывают существенное влияние на свойства материала. Различают три типа дефектов кристаллического строения: точечные, линейные и поверхностные. Точечные дефекты Точечные дефекты характеризуются малыми размерами во всех трех измерениях. Величина их не превышает нескольких атомных диаметров. К точечным дефектам относятся: а) свободные места в узлах кристаллической решетки — вакансии (дефекты Шоттки); б) атомы, сместившиеся из узлов кристаллической решетки в межузельные промежутки — дислоцированные атомы (дефекты Френкеля); в) атомы других элементов, находящиеся как в узлах, так и в междоузлиях кристаллической решетки — примесные атомы. Точечные дефекты образуются в процессе кристаллизации под воздействием тепловых, механических, электрических воздействий, а также при облучении нейтронами, электронами, рентгеновскими лучами. Вакансии и дислоцированные атомы могут появляться вследствие тепловых движений атомов. В характерных для металлов решетках энергия образования дислоцированных атомов значительно больше энергии образования тепловых вакансий. Поэтому основными точечными дефектами в металлах являются тепловые вакансии. При комнатной температуре концентрация вакансий сравнительно невелика и составляет около 1 на 1018 атомов, но резко повышается при нагреве, особенно вблизи температуры плавления. Точечные дефекты не закреплены в определенных объемах металла, они непрерывно перемещаются в кристаллической решетке в результате диффузии. Присутствие вакансий объясняет возможность диффузии — перемещения атомов на расстояния, превышающие средние межатомные расстояния для данного металла. Перемещение атомов осуществляется путем обмена местами с вакансиями. Различают самодиффузию и гетеродиффузию. В первом случае перемещения атомов не изменяют их концентрацию в отдельных объемах, во втором — сопровождаются изменением концентрации. Гетеродиффузия характерна для сплавов с повышенным содержанием примесей. Точечные дефекты приводят к локальным изменениям межатомных расстояний и, следовательно, к искажениям кристаллической решетки. При этом увеличивается сопротивление решетки дальнейшему смещению атомов, что способствует некоторому упрочнению кристаллов и повышает их электросопротивление. Вакансии, дислоцированные атомы и другие точечные дефекты обнаружены при исследовании металлов с помощью автоионного микроскопа, дающего увеличение свыше 106 раз. ЗадачаИсходные данные: Количество углерода в исследуемом сплаве – 0,8% Температура 650 0С На рисунке 1 показана диаграмма Fe-Fe3C и кривая охлаждения исследуемого сплава. С п л а в – эвтектоидная сталь (С = 0,8 %). Кристаллизация сплава начинается при температуре, соответствующей точке 1, и заканчивается в точке 2 с образованием аустенита. До температуры критической точки S (727 °С) сталь не претерпевает никаких фазовых превращений. При температуре 727 °С (точка S) во всем объеме аустенита начинается эвтектоидное превращение, которое подчиняется общим законам кристаллизации и происходит путем образования центров кристаллизации феррита и цементита с последующим ростом кристаллов этих фаз. В связи с тем, что углерод в аустените распределен неравномерно (наличие флуктуаций), появление центров кристаллизации существенно облегчается. При этом ведущей фазой при превращении является цементит, зародыши которого возникают по границам зерен аустенита. Зародыши зерен цементита растут в форме тонких пластин, направленных вглубь зерен аустенита. Для роста пластинки цементита необходимо, чтобы к ней диффундировал углерод из соседних участков. В результате аустенит, расположенный около пластинки, обедняется углеродом, перестраивается решетка (Feg ↔ Fea), и в результате этого создаются условия для образования феррита. Следовательно, по обе стороны пластинки цементита растут пластинки феррита (рис. 1 а).  Рис. 1. Схема образования перлита: а – образование первого зерна; б – образование следующего зерна Рост пластинки феррита ввиду малой растворимости в ней углерода приводит к вытеснению излишков последнего в соседние участки аустенита, где образуется новая пластинка цементита. Семейство пластинок феррита и цементита составляет зерно перлита. Граница зерна перлита сама становится поверхностью, от которой начинается формирование второго зерна (рис. 1, б). Значит, в пределах одного аустенитного зерна могут образовываться несколько перлитных зерен.
П(Ф + ЦII). Структура перлита приведена на рис. 2, из которого видно пластинчатое строение смеси феррита и цементита. Толщина пластинок феррита и цементита не одинакова. Пластинки феррита толще пластинок цементита в среднем в 7,5 раз. Очень важной характеристикой перлита служит межпластинчатое расстояние, которое равно суммарной толщине соседних пластин феррита и цементита или расстоянию между ближайшими пластинками одной фазы. При медленном охлаждении образуется крупнопластинчатый перлит с межпластинчатым расстоянием 0,5…1,0 мкм. При увеличении скорости охлаждения образуется более тонкопластинчатый перлит. С уменьшением толщины пластин феррита и цементита увеличиваются твердость и прочность стали. Изменяя скорость охлаждения, можно получать перлит разной дисперсности, регулируя свойства стали в широком диапазоне. В точке заданной температуры химический состав сплава состоит из: 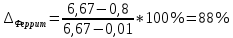 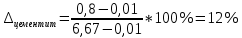 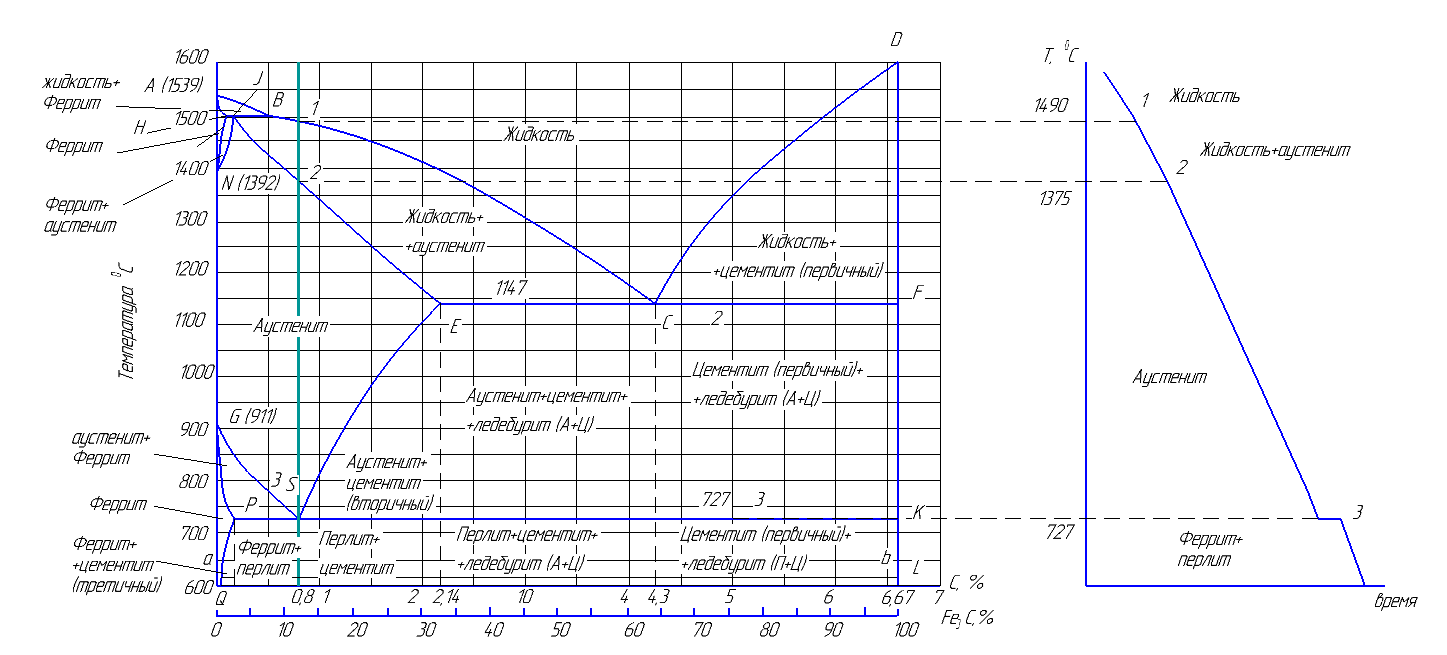 Рис. 3. диаграмма Fe-Fe3C и кривая охлаждения исследуемого сплава Литература:1. Материаловедение и технология конструкционных материалов: практикум/ Э.Г. Бабенко [и др.] Хабаровск: Изд-во ДВГУПС. 2012 – 160 с.: ил. 2. Конструкционные материалы для деталей технических устройств железнодорожного транспорта: учеб. пособие / Э.Г. Бабенко - Хабаровск: Изд-во ДВГУПС. 2014 – 223 с.: ил. |