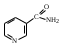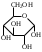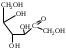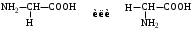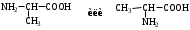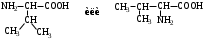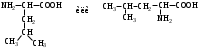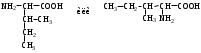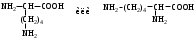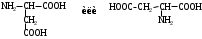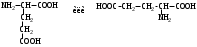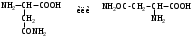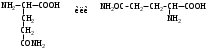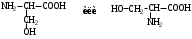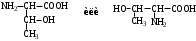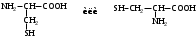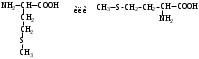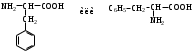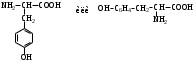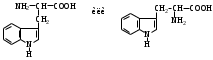Краткая теория. Краткая теория для подготовки к экзамену. (Более подробно можно посмотреть из раздела эиос в лекционном блоке)
 Скачать 1.47 Mb. Скачать 1.47 Mb.
|
|
ФОРМУЛЫ
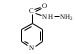
Г  ЕТЕРОЦИКЛЫ ЕТЕРОЦИКЛЫ
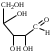
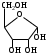
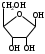
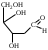
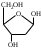
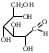
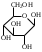
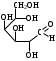
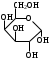
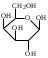
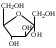
У 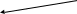  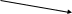 ГЛЕВОДЫ ГЛЕВОДЫмоносахариды олигосахариды полисахариды альдопентоза восстанавливающие гомополисахариды рибоза лактоза (-галактоза+-глюкоза) декстран дезоксирибоза мальтоза (-глюкоза+-глюкоза) гликоген ксилоза целлобиоза (-глюкоза+-глюкоза) целлюлоза альдогексоза крахмал (амилоза+ манноза невосстанавливающие амилопектин) глюкоза сахароза (-глюкоза+-фруктоза) галактоза гетерополисахариды кетогексоза фруктоза  Т    ипы гликозидных связей: ипы гликозидных связей: О О лактоза (14) мальтоза (14) целлобиоза (14) сахароза (12) амилоза (14) амилопектин (14) и (16) гликоген (14) и (16) д  екстран (16) екстран (16)  О О Циклы: пиранозный фуранозный номерация Р  еакции: восстановление СН2ОН еакции: восстановление СН2ОНо  кисление: СООН кисление: СООНкачественная для крахмала (амилозы): синее окрашивание с йодом ц 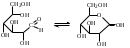 икло-оксо-таутомерия: икло-оксо-таутомерия: (для моносахаридов и дисахаридов, кроме сахарозы) В природе встречаются D-изомеры Принадлежность к D или L ряду определяется по последнему хиральному центру. У глюкозы – это у С5 углерода, у рибозы – С4 углерод.
АМИНОКИСЛОТЫ
НЕЗАМЕНИМЫЕ: Только Врач И Фармацевт Могут Лечить Людей Таблетками (кроме тирозина) Кислотная аминокислота (рН<7) -СООН групп больше, чем -NH2 Основная аминокислота (рН>7) -NH2 групп больше, чем -СООН Нейтральная аминокислота (рН=7) -СООН групп и -NH2 групп одинаковое кол-во В составе белков присутствуют -аминокислоты (NH2 и СООН группы у одного и того же углерода) классификация по радикалу   гидрофобные гидрофильные (   радикал состоит только из С и Н) (в радикале есть О, N,S) радикал состоит только из С и Н) (в радикале есть О, N,S)валин, аланин незаряженные заряженные (в радикале нет СООН или NН2) (есть СООН или NН2) серин, цистеин лизин Реакции: декарбоксилирование (отщепление СО2 от карбоксильной группы) гистидин гистамин триптофан триптамин трансаминирование (получение заменимых аминокислот) качественные реакции: -аминокислоты – нингидриновая пептидная связь – биуретовая В природе встречаются L-аминокислоты. Dи L-форм не имеет глицин, так как у него нет хирального центра. Число стереоизомеров определяется как 2n, где n – число хиральных центров. Для -аминокислот, как правило 2 стереоизомера, так как имеется 1 хиральный центр. Аминокислоты при связывании образуют пептиды: 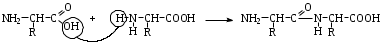 При этом образуется пептидная связь. 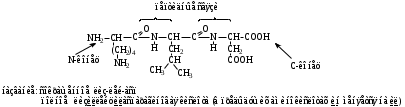 Белки – это полипептиды: Первичная структура белка (линейная) образуется за счет пептидных связей. Вторичная структура белка (спираль) образуется за счет водородных связей Третичная структура белка (глобула) стабилизируется за счет водородных, ионных, гидрофобных, дисульфидных, межмолекулярных взаимодействий. Четвертичная структура (несколько глобул), например гемоглобин – 4 глобулы. Дисульфидные мостики может образовать аминокислота цистеин НУКЛЕИНОВЫЕ КИСЛОТЫ Нуклеиновые кислоты (полинуклеотиды)  нуклеотид щелочной гидролиз   Фосфорная кислота Нуклеозид или соль (NaH2PO4) кислотный гидролиз   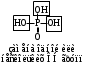 углевод нуклеиновое основание 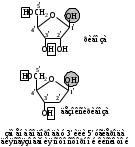 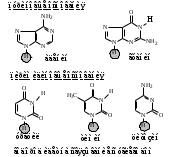 л 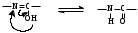 актим-лактамная таутомерия актим-лактамная таутомерияКомплементарные пары: А-Т (или А-У) и Г-Ц РНК состоит из остатка фосфорной кислоты, рибозы и АЦГУ ДНК состоит из остатка фосфорной кислоты, дезоксирибозы и АЦГТ Рибонуклеозиды: аденозин, гуанозин, цитидин и уридин Дезоксирибонуклеозиды: дезоксиаденозин, дезоксигуанозин, дезоксицитидин, тимидин Нуклеозиды гидролизуются только в кислой среде, как и олигосахариды и полисахариды. 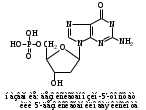 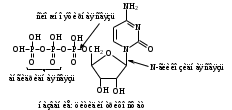 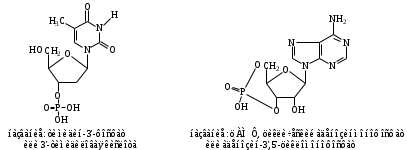 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

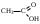
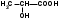
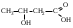
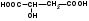
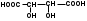

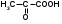
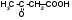
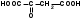
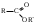
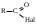 Hal – это Cl, Br, J
Hal – это Cl, Br, J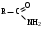
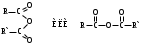
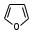 фуран
фуран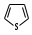 тиофен
тиофен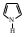 пиррол
пиррол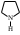 пирролидин
пирролидин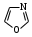 оксазол
оксазол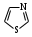 тиазол
тиазол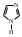 имидазол
имидазол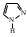 пиразол
пиразол пиридин
пиридин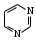 пиримидин
пиримидин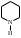 пиперидин
пиперидин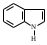 индол
индол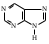 пурин
пурин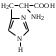
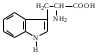
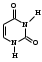
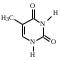
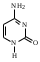
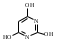
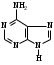
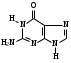
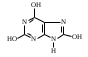
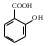

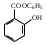
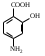 пара-аминосалициловая кислота
пара-аминосалициловая кислота