|
|
фармхим. Курсовая работа на тему
Министерство здравоохранения Украины
Запорожский государственный медицинский университет
Кафедра фармацевтической химии
Курсовая работа
на тему:
“Лекарственные препараты производные триазола: тиотриазолин. Производные имидазола: клонидина гидрохлорид (клофелин). Методы качественного и количественного определения. Применение в медицине”
Выполнила:
студентка III курса 1группы
фармацевтического факультета
Ярощук Ольга Михайловна
Проверил:
Ac. Антипенко Л.Н.
Запорожье – 2012
Оглавление
Введение…………………………………………………………………….…3
Производные имидазола………………………………...…………………....4
Получение имидазола……………………………...………………….4
Химические свойства имидазола……………………………………..4
Клофелин……………………………………………………………….6
Получение………………………………………..………………….6
Идентификация…………………………………..…………………7
Количественное определение……………………..……………….8
Применение…………………………………………..……………..9
Производные триазола…………………………………………..…………...9
Получение триазола……………………………………….………....10
Тиотриазолин……………………………………………….………...11
Получение………………………………………………...………..11
Идентификация и количественное определение………………..12
Применение………………………………..……………...……….12
Выводы……………………………………………………………………….14
Список литературы………………………………………………………….15
ВВЕДЕНИЕ
Имидазол и триазол – пятичленные гетероциклы с двумя гетероатомами. У имидазола два атома азота, а у триазола – три атома азота. Значение производных имидазола и триазола очень велико. На их основе изготовлены препараты, применяющиеся для лечения многих заболеваний, в том числе и онкологических. Имидазольное ядро входит в состав таких важных для человека веществ, как азотистые основания, витамины, ферменты, аминокислоты.
Цель данной курсовой работы – показать важность этих двух соединений, обобщив материал из разных отраслей науки (химия, фармакология, медицина), применение производных этих веществ в лечебной практике и повседневной жизни.
ПРОИЗВОДНЫЕ ИМИДАЗОЛА
ПОЛУЧЕНИЕ ИМИДАЗОЛА
Имидазол получают конденсацией глиоксаля с аммиаком в присутствии формальдегида:

Производные имидазола получают аналогично, действую аммиаком и формальдегидов на производные глиоксаля:
 [5] [5]
ХИМИЧЕСКИЕ СВОЙСТВА ИМИДАЗОЛА:
Имидазол – более сильное основание, чем пиррол. Амфотерность приводит к тому, что его участие в той или иной реакции зависит от среды: в кислой среде кольцо заряжается положительно, в щелочной – отрицательно.

Реакции электрофильного замещения протекают либо по атомам азота, либо по атомам углерода, но наиболее предпочтителен первый вариант.
Такой механизм реакции требует наименьшие энергетические затраты.
Производные имидазола могут вступать в реакцию с галоидным алкилом с образованием солей:


Однако помимо реакций электрофильного замещения молекула имидазола может вступать и в реакции нуклеофильного замещения:

Для имидазола возможны и специфические реакции: металлирование и карбоксилирование:


Имидазол также может вступать в конденсацию с альдегидами:  [1] [1]
ФЕНИЛМИМДАЗОЛИЛЭТИЛЕН
Клонидина гидрохлорид (клофелин)
Clonidini hydrochloridum

Клофелин или 2-(2,6-дихлорфениламино)-имидазолина гидрохлорид. Другие названия: Гемитон, Катапресан.[2]
Это белый или почти белый кристаллический порошок. Растворим в воде, спирте 96%, практически нерастворим в хлороформе. [3]
Получение клофелина
В последние годы были получены новые препараты, производные имидазола (этимизол) и имидазолина (клофелин). Заслуга в создании клофелина пренадлежит Р.Г. Глушкову,В.Г.Гранику (ВНИХФИ). Этот оригинальный метод синтеза клофелина основан на использовании в качестве исходного продукта тетраметилтиурамдисульфида (рис.1): [5]
 Рис.1 Схема Рис.1 Схема
Определение подлинности.
ЛС должно отвечать требованиям по специфическому удельному вращению (поляриметрия). Подлиность определяют ИК-спектрометрический и методом ТСХ, используя стандартный образец. Цветная реакция – образование окрашенных комплексов пероксида хрома(VI) (фиолетовая окраска в метиленхлориде). Кроме того, водный раствор препарата дает реакцию на хлориды.
В основе оценки подлинности, испытаний на чистоту и количественного определения лежат химические свойства ЛВ рассматриваемой группы.
Клофелин, в отличии от других препаратов этой группы, является гидрохлоридом, поэтому дает положительную реакцию на хлориды [7].
Кислотно-основные свойства. Как уже отмечалось выше, все производные имидазола являются слабыми монокислотными основаниями. Реакцией с более сильными основаниями в водных растворах солей можно выделить основные формы ЛВ, которые мало растворимы и имеют характерные температуры плавления. По ней определяют подлинность клофелина.[6]
Как производные азотистых оснований препараты имидазола взаимодействуют с общеалкалоидным осадительным реактивом – пикриноврй кислотой. Для идентификации ЛВ применяют определение температуры плавления образующихся пикратов.
Реакции комплексообразования. Для идентификации препаратов имидазола используют также реакцию с нитропруссидом натрия (динатриевая соль пентацианонитрозилферрата (II) – Na2[Fe(CN)5NO]). При этом образуются устойчивые окрашенные продукты (красного и красно-фиолетового цветов).[5]
Испытания на чистоту.
Водный раствор (2,50г в 50мл Н2О) имеет рН=3,5 – 4,5, прозрачен, его окраска не превышает по интенсивности окраску стандартного образца, чем окраску раствора СО.
Родственные примеси (изопилокарпин, пилокарпиновая кислота) определяют методом жидкостной хроматографии. Содержание железа на должно превышать 10 мкг/г; сульфатная зола <0,1%.[3]
Количественное определение
Основные свойства ЛВ рассматриваемой группы используют для их количественного определения методом титрования в неводных средах. В качестве профильного растворителя используют ледяную уксусную кислоту. Титрантом является хлорная кислота. Для связывания хлорид-иона добавляют ацетат ртути (II) Hg(CH3COO)2. Количественное определение клофелина проводят в присуцтвии уксусного ангидрида с добавлением муравьиной кислоты. Этот метод используется при промышленной стандартизации (рис.2).

Рис.2 Схема количественного определения клофелина
Определение клофелина и пилокарпина при внутриаптечном контроле проводят алкалиметрическим методом. В качестве титранта применяют раствор NaOH, индикатором служит фенолфталеин. Титрование проводят в присутствии хлороформа, в который экстрагируется образующееся основание. Таким образом, удается предотвратить реакцию гидролитического расщепления ЛВ.[7]
Применение клофелина
Клофелин является хорошим α-адреноблокирующим средством, поэтому его назначают в качестве антигипертензивного средства при различных формах гипертонии, а в глазной практике – для лечения глаукомы. Клофелин оказывает выраженное гипотензивное действие; снижает артериальное давление. Препарат оказывает выраженный обезболивающий и седативный, успокаивающий эффект, уменьшает чувство страха, снижает внутриглазное давление.[2]
ПРОИЗВОДНЫЕ ТРИАЗОЛА
Триазолы - органические соединения класса гетероциклов, пятичленный цикл с тремя атомами азота и двумя атомами углерода в цикле.
Изомерия
Существует два изомерных триазола: 1,2,3-триазол (вицинальный триазол, озотриазол - формула Ia, Ib) и 1,2,4-триазол (симметричный триазол, пирродиазол - формула IIa, IIb). Незамещённые или C-замещённые триазолы могут существовать в двух таутомерных формах.[4]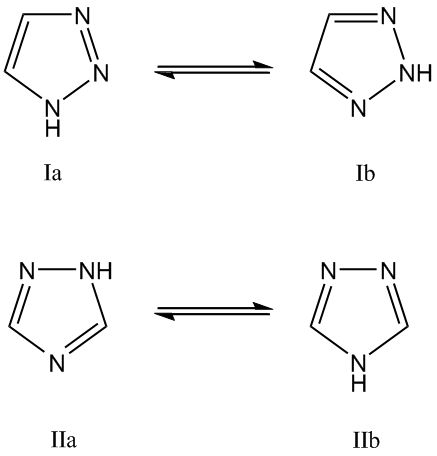
Триазолы и их алкил- или арилпроизводные представляю собой бесцветные кристаллы или высококипящие жидкости. Хорошо растворимы в большинстве органических растворителей; незамещённые триазолы растворимы в воде. Проявляют кислотные и слабые основные свойства.
Триазолы относятся к 6π-электронным ароматическим системам. Вступают в реакции электрофильного замещения по атомам углерода или азота. Наиболее характерны реакции алкилирования и ацилирования. 1,2,3-триазол и его 1-замещенные гомологи алкилируются акилгалогенидами, диметилсульфатом, диазометаном, вступают в реакцию Манниха.
В щелочной среде 1,2,4-триазолы алкилируются до 1-алкилпроизводных и с дальнейшим образованием четвертичных солей по атому N-4.
В кислой среде электрофильное замещение триазолов не происходит, так как они в кислой среде превращаются в неактивные триазолиевые катионы.
Устойчивы к нагреванию, действию кислот и оснований, некоторых окислителей (KMnO4, H2O2) и восстановителей (Zn в CH3COOH, Na в NH3, LiAlH4).[1]
ПОЛУЧЕНИЕ ТРИАЗОЛА
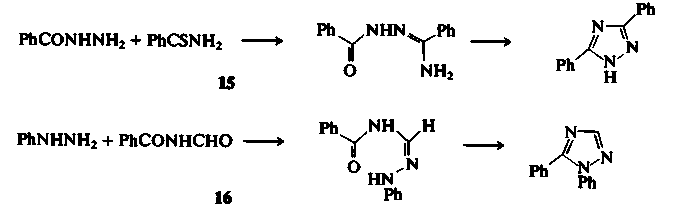
Существует много удобных методов синтеза 1,2,4-триазолов, наиболее важные из которых основаны на создании и циклизации структур типа N—С—N—N—С и С—N—С—N—N. В качестве примера первого типа можно привести термическую конденсацию ацилгидразида с амидом или (что лучше) с тиоамидом (реакция Пеллиццари); так, бензоилгидразид вступает в реакцию с тиобенза-мидом при 140 °С с образованием 3,5-дифенил-1,2,4-триазола (15). Примером второго типа циклизации служит реакция Эйнхорна — Бруннера, в которой гидразин или монозамещенный гидразин конденсируется с диациламином в присутствии слабой кислоты. Так, при взаимодействии фенилгидразина и N-формальбензамида образуется с хорошим выходом 1,5-дифенил-1,2,4-триазол(16).(рис.3) [10]
 [11] [11]
Рис.3 Схема получения триазола
Производные 1,2,3-триазола применяют в качестве оптических отбеливателей. Триазолы имеют важное значение в медицинской химии, так как N-незамещенные триазолы можно рассматривать как аналоги карбоновых кислот: величины их рК, сравнимы , и они представляют собой плоские, делокализованные системы с примерно такими же пространственными требованиями.[9]
Тиотриазолин Тhiotriazolin

Морфолиния 3-метил-1,2,4-триазолил-5-тиоацетат [8]
Кристалический порошок белого или белого с сероватым или желтоватым оттенком, со слабым специфическим запахом. Легко растворим в воде, умеренно растворим в 96%-ом спирте, практически не растворим в ацетоне, гексане и хлороформе.
Получение тиотриазолина проводят по схеме(рис.4):

5-меркапто-3-метил-1,2,4триазол 3-метил-1,2,4-триазолил-5-тиоуксусная к-та

Рис.4
Идентификация:
По физико-химическим показателям: температура плавления (от 147о С до 152оС, ИК-спектроскопия.
При нагревании субстанции к расплавления и закипания выделяются пары, от которых влажная лакмусовая бумага синеет.
В парах вещества при нагревании наблюдается побурение полоски фильтровальной бумаги, пропитанной раствором свинца(II) ацетатом.
При нагревании вещества с п-диметиламинобензальдегидом и смесью уксусного ангидрида и кислоты уксусной ледяной (1:4) появляется оранжево-коричневое окрашивание.[8]
Количественное определение
Ацидиметрия в неводной среде, прямое титрование с параллельным проведениям контрольного опыта, s=1/2 (рис.5)

Рис.5
Применение тиотриазолина
В лекарственных формах (таблетки, инъекционные растворы, мази, глазные капли), а также в комбинированных лекарственных формах (тиацетам, индотрил, тиодарон) тиотриазолин определяют с помощью спектрофотометрии при длине волны 232нм или хроматографически.
Показания:
хронический гепатит различной этиологии, цирроз печени; ИБС: острый мелко- или крупноочаговый инфаркт миокарда, стенокардия напряжения и покоя, постинфарктный кардиосклероз, нарушения ритма сердца.
Тиотриазолин, как кардиопротектор, можно комбинировать с препаратами для лечения ишемической болезни сердца, как гепатопротектор - сочетать с традиционными препаратами для лечения заболеваний печенки.[2]
Выводы
В данной курсовой удалось обобщить лишь небольшую часть сложного и многогранного материала, классифицировать этот материал, показать на его основе значимость производных имидазола и триазола в жизни человека, показать основные способы получения имидазола и триазола, связать строение имидазола и триазола с их химическими свойствами, описать важнейшие производные имидазола и триазола, привести их формулы и назвать по систематической и рациональной номенклатурам, привести синонимы некоторых лекарственных средств, их основные физические свойства, значение и применение.
Пройдет время, и на основе этих веществ будут синтезированы новые, более сложные препараты, которые, возможно, победят рак, СПИД, нервные и сердечно-сосудистые заболевания.
Список литературы
Иванский А. "Химия гетероциклических соединений" М.: 1977
Машковский М. Д. "Лекарственные средства (в 2-х т.) М.: 1986
Фармакопея. Десятое издание 1968г
Химический энциклопедический словарь М.: "Химия", 1991г
Беликов В.Г. Фармацевтическая химия: Учеб. для фармац. ин-тов и фармац. фак.мед. ин-тов. – М:. Высш. шк. – 768с.
Г.А.Мелентьева. Фармацевтическая химия. Изд. 2-е, перераб. и доп. Т.І.М:. «Медецина», 1976, 862с.
Глушенко Н.Н. Фармацевтическая химия. Учебник для студ. сред. проф. учеб. заведений./ Н.Н.Глушенко, Т.В.Плетенева, В.А.Попков. –М:.Издательский центр «Академия», 2004 – 384с.
Фармацевтична хімія. Навчальний посібник./За загальною редакцією П.В.Безуглого.- Вінниця, НОВА КНИГА, 2006.-552с.
Каппан Г.И., Кукаленко С.С. Триазолы и их пестицидная активность.(ВНИИХСЗР. СССР). М., НИИТЭХИМ. 1983, Серия Современные проблемы химии и химической промышленности. вып. 2 (140).
Ресурсы Интернета: http://www.za4et.net.ru (12.03.12)
http://www.referat.wwww4.com(12.03.12)
|
|
|
 Скачать 252.74 Kb.
Скачать 252.74 Kb.
 [5]
[5]






 [1]
[1]

 Рис.1 Схема
Рис.1 Схема 

 [11]
[11]


