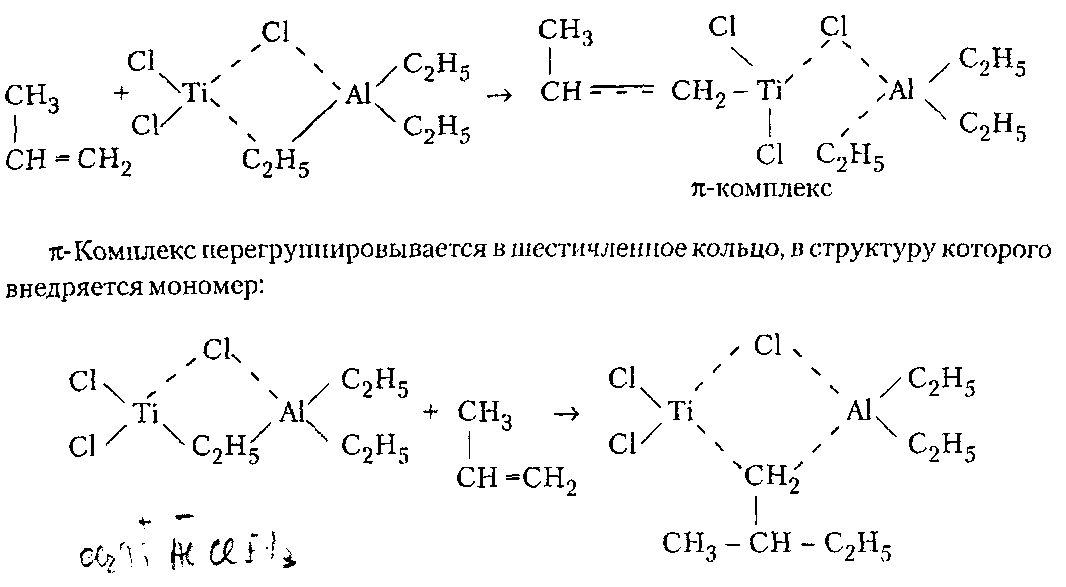
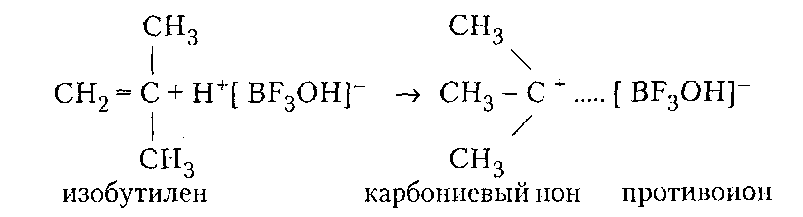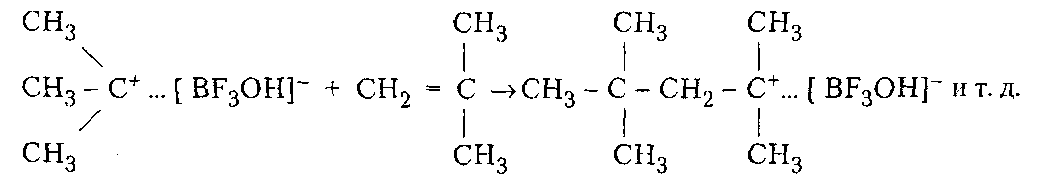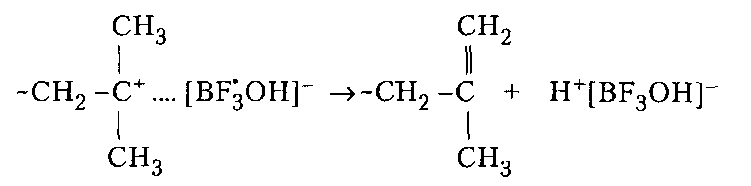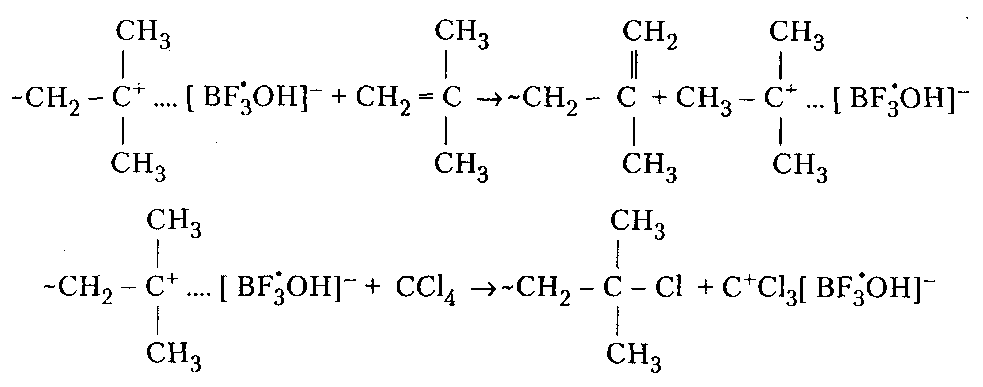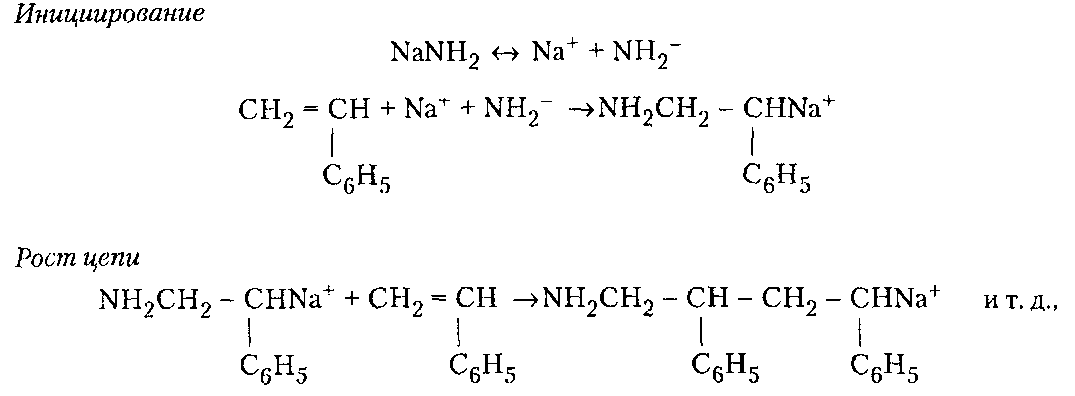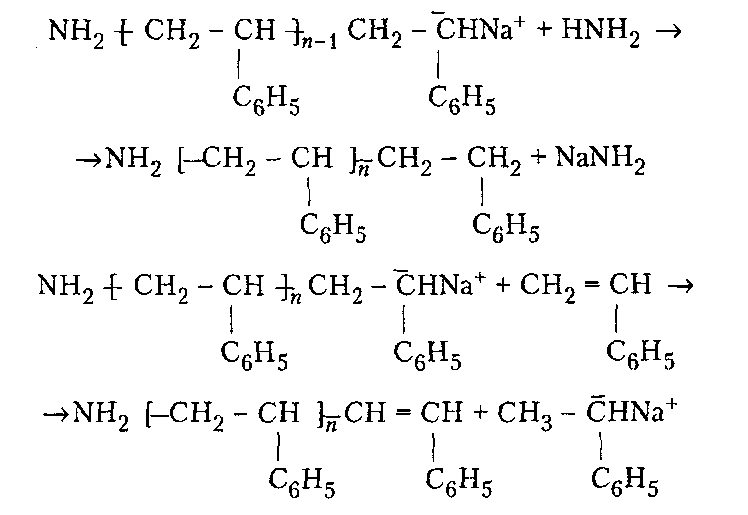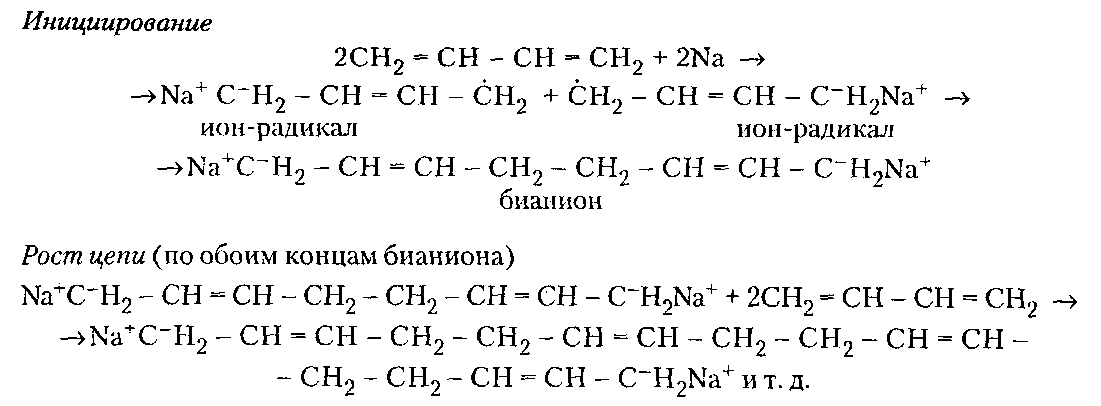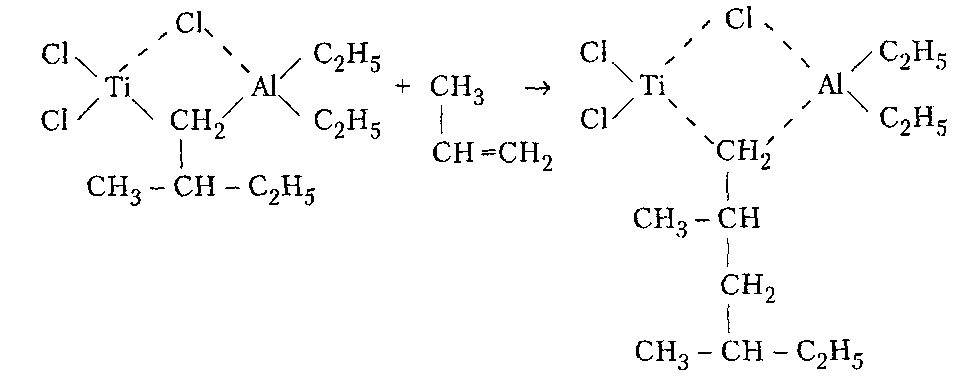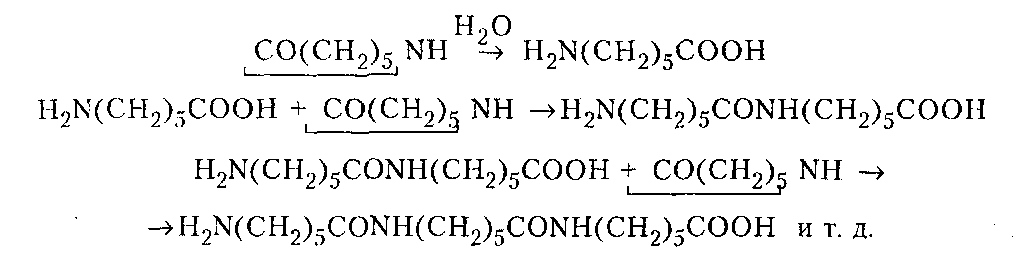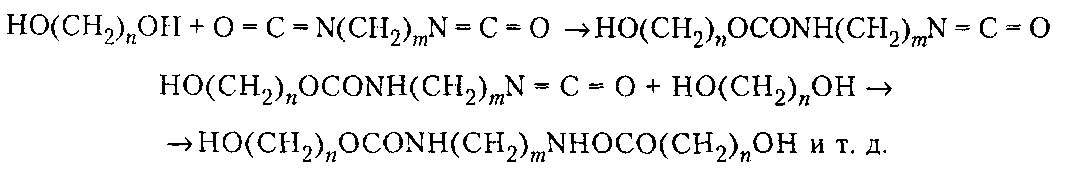Производство ВМС на предпр. НХ. Производство ВМС на предпр. Лекции по курсу производство вмс на предприятиях нефтехимии
 Скачать 2.6 Mb. Скачать 2.6 Mb.
|
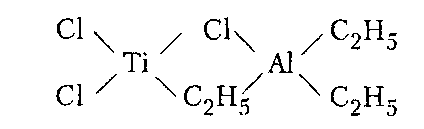
98%) степени завершенности реакции (или конверсии мономеров). Вместе с тем поликонденсация отличается от ступенчатой полимеризации выделением в ходе реакции низкомолекулярных продуктов.ПОЛУЧЕНИЕ ПОЛИМЕРОВПодавляющее большинство высокомолекулярных соединений получают в резуль тате реакций полимеризации и поликонденсации. ПолимеризацияПолимеризация — это процесс получения полимеров, при котором построение макромолекул происходит путем последовательного присоединения молекул низкомолекулярного вещества (мономера) к активному центру, находящемуся на конце растущей цепи. Для полимеризации обязательными являются стадии инициирования и роста цепи. Инициирование — это превращение небольшой доли молекул мономера М в активные центры AM*, способные присоединять к себе новые молекулы мономера. С этой целью в систему вводят возбудители (инициаторы I или катализаторы) полимеризации. Инициирование полимеризации можно представить таким образом: 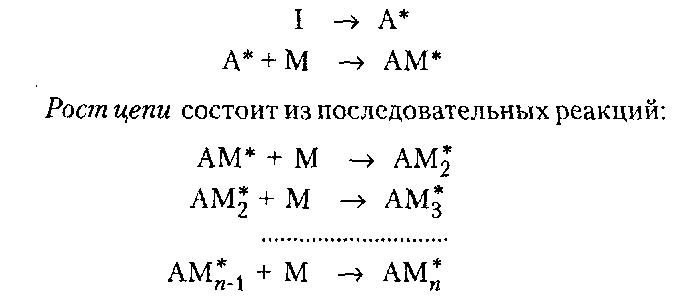 Если в полимеризации участвует один мономер, то получают гомополимеры, если два или более — то сополимеры. В зависимости от природы активного центра различают радикальную и ионную полимеризацию и сополимеризацию. Радикальная полимеризацияРадикальная полимеризация всегда протекает по цепному механизму. Функции активных промежуточных продуктов при радикальной полимеризации выполняют свободные радикалы. К числу распространенных мономеров, вступающих в радикальную полимеризацию, относятся винильные мономеры: этилен, винилхлорид, винилацетат, винилиденхлорид, тетрафторэтилен, акрилонитрил, метакрилонитрил, метилакрилат, метилметакрилат, стирол и диеновые мономеры (бутадиен, изопрен, хлоропренидр.). Радикальной полимеризации свойственны все признаки цепных реакций, известных в химии низкомолекулярных соединений (например, взаимодействие на свету хлора и водорода). Такими признаками являются: резкое влияние незначительного количества примесей на скорость процесса, наличие индукционного периода и проте кание процесса через последовательность трех зависящих друг от друга стадий — образование активного центра (свободного радикала), рост цепи и обрыв цепи. Принципиальное отличие полимеризации от простых цепных реакций заключается в том, что на стадии роста кинетическая цепь воплощается в материальную цепь растущего макрорадикала, и эта цепь растет до образования макромолекулы полимера. Инициирование радикальной полимеризации сводится к созданию в реакционной среде свободных радикалов, способных начать реакционные цепи. Стадия инициирования включает две реакции: возникновение первичных свободных радикалов инициатора R* (1а) и взаимодействие свободного радикала с молекулой мономера (16) с образованием радикала М*: 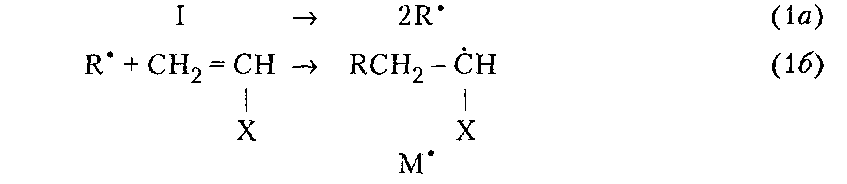 Реакция (1б) протекает во много раз быстрее, чем реакция (1а). Поэтому скорость инициирования полимеризации определяет реакция (1а), в результате которой генерируются свободные радикалы R*. Свободные радикалы, представляющие собой частицы с неспаренным электроном, могут образовываться из молекул под влиянием физического воздействия — теплоты, света, проникающей радиации, когда в них накапливается энергия, достаточная для разрыва π-связи. В зависимости от вида физического воздействия на мономер при инициировании (образование первичного радикала М*) радикальную полимеризацию подразделяют на термическую, радиационную и фотополимеризацию. Кроме того, инициирование может осуществляться за счет распада на радикалы специально вводимых в систему веществ — инициаторов. Этот способ называется вещественным инициированием. Термическое инициирование заключается в самоинициировании при высоких тем пературах полимеризации чистых мономеров без введения в реакционную среду специальных инициаторов. В этом случае образование радикала происходит, как правило, вследствие разложения небольших количеств пероксидных примесей, которые могут возникать при взаимодействии мономера с кислородом воздуха. На практике таким путем получают так называемый блочный полистирол. Однако широкого распространения метод термического инициирования полимеризации не нашел, поскольку он требует больших затрат тепловой энергии, а скорость полимеризации в большинстве случаев невелика. Ее можно увеличить, повышая температуру, но при этом снижается молекулярная масса образующегося полимера. Фотоинициирование полимеризации происходит при освещении мономера светом ртутной лампы, при котором молекула мономера поглощает квант света и переходит в возбужденное энергетическое состояние. Соударяясь с другой молекулой мо номера, она дезактивируется, передавая последней часть своей энергии, при этом обе молекулы превращаются в свободные радикалы. Скорость фотополимеризации рас тет с увеличением интенсивности облучения и, в отличие от термической полимери зации, не зависит от температуры. Радиационное инициирование полимеризации в принципе аналогично фотохимическому. Радиационное инициирование состоит в воздействии на мономеры излучений высокой энергии (γ-лучи, быстрые электроны, α-частицы, нейтроны и др.). Преимуществом фото- и радиационно-химического способов инициирования является возможность мгновенного «включения и выключения» излучения, а также проведение полимеризации при низких температурах. Однако все эти способы технологически сложны и могут сопровождаться протеканием в получаемых полимерах побочных нежелательных реакций, например деструкции. Поэтому на практике чаще всего используют химическое (вещественное) инициирование полимеризации. Химическое инициирование осуществляется введением в среду мономера низко молекулярных нестойких веществ, имеющих в своем составе связи с низкой энергией — инициаторов, легко распадающихся на свободные радикалы под влиянием теплоты или света. Наиболее распространенными инициаторами радикальной полимеризации являются пероксиды и гидропероксиды (пероксид водорода, перок- сид бензоила, гидропероксиды mpem-бутила и изопропилбензола и др.), азо- и диазосоединения (динитрил азобисизомасляной кислоты, диазоаминобензол и др.), персульфаты калия и аммония. Ниже представлены реакции распада некоторых инициаторов. Пероксид трет-бутила (алкилпероксид): 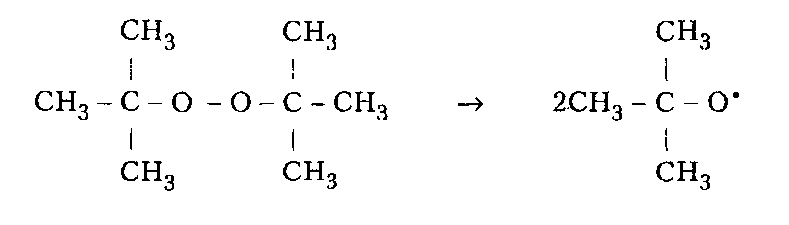 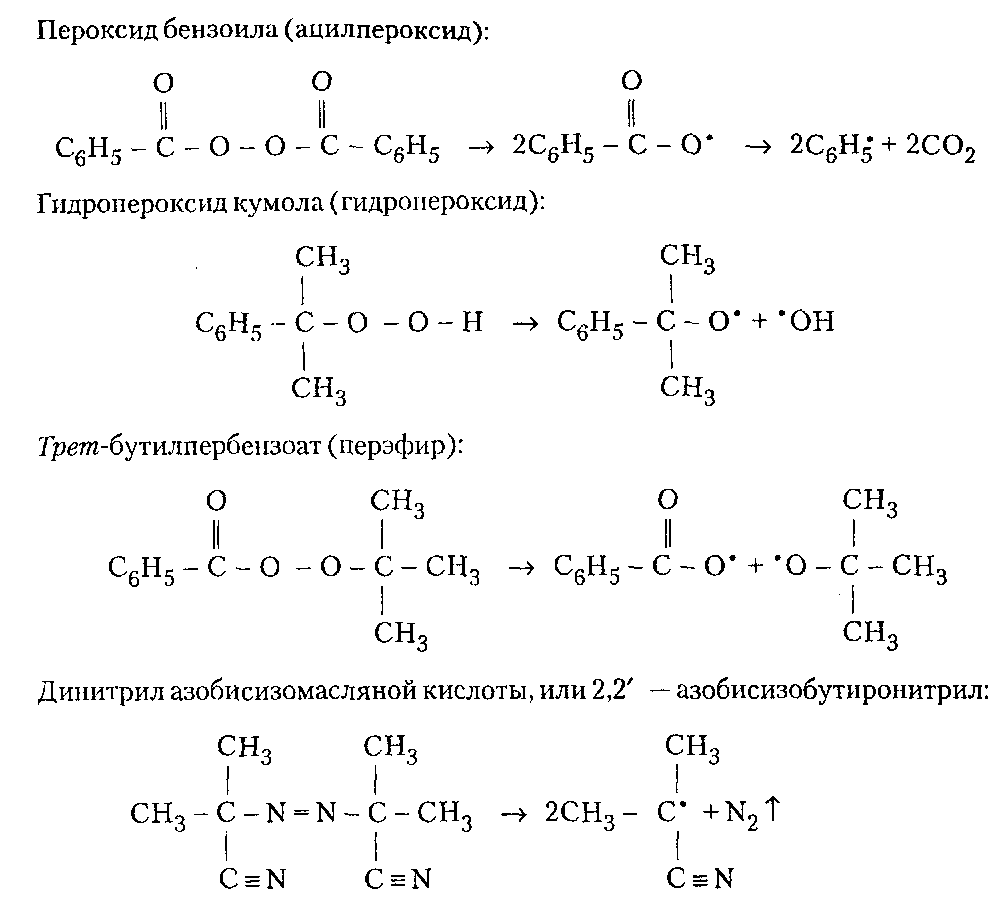 Активность и возможность применения инициаторов радикальной полимеризации определяется скоростью их разложения, которая зависит от температуры. Выбор конкретного инициатора обусловливается той температурой, которая необходима для проведения синтеза полимера. Так, динитрил азобисизомасляной кислоты применяют при 50-70 °С, пероксид бензоила — при 80-95°С, а пероксид трет-бутила — при 120-140°С. Эффективными инициаторами, позволяющими проводить процесс радикальной полимеризации при комнатной и пониженной температурах, являются окислительно-восстановительные системы. В качестве окислителей используют обычно пероксиды, гидропероксиды, персульфаты и др. Восстановителями являются соли металлов переменной валентности (Fe, Со, Сu) в низшей степени окисления, сульфиты, амины и др. Реакция окисления-восстановления проходит в среде, содержащей мономер, с образованием инициирующих полимеризацию свободных радикалов. Можно подобрать пары окислитель-восстановитель, растворимые в воде (например, пероксид водорода-сульфат железа (II)) или в органических растворителях (например, пероксид бензоила — диметиланилин). В соответствии с этим радикальную полимеризацию можно инициировать как в водных, так и в органических средах. Например, распад пероксида водорода в присутствии солей железа (II) может быть представлен следу ющими уравнениями: 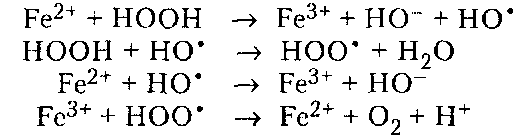 Радикалы НО* и НОО*, присоединяясь к молекуле мономера, инициируют радикальную полимеризацию. Рост цепи осуществляется последовательным присоединением молекул мономера к радикалам (2), возникшим при реакции (1б), например: 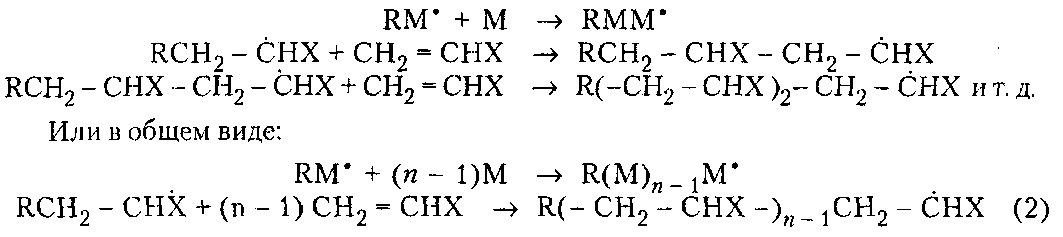 В цепном процессе радикальной полимеризации рост кинетической цепи происходит практически мгновенно с образованием материальной цепи макрорадикала и заканчивается ее обрывом. Обрыв цепи представляет собой процесс прекращения роста кинетической и материальной цепей. Он приводит к исчезновению в системе активных радикалов или к замене их малоактивными радикалами, не способными присоединять молекулы мономера. На стадии обрыва образуется макромолекула полимера. Обрыв цепи может происходить по двум механизмам:
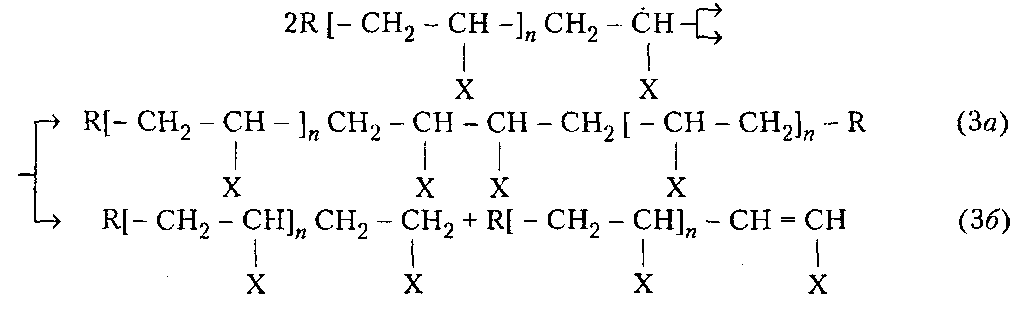 При обрыве цепей рекомбинацией остатки инициатора находятся на обоих концах макромолекулы; при обрыве цепей диспропорционированием — на одном конце. По мере роста цепей макрорадикалов увеличивается вязкость системы и уменьшается их подвижность, вследствие чего обрыв цепей затрудняется и общая скорость полимеризации возрастает. Это явление известно как гель-эффект. Гель-эффект обусловливает повышенную полидисперсность полимеров, что обычно приводит к ухудшению их механических свойств. Ограничение материальных цепей при ради кальной полимеризации может происходить также путем присоединения макрора дикала к первичному радикалу (обрыв на инициаторе) и в результате реакций передачи цепи. Передача цепи заключается в отрыве растущим макрорадикалом подвижного атома от молекулы какого-либо вещества — растворителя, мономера, полимера, примесей. Эти вещества называются передатчиками цепи. В результате макрорадикал превращается в валентно-насыщенную макромолекулу и образуется новый радикал, способный к продолжению кинетической цепи. Таким образом, при реакциях передачи материальная цепь обрывается, а кинетическая — нет. Реакцию передачи цепи на растворитель (например, четыреххлористый углерод) можно представить следующим образом: Образующиеся при этом из молекул растворителя свободные радикалы могут присоединять молекулы мономера, то есть продолжать кинетическую цепь: Если их активность отличается от активности первичных радикалов, то изменяется и скорость полимеризации. При передаче цепи на полимер образуются разветвленные макромолекулы: 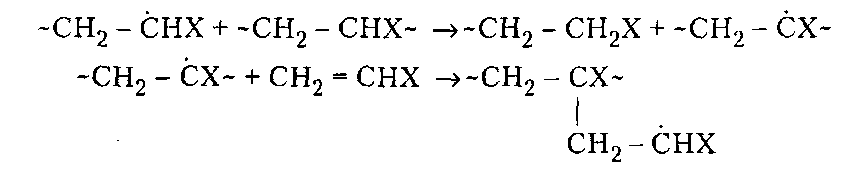 Вероятность передачи цепи на полимер возрастает при высокой конверсии мономера, когда концентрация макромолекул в системе велика. Роль агента передачи цепи в некоторых случаях может играть сам мономер, если его молекулы содержат подвижный атом водорода. В таком случае растущий радикал не присоединяет к себе новую молекулу мономера по двойной связи, а отрывает у нее подвижный атом водорода, насыщая свою свободную валентность и одновременно превращая молекулу мономера в мономерный радикал. Это имеет место при полимеризации винилацетата: 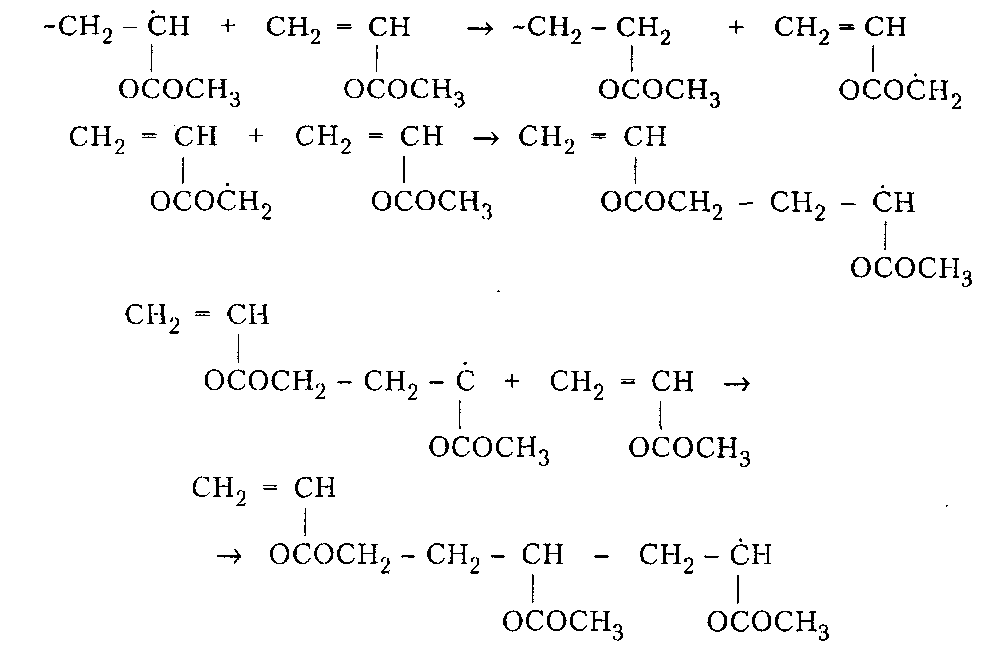 Реакции передачи цепи па растворитель лежат в основе получения теломеров. Если полимеризацию какого-либо мономера проводить при высоких концентрациях растворителя, молекулы которого содержат подвижные атомы водорода или галогена, то продуктом реакции будут вещества с невысокой молекулярной массой, состоящие из нескольких мономерных звеньев, содержащих по концам фрагменты молекул растворителя. Эти вещества называют теломерами, а реакцию их получения — теломеризацией. Реакции передачи цепи могут быть использованы для регулирования молекулярной массы полимеров и даже для предотвращения их образования. Этим широко пользуются на практике, часто применяя при полимеризации передатчики-регуляторы цепи, а при хранении мономеров — ингибиторы. Регуляторы цепи — это вещества, которые обрывая растущие цепи полимера, практически не влияют при этом на общую скорость процесса. Типичными регуляторами цепи являются меркаптаны, содержащие подвижный атом водорода в меркаптогруппе. Передачу цепи на них можно представить следующим образом: Полимеры, синтезированные в присутствии регуляторов цепи, отличаются оптимальным для переработки значением средней молекулярной массы и ММР. Ингибиторы — это вещества, которые обрывают растущие цепи полимера, превращаясь при этом в соединения, не способные инициировать полимеризацию. В качестве ингибиторов обычно используют вещества, передача цепи на которые приводит к образованию неактивных (стабильных) радикалов. На практике для ингибирования радикальной полимеризации и хранения мономеров часто применяют гидрохинон, бензохинон, ароматические амины, нитробензол. Кинетика радикальной полимеризации Теоретические и практические сведения о влиянии различных факторов на радикальную полимеризацию, а именно конверсию мономера и, соответственно, выход полимера, его молекулярные параметры (молекулярная масса, полидисперсность и ММР) могут быть получены при изучении закономерностей развития этого про цесса во времени, то есть его кинетики. Из трех основных элементарных стадий — инициирования, роста и обрыва цепи — самой медленной и энергоемкой является инициирование. Для ее начала требуется энергия активации 84-126кДж/моль, что в 3-4 раза превышает энергию активации стадии роста цепи и почти в 10 раз энергию активации стадии обрыва. Инициатор характеризуется эффективностью. Рассмотрим подробнее стадию распада инициатора на радикалы. 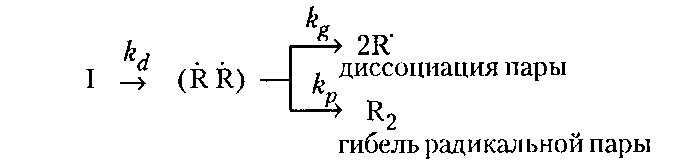 Инициатор распадается на два радикала, которые могут дать начало двум кинетическим цепям. Однако радикальная пара находится в окружении молекул среды, которые создают плотное окружение, называемое клеткой. Плотность среды препятствует быстрому диффузионному разделению радикальной пары, поэтому часть радикалов гибнет путем рекомбинации без выхода в объем. Эффективность инициирования (вероятность зарождения цепей) выражается следующим уравнением: 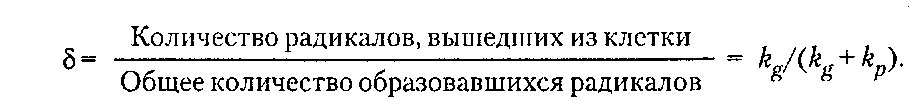 Для определения δ используют ингибиторный метод. Особенно важно учитывать δ в средах с низкой молекулярной подвижностью, где выход радикалов из клетки мал. Это хорошо иллюстрирует следующий пример. При переходе от жидкого этилбензола с высокой молекулярной подвижностью к полистиролу с чрезвычайно низкой молекулярной подвижностью эффективность инициирования уменьшается в 20 раз: с 0,6 до 0,03. Общая скорость радикальной полимеризации V равна скорости расходования мономера М при взаимодействии его с растущим радикалом. Исходя из закона действующих масс, скорость каждой элементарной реакции v процесса полимеризации можно представить следующими уравнениями: 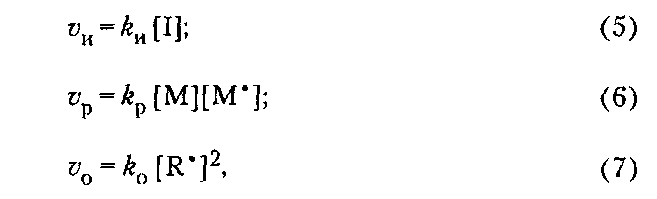 где vи и kи, vp и kp, v0 и ko — скорость и константа скорости реакций инициирования, юста и обрыва цепи соответственно; [I], [М*], [R], [М] — концентрации инициатора, радикалов, растущих радикалов и мономера соответственно. Так как число мономерных молекул, участвующих при инициировании в реакции с первичным радикалом, очень мало по сравнению с числом молекул мономера, участвующих в росте цепи (инициатор обычно вводится в количестве до 1 % от массы мономера), концентрацию мономера можно считать постоянной, и тогда При радикальной полимеризации через несколько секунд после начала реакции устанавливается стационарный режим процесса: радикалы возникают при инициировании и исчезают при обрыве с одинаковой скоростью, то есть vu = voа d[M*]/dt = 0. Тогда [М*] = (kи/ko)1/2[I] 1/2 и уравнение общей скорости полимеризации принимает вид: 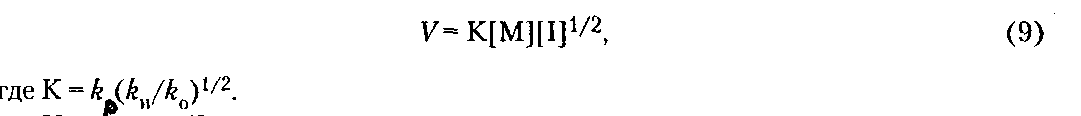 Уравнение (9) справедливо в начальной стадии полимеризации, когда конверсия мономера и выход полимера невысоки (10-15 %). Молекулярная масса полимера так же, как и степень полимеризации п, определяется длиной кинетической цепи, которая зависит от соотношения скоростей реакций обрыва и роста цепи Чем больше vp по сравнению с vo, тем больше молекул мономера успевает присоединиться к растущему радикалу до обрыва цепи, тем больше длина цепи. Учитывая уравнение (9) и условие стационарности процесса, получают 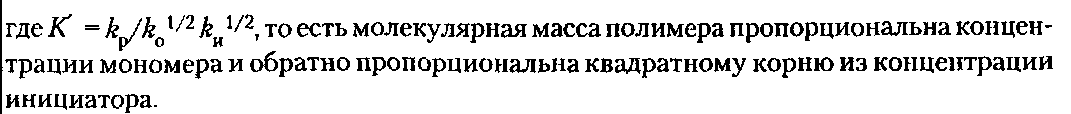 Физический смысл уравнений (9) и (11) заключается в следующем. Молекулярная масса полимера и скорость радикальной полимеризации находятся в прямой зависимости от концентрации мономера, повышение которой вызывает ускорение процесса и увеличение длины цепных молекул. Подобным образом на скорость и мо лекулярную массу полимера влияет увеличение давления, так как сжатие сближает реагирующие молекулы, облегчая процесс полимеризации. С увеличением концентрации инициатора в системе растет число радикалов. Эти радикалы реагируют с большим числом молекул мономера, увеличивая тем самым скорость превращения их в макрорадикалы, то есть скорость полимеризации. Но увеличение концентрации радикалов способствует повышению вероятности их столкновения, то есть возрастанию скорости обрыва цепи полимеризации. Это приводит к снижению молекулярной массы полимера. Аналогичным образом на кинетику радикальной полимеризации влияет температура. Обычно скорость полимеризации возрастает в 2-3 раза при повышении температуры на 10°С. Повышение температуры облегчает распад инициатора на радикалы, вместе с тем возрастает подвижность всех частиц системы — молекул и радикалов, — следовательно, увеличивается вероятность столкновения частиц. Это приводит к тому, что возрастают скорости реакций роста и обрыва цепи. Таким образом, с повышением температуры всегда общая скорость полимеризации увеличивается, а молекулярная масса полимера уменьшается, возрастает доля низкомолекулярных фракций. Повышение температуры способствует одновременно образованию разветвленных макромолекул, нарушению химической регулярности построения полимерной цепи, так как увеличивается вероятность вхождения мономеров в цепь по принципу «голова-голова» или «хвост-хвост». На скорость полимеризации и молекулярную массу полимера существенное влияние оказывают различные примеси и кислород воздуха, причем кислород в зависимости от природы мономера и условий полимеризации может ускорять или замед лять полимеризацию. Кислород замедляет фотополимеризацию винилацетата, но ускоряет фотополимеризацию стирола, ингибирует инициированную пероксидом бензоила полимеризацию винилхлорида, которая с хорошим выходом полимера и высоким значением молекулярной массы протекает в атмосфере азота или аргона. Поэтому для получения полимеров используют мономеры высокой степени чистоты ( |