Иммунную система. Иммунная система. Общие понятия. Лекция Иммунная система общие понятия
 Скачать 0.69 Mb. Скачать 0.69 Mb.
|
|
Антигенами называются структурно чужеродные для данного конкретного организма вещества (высокомолекулярные соединения - белки и полисахариды), способные вызвать иммунный ответ. Носителями таких чужеродных веществ будут бактерии, вирусы, грибки, трансплантаты, опухолевые клетки. Иммуногенность - это способность антигена вызывать иммунный ответ, а антигенность - это способность антигена связываться с антителом. Антигены характеризуются антигенной специфичностью и иммуногенностью 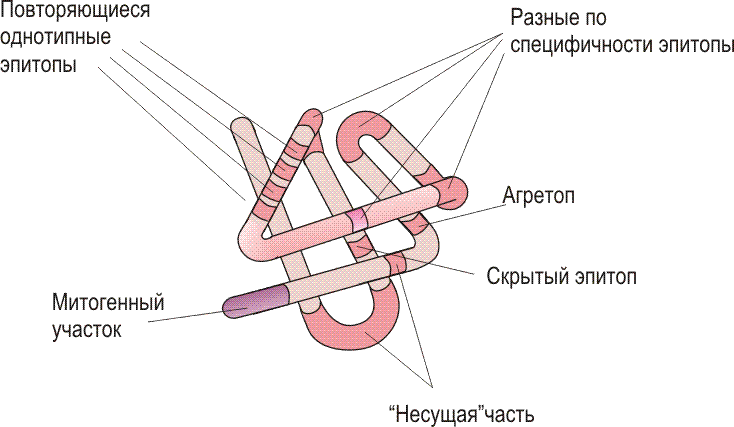 Условный образ антигена. На рисунке представлены детерминантны - участки полипептида, характеризующиеся особенностями включения иммунной системы в работу. Отмечены: 1) разные по специфичности эпитопы (В-клеточные эпитопы), которые инициируют иммунный ответ только при участии Т-хелперов; 2) участки, получившие название "несущей" части или Т-клеточные эпитопы; 3) в процесс презентации антигена в иммуногенной форме в комплексе с молекулами МНС включены участки антигена, называемые агротопами; 4) ряд антигенов, имеющих повторяющиеся однотипные эпитопы, и митогенные участки, инициируют иммунный ответ без включения в ответ Т-хелперов. Соединения с молекулярной массой менее 10000, например лекарственные средства, сами по себе не иммуногенны. Такие соединения принято называть гаптенами. Гаптены приобретают иммуногенность лишь после соединения с высокомолекулярным белком-носителем. Гаптены не могут стимулировать выработку антител, но могут связываться с ними. Гаптены - простые химические соединения, в основном ароматического ряда, не в состоянии запускать иммунный процесс, демонстрируя тем самым отсутствие иммуногенных свойств. В то же время они обладают вполне конкретной специфичностью, т.е. способностью вступать в реакции взаимодействия с предсуществующими к ним антителами . Обычно гаптен - небольшая функциональная группа, представляющая собой одну детерминанту. Гаптенами могут быть органические соединения, фениларсонат, моно- и олигосахариды, а также олигопептиды. Наиболее часто используемый гаптен - динитрофенил (ДНФ). Гаптены могут связываться с уже имеющимся антителом или поверхностным рецептором на специфической B-клетке, но не способны вызвать образование антител, поскольку гаптены не иммуногенны. Однако они приобретают иммуногенность при соединении с подходящим белком-носителем. В настоящее время установлено, что функция носителя заключается в стимуляции T-хелперов , помогающих B-клеткам реагировать на гаптен. Изучение гаптенов указывало на то обстоятельство, что антитела или антигенраспознающие рецепторы B-лимфоцитов и антигенраспознающие рецепторы T-лимфоцитов взаимодействуют не с целой антигенной молекулой, а с отдельными ее участками - эпитопами . При этом В- и Т-лимфоциты распознают разные по характерологическим особенностям эпитопы. Эпитоп это часть антигена, взаимодействующая с паратопом . Эпитопы часто включают аминокислотные остатки, которые находятся далеко друг от друга в первичной последовательности, но собраны в один эпитоп в результате упаковки полипептидной цепи в нативном белке. В этих случаях принято говорить о прерывистых или комбинированных эпитопах в отличие от непрерывных или секвенциальных эпитопах. Изучение вопросов взаимодействия иммунокомпетентных клеток привела к изучению гуморальных регуляторов межклеточных отношений – цитокининов. Основное различие между этими двумя типами иммунореактивности состоит в том, что приобретенный иммунитет высокоспецифичен в отношении каждого конкретного возбудителя. Кроме того, повторная встреча с тем или иным патогенным микроорганизмом не приводит к изменениям врожденного иммунитета, но повышает уровень приобретенного. Общая характеристика. Клетки иммунной системы (иммуно- циты) могут быть разделены натри основные группы. Иммунокомпетентные клетки, способные к специфическому ответу на действие антигенов. Этими свойствами обладают исключительно лимфоциты, каждый из которых изначально обладает рецепторами для какого-либо антигена. Вспомогательные клетки (антиген-представляющие), способные отличать собственные антигены от чужеродных и представлять их иммунокомпетентным клеткам, без чего невозможен иммунный ответ на большинство чужеродных антигенов. Клетки антиген-неспецифической защиты, отличающие компоненты собственного организма от чужеродных частиц, в первую очередь от микроорганизмов, и уничтожающих последние путем фагоцитоза или цитотоксическо- го воздействия. На клеточном уровне ведущую роль играют Т и В –лимфоциты. Основная функция этого клеточного типа – участие в формировании гуморального иммунного ответа посредством специфических иммуноглобулинов. Иммунокомпетентные клетки. Лимфоциты включают две основные группы лимфоцитов (В- и Т-лимфоциты), которые которые морфологически не отличимы друг от друга, формируются в результате пролиферации и дифференцировки стволовых клеток В ходе дифференцировки лимфоциты приобретают рецепторный аппарат, определяющий их способность взаимодействовать с другими клетками организма и отвечать на антигенные воздействия, формировать клоны клеток — потомков, реализующих конечный эффект иммунной реакции (образование антител или цитолитических лимфоцитов). Т-лимфоциты составляют около 80% всех лимфоцитов крови и лимфатических узлов, содержатся во всех тканях организма. Они осуществляют две основные функции — регуляторную и эффекторную. В отличие от В-лимфоцитов они,функция которых функция которых реализуется через гуморальные продукты – антитела, Т-лимфоциты разрушают чужеродные клетки (трансплантаты, опухолевые клетки, вирустрасформированные клетки) при непосредственном контакте с данными клеточными формами. Регуляторные клетки обеспечивают развитие иммунного ответа другими клетками, регулируют его дальнейшее течение. Эффекторные Т-лимфоциты осуществляют эффект иммунной реакции чаще всего в форме цитолиза клеточных структур, к антигенам которых возникла иммунная реакция. Т-лимфоциты составляют 70-80%, а В-лимфоциты - 10-15% лимфоцитов крови. Оставшиеся лимфоциты называются нулевыми клетками. Кроме того, можно выделить субпопуляцию нормальных киллеров. Нормальные киллеры ( NK )- это большие зернистые лимфоциты с характерной морфологией: основная часть обильной цитоплазмы содержит несколько митохондрий , свободные рибосомы с отдельными элементами шероховатого эндоплазматического ретикулума , аппарат Гольджи и характерные электроноплотные гранулы, связанные с мембраной. Большие зернистые лимфоциты с активностью нормальных киллеров выполняют цитотоксические функции, также как и цитотоксические T-лимфоциты . В образовании антител центральная роль принадлежит B-лимфоцитам. При этом B-лимфоциты обеспечивают специфический приобретенный иммунитет совместно с другими малыми лимфоцитами - T-лимфоцитами, используя разнообразные механизмы, направленные в большинстве случаев на расширение пределов эффективности врожденного иммунитета. Лимфоциты класса T образуются в зобной железе, или тимусе, откуда они и получили свое обозначение - "T": предшественники T-лимфоцитов поступают в тимус, где и происходит их созревание. T-лимфоциты подразделяются на ряд подклассов. Главные из них это две различные, неперекрывающиеся субпопуляции: клетки одной из них несут маркер CD4 и в основном "помогают" в осуществлении иммунного ответа или индуцируют его (T-хелперы), клетки другой несут маркер CD8 и обладают преимущественно цитотоксической активностью (цитотоксические T-лимфоциты ( T-киллеры )). Одни CD4 T-клетки участвуют в регуляции дифференцировки B-лимфоцитов и образования антител . Другие CD4 T-клетки взаимодействуют с фагоцитами , помогая им в разрушении микробных клеток. Обе эти субпопуляции CD4 T-клеток названы хелперными T-клетками. Получены очевидные функциональные доказательства существования отдельной субпопуляция антигенспецифичных T-супрессоров , способные подавить иммунный ответ либо путем прямого цитотоксического воздействия на антигенпрезентирующие клетки , либо путем выделения "супрессивных" растворимых белков - цитокинов , либо путем передачи сигнала отрицательной регуляции. Третья группа T-лимфоцитов распознает и разрушает клетки, инфицированные вирусами или иными внутриклеточно размножающимися патогенами. Этот тип CD8 T-лимфоцитов назван цитотоксическими T-лимфоцитами . Как правило, распознавание антигена T-клетками происходит только при условии его презентации на поверхности других клеток в ассоциации с молекулами MHC . В распознавании участвует специфичный к антигену T-клеточный рецептор , функционально и структурно сходный с тем поверхностным иммуноглобулином sIg , который у B-клеток служит антигенраспознающим рецептором . В-лимфоциты составляют 10—15% лимфоцитов крови, 20-25% клеток лимфатических узлов. В-лимфоциты выполняют в организме две роли: обеспечивают продукцию антител и участвуют в представлении антигенов Т-лимфоцитам. В-лимфоциты имеют поверхностные рецепторы для антигенов, представляющих собой молекулы иммуноглобулинов, чаще всего классово и М, фиксированные на наружной поверхности мембраны. В-лимфоцит созревает в костном мозге. На каждом лимфоците формируются 200—500 тыс. рецепторов только для одного антигена. Созревающий лимфоцит покидает костный мозг и становится антиген-ре- активной клеткой, то есть клеткой, способной к взаимодействию с одним из многочисленных антигенов существующих в природе . В-лимфоцита после контакта с антигеном может идти Т-зависимым либо Т-независимым путем. Т-зависимый путь, характерный для ответа на большинство антигенов, осуществляется с помощью цитокинов, продуцируемых Г-хелперными лимфоцитами (CD4). При воздействии антигена одновременно с В-лимфоцитами активируются и Т-хелперы (Тх). Гх продуцируют ИЛ-2, стимулирующий пролиферацию В-лимфоцитов и их первое деление. Т-независимый путь формирования иммунного ответа В-лимфоцитами осуществляется без помощи Т-лимфоцитов и индуцируется некоторыми небелковыми, в том числе микробными, антигенами. Т-независимые антигены обладают митогенным действием и способствуют формированию клона клеток, продуцирующих IgM-антитела. Т-независимый путь иммунного ответа В-лимфоци гов более примитивен и менее эффективен, так как не сопровождается формированием иммунной памяти и при нем не происходит переключение синтеза антител с IgM на другие классы имМакрофаги (мононуклеарные фагоциты): общие сведения Мононуклеарные фагоциты (макрофаги) составляют наиболее важную группу способных к фагоцитозу долгоживущих клеток. Тканевые макрофаги и их предшественники - моноциты , промоноциты и монобласты - образуют систему мононуклеарных фагоцитов . Макрофаги - это долгоживущие фагоциты , имеющие много общих функций с нейтрофилами . Кроме того, макрофаги в качестве секреторных клеток участвуют во многих сложных иммунных и воспалительных реакциях, в которых не участвуют нейтрофилы. Моноциты, как и нейтрофилы, покидают сосудистое русло путем диапедеза , но дольше циркулируют в крови: их период полуциркуляции составляет от 12 до 24 ч. После того как моноциты попадают в ткани, они превращаются в макрофаги, выполняющие специфические функции в зависимости от анатомической локализации. Особенно богаты этими клетками селезенка , печень , костный мозг и легкие , где функция макрофагов состоит в удалении из крови микроорганизмов и других вредных частиц. Альвеолярные макрофаги , купферовские клетки , клетки микроглии , дендритные клетки , макрофаги селезенки, брюшины, костного мозга и лимфоузлов - все они выполняют специфические функции. Мононуклеарные фагоцитов выполняет две основные функции, осуществляемые двумя разными типами клеток костномозгового происхождения: - "профессиональными" макрофагами, главная роль которых - устранение корпускулярных антигенов, и - антигенпрезентирующими клетками (АПК) , роль которых заключается в поглощении, процессинге и представлении антигена T-клеткам. - антигенпрезентирующими клетками (АПК) , роль которых заключается в поглощении, процессинге и представлении антигена T-клеткам. Макрофаги образуются из промоноцитов костного мозга , которые после дифференцировки в моноциты крови задерживаются в тканях в виде зрелых макрофагов, где и формируют систему мононуклеарных фагоцитов . Особенно высоко их содержание в печении медулярных синусах лимфатических узлов . Макрофаги - долгоживущие клетки с хорошо развитыми митохондриями и шероховатым эндоплазматическим ретикулумом . Роль макрофагов в иммунитете исключительно важна - они обеспечивают фагоцитоз , переработку и представление антигена T-клеткам. Макрофаги вырабатывают ферменты, некоторые белки сыворотки , кислородные радикалы , простагландины и лейкотриены , цитокины ( интерлейкины , фактор некроза опухолей и другие). Макрофаги секретируют лизоцим, нейтральные протеазы, кислые гидролазы, аргиназу, многие компоненты комплемента, ингибиторы ферментов ( антиактиватор плазминогена , альфа2-макроглобулин ), транспортные белки ( трансферрин , фибронектин , транскобаламин II ), нуклеозиды и цитокины ( ФНО альфа , ИЛ-1 , ИЛ-8 , ИЛ-12 ). ИЛ-1 выполняет много важных функций: воздействуя на гипоталамус, вызывает лихорадку ; стимулирует выход нейтрофилов из костного мозга; активирует лимфоциты и нейтрофилы . ФНОальфа (называемый также кахектином ) - это пироген . Во многом он дублирует действие ИЛ-1, но кроме того, играет важную роль в патогенезе септического шока , вызванного грамотрицательными бактериями. Под влиянием ФНОальфа резко увеличивается образование макрофагами и нейтрофилами перекиси водорода и других свободных радикалов . При хроническом воспалении ФНОальфа активирует катаболические процессы и тем самым способствует развитию кахексии - симптома многих хронических заболеваний. Макрофаги продуцируют также активные формы кислорода , производные арахидоновой кислоты , фактор активации тромбоцитов , хемокины , колониестимулирующие факторы , факторы, стимулирующие пролиферацию фибробластов и разрастание мелких сосудов. Макрофаги регулируют пролиферацию лимфоцитов, разрушают опухолевые клетки, вирусы и некоторых бактерий ( Mycobacterium tuberculosis , Listeria monocytogenes ). В уничтожении внутриклеточных паразитов макрофагам принадлежит ключевая роль. Для этого они сливаются в гигантские клетки, которые под влиянием провоспалительных цитокинов объединяются в гранулемы. Образование гигантских клеток, возможно, регулирует интерферон гамма Основная функция макрофагов сводится к борьбе с теми бактериями, вирусами и простейшими, которые могут существовать внутри клетки-хозяина, при помощи мощных бактерицидных механизмов, которыми обладают макрофаги. Таким образом, макрофаги являются одним из орудий врожденного иммунитета . Кроме того макрофаги наряду с B - и T-лимфоцитами участвуют и в приобретенном иммунном ответе , являясь "дополнительным" типом клеток иммунного ответа: макрофаги являются фагоцитирующими клетками, чья функция - "проглатывание" иммунногенов и процессирование их для представления T-лимфоцитам в форме, пригодной для иммунного ответа. Основные функции макрофагов представлены на рис. 10-9 . T-лимфоциты распознают инфицированный макрофаг по экспонированию на его поверхности микробного антигена, находящегося в комплексе с гликопротеином MHC класса II , который в данном случае служит сигналом макрофага. В результате распознавания T-клетки выделяют лимфокины , стимулирующие внутриклеточное уничтожение возбудителя макрофагом (см. Макрофаги: уничтожение паразитов, избегающих фагоцитоза ; и Лимфокины, действующие на макрофаги ). В отличие от лимфоцитов, макрофаги не обладают способностью специфичного узнавания. Кроме того, макрофаги, по-видимому, отвечают за индукцию толерантности. Помимо специфического иммунного ответа организм способен развивать специфическую ареактивность к тому или иному антигену . Это состояние приобретенной ареактивности получило название иммунологической толерантности ; ее индуцирует предшествующий контакт с антигеном. Феномен приобретенной толерантности (терпимости), как и феномен иммунологической реактивности, строго специфичен, и индуцируемая ареактивность к одному антигену не отменяет полноценного ответа к другому. Активно функционирующие механизмы толерантности необходимы для предупреждения воспалительных реакций в ответ на многие безвредные антигены, попадающие в организм с воздухом и пищей и действующие на слизистую оболочку дыхательных путей и желудочно-кишечного тракта. Однако наиболее важна толерантность к собственным антигенам организма; она предотвращает иммунный ответ против собственных тканей. Между тем такая возможность существует, поскольку иммунная система продуцирует самые разнообразные антигенспецифические рецепторы, в том числе способные реагировать с аутоантигенами. При аутоиммунных заболеваниях макрофаги удаляют из крови иммунные комплексы и другие иммунологически активные вещества. Макрофаги участвуют в заживлении ран , удалении отживших клеток и образовании атеросклеротических бляшек .муноглобулинов. ОРГАННЫЙ УРОВЕНЬ. Органный уровень указывает на морфологические границы и "место действия" формирующегося иммунного ответа. На этом уровне изучают:клеточный состав и гистологические сдвиги в органах, где реализуются механизмы иммунитета; взаимодействие органов между собой в процессе иммуногенеза, потенциальную роль отдельных органов при гуморальном и клеточном иммунном реагировании ; факторы, объединяющие иммунореактивные органы в единую систему; их онто- и филогенетическое происхождение. Лимфоидную и кроветворную системы объединяют в единый лимфомиелоидный комплекс . В него входят: костный мозг , тимус , селезенка , лимфатические узлы и лимфоидная ткань слизистых оболочек , включая миндалины глоточного кольца и пейеровы бляшки повздошной кишки. Все эти органы и ткани связаны между собой сетью кровеносных и лимфатических сосудов, обеспечивающих межорганный обмен клеточными элементами ( рис. В.6 ). 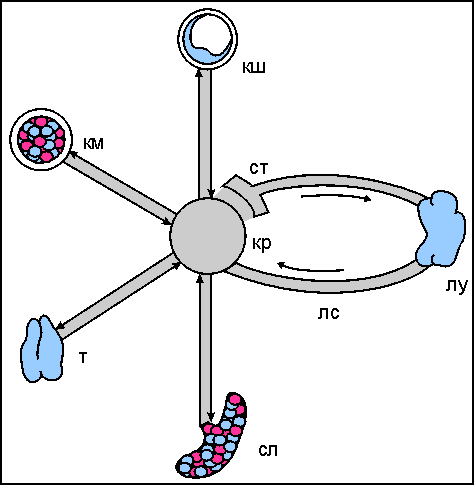 |
