Навчальнометодичний посібник з дисципліни Біологічна хімія
 Скачать 1.66 Mb. Скачать 1.66 Mb.
|
|
Гормони та їх посередники
Гормони цієї групи здійснюють трансформацію регуляторного сигналу в специфічну функціональну активність клітини-мішені за рахунок таких молекулярних механізмів: взаємодії гормону на поверхні плазматичної мембрани з білковим рецептором з утворенням гормон-рецепторного комплексу; передачі хімічного сигналу з рецептора, модифікованого за рахунок взаємодії з лігандом (гормоном, іншим біорегулятором), через трансформуючі білки – трансдуктори (G-білки) на внутрішньоклітинні сигнальні системи; утворення (або вивільнення) внутрішньоклітинних сигнальних молекул – вторинних посередників (циклічних нуклеотидів – цАМФ, цГМФ, фосфоінозитолів, іонів Са 2+); взаємодії вторинних посередників з ферментами клітини з включенням через активацію специфічних протеїнкіназ, ефекторних систем клітини, тобто послідовних стадій розвитку клітинної біохімічної реакції на гормональний стимул. Біохімічні системи забезпечення внутрішньоклітинної передачі гормонального сигналу Система трансдукції хімічного сигналу, що його сприймає клітина від біорегулятора, включає взаємодію модифікованого гормон-рецепторного комплексу з білками-трансдукторами, які здійснюють трансформацію та подальшу передачу регуляторного сигналу. Білки – трансдуктори (G-білки або N-білки) – внутрішньомембранні білки, які сприймають хімічний сигнал від рецептора, модифікованого за рахунок взаємодії з гормоном або медіатором, та спричиняють зміни функціональної активності ефекторних систем клітини. Відомо понад 200 різноманітних G-білків, які поділяють на декілька типів: Gs – білки (стимулюючі) активують аденілатциклазу, що сприяє утворенню головного вторинного посередника – цАМФ; Gi – білки (інгібуючі) інгібують аденілатциклазу; Gq – білки активують фосфоліпазу С – фермент, який спричинює запуск фосфоінозитолного циклу – ферментної системи, яка підвищує концентрацію Са2+ в цитозолі за рахунок його вивільнення з внутрішньоклітинних депо; Gt - це трансдуцин, який бере участь в АДФ-рибозилювання при дії холерного токсину. Холерний токсин проникає в клітини кишкового епітелію за допомогою рецептор-залежного ендоцитозу. У цитоплазмі клітини дисульфидний зв'язок між доменами A1 і A2 відновлюється і A1 дисоціює з комплексу. Субодиниця A1 каталізує перенесення АДФ-рибози із НАД+ (АДФ-рибозилювання) на α-субодиницю Gs білка, який стимулює активність аденілатциклази. Стимуляція аденілатциклази підвищує вміст внутрішньоклітинного цАМФ. У свою чергу цАМФ запускає сигнальний шлях, який призводить до відтоку хлорид-іонів та інших аніонів з клітини і до припинення надходження в клітину іонів натрію. Додаткові відтік іонів натрію відбувається спільно з аніонами. Іони натрію котранспортируються з молекулами води, тому концентрація води в клітині при цих процесах істотно знижується. Порушення водно-сольового балансу призводить до діареї, при якій організм втрачає до 2 літрів води в годину. За молекулярної будовою G-білки є тримерами, що складаються з трьох субодиниць (α, β, γ). α-субодиниця володіє ГТФазною активністю: утворення гормон-рецепторного комплексу та передача регуляторного сигналу на каталітичну субодиницю ферменту аденілатциклази супроводжується конформаційними змінами α-субодиниці, гідролізом ГТФ до ГДФ та Фн і відщепленням димеру βγ від α-ГТФ. G-білок повертається в неактивну форму. При наступній активації рецептора і заміні молекули ГДФ на ГТФ цикл повторюється. Таким чином, α-субодиниця G-білка здійснює човниковий рух, переносить сигнал від рецептора, активованого первинним посередником (гормоном) на фермент, який каталізує утворення вторинного посередника. Вторинні посередники – циклічні нуклеотиди. Сигнал на подальше включення каскаду біохімічних реакцій передається вторинними посередниками або месенджерами (messenger – посланець. вісник, англ.) – біомолекулами, що передають інформацію від гормону (первинного месенджера) на ефекторні системи клітини. До вторинних месенджерів належать: циклічні нуклеотиди – циклічний аденозинмонофосфат (3 ',5'-АМФ; цАМФ) і циклічний гуанозинмонофосфат (3',5' -ГМФ, цГМФ), фосфоінозитоли, діацилгліцерол та іони Са2+. Зростання внутрішньоклітинної (цитозольної) концентрації зазначених вторинних посередників здійснюється шляхом активації аденілатциклази з утворенням цАМФ; активації гуанілатциклази з утворенням цГМФ; активації фосфоліпази С, що призводить до включення фосфоінозитолного каскаду – механізму мобілізації внутрішньоклітинного Са2+; надходження Са2+ з екстрацелюлярного простору за рахунок відкриття кальцієвих каналів на плазматичній мембрані. Аденілатциклазна система каталізує утворення цАМФ з АТФ, а гуанілатциклазна – утворення цГМФ з ГТФ. 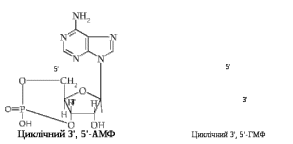 Гормони, взаємодія яких з рецептором клітини-мішені призводить до утворення цАМФ, діють через трикомпонентну систему, яка включає білок-рецептор (Rs або RІ), G-білок (Gs або Gi ) і власне фермент аденілатциклазу, яка розташована на внутрішній поверхні мембрани і каталізує утворення цАМФ з АТФ. Аденілатциклаза – ключовий фермент аденілатциклазної системи, містить 12 трансмембранних доменів. На його активність впливають як позаклітинні, так і внутрішньоклітинні регулятори. Позаклітинні регулятори (гормони, ейкозаноїди, біогенні аміни) здійснюють регуляцію через специфічні рецептори, які за допомогою -субодиниць G-білків передають сигнали на аденілатциклазу. Регуляція активності аденілатциклази внутрішньоклітинним кальцієм дозволяє клітині інтегрувати активність двох основних вторинних месенджерів – цАМФ та іонів Са2+. До гормонів, що використовують цАМФ як вторинний посередник, належать адреналін, вазопресин, глюкагон, хоріонічний гонадотропін, дофамін (при взаємодії з D1-рецепторами), кальцитонін, кортикотропін, ліпотропін, лютеїнізуючий гормон, меланоцитостимулюючий гормон, норадреналін (при взаємодії з β-рецепторами), тиреотропний гормон, фолікулостимулюючий гормон. Існує певна група біорегуляторів, що гальмують аденілатциклазу і зменшують внутрішньоклітинний рівень цАМФ (діють через Gi-білок); до них належать ангіотензин ІІ, ацетилхолін (при взаємодії з м-холінорецепторами), дофамін (при взаємодії з D2-рецепторами), норадреналін (при взаємодії з α2-адренорецепторами), опіоїдні пептиди, соматостатин. На аденілатциклазний шлях передачі сигналу в клітину впливають деякі бактеріальні токсини. Наприклад, токсин, який утворює холерний вібріон, каталізує реакцію перенесення АДФ-рибози з НАД на α-ланцюг Gs-білка (реакція рибозилування), що переводить білок у постійно активний стан з втратою чутливості до гормональних сигналів. Унаслідок цього в клітинах кишки зростає рівень цАМФ, який викликає інтенсивну секрецію кишкового соку. Тому при холері швидко розвивається тяжка діарея та дегідратація організму. Внаслідок дії гормонів, що активують аденілатциклазу, у клітині підвищується рівень цАМФ. Останній зв'язується з неактивним тетрамером протеїнкінази, внаслідок чого відбувається його дисоціація на 2 регуляторні та 2 каталітичні субодиниці і в такий спосіб активуються каталітичні субодиниці, тобто протеїнкіназа переходить з неактивної форми в активну (рис. 8). Активні протеїнкінази каталізують фосфорилювання різних білків (у тому числі, ферментів) за схемою:  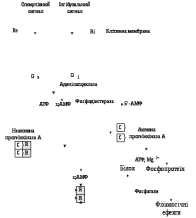 Рис. 8. Гормональна регуляція внутрішньоклітинних процесів через цАМФ-залежні протеїнкінази 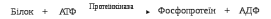 Білки, що утворилися під час фосфорилювання, викликають різноманітні біологічні ефекти. Одні білки після фосфорилювання протеїнкіназами активуються, активність інших гальмується. Наприклад, при дії адреналіну та глюкагону – гормонів, що збільшують рівень цАМФ у клітинах, активовані протеїнкінази фосфорилюють глікогенфосфорилазу, переводять її із неактивної форми в активну і забезпечують розпад глікогену в печінці та скелетних м'язах. У цей же час у результаті фосфорилювання відбувається інактивація ферменту глікогенсинтази, що призводить до гальмування синтезу глікогену. За допомогою цАМФ можуть здійснюватися два основних шляхи регуляції активності ферментів: перший – зміна активності молекул ферментів, за рахунок їх ковалентної модифікації, тобто фосфорилювання. Другий шлях – зміна кількості ферменту за рахунок зміни швидкості його біосинтезу та деградації. Зміна кількості цАМФ в клітині під впливом різних гормонів може здійснюватися через фосфодіестеразу, яка каталізує гідроліз цАМФ (або цГМФ) з утворенням неактивного метаболіту АМФ (або ГМФ). Її активаторами є іони Са2+, комплекс Са2+-кальмодулін, цГМФ. Речовини, які інгібують фосфодіестеразу, чинять ефект, подібний до дії гормону, наприклад, інгібітори фосфодіестерази похідні ксантинів (кофеїн, еуфілін, теофілін) підвищують рівень цАМФ, імітуючи ефект, який створюють ендогенні гормони. Аналогічно, як у випадку з цАМФ, гормони та інші позаклітинні регулятори стимулюють утворення циклічного нуклеотиду – цГМФ під дією ферменту гуанілатциклази, яка існує в розчинній і мембранозв’язаній формах. Активування гуанілатциклази призводить до утворення цГМФ з ГТФ. Циклічний ГМФ активує цГМФ-залежну протеїнкіназу G, яка фосфорилює білки. Протеїнкіназа G присутня не у всіх тканинах, її виявляють у легенях, гладких м’язах, мозочку та тромбоцитах. Ізоформи протеїнкінази G можуть бути зв’язані з мембраною або знаходяться в цитоплазмі. Розчинна протеїнкіназа G складається з двох субодиниць, кожна з яких має два центри для зв’язування цГМФ. Приєднання останнього до регуляторних центрів спричинює конформаційні зміни субодиниць і посилює каталітичну активність ферменту. Подібно до протеїнкіназ А і С, протеїнкіназа G специфічна до певних білкових субстратів, котрі вона фосфорилює за залишками серину та треоніну. Вторинні посередники – іони кальцію, інозитолтрифосфат і діацилгліцерол. Іони кальцію – внутрішньоклітинні месенджери та регулятори багатьох ферментних систем і фізіологічних функцій клітин, зокрема поділу та росту, клітин, скорочення м'язових та інших скоротливих білків, згортання крові, секреції гормонів і нейромедіаторів, передачі нервового імпульсу тощо. Їх внутрішньоклітинна концентрація дуже низька (10–7 моль/л) порівняно з позаклітинною (10–3 моль/л). Регуляторна функція Са2+ (передавання сигналу від гормону, медіатора та активація ефекторних біохімічних систем) здійснюється шляхом зростання внутрішньоклітинної (цитозольної) концентрації цих іонів (від 10-7 – 10-9 до 10-6 М). Це значне зростання концентрації вільного Са2+ здійснюється шляхом включення зовнішньоклітинним біорегулятором одного з таких механізмів: - відкриття кальцієвих каналів (рецепторчутливих каналів) на плазматичній мембрані та входу в клітину екстрацелюлярного Са2+ (механізм, що реалізується здебільшого при взаємодії нейромедіаторів з іонотропними рецепторами); - виходу іонів кальцію у цитозоль з його внутрішніх депо – мітохондрій і цистерн (канальців) ендоплазматичного (саркоплазматичного) ретикулуму (мобілізація кальцію з внутрішніх депо); включення цього механізму потребує стимуляції гормоном чи іншим біорегулятором фосфоінозитидної системи, інтермедіати якої і спричиняють вихід кальцію з органел. Перехід клітини з активного стану до функціонального спокою відбувається в результаті зменшення цитозольної концентрації кальцію до вихідної, що забезпечується «викачуванням» Са2+ з цитозолю в екстрацелюлярний простір і «закачуванням» іонів у внутрішньоклітинні депо. Цей процес є енергозалежним транспортом проти градієнта концентрації і досягається за рахунок функціонування Са2+-АТФаз плазматичних мембран і мембран внутрішньоклітинних органел. Універсальним акцептором хімічного регуляторного сигналу від іонів Са2+ є кальмодулін (КМ) – білок з молекулярною масою близько 17 000 Да, який може зв'язувати чотири іони кальцію. Специфічне зв'язування Са2+ з молекулою КМ призводить до змін конформації білка, який набуває властивості взаємодіяти з чутливими до КМ білками, у тому числі активувати цАМФ-залежну фосфодіестеразу, Са2+–кальмодулінзалежні протеїнкінази, Са2+-АТФазу плазматичних мембран кардіоміоцитів і еритроцитів, кіназу фосфорилази м'язів й інші ферменти. При підвищенні внутрішньоклітинної концентрації Са2+ підвищується активність гуанілатциклази і синтез цГМФ. Вважають, що швидкі ефекти кальцію пов'язані iз мобілізацією його з органел клітини, а повільні – із надходженням ззовні або зі зменшенням виходу кальцію з клітини. Встановлення біологічної ролі деяких фосфоінозитидів, що спричинюють вихід кальцію із внутрішньоклітинних депо, відкрило додатковий механізм у дії гормонів – фосфоінозитидну систему. Система фосфоінозитидного циклу включає три етапи: 1) взаємодія гормону з рецептором з подальшим зростанням спорідненості до G-білка та утворенням -ГТФ; 2) метаболізм ліпідного матриксу, зокрема, фосфатидилінозитидів; 3) подальші реакції індукції вивільнення Са2+ з клітинних депо, фосфорилювання мембраних і цитозольних білків. Фосфоліпаза С, яка активується внаслідок зв’язування з нею -ГТФ, розщеплює фосфатидилінозитол-4,5-дифосфат (ФІФ2), який є одним з компонентів плазматичної мембрани, до інозитол-1,4,5-трифосфату (ІФ3) і діацилгліцеролу (ДАГ), які є вторинними посередниками. ІФ3 спричинює вивільнення іонів кальцію з клітинних депо, що на короткий час збільшує їх концентрацію в цитоплазмі і сприяє утворенню комплексів Са2+-КМ, які активують специфічні протеїнкінази (рис. 9). Інший продукт гідролізу – ДАГ активує Са2+-фосфоліпідзалежну протеїнкіназу С, яка переміщається з цитоплазми в плазматичну мембрану, де її чутливість до активації кальцієм збільшується у понад 100 разів. Активність протеїнкінази С додатково стимулюють іони Са2+ та фосфатидилсерин. Спільна дія Са2+-залежних протеїнкіназ і протеїнкінази С зумовлює активацію шляхом фосфорилювання низки клітинних білків, які беруть участь у реалізації клітинної відповіді (секреція гормонів, нейромедіаторів, ферментів, скорочення м'язів, агрегації тромбоцитів, транспорту іонів, глюкози та інших речовин через мембрани).   Рис. 9. Фосфоінозитолзалежна регуляція клітинних функцій: Р – рецептор, ФІФ2 – фосфатидилінозитол-4,5-дифосфат, , ІФ3 – інозитол-1,4,5-трифосфат; ДАГ – діацигліцерол, Фл С – фосфоліпаза С, ПК С – протеїнкіназа С, КМ – кальмодулін, ЕР – ендоплазматичний ретикулум Припинення передачі сигналу через фосфоінозитидна систему здійснюється завдяки інактивації вторинних посередників і дефосфорилування білків. Від ІФ3 поступово відщеплюються фосфатні групи. Цей процес інгібують іони літію, надмірне надходження яких в організм призводить до порушень обміну фосфоінозитолів, що, вочевидь, лежить в основі терапевтичної дії іонів літію при маніакально-депресивних психозах. ДАГ інактивується двома шляхами: частина його перетворюється на фосфатидну кислоту, а інша розщеплюється до вихідних компонентів – гліцеролу та жирних кислот, зокрема арахідонової – попередника простагландинів і лейкотрієнів. Із фосфатидної кислоти та інозитолу синтезується фосфатидилінозитол, а згодом – фосфатидилінозитол-4,5-дифосфат. Для цього використовуються молекули ЦТФ і АТФ. Через фосфоінозитидна систему реалізується дія катехоламінів (при їх зв'язуванні з α1-адренорецепторами), тиреоліберину, гонадоліберину, вазопресину, ангіотензину ІІ, гастрину, холецистокініну, брадикініну та інших гормонів. Мембранний механізм дії гормонів Передача сигналу від низки гормонів (наприклад, інсулін, інсуліноподібний фактор росту (ІФР-1, ІФР-2)), здійснюється без участі вторинних посередників, для них характерний мембранний механізм дії. Зв’язуючись із рецепторами на поверхні плазматичних мембран адипоцитів, інсулін змінює їх проникність для низки речовин (глюкози, амінокислот) та іонів. Проникність мембрани відбувається внаслідок зв’язування гормону з її транспортними системами, що спричинює або зміну конформації транспортних білків (внаслідок фосфорилювання) або збільшення кількості білків-переносників, які містяться всередині клітини, а під впливом гормону переміщаються в плазматичну мембрану. Потрапивши всередину клітини, метаболіти чинять вплив на біохімічні процеси, а іони змінюють електричний потенціал мембрани. Інсуліновий рецептор – тирозинова протеїнкіназа, яка фосфорилює білки за ОН-групами тирозину. Він складається з двох - і двох -субодиниць, з’єднаних між собою дисульфідними зв’язками та нековалентними взаємодіями (рис. 10).  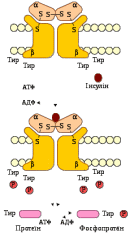 Рис. 10 Активація рецептора інсуліну Субодиниці за хімічною природою належать до глікопротеїнів, вуглеводна частина яких знаходиться на зовнішній поверхні мембрани. Центр зв’язування інсуліну утворений N-кінцевими доменами -субодиниць. -Субодиниці пронизують мембранний бішар, вони не беруть участі в зв’язуванні інсуліну, але на їх внутрішньоклітинних доменах знаходиться каталітичний центр тирозинової протеїнкінази. За відсутності інсуліну рецептори не проявляють тирозинкіназної активності. Приєднання інсуліну до -субодиниць активує фермент, для якого субстратом слугують самі -субодиниці, тобто відбувається їх трансфосфорилування (одна -субодиниця фосфорилує іншу) за кількома тирозиновими залишками. Це, своєю чергою, призводить до зміни субстратної специфічності тирозинової протеїнкінази, вона набуває здатності фосфорилувати інші транспортні білки, про що говорилося вище. Дефосфорилування рецептора та його повернення в неактивний стан відбувається за участі тирозинової фосфопротеїн фосфатази; спорідненість між інсуліном і рецептором втрачається у випадку фосфорилування останнього протеїнкіназою А за залишками серину та треоніну. Цитозольний механізм дії гормонів стероїдні гормони, похідні вітамінів групи D, а також йодтироніни, які за ліпофільністю займають проміжне місце між стероїдами та водорозчинними гормонами, і їх молекули здатні проникати через ліпідній бішар плазматичної мембрани клітин, проявляють свою дію за цитозольним механізмом. Специфічні рецептори зазначених гормонів містяться в цитоплазмі клітин-мішеней. Вони є білками з молекулярною масою 50 – 190 кДа, мають високу спорідненість до свого гормону за рахунок стереоспецифічності. Молекулярний механізм дії стероїдних і тиреоїдних гормонів реалізується послідовністю таких клітинних і біохімічних реакцій: проникнення гормона всередину клітини через подвійний ліпідний шар клітинної мембрани → взаємодія гормона з цитозольним рецептором зі зміною конформації останнього та зниження спорідненості до білків-шаперонів, які від’єднуються від комплексу гормон-рецептор → утворення гормон-рецепторного комплексу → транслокація гормон-рецепторного комплексу в ядро → взаємодія комплексу зі специфічною ділянкою ДНК хроматину (енхансером або сайленсером) → зростання (при взаємодії з енхансером) або зниження (при взаємодії з сайленсером) доступності промотора для РНК-полімерази → збільшення (або зменшення) швидкості транскрипції мРНК → збільшення (або зменшення) швидкості трансляції → зміна кількості ферментних білків, які реалізують вплив гормона на метаболізм і функціональний стан клітини (рис. 11). 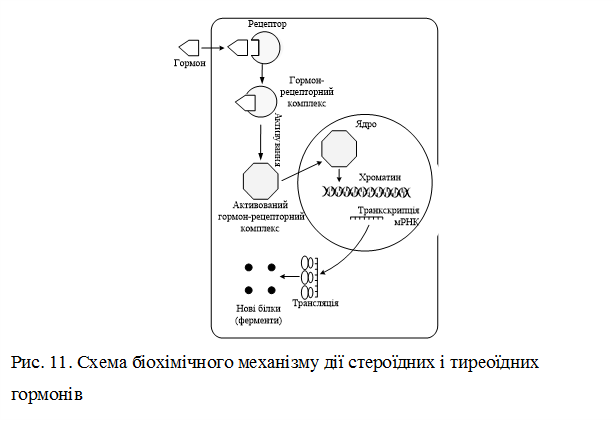 Взаємодія білкових рецепторів гормонів з ДНК відбувається в певних місцях промоторних ділянок геному, що знаходяться "зліва" від сайтів ініціації транскрипції (приблизно 250 нуклеотидів) і регулюють експресію розташованих на відстані генів (справа від промотора та сайту ініціації транскрипції). Ділянки ДНК, які можуть взаємодіяти з доменами гормонального рецептора, мають будову паліндромів і складаються зі специфічних для кожного рецептора 6 пар нуклеотидних послідовностей, розташованих зліва та справа від проміжної 3-нуклеотидної послідовності (-NNN-) – " спейсера". Отже, на відміну від білкових гормонів, що спричинюють активацію ферментів, дія на клітини-мішені стероїдних гормонів призводить до стимуляції біосинтезу нових ферментних молекул за рахунок активації процесів транскрипції їх мРНК. |
