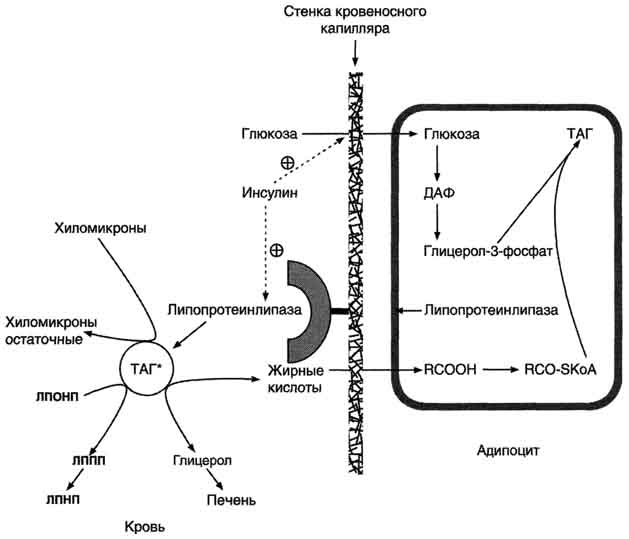
Обмен липидов коллоквиум вопросы
 Скачать 337.5 Kb. Скачать 337.5 Kb.
|
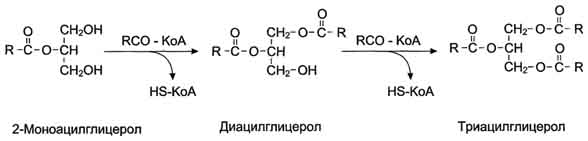
КоА участвует в реакции этерификации 2-моноацилглицерола с образованием сначала диацилгли-церола, а затем триацилглицерола. Реакции ресинтеза жиров катализируют ацилтранеферазы. Всасывание продуктов переваривания липидов в тонком кишечнике. Ресинтез липидов в энтероцитах и его биологическое значение. Гепатоэнтеральная циркуляция желчных кислот. Основные пути превращений хиломикронов. Всасывание продуктов гидролиза липидов в тонком кишечнике. ресинтез жиров Образование смешанных мицелл и всасывание продуктов гидролиза Продукты гидролиза липидов - жирные кислоты с длинным углеводородным радикалом, 2-моноацилглицеролы, холестерол, а также соли жёлчных кислот образуют в просвете кишечника структуры, называемые смешанными мицеллами. Смешанные мицеллы построены таким образом, что гидрофобные части молекул обращены внутрь мицеллы, а гидрофильные - наружу, поэтому мицеллы хорошо растворяются в водной фазе содержимого тонкой кишки. Стабильность мицелл обеспечивается в основном солями жёлчных кислот. Мицеллы сближаются со щёточной каймой клеток слизистой оболочки тонкого кишечника, и липидные компоненты мицелл диффундируют через мембраны внутрь клеток. Вместе с продуктами гидролиза липидов всасываются жирорастворимые витамины A, D, Е, К и соли жёлчных кислот. Наиболее активно соли жёлчных кислот всасываются в подвздошной кишке. Жёлчные кислоты далее попадают через воротную вену в печень, из печени вновь секретируются в жёлчный пузырь и далее опять участвуют в эмульгировании жиров. Этот путь жёлчных кислот называют "энтерогепатическая циркуляция". Каждая молекула жёлчных кислот за сутки проходит 5- 8 циклов, и около 5% жёлчных кислот выделяется с фекалиями. Всасывание жирных кислот со средней длиной цепи, образующихся, например, при переваривании липидов молока, происходит без участия смешанных мицелл. Эти жирные кислоты из клеток слизистой оболочки тонкого кишечника попадают в кровь, связываются с белком альбумином и транспортируются в печень. Ресинтез жиров в слизистой оболочке тонкого кишечника После всасывания продуктов гидролиза жиров жирные кислоты и 2-моноацилглицеролы в клетках слизистой оболочки тонкого кишечника включаются в процесс ресинтеза с образованием триацилглицеролов (рис. 8-16). Жирные кислоты вступают в реакцию этерификации только в активной форме в виде производных коэнзима А, поэтому первая стадия ресинтеза жиров - реакция активации жирной кислоты: HS КоА + RCOOH + АТФ → R-CO |
| Вид | Размеры | Функция |
| Липопротеины высокой плотности (ЛВП) | 8-11 нм | Транспорт холестерина от периферийных тканей к печени |
| Липопротеины низкой плотности (ЛНП) | 18-26 нм | Транспорт холестерина, триацилглицеридов и фосфолипидов от печени к периферийным тканям |
| Липопротеины промежуточной (средней) плотности ЛПП (ЛСП) | 25-35 нм | Транспорт холестерина, триацилглицеридов и фосфолипидов от печени к периферийным тканям |
| Липопротеины очень низкой плотности (ЛОНП) | 30-80 нм | Транспорт холестерина, триацилглицеридов и фосфолипидов от печени к периферийным тканям |
| Хиломикроны | 75-1200 нм | Транспорт холестерина и жирных кислот, поступающих с пищей, из кишечника в периферические ткани и печень |
Нековалентная связь в липопротеинах между белками и липидами имеет важное биологическое значение. Она обусловливает возможность свободного обмена липидов и модуляцию свойств липопротеинов в организме.
Липопротеины являются:
структурными элементами мембран клеток животных организмов;
транспортными белками, транспортирующими холестерин и другие стероиды, фосфолипиды и др.
Апопротеин А1 синтезируется также в кишечнике, где входит в состав хиломикронов, но при липолизе в крови быстро переносятся на ЛВП. Апопротеин С синтезируется в печени, выделяется в кровоток и уже в кровотоке переносится на ЛВП. Новообразованный ЛВП похож на диск: фосфолипидный бислой, включающий свободный холестерин и апопротеин. Апопротеин А1 — активатор фермента лецитинхолестеринацилтрансферазы (ЛХАТ). Этот фермент связан с поверхностью ЛВП в плазме крови. ЛХАТ катализирует реакцию между фосфолипидом ЛВП и свободным холестерином частицы. При этом образуются эфиры холестерина и лизолецитин. Неполярные эфиры холестерина перемещаются внутрь частицы, освобождая место на поверхности для захвата нового холестерина, лизолецитин — на альбумин крови. Неполярное ядро раздвигает бислой, ЛВП приобретает сферическую форму. Этерифицированный холестерин переносится с ЛВП на ЛОНП, ЛНП и хиломикроны специальным белком ЛВП — переносчиком эфиров холестерола (апопротеин D), в обмен на фосфолипиды и триглицериды. ЛВП поглощается клетками печени с помощью рецепторного эндоцитоза через рецептор апопротеина Е.
Специфичности рецепторов апопротеинов Е и В-100 частично пересекаются. Они находятся на поверхности мембран клеток в клатриновой кавеоле. При соединении с лигандами кавеола замыкается в везикулу и липопротеин эндоцитируется. В лизосомах эфиры холестерина гидролизуются и холестерин поступает в клетку.
Липолиз. Бета-окисление высших жирных кислот. Биологическое значение. Локализация в клетке, схема процесса, энергетический эффект.
Липо́лиз — процесс расщепления жиров на составляющие их жирные кислоты под действием липазы.
Липолиз протекает в митохондриях, куда жирные кислоты доставляются с помощью переносчика — карнитина. В процессе липолиза происходят циклические превращения молекул жирных кислот с отщеплением от них двухуглеродных производных KoA (CH3—CO—SKoA) (β-окисление жирных кислот) или одноуглеродных производных KoA (α-окисление жирных кислот); протекание одного цикла окисления жирной кислоты, сопровождается синтезом по одной молекуле ФАДН и НАДН.
Фермент триглицеридлипаза расщепляет триглицериды на диглицериды и жирные кислоты, на следующей стадии активны диглицеридлипаза и моноглицеридлипаза. В результате работы этих ферментов образуются конечные продукты липолиза — глицерин и жирные кислоты.
Липолиз является важнейшим энергетическим процессом в клетке, который обеспечивает синтез самого большого количества АТФ. Например, при окислении одной молекулы пальмитата (CH3(CH2)14COOH), образуется 131 молекула АТФ, две из которых используются для активации пальмитата.
Окисление ВЖК происходят в митохондриях клеток, и называется бетта окислением. Доставка их к тканям и органам происходит при участии альбумина, а транспорт из цитоплазмы в митохондрии при участии карнитина.
Процесс бета-окисления ВЖК складывается из следующих этапов:
-активация ВЖК на наружной поверхности мембраны митохондрий при участии АТФ, конзима А и ионов магния с образованием активной формы ВЖК (ацил - КоА).
-транспорт жирных кислот внутрь митохондрий возможен при присоединении активной формы жирной кислоты к карантину, находящемуся на наружной поверхности внутренней мембраны митохондрий. Образуется ацил-карнитин, обладающий способностью проходить через мембрану. На внутренней поверхности комплекс распадается и карнитин возвращается на наружную поверхность мембраны.
-внутримитохондриальное окисление жирных кислот состоит из последовательных ферментативных реакций. В результате одного завершенного цикла окисления происходит отщепление от жирой кислоты одной молекулы ацетил-КоА, т.е. укорочение жирнокислотной цепи на два углеродных атома.Приэтом в результате двух дегидрогеназных реакций восстанавливается ФАД до ФАДН2 и НАД+ до НАДН2.
Распад глицерина. Схема процесса, энергетический эффект. Анаболические превращения глицерина.
При окислении глицерина образовались конечные продукты:
СО2 на этапе превращения:
1. ПИРУВАТА
2. ИЗОЦИТРАТА
3. Альфа-КЕТОГЛУТАРАТА
Н2О на этапе превращения:
1 . альфа -ГЛИЦЕРОФОСФАТА
2. ГЛИЦЕРАЛЬДЕГИД-3-ФОСФАТА
3. 2-ФОСФОГЛИЦЕРАТА
4. ПИРУВАТА
5. ИЗОЦИТРАТА
6. Альфа-КЕТОГЛУТАРАТА
7. СУКЦИНАТА
8. МАЛАТА
АТФ выделилось за счёт реакций
А) Субстратного фосфорилиования на этапах превращения:
1. 1,3-дифосфоглицерата
2.2-фосфоенолпирувата
3.Сукцинил-КоА
Б) Окислительного фосфорилирования на этапах превращения:
1.Альфа-глицерафосфата
2.Глицеральдегид-3 фосфата
3.Пирувата
4.Изоцитрата
5. Альфа-КЕТОГЛУТАРАТА
6.Сукцината
7.Малата
Если глицерин распадается по пути к углеводам, то происходит дегидрирование.
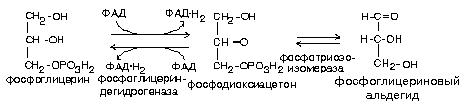
Митохондриальная фосфоглицериндегидрогеназа содержит в качестве небелковой части ФАД, а цитоплазматическая - НАД. В митохондриях отщепляемый водород переносится по укороченной цепи митохондриального окисления, и образуется 2 молекулы АТФ (фосфоглицерин (ФГА) - субстрат укороченной цепи).
Для фосфоглицеринового альдегида существует два варианта дальнейших превращений:
ФГА может окисляться в ГБФ-пути до СО2 и Н2О с образованием 21 молекулы АТФ.
ФГА может вступить в реакции гликонеогенеза с образованием углеводов - глюкозы или гликогена (смотрите тему «Метаболизм углеводов и его регуляция»).
Суммарный энергетический эффект окисления одной молекулы глицерина равен 22 АТФ.
Липогенез в печени и жировой ткани. Виды жировой ткани, особенности метаболизма. Ожирение. Роль лептина.
Синтез жиров в жировой ткани и печени
Синтез жиров происходит в абсорбтивный период в печени и жировой ткани. Непосредственными субстратами в синтезе жиров являются ацил-КоА и глицерол-3-фосфат. Метаболический путь синтеза жиров в печени и жировой ткани одинаков, за исключением разных путей образования глицерол-3-фосфата.
Образование глицерол-3-фосфата
Синтез жиров в печени и жировой ткани идёт через образование промежуточного продукта - фосфатидной кислоты (рис. 8-21).
Предшественник фосфатидной кислоты - глицерол-3-фосфат, образующийся в печени двумя путями:
восстановлением дигидроксиацетонфосфата - промежуточного метаболита гликолиза;
фосфорилированием глицеролкиназой свободного глицерола, поступающего в печень из крови (продукт действия ЛП-липазы на жиры ХМ и ЛПОНП).
В жировой ткани глицеролкиназа отсутствует, и восстановление дигидроксиацетонфосфата - единственный путь образования глицерол-3-фосфата. Следовательно, синтез жиров в жировой ткани может происходить только в абсорбтивный период, когда глюкоза поступает в адипоциты с помощью белка-переносчика глюкозы ГЛЮТ-4, активного только в присутствии инсулина, и распадается по пути гликолиза.
Синтез жиров в жировой ткани
В жировой ткани для синтеза жиров используются в основном жирные кислоты, освободившиеся при гидролизе жиров ХМ и ЛПОНП (рис. 8-22). Жирные кислоты поступают в адипоциты, превращаются в производные КоА и взаимодействуют с глицерол-3-фосфатом, образуя сначала лизофосфатидную кислоту, а затем фосфатидную. Фосфатидная кислота после дефосфорилирования превращается в диацилглицерол, который ацилируется с образованием триацилглицерола.
Кроме жирных кислот, поступающих в адипоциты из крови, в этих клетках идёт и синтез жирных кислот из продуктов распада глюкозы. В адипоцитах для обеспечения реакций синтеза жира распад глюкозы идёт по двум путям: гликолиз, обеспечивающий образование глицерол-3-фосфата и ацетил-КоА, и пентозофосфатный путь, окислительные реакции которого обеспечивают образование NADPH, служащего донором водорода в реакциях синтеза жирных кислот.
Молекулы жиров в адипоцитах объединяются в крупные жировые капли, не содержащие воды, и поэтому являются наиболее компактной формой хранения топливных молекул. Подсчитано, что, если бы энергия, запасаемая в жирах, хранилась в форме сильно гидратированных молекул гликогена, то масса тела человека увеличилась бы на 14-15 кг.
392
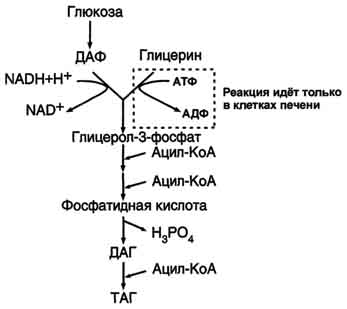
Рис. 8-21. Синтез жиров в печени и жировой ткани.
Синтез ТАГ в печени. Образование ЛПОНП в печени и транспорт жиров в другие ткани
Печень - основной орган, где идёт синтез жирных кислот из продуктов гликолиза. В гладком ЭР гепатоцитов жирные кислоты активируются и сразу же используются для синтеза жиров, взаимодействуя с глицерол-3-фосфатом. Как и в жировой ткани, синтез жиров идёт через образование фосфатидной кислоты. Синтезированные в печени жиры упаковываются в ЛПОНП и сек-ретируются в кровь (рис. 8-23).
В состав ЛПОНП, кроме жиров, входят холестерол, фосфолипиды и белок - апоВ-100. Это очень "длинный" белок, содержащий 11 536 аминокислот. Одна молекула апоВ-100 покрывает поверхность всего липопротеина.
ЛПОНП из печени секретируются в кровь (рис. 8-23), где на них, как и на ХМ, действует ЛП-липаза. Жирные кислоты поступают в ткани, в частности в адипоциты, и используются для синтеза жиров. В процессе удаления жиров из ЛПОНП под действием ЛП-липазы ЛПОНП сначала превращаются в ЛГШП, а затем в ЛПНП. В ЛПНП основными липидными компонентами служат холестерол и его эфиры, поэтому ЛПНП являются липопротеинами, доставляющими холестерол в периферические ткани. Глицерол, освободившийся из липопротеинов, кровью транспортируется в печень, где опять может использоваться для синтеза жиров.
Скорость синтеза жирных кислот и жиров в печени существенно зависит от состава пищи. Если в пище содержится более 10% жиров, то скорость синтеза жиров в печени резко снижается.
Б. Мобилизация жиров из жировой ткани
Адипоциты (место депонирования жиров) располагаются в основном под кожей, образуя подкожный жировой слой, и в брюшной полости, образуя большой и.малый сальники. Мобилизация жиров, т.е. гидролиз до глицерола и жирных кислот, происходит в постабсорбтивный период, при голодании и активной физической работе. Гидролиз внутриклеточного жира осуществляется под действием фермента гормончувствительной липазы - ТАГ-липазы. Этот фермент отщепляет одну жирную кислоту у первого углеродного атома глицерола с образованием диацилглицерола, а затем другие липазы гидролизуют его до глицерола и жирных кислот, которые поступают в кровь. Глицерол как водорастворимое вещество транспортируется кровью в свободном виде, а жирные кислоты (гидрофобные молекулы) в комплексе с белком плазмы - альбумином.
393