Пат физ устно экзамен. патфиз устно. Общая патофизиология патофізіологія як наука та навчальна дисципліна. Методи патофізіології
 Скачать 1.7 Mb. Скачать 1.7 Mb.
|
|
33.50. Что такое зоб? Какие его виды выделяют? Какой патогенез эндемического зоба? Зобом называют видимое увеличение щитовидной железы. Выделяют три вида зоба. 1. Диффузный токсический зоб- гипертиреоидный (болезнь Гревса, базедова болезнь). Характеризуется признаками гиперфункции щитовидной железы. 2. Спорадический зоб - эутиреоидный. Увеличение массы щитовидной железы не сопровождается выраженными изменениями ее функциональной активности. 3. Эндемический зоб - гипотиреоидной. Проявляется клиникой гипофункции щитовидной железы. Причиной эндемического зоба является недостаточное содержание йода в воде и продуктах питания, что связано с особенностями почвы и подземных вод в определенных регионах и местностях земного шара. Дефицит йода приводит к нарушению образования тире-оидних гормонов, содержание которых в крови уменьшается. Это вызывает усиление продукции тиреолиберин и тиреотропного гормона (ТТГ). Последний, воздействуя на ткань щитовидной железы, стимулирует процессы гипертрофии и гиперплазии - развивается зоб. Поскольку увеличение железы не устраняет дефицит тиреоидных гормонов (причину - недостаточность йода - не ликвидировано), то повышенная продукция ТТГ сохраняется и продолжается его действие на ткань железы зоб прогрессирует. 128. Порушення функції паращитоподібних залоз: види, причини, механізми розвитку, клінічні та патофізіологічні прояви. Порушення функції статевих залоз: первинні та вторинні стани гіпер- і гіпогонадизму. Причини та механізми розвитку, екстрагенітальні прояви порушень функції статевих залоз. Патологія епіфіза: гіпо- та гіперфункція, основні прояви. 33.51. Как осуществляется регуляция образования и секреции паратирина паращитовидных желез? Назовите основные биологические эффекты паратгормона. Образование и секреция паратирина (паратгормона) регулируется содержанием ионов кальция в плазме крови. Секреция этого гормона возрастает при уменьшении концентрации ионов Са 2+ в плазме, и наоборот, уменьшается при увеличении содержания этих ионов. Кроме того, высвобождение паратирина в кровь угнетает 24,25- (ОН) 2 витамин D, образующийся в почках (см. Разд. 24). Биологические эффекты паратирина (подробно см. Гл. 24): 1. Воздействие на костную ткань - активация функции остеокластов. 2. Действие на почки - угнетение реабсорбции фосфата. 3. Активация преобразования в почках витамина D в его гормональную форму- 1,25- (ОН) 2 витамин D. Следствием всех указанных эффектов является увеличение концентрации ионов кальция в плазме крови. 33.52. Каковы причины и чем проявляется гипопаратиреоз? Причины гипопаратиреоз -гипофункции паращитовидных желез: 1) случайное повреждение или удаление паращитовидных желез при операциях на щитовидной железе; 2) повреждения паращитовидных желез при лечении радиоактивным йодом болезней щитовидной железы; 3) аутоиммунные повреждения паращитовидных желез 4) врожденное недоразвитие паращитовидных желез; 5) нечувствительность клеток-мишеней к действию паратирина - псевдогипопаратиреоз. Основным проявлением гипопаратиреоз является гипокальциемия. Она обусловливает развитие паратиреопривнои тетании, что проявляется резким повышением нервно-мышечной возбудимости, множественными фибриллярная сокращениями мышц всего тела. затем возникают приступы клонических судорог, переходящие в тонические. Судорожные сокращения могут распространяться и на внутренние органы (пилороспазм, ларингоспазм). Во время одного из таких приступов наступает смерть. При хроническом гипопаратиреозе у животных развивается клиническая картина парат-реопривнои кахексии. Она характеризуется похуданием, анорексией, повышенной нервно-мышечной возбудимостью, диспепсией и разнообразными трофическими нарушениями. 33.53. Каковы причины и чем проявляется гиперпаратиреоз? Причины гиперпаратиреоза - гиперфункции паращитовидных желез: 1) опухоль - аденома паращитовидных железы; 2) гиперфункция паращитовидных желез, обусловленная уменьшением чувствительности их эндокринных клеток к ионам кальция - нарушение регуляции по принципу отрицательной обратной связи. Гиперпаратиреоз оказывается двумя группами связанных между собой изменений. И. Нарушение костной ткани-генерализованная фиброзная остеодистрофия. Обусловлена повышением активности остеокластов и подавлением функции остеобластов. Проявляется болью в костях и суставах, размягчением костей, резкой деформацией скелета. Развивается деминерализация костной ткани (остеомаляция), что обусловливает повышение содержания ионов кальция в плазме крови - гипер- кальциемии. II. Гиперкальциемия. С ней связаны: а) кальцификация мягких тканей (почек, сосудов, легких). В тяжелых случаях развивается почечная недостаточность б) образование кальциевых камней в почках; в) нарушение возбудимости нервной системы и мышц - мышечная слабость, депрессия, нарушение памяти; г) артериальная гипертензия; г) усиление желудочной секреции. 33.54. Как осуществляется регуляция образования и секреции мужских половых гормонов? Назовите их основные биологические эффекты. Эндокринные клетки семенников (интерстициальные клетки, или клетки Лейдига) синтезируют и секретируют мужские половые гормоны - андрогены, среди которых основным является тестостерон. Регуляция образования андрогенов осуществляется при участии системы гипоталамус-аденогипофиз по схеме: гипоталамус → гонадолиберина → аденогипофиз → злое-низуючий гормон → интерстициальные клетки семенников → тестостерон → клетки Сертоли семенников → ингибин → торможения функциональной активности соответствующих образований гипоталамуса и аденогипофиза → уменьшение образования гонадолиберина и лютеинизирующего гормона → уменьшение синтеза и секреции андрогенов → активация гипоталамуса и т. д. Основные биологические эффекты тестостерона: 1. Эмбриональное дифференцировки. Андрогены обеспечивают дифференцировки половых желез и половых органов в период эмбрионального развития. образующийся под влиянием хорионического гонадотропина (в период между 6 и 16 неделями), тестостерон активирует формирование мужских половых органов с вольфова пролива, урогениталь-ного синуса и бугорка, одновременно подавляя развитие женских половых органов. Кроме того, андрогены обеспечивают дифференцировки структур центральной нервной системы "по мужскому типу», определяя в дальнейшем мужской тип полового поведения. 2. Половое созревание и развитие вторичных половых признаков у особей мужского пола. Поскольку андрогены стимулируют деятельность сальных желез, то в пубертатном периоде кожа становится жирной, часто происходит инфицирование сальных желез - появляются угри. 3. Регуляция сперматогенеза. Тестостерон активирует деятельность миоэпителиальных клеток семенников (клеток Сертоли) и эпителиальных клеток протоков, которые в свою очередь оказывают влияние на интенсивность деления половых клеток и их созревания. Такое действие тестостерона не связана с поступлением его в кровь, а является местной. 4. Регуляция полового поведения. Андрогены имеют отношение к формированию полового влечения (либидо) и способности к копуляции. Это связано с тем, что тестостерон влияет на преоптическое зону гипоталамуса (центр полового поведения) и облегчает спинномозговые рефлексы, важные для копуляции. Временная недостаточность андрогенов в период половой дифференцировки и развития мозга приводит к формированию в дальнейшем гомосексуальной ориентации. 5. Анаболическое действие. Тестостерон активирует процессы белкового синтеза. Именно с этим связан влияние андрогенов на рост скелета и мышц (усиление роста костей в длину, увеличение мышечной массы). 33.55. Каковы причины и основные проявления мужского гипогонадизма? Мужской гипогонадизм - это гормональная недостаточность мужских половых за- лоз. Его причинами могут быть: и. Центральные (дисрегуляторные) нарушение-уменьшение образования гонадоли-берину в гипоталамусе, лютеинизирующего гормона в аденогипофизе. Это может быть связано с поражением указанных структур, а также с гиперфункцией эпифиза, в случае которой увеличение образования мелатонина сопровождается угнетением синтеза гонадотропных гормонов. II. Собственно железистые нарушения: а) кастрация - удаление семенников; б) фиброз яичек после некоторых вирусных инфекционных заболеваний, осложненных орхитом (например, после эпидемического паротита) в) нарушение развития яичек. После потери яичек развивается комплекс нарушений под названием евнухизм. Гипофункцию яичек при их сохранении обозначают термином "евнухоидизм". III. Периферические нарушения: а) уменьшение чувствительности клитин-мтшенеы к действию андрогенов; б) увеличенное связывание тестостерона с белками плазмы крови в) усиленное разрушение андрогенов в печени. Проявления мужского гипогонадизма зависят от того, в какой период онтогенеза он развивается. Гипогонадизм к периоду полового созревания может проявляться: • синдромом тестикулярной феминизации (наследственно обусловленным мужским псевдо-гермафродитизмом). Этот синдром обусловлен нарушениями дифференцировки половой системы по мужскому типу в период эмбриогенеза; • слабо выраженными вторичными половыми признаками; • угнетением сперматогенеза; • отсутствием полового влечения; • нарушением окостенения эпифизарных хрящей при сохраненном влиянии СТГ - развивается евнухоидный, или гипогонадний, гигантизм; ° слабым развитием скелетной мускулатуры (отсутствие анаболических эффектов андрогенов). Гипогонадизм после завершения полового созревания характерен, в частности, для процесса старения. Он проявляется: • некоторым уменьшением выраженности вторичных половых признаков; • нарушениями сперматогенеза; • развитием импотенции; • анаболическими нарушениями - уменьшением массы скелетных мышц и работоспособности. 33.56. Каковы причины и основные проявления мужского гипергонадизму? Мужской гипергонадизм может развиваться в детском возрасте до периода полового созревания и у взрослых. У детей гипергонадизм чаще всего связан с опухолями и воспалительными процессами в гипоталамусе, а также гипофункцией эпифиза. Все эти причины вызывают увеличение продукции гонадотропных гормонов и, как следствие, андрогенов. Клинически такой гипергонадизм оказывается преждевременным половым созреванием. Причиной гиперфункции половых желез у взрослых является добро- и злокачественные опухоли, растущие из интерстициальных клеток. При этом выраженных клинических признаков, связанных с гиперандрогенемии, нет. В случае злокачественных новообразований характерны отсутствие кахексии, сохранения мышечной массы и силы мышц. 33.57. Какие гормоны относятся к женских половых? Как осуществляется регуляция их образования и секреции? Местом синтеза женских половых гормонов являются яичники. Здесь образуется три группы гормонов. I. Эстрогены: эстрадиол, эстрон, эстриол. Продуцируются эпителиальными клетками фолликулов. II. Прогестишы, среди которых основным является прогестерон. Образуются клетками желтого тела. III. Минорные гормоны: ингибин (подавляет образование ФСГ в аденогипофизе) ирелаксин (размягчает лобковые сращения, тазовые связи, шейку матки, расслабляет гладкие мышцы матки). В регуляции образования и секреции женских половых гормонов решающее значение имеют система гипоталамус-аденогипофиз-яичники и механизмы положительного и отрицательного обратной связи. В передовуляцийний период под влиянием ФСГ усиливается образование и секреция эстрогенов, которые по принципу положительной обратной связи стимулируют образование гонадолиберина в гипоталамусе и лютеинизирующего гормона (ЛГ) в аденогипофизе (обеспечивают "пик ЛГ»). Последний вызывает повышение секреторной активности клеток, продуцирующих прогестины. В писляовуляцийний период эстрогены и прогестины по принципу отрицательной обратной связи подавляют образование гонадолиберина и гонадотропных гормонов аденогипофиза, что ведет в итоге к уменьшению секреции и самых женских половых гормонов. 33.58. Назовите основные биологические эффекты женских половых гормонов. I. Половое созревание и развитие вторичных половых признаков у особей женского пола. Эти эффекты обусловлены эстрогенами, секреция которых начинает расти в период полового созревания. II. Обеспечение! циклических изменений в организме женщины - подготовка половых органов к оплодотворению и имплантации яйцеклетки. Это осуществляется благодаря участию женских половых гормонов вместе с ФСГ и ЛГ в гормональном контроле овуляции и менструального цикла. III. Обеспечение беременности, родов и лактации. Так, эстрогены вызывают быстрый рост мышц матки, стимулируют рост системы протоков молочных желез. Прогестины блокируют сократительную активность беременной матки, стимулируют рост железистого эпителия молочных желез. С уменьшением продукции прогестинов плацентой связывают наступление родов. IV. Экстра генитальные эффекты. Эстрогены влияют на: а) костную ткань, обеспечивая условия для своевременного окостенения епифи-Зарн хрящей; б) печень, активируя синтез целого ряда белков (транспортных белков, факторов свертывания, ангиотензиногена, липопротеидов высокой плотности) в) кровеносные сосуды, регулируя процессы ангиогенеза, сосудистый тонус. С действием прогестинов связывают увеличение базальной температуры тела в писляовуляцийний период. 33.59. Каковы причины и основные проявления женского гипогонадизма? Выделяют следующие группы причин женского гипогонадизма. I. Центральные (дисрегуляторные) нарушения. Могут быть обусловлены психогенными факторами, поражениями гипоталамуса (дефицит гонадолиберина), гипофункцией аденогипофиза (дефицит ФСГ и ЛГ), гиперфункцией эпифиза (уменьшение образования гонадотропных гормонов при увеличении синтеза мелатонина). II. Собственно железистые нарушения: а) наследственно обусловлена аплазия яичников; б) дегенерация яичников (воспалительная, кистозная) в) аутоиммунное повреждение женских половых желез г) хирургическое удаление яичников. III. Периферические нарушения: а) уменьшение чувствительности клеток-мишеней к действию женских половых гормонов; б) повышенное связывание их белками плазмы крови в) усиленное разрушение женских половых гормонов в печени. Клинические проявления гипофункции половых желез зависят от времени наступления гипо- гонадизму. Если он развивается до наступления полового созревания, то формируется комплекс нарушений под названием "овариальный евнухоидизм": слабое развитие вторичных половых признаков, первичная аменорея, высокий рост. Развитие гипогонадизма в детородном возрасте сопровождается нарушениями циклических процессов в организме женщины (нарушения менструального цикла), бесплодием, преждевременным климаксом. После менопаузы развиваются климактерические изменения - нестабильность сосудистого тонуса, остеопороз и др. 33.60. Каковы причины и основные проявления женского гипергонадизму? В основе женского гипергонадизму, при котором увеличивается секреция женских половых гормонов, могут лежать центральные (дисрегуляторные) нарушения и собственно железистые причины. Центральные нарушения, обусловленные увеличением секреции гонадолиберина и гонадотропных гормонов, могут проявляться развитием синдрома преждевременного полового созревания и синдрома мнимой беременности. Для первого характерны раннее появление вторичных половых признаков, раннее начало менструаций и вероятность забеременеть (в возрасте 7-8 лет). Второй синдром проявляется аменореей и всеми внешними признаками беременности. При этом имеет место повышенная продукция пролактина клетками аденогипофиза. К собственно железистых причин женского гипергонадизму относят кистозные процессы и опухоли яичников, продуцирующих гормоны. При этом развивается гипертрофия эндометрия, нарушается менструальный цикл, возобновляются маточные кровотечения в менопаузе. 33.61. В чем сущность эндокринной функции эпифиза? Чем могут проявляться ее нарушения? Пинеалоцитов (эндокринные клетки эпифиза) продуцируют гормон мелатонин - производную соединение аминокислоты триптофана. Уровень его секреции зависит от освещенности сетчатки глаза, информация от которого через сложные проводнику пути, в том числе гипоталамус и спинной мозг поступает в эпифиз. В светлое время суток секреция мелатонина тормозится, в темноте, наоборот, растет. Так, у человека в ночное время (с 23 до 7 часов.) Высвобождается 70% общего суточного количества мелатонина. С секрецией мелатонина связывают функцию эпифиза, что ее обозначают как "биологические часы". Среди известных ныне биологических эффектов мелатонина - угнетение образования и секреции гонадотропных гормонов аденогипофиза, уменьшение продукции ТТГ, АКТГ и СТГ. Патологию эпифиза мало изучено. Известно, что при увеличении продукции мелатони-на происходит задержка полового развития, а при уменьшении его секреции, наоборот - преждевременное половое созревание. 33.62. Какими изменениями в организме могут проявляться нарушения эндокринной функции поджелудочной железы? Эндокринную функцию выполняют клетки островков поджелудочной железы, продуцирующие инсулин (бета-клетки) и глюкагон (альфа-клетки). Уменьшение синтеза и секреции инсулина приводит к развитию сахарного диабета (см. Разд. 20). Увеличение образования инсулина - гиперинсулинизм - бывает в случае возникновения опухолей, развивающихся из β-клеток панкреатических островков и продуцируют инсулин; при спонтанной идиопатической гипогликемии у детей на начальных стадиях сахарного диабета, при ожирении, демпинг-синдроме (состояние после резекции желудка), некоторых эндокринных заболеваниях (акромегалия, тиреотоксикоз, болезнь Иценко-Кушинга). Основные проявления гиперинсулинизма обусловленные гипогликемической, анаболическим и Мито-генной действием инсулина (см. Разд. 20). Под влиянием избытка инсулина развивается синдром гипогликемии (вплоть до гипогликемической комы), ожирение, склеротические поражения кровеносных сосудов. Второй гормон поджелудочной железы - глюкагон имеет гипергликемизирующее и липолитич-на действие, стимулирует секрецию инсулина. Увеличение секреции глюкагона бывает в случае развития опухоли с а-клеток островков поджелудочной железы (глюкагонома) и проявляется развитием вторичного сахарного диабета (см. Разд. 20). Описаны синдромы недостаточности глюкагона. Для них характерна спонтанная гипогликемия, которую наблюдают у детей. 129. Поняття про стрес як неспецифічну, стереотипну адаптаційну реакцію організму на дію надзвичайних подразників. Стадії розвитку загального адаптаційного синдрому. Механізми довготривалої адаптації. Поняття про стресорні ушкодження та «хвороби адаптації". Принципи запобігання стресорним ушкодженням. 33.38. Что такое стресс и общий адаптационный синдром? Стресс - это состояние напряжения неспецифических адаптационных механизмов, возникает в случае действия на организм избыточных по силе или патогенных факторов (рис. 155). Клинически стресс проявляется комплексом структурных, функциональных и биохимических изменений, получивших название общего адаптационного синдрома. Термин "стресс" впервые ввел в употребление Г. Селье в 1936 33.39. Морфологические признаки характерны для общего адаптационного синдрома? Действие на организм многочисленных патогенных факторов, независимо от их свойств и происхождения, дает стандартный ответ - так называемую морфологическую триаду: 1) гипертрофию коры надпочечников; 2) инволюцию тимико-лимфоцитарной системы (атрофия вилочковой железы и лимфатических узлов); 3) образование язв и эрозий в желудке и в кишечнике. 33.40. Какие стадии выделяют в развитии стресса? I. Стадия тревоги: а) пидстадии шока. Характеризуется кратковременным уменьшением резистентности к патогенного фактора; б) пидстадии контршоку. Сопротивляемость организма сначала возобновляется, а затем повышается. II. Стадия резистентности. Характеризуется стойким и длительным увеличением сопротивляемости организма как к фактору, который вызвал стресс, так и в других патогенных агентов. III. Стадия истощения. Наступает при очень интенсивной или длительной действия патогенного фактора, а также в условиях функциональной слабости адаптационных механизмов. Сопровождается уменьшением резистентности организма к патогенным воздействиям (рис. 156). " 33.41. Какие механизмы участвуют в реализации стресса? Многочисленные инициаторы стресса ( cmpecopu ) - травма, холод, боль, эмоции, кровотечение, физическая нагрузка, гипогликемия, инфекции и др. - за нарушения гомеостаза или предвестников такого нарушения вызывают возбуждение высших нервных регупя- торных центров и связанное с этим высвобождение большого количества гормонов. При этом большое значение имеют такие процессы. I. Активация системы гипоталамус-аденогипофиз. В результате происходит выделение АКТГ, СТГ, ТТГ, которые в соответствии стимулируют секрецию глюкокортикоидов, соматомединов, тиреоидных гормонов. II. Активация вегетативной нервной системы (симпатической и парасимпатической) сопровождается поступлением в кровь катехоламинов, инсулина, глюкагона. III. Активация альдостерон-вазопресиновои системы ведет к увеличению содержания в крови ангиотензина, альдостерона, вазопрессина (АДГ) (рис. 157). 33.42. Какое участие различных гормонов в развитии стресса? Гормоны, выделяемые во время стресса, определяют развитие трех последовательных фаз этой реакции. И. Острая фаза. Гормоны, высвобождающиеся в эту фазу, обеспечивают защиту от падения артериального давления и объ ему циркулирующей крови. Это достигается увеличением общего периферического сопротивления и сохранением воды в организме. Указанные реакции связаны с усиленным поступлением кровь катехоламинов, глюкокортикоидов, ангиотензина II, альдостерона, вазопрессина. ее. Подострая фаза. Характеризуется мобилизацией ресурсов для энергетического и пластического обеспечения систем, осуществляющих адаптацию. Этому служит перераспределение указанных ресурсов между активно функционирующими органами (сердце, головной мозг) и структурами, находятся в относительном покое (скелетные мышцы, пищеварительный канал, лимфоидная и жировая ткани). Метаболические изменения в эту фазу обусловлены увеличением секреции катехоламинов, глюкокортикоидов, глюкагона и уменьшением выделения инсулина. Приведенные выше контринсулярные гормоны, усиливая гликогенолиз, глюконеогенез, липолиз и протеолиз, вызывают увеличение содержания в крови глюкозы, аминокислот, свободных жирных кислот. III. Фаза долгосрочной адаптации. Характеризуется структурными изменениями (гипертрофией, гиперплазией) органов и тканей, обеспечивают адаптацию и находятся в состоянии гиперфункции. В ее реализации участвуют инсулин, СТГ, Соматомедин, тиреоидные гормоны, факторы роста - истинные и тканевые гормоны, активирующие анаболические процессы и формируют так называемый структурный след адаптации. 33.43. Что такое «болезни адаптации»? Какие заболевания к ним относят? Болезни адаптации- это заболевание, в развитии которых ведущая роль принадлежит избыточном стресса и так называемым стрессорным механизмам повреждения. При большой интенсивности и продолжительности стресс из механизма адаптации может превратиться в механизм патогенеза. К болезням адаптации относят: а) психосоматические заболевания (ишемической болезни сердца, гипертонической болезни, язвенной болезнью желудка и двенадцатиперстной кишки); б) болезни обмена веществ (сахарный диабет); в) аллергические и воспалительные заболевания (бронхиальную астму, ревматизм). 130. Загальна характеристика патології нервової системи, принципи класифікації порушень її діяльності. Особливості розвитку типових патологічних процесів у нервовій системі. 34.1. Как классифицируют нарушение деятельности нервной системы? I. По анатомическим принципу выделяют: 1) нарушение периферической нервной системы; 2) нарушение центральной нервной системы, в том числе нарушения функции спинного мозга, продолговатого, среднего и т. Д. ее. По происхождению выделяют наследственно обусловленные и приобретенные нарушения нервной системы. Приобретенные могут быть первичными и вторичными. Первичные расстройства возникают вследствие прямого действия на нервную систему патогенных факторов: физических (травма, радиация, термические воздействия), химических (токсины, яды), биологических (вирусы, бактерии), социальных (слово). Вторичные расстройства обусловлены прежде всего нарушениями гомеостаза (гипоксия, гипогликемия, ацидоз и т. П.), Иммунными факторами (аутоаллергическое реакции), расстройствами мозгового кровообращения. III. Клеточный принцип предусматривает такие виды нарушений функции нейронов: 1) нарушение электрофизиологических процессов; 2) расстройства нейрохимических (медиаторных) процессов; 3) нарушение Аксонный транспорта. IV. В зависимости от вида нарушенных функций различают следующие расстройства деятельности нервной системы: 1) нарушение сенсорных функций (чувствительности) 2) нарушение эффекторных функций: двигательной, вегетативной, трофической; 3) нарушение интегративных функций. 131. Порушення сенсорних функцій нервової системи. Розлади механо-, термо-, пропріо- і ноцицепції. Порушення проведення сенсорної інформації. Синдром Броун-Секара. Прояви ушкодження таламічних центрів і сенсорних структур кори головного мозку. 34.2. Которые выделяют виды нарушений соматовисцеральнои чувствительности? Понятие соматовисцеральнои чувствительности охватывает чувствительность кожи (тактильную, температурную, болевую), глубокую чувствительность (проприорецепцию) и болевую чувствительность всего тела (ноцицепции). Различают следующие виды нарушений соматовисцеральнои чувствительности: 1) гиперестезия - повышение чувствительности; 2) гипестезия - уменьшение чувствительности; 3) анестезия - отсутствие чувствительности. 34.3. Какие проводнику пути обеспечивают поступление информации о различных видах чувствительности от периферических рецепторов в центральную нервную систему? 1. лемнисковый путь (рис. 159). Проводит все виды глубокой (проприоцептивной) чувствительности, а также тактильную чувствительность от специализированных механорецепторов кожи (сложная тактильная чувствительность). Состоит из трех нейронов. Первые нейроны (И) - псевдоуниполярные клетки спинномозговых ганглиев. Аксоны этих клеток входят через задние корешки в спинной мозг и поднимаются вверх в составе задних канатиков, образуя пучки Голля и Бурдаха. Тела вторых нейронов (II) содержатся в продолговатом мозге (n. Gracilis и n. Cuneatus). их аксоны переходят на противоположную сторону, пересекаясь с аксонами контр-латеральных нейронов и образуют медиальную петлю (lemniscus medialis). Тела третьих нейронов (III) содержатся в таламусе. их аксоны идут в кору головного мозга, в соответствующие сенсорные зоны. 2. Антеро-латеральный путь (неоспиноталамичний тракт) (рис. 160). Проводит температурную, простейшие виды тактильной (от механочутливих свободных нервных окончаний) и кожную болевую (ранний боль) чувствительность. Первые нейроны (I) клетками спинномозговых ганглиев. Тела вторых (II) нейронов содержатся в задних рогах спинного мозга. их аксоны посегментно переходят на противоположную сторону спинного мозга, перекрещиваются и в составе боковых канатиков поднимаются в таламус, где содержатся тела третьих нейронов (III), посылают свои отростки в сенсорные зоны коры головного мозга. 3. Екстралемнисковий путь (рис. 161). Проводит болевую чувствительность (поздний боль, глубокий и висцеральный боль). В отличие от двух предыдущих, является багатонейронним и филогенетически более древним. Тела первых нейронов (и) содержатся в спинномозговых ганглиях, а вторых (II) - в задних рогах спинного мозга. Аксоны последних частично переходят на другую сторону, а частично с этой же стороны идут вверх в составе боковых канатиков, образуя два тракта: спиноретикулярний и палеоспиноталамичний. В ретикулярной формации ствола мозга, куда поднимаются аксоны вторых нейронов, происходит многократное переключение на другие нервные клетки. от ретикулярнои формации информация поступает в творения лимбической системы (эмоциональные компоненты реакций), центры гипоталамуса (вегетативные компоненты реакций), таламус, кору головного мозга и др. 34.4. Какие механизмы могут лежать в основе нарушений соматовисцеральнои чувствительности? 1. Нарушение рецепции. При увеличении порога возбуждения рецепторов возникает гипестезия, при уменьшении - гиперестезия. 2. Повреждение периферических нервов. При этом выпадают все виды чувствительности в зоне иннервации данного нерва. Как правило, зона выпадения чувствительности меньше зоны иннервации, объясняющих некоторым перекрыванием зон иннервации различных нервов. 3. Повреждение задних корешков спинного мозга. Характеризуется выпадением всех видов чувствительности в зоне соответствующих сегментов. 4. Повреждение спинного мозга. При пересечении половины спинного мозга (левой или правой) развивается синдром Броун-Секара (см. запрос. 34.5). Полное сечение спинного мозга ведет к исчезновению всех видов чувствительности с обеих сторон ниже уровня пересечения. 5. Нарушение функции подкорковых структур, участвующих в осуществлении сенсорных функций. Наибольшее значение имеет поражение ядер таламуса. 6. Поражение сенсорных зон коры головного мозга. Нарушение нейронов постцен-тральной извилины причиной расстройств сложной тактильной и проприоцеп-тивной чувствительности на противоположной стороне тела. Повреждения теменной доли вызывает развитие комплекса нарушений под названием "аморфосинтез". У человека (не является левшой) аморфосинтез обнаруживают после удаления коры правого полушария большого мозга. При этом исчезает представление о пространственном расположении частей тела на противоположной стороне. Человек не может надеть одежду или привести его в порядок на левой половине, не может побрить левую половину лица или зачесать волосы на левом боку. Если же поражены теменную долю с левой стороны, то аморфосинтез дополняется агнозией - неспособностью распознавать части тела, предметы, их изображения и расположения в пространстве. 34.5. Когда возникает синдром Броун-Секара? Чем он проявляется? Синдром Броун-Секара развивается после пересечения половины спинного мозга (левой или правой). Характеризуетсядиссоциацией расстройств чувствительности. Так, ниже уровня пересечения с той же стороны выпадают проприоцептивная и сложные виды тактильной чувствительности (повреждается лемнисковый путь к его пересечения), а с противоположной стороны - температурная, простая тактильная и частично болевая чувствительность (повреждается антеро-латеральный путь после пересечения). 132. Біль. Особливості болю як виду чутливості. Принципи класифікації болю. Соматичний біль. Вісцеральний біль. Сучасні уявлення про причини та патогенез болю: теорія розподілу імпульсів («ворітна теорія»), теорія специфічності. Патологічний біль: невралгія, каузалгія, фантомний, таламічний. Периферичні, периферично - центральні і центральні механізми розвитку патологічного болю. Емоційні, вегетативні, рухові реакції організму на біль. Емоційно-больовий стрес, больовий шок. Природні антиноцицептивні механізми. Принципи та методи протибольової терапії. 34.6. Что такое боль? Чем он отличается от других видов чувствительности? Боль - это неприятное сенсорное и эмоциональное ощущение, связанное с угрозой или самим повреждением тканей. Особенности боли как вида чувствительности: 1. Боль дает мало информации об окружающем мире, зато информирует об опасности, которая может возникнуть или уже возникла вследствие действия повреждающих факторов, - защитная функция боли. 2. В отличие от других видов чувствительности к боли не развивается адаптация. В связи с этим боль может быть причиной страданий больного. 3. Боль сопровождается сложными эмоциональными, вегетативными и двигательными реакциями. 4. Боль может быть патогенетическим механизмом развития генерализованных патологических процессов, в частности шока. 34.7. Как классифицируют боль? I. По клинической характеристикой (субъективным ощущением) боль может быть острый и тупой, локализованный и диффузный, иметь характер пощипывание, покалывание, жара и т. П. II . В зависимости от продолжительности болевых ощущений боль может быть острым и хроническим. Острая боль быстро проходит после прекращения действия болевых стимулов, хронический является длительным, он приносит страдания больному. III . По значению для организма боль может быть физиологическим и патологическим. Физиологический боль имеет защитное значение. Он сигнализирует о повреждении или его возможность, инициирует определенные поведенческие реакции, направленные на устранение повреждения, ограничивает функции пораженного органа. Патологический боль не несет сигнальной функции, он становится механизмом нарушения жизнедеятельности, в том числе и мозга, приводит к расстройствам функций различных органов и систем. IV . По механизмам развития различают соматический и висцеральный боль. Соматический боль разделяют на поверхностный иглубокий (рис. 162). 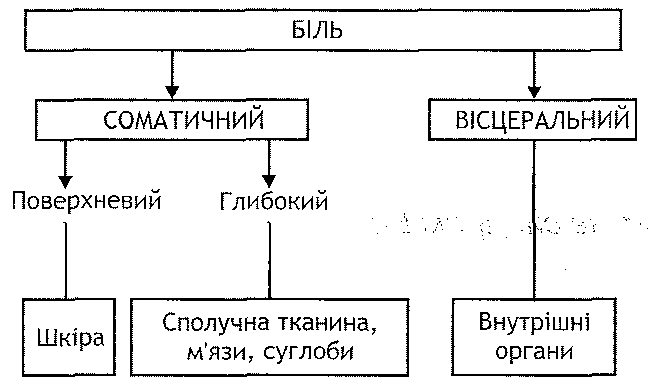 Рис. 162. Классификация боли по механизмам развития 34.8. Что такое соматический поверхностный боль? На какие виды его разделяют? Соматический поверхностный боль - это боль, возникающая в коже. Различают два его вида: ранней и поздней боль. Если нанести сильную механическую травму, то сразу же возникает острый, резкий, хорошо локализованная боль быстро проходит после завершения действия патогенного фактора - это так называемый ранний боль. Через некоторое время (0,5-1 с) возникает поздний боль. Это тупая, ноющая, диффузный боль. Он продолжается еще некоторое время после прекращения действия патогенного фактора. 34.9. Дайте сравнительную характеристику раннего и позднего боли.
34.10. Что такое соматический глубокую боль? Приведите примеры. Соматический глубокую боль - это боль, возникающая в глубоких тканях. К нему относят головная, зубная боль, боль в мышцах и суставах. Имеет много общего с поздним соматическим поверхностным болью. Он часто тупой, не имеет четкой локализации, сопровождается аффективными (общее недомогание, болезненное состояние) и вегетативными (тошнота, потливость, снижение артериального давления) реакциями. Подробно см. характеристику позднего боли (запрос. 34.9). 34.11. Что такое висцеральный боль? Чем он характеризуется? Висцеральный боль - это боль, возникающая во внутренних органах. Его источниками могут быть париетальная брюшина и корень брыжейки, париетальная плевра и перикард, мышечные органы (сердце, артерии, полые органы). Развитие боли в гладкомышечных полых органах может быть связан как с быстрым и резким их растяжением, так и с сильным сокращением (спазмом) гладких мышц, вследствие чего нарушается кровоснабжение и возникает ишемия. Приступы такой боли получили название колик. Для висцеральной боли характерны: 1) аффективные реакции (подавленное эмоциональное состояние, общее недомогание, состояние болезни) 2) вегетативные реакции "- тошнота, потливость, падение артериального давления 3) рефлекторное сокращение скелетных мышц (напряжение мышц брюшной стенки, вынужденная поза и др.). 34.12. Какие бывают виды боли в зависимости от его локализации? 1. Местный боль - локализуется в месте действия раздражителя; там, где развивается патологический процесс. 2. Проекционный боль - место, на которое действует болевой раздражитель, не совпадает с тем, где боль ощущается. Например, при повреждении межпозвоночных дисков сдавливаются спинномозговые нервы. При этом болит и участок, получает иннервацию от ущемленного нерва, то есть имеет место проекция боли на участки, иннервацию которых осуществляет поврежден нерв. 3. Отраженный (иррадийований, рефлекторный) боль. Болевое ощущение, возникающее в результате воздействия на внутренние органы, часто локализуется не в данном органе (или не только в нем), а в отдаленных поверхностных участках кожи. Боль всегда отражается на участки периферии, которые получают иннервацию от того же сегмента спинного мозга, и пораженный внутренний орган. Если речь идет о поверхность кожи, то боль отражается на определенном дерматомы. Поскольку органы получают иннервацию более чем от одного спинномозгового сегмента, то боль отражается на нескольких дерматомах. Вместе они образуют зону Геда для данного органа. 34.13. Назовите возможные причины боли. Боль вызывают болевые стимулы - факторы, обусловливающие сильное раздражение или повреждение ткани. К ним относят: 1) механические болевые стимулы; 2) термические болевые стимулы (температура выше 45 ° С); 3) химические болевые стимулы - ацетилхолин, серотонин, гистамин, кинины, простагландины Е субстанция Р, ионы Н + (при рН <6), ионы К + (при концентрации более 20 ммоль / л); 4) повреждения нервных проводников. 34.14. Какие существуют теории механизмов боли? I. Теория интенсивности. ее сторонники считают, что в организме нет специальных болевых рецепторов. Боль возникает в том случае, когда низькопорогови механо и терморецепторы стимулируются с интенсивностью, превышающей определенный уровень. Если фактор действует с низкой или средней интенсивностью, то возникает тактильное или температурное чувство, если же интенсивность высока - то ощущение боли. II. Теория распределения импульсов. ее сущность заключается в том, что болевой стимул вызывает особый ход нервных импульсов, отличающийся от распространения разрядов, которые возникают при воздействии неушкоджувальних факторов. На этом строится так называемая "воротная теория" боли (Мелзак, Уолл), что придает большое значение в формировании болевых ощущений желатинозного субстанции спинного мозга (substantia gelatmosa, SG; рис. 164). Нейроны SG осуществляют пресинаптическое торможения, блокируя прохождение импульсов в нейроны задних рогов спинного мозга по толстых и тонких нервных волокнах. Если нейроны SG возбуждаются, происходит пресинаптическое торможения - "ворота" закрыты. Если нейроны SG сами заторможены, то пресинаптическое торможения снимается - "ворота" открыты. Интенсивная стимуляция толстых миелинизированных нервных волокон вызывает возбуждение нейронов SG - "ворота" закрываются, и проведение импульсов в спинной мозг уменьшается. При интенсивном возбуждении тонких немиелинизированные волокон, проводящих боль, происходит торможение нейронов SG - снимается пресинаптическое торможения и облегчается поступления импульсов в задние рога спинного мозга. III. Теория специфичности. Предполагает существование специфических болевых рецепторов - ноцщепторив. Они отвечают только на интенсивные стимулы и таким образом участвуют в формировании болевых ощущений. Выделяют следующие виды ноцицепторов: а) механочутливи ноцицепторы (содержатся в коже, скелетных мышцах) б) термочувствительные ноцицепторы - возбуждаются при температуре выше 45 ° С (рецепторы горячего) в) полимодальные ноцицепторы - возбуждаются как механическими, так и температурными болевыми стимулами; г) хемочутливи ноцицепторы - возбуждаются химическими болевыми стимулами; д) висцеральные ноцицепторы - возбуждаются растяжением стенки гладкомышечные вых органов или спастическим сокращением. 34.15. Что такое хроническая боль? Назовите его клинические формы. Хроническим называют сильный, длительный боль, истощает, приносит страдания больному. Выделяют следующие формы хронической боли. 1. Невралгия- болевой синдром, связанный с нарушениями функции периферического нерва при вирусных инфекциях, авитаминозах, нарушениях кровообращения, расстройствах обмена веществ (сахарный диабет). Особенно тяжелой является невралгия тройничного нерва, которая проявляется приступами настолько сильной боли, что больные не в состоянии принимать пищу и разговаривать. Возникновение такой боли провоцирует действие очень слабых раздражителей, например, прикосновение к углу рта. 2. Каузалгия - сильный жгучая боль, возникающая при повреждении крупных соматических нервов (неполное пересечения нерва). У больного возникает ощущение, будто на кожу льют кипяток или прикладывают руку к раскаленных предметов, или держат ее в огне. Даже легкое прикосновение к коже, что ее иннервирует поврежден нерв, вызывает нестерпимую боль. Кроме того, боль могут провоцировать неожиданные зрительные и слуховые раздражители. 3. Фантомная боль. Возникает после ампутации конечностей - "болит" концовка, которой уже нет. При этом боль очень сильная и часто невыносим. 4. таламического боль - тяжелый спонтанную боль во всей половине тела с гиперпатия (субъективным впечатлением повышенной чувствительности). Развивается при поражениях ядер таламуса. 34.16. Какие механизмы могут лежать в основе формирования хронической боли? |
