Общие рекомендации
 Скачать 4.72 Mb. Скачать 4.72 Mb.
|
|
Паразиты рода Лейшмания. Обитают в организме позвоночных, где они встречаются в лейшманиальной безжгутиковой внутриклеточной форме. В их организме превращаются в лептомональную жгутиковую форму. Попадая в организм человека, вызывают лейшманиозы – трансмиссивные тропические и субтропические заболевания человека и животных. Лейшмания доновани, 1903г. Селезенка больного человека. Индийский кала-азар, черная лихорадка, дум-дум, висцеральный лейшманиоз. Попадая в организм с кровью больного, лейшмании образуют жгутиковую форму. Висцеральный лейшманиоз часто поражает детей до 12 лет. У переболевших вырабатывается стойкий иммунитет. Течение болезни характеризуется анемией, лейкопенией, волнообразной лихорадкой. Встречается в Индии, Кении, Азии, Казахстане Закавказье. Диагностика – пунктаты костного мозга, лимфатических узлов, мазки крови. Тропическая лейшмания. Болезнь Боровского (1898), кожный лейшманиоз. Характеризуется поражениями кож, образованием язв, после которых остаются рубцы. Размер язв до 10-15 см. существует антропонозный, поздно проявляющийся подтип кожного лейшманиоза, встречающийся в городах и поселках городского типа на Ближнем Востоке, Южной Европе, индии. Основной источник – человек, переносчик - москиты. Язвы образуются на открытых участках тела, затем они рубцуются. Зоонозный подтип (раноизъязвляющийся, полупустынно-сельский, остро некротизирующий, Пендинская язва). Имеет сезонность с лётом москитов. Резервуар – мыши, суслики, особенно – большая песчанка. Москиты питаются кровью в сумерки, в природе существует очаг. При зоонозном подвиде чаще поражаются нижние конечности. Язвы могут также покрывать все тело. Подтип распространен в Азии, Африке, на юге России, Туркмении, Узбекистане. Диагностика – по обнаружению простейших в кожных пробах вокруг ран. Лейшмании Leischmania (кл. Жгутиковые) — возбудители лейшманиозов. Заболевания человека вызываются несколькими видами и подвидами паразитов, которые объединяются в четыре комплекса: L. donovani — возбудитель висцерального лейшманиоза, L. tropica — возбудитель кожного лейшманиоза, L. mexicana — возбудитель лейшманиоза Центральной Америки, L. brasiliensis — возбудитель бразильского лейшманиоза. Все виды сходны морфологически и имеют одинаковые циклы развития. Они существуют в двух формах: в безжгутиковой, или лейшманиальной, и жгутиковой; или промастиготной (рис. 19.8). Лейшманиальная форма очень мелка — 3—5 мкм в диаметре. Характерной чертой ее является круглое ядро, занимающее около '/4 цитоплазмы; жгутика нет, но перпендикулярно клеточной поверхности располагается палочковидный кинетопласт. Эти формы обитают в клетках ретикулоэндотелиальной системы человека и ряда млекопитающих (грызунов, собак, лис). Промастиготная форма удлинена — до 25 мкм, спереди находится жгутик, у основания которого хорошо виден такой же кинетопласт, что и в безжгутиковой стадии паразита. Обитает в пищеварительной системе москитов. Безжгутиковая форма, посеянная на культуральную среду, превращается в жгутиковую. Лейшманиозы широко распространены в странах с тропическим и субтропическим климатом на всех континентах там, где обитают москиты. Они—типичные природно-очаговые заболевания (см. § 18.13). Природными резервуарами являются грызуны, дикие и домашние хищники. Заражение человека происходит при укусе инвазированными москитами. По патогенному действию лейшманий заболевания, которые они вызывают, делят на три основные формы: кожный, слизисто-кожный и висцеральный лейшманиозы. При кожном лейшманиозе очаги поражения находятся в коже. Это самый распространенный тип лейшманиоза, протекающий относительно доброкачественно. Возбудителями кожного лейшманиоза в Африке и Азии являются L. tropica, а в Западном полушарии — L. mexicana и ряд штаммов L. brasiliensis. Лейшманий L. tropica и L. mexicana вызывают на коже длительно не заживающие язвы на месте укусов москитами. Язвы заживают через несколько месяцев после образования, а на их месте на коже остаются глубокие рубцы. Некоторые формы L. brasiliensis способны распространяться по лимфатическим сосудам кожи с образованием многочисленных кожных язв в отдалении от мест укусов. Слизисто-кожный лейшманиоз вызывается подвидом L. brasiliensis brasiliensis. При этой форме заболевания паразиты проникают из кожи по кровеносным сосудам в носоглотку, гортань, мягкое нёбо, половые органы, поселяются в макрофагах соединительных тканей этих органов и вызывают здесь деструктивные воспаления. Висцеральный лейшманиоз вызывает L. donovani. Заболевание начинается через несколько месяцев или даже лет после заражения как системная инфекция. Паразиты размножаются в макрофагах и в моноцитах крови. Нарушаются функции печени, кроветворение. Очень велика интоксикация. При отсутствии лечения заболевание заканчивается смертью. Лабораторная диагностика основана на микроскопировании мазков из кожных язв при кожном и слизисто-кожном лейшманиозах, пунктатов лимфатических узлов и костного мозга при висцеральном лейшманиозе. В окрашенных препаратах обнаруживается лейшманиальная форма паразитов как внутри клеток, так и внеклеточно. В сомнительных случаях производят посев материала, взятого от больного, на специальную культуральную среду, на которой лейшманий приобретают промастиготную форму, активно передвигаются и легко обнаруживаются при микроскопировании. Используют также и биологические пробы — заражение лабораторных грызунов. Профилактика — в первую очередь, это борьба с переносчиками и уничтожение природных резервуаров (грызунов и бродячих собак), а также профилактические прививки. Доновани:
Тропика:
136.Малярийные плазмодии. Систематическое положение, морфология, географическое распространение, цикл развития, видовые отличия. Борьба с малярией. Задачи противомалярийной службы на современном этапе. тип Protozoa класс Sporozoa Малярийные плазмодии Plasmodium (кл. Споровики) — возбудители малярии. Известны следующие виды малярийных плазмодиев, паразитирующие у человека: Р. vivax — возбудитель трехдневной малярии, Р. falciparum — возбудитель тропической малярии, Р. malariae — возбудитель четырехдневной малярии, Р. ovale— возбудитель овале-малярии, близкой к трехдневной. Три первых вида широко распространены в тропических и субтропических климатических поясах, последний — только в тропической Африке. Все виды сходны морфологически и жизненными циклами, отличаясь друг от друга деталями строения и некоторыми особенностями цикла развития, проявляющимися в основном продолжительностью его отдельных периодов. Жизненный цикл малярийных плазмодиев типичен для споровиков, включая стадии бесполого размножения в виде шизогонии, полового процесса и спорогонии. Окончательным хозяином паразитов является комар р. Anopheles (см. разд. 21.22), а промежуточным — только человек. Комар является одновременно и переносчиком. Поэтому малярия — типичное антропонозное трансмиссивное заболевание. Со слюной зараженного комара при укусе плазмодии попадают в кровь человека (рис. 19.10). Развитие паразитов в организме человека происходит синхронно. С током крови они разносятся по организму и поселяются в клетках печени. Здесь они растут и размножаются шизогонией таким образом, что один паразит делится на тысячи дочерних особей. Клетки печени при этом разрушаются и паразиты, называющиеся на этой стадии мерозоитами, поступают в кровь и внедряются в эритроциты. С этого момента начинается эритроцитарная часть цикла развития плазмодия. Паразит питается гемоглобином, растет и размножается шизогонией. При этом каждый плазмодий делится на 8—24 мерозоита. После разрушения эритроцита мерозоиты попадают в плазму крови и оттуда в новые эритроциты, после чего весь цикл эритроцитарной шизогонии повторяется. 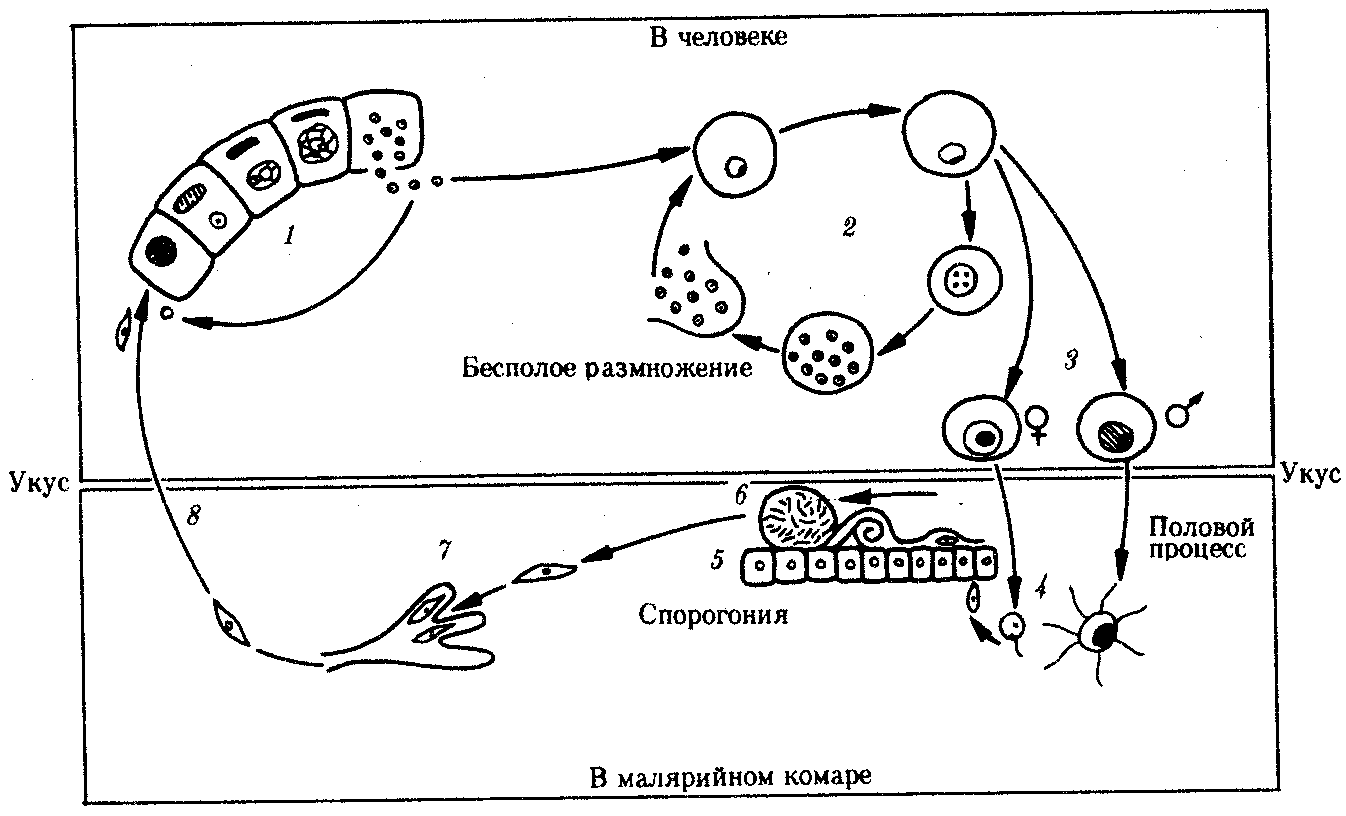 Рис. 19.10. Жизненный цикл малярийного плазмодия: 1 — преэритроцитарная шизогония в клетках печени, 2 — эритроцитарная шизогония, 3 — образование гаметоцитов, 4 — оплодотворение, 5 — спорогония в стенке желудка комара, 6 — овоциста со споромитами, 7 — проникновение спорозоита в слюнные железы комара, 8— заражение человека Из части мерозоитов в эритроцитах образуются незрелые половые клетки — мужские и женские гаметоциты. Они являются инвазионной стадией для комара. Дальнейшее их развитие возможно только в его пищеварительной системе. При укусе больного человека комаром гаметоциты попадают в желудок последнего, где из них образуются зрелые гаметы. В результате оплодотворения в желудке комара образуется подвижная зигота, которая перемещается на наружную поверхность стенки желудка и покрывается оболочкой, формируя ооцисту. С этого момента начинается период спорогонии, когда содержимое ооцисты многократно делится, образуя около 10000 спорозоитов — тонких серповидных клеток, которые после разрыва оболочки поступают в слюнные железы комара. При кровососании спорозоиты поступают в кровяное русло человека. Таким образом, в организме человека плазмодий размножается только бесполым путем — шизогонией, человек является его промежуточным хозяином. В организме комара проходят две другие стадии цикла развития паразита: половой процесс — гаметогония и образование спорозоитов за счет деления под оболочкой ооцисты — спорогония. Поэтому малярийный комар является окончательным хозяином этого паразита. Выход большого количества мерозоитов из эритроцитов сопровождается выбросом в плазму крови значительной массы токсических продуктов жизнедеятельности. Их воздействие на организм приводит к резкому повышению температуры, ознобу, слабости и головным болям. Такое состояние возникает внезапно и длится в среднем 1,5—2 ч. Вслед за этим наступает чувство жара, сухость во рту, жажда. Температура тела достигает 40—41°С. Через несколько часов все перечисленные симптомы исчезают, и больные обычно засыпают. Весь приступ может продолжаться от 6 до 12 ч. При трехдневной и овале-малярии промежутки между приступами составляют 48 ч, число таких приступов может достигать 10—15, после чего они прекращаются за счет повышения уровня специфического иммунитета, но паразиты в крови еще могут обнаруживаться. В таком случае человек становится паразитоносителем и продолжает представлять опасность для окружающих как возможный источник заражения. Естественный отбор приводит к возникновению новых антигенных вариантов возбудителя, которые обеспечивают возможность наступления рецидивов заболевания. Рецидивы могут повторяться несколько раз, но постепенно популяция эритроцитарных паразитов полностью погибает. Однако в течение 3—5 лет инвазия может вновь активизироваться за счет находящихся в латентном состоянии в печени экзоэритроцитарных шизонтов, которые могут выходить из печеночных клеток и внедряться в эритроциты. Таким образом, весь процесс болезни может начаться снова. При малярии, вызываемой Р. malariae, приступы повторяются через 72 ч. Часто встречается и бессимптомное носительство. Экзоэритро-цитарной стадии в цикле развития этого паразита нет, поэтому поздние рецидивы невозможны, хотя инвазия характеризуется упорным течением и длится до 40 лет. При тропической малярии вначале приступы развиваются через разные промежутки времени, а позже — через 24 ч. От осложнений со стороны центральной нервной системы или почек возможна смерть больного. Шизонты в клетках печени не сохраняются, а заболевание может продолжаться до 18 мес. Все виды малярийных плазмодиев могут инвазировать человека и при гемотрансфузии (переливание крови). В этом случае ни у одного из паразитов не формируется экзоэритроцитарной стадии. Поэтому поздних рецидивов в этом случае не бывает. Гемотрансфузионный способ заражения наиболее часто встречается при четырехдневной малярии в связи с тем, что при этой форме болезни шизонты в эритроцитах находятся в очень малом количестве и могут не обнаруживаться при исследовании крови доноров. Иногда человек может быть инвазирован одновременно двумя или тремя видами плазмодиев. В таком случае малярийные приступы не имеют четкой периодичности и клинический диагноз затруднен. Лабораторный диагноз малярии можно поставить только в период, соответствующий стадии эритроцитарной шизогонии, когда в крови удается обнаружить паразитов. Плазмодий, недавно проникший в эритроцит, имеет кольцевидную форму. Его цитоплазма выглядит как ободок, окружающий крупную вакуоль с продуктами диссимиляции. Ядро паразита смещено к краю клетки. Следующая стадия называется амебовидным шизонтом. У паразита появляются ложноножки, а вакуоль увеличивается. Наконец плазмодий занимает почти весь эритроцит. Следующая стадия развития паразита — фрагментация шизонта. На фоне деформированного эритроцита обнаруживаются множественные мерозоиты, в каждом из которых лежит ядро. Кроме бесполых клеток в эритроцитах можно увидеть и гаметоциты. Они отличаются крупными размерами, не имеют псевдоподий и вакуолей (рис. 19.11). 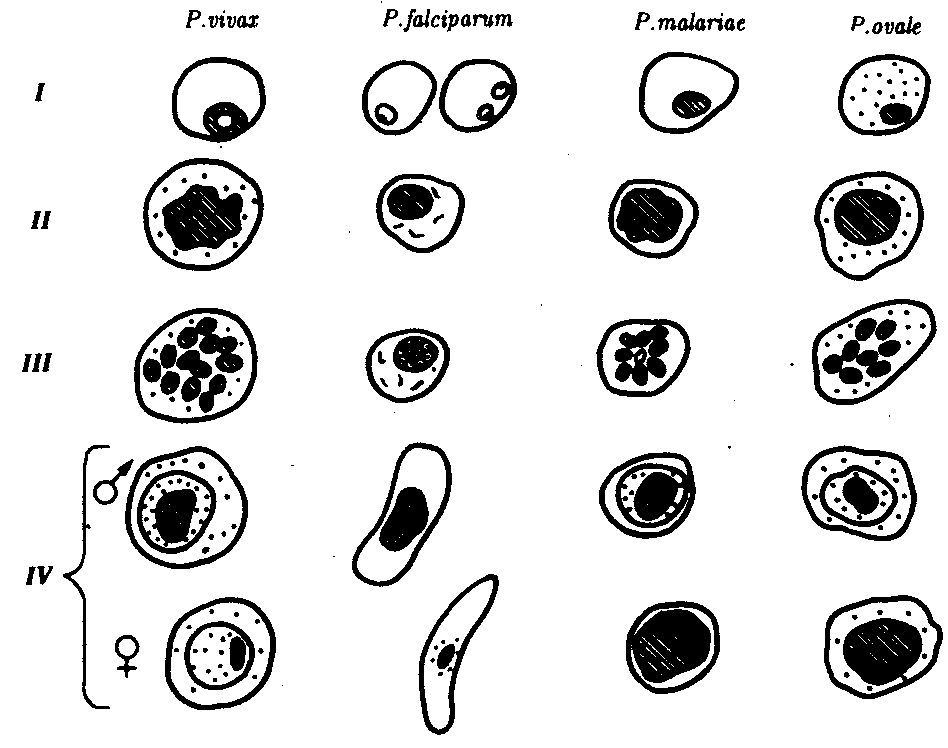 Рис. 19.11. Малярийные плазмодии. Стадии развития в эритроцитах: I—стадия кольца, II—стадия амебовидного шизонта, III—стадия фрагментации, IV—гаметоциты Профилактика малярии — раннее выявление и лечение больных, профилактическое лечение в зонах широкого распространения малярии. Как и при любых трансмиссивных заболеваниях, необходима прицельная борьба с переносчиками. 137.Токсоплазма. Систематическое положение, морфология, географическое распространение, цикл развития, пути заражения, патогенное действие, обоснование методов лабораторной диагностики, меры профилактики. тип Protozoa класс Sporozoa Токсоплазма Toxoplasma gondii — возбудитель токсоплазмоза. Имеет форму полумесяца, один конец которого заострен более другого. В центре располагается крупное ядро. Длина паразита 4—7 мкм (рис. 19.7). 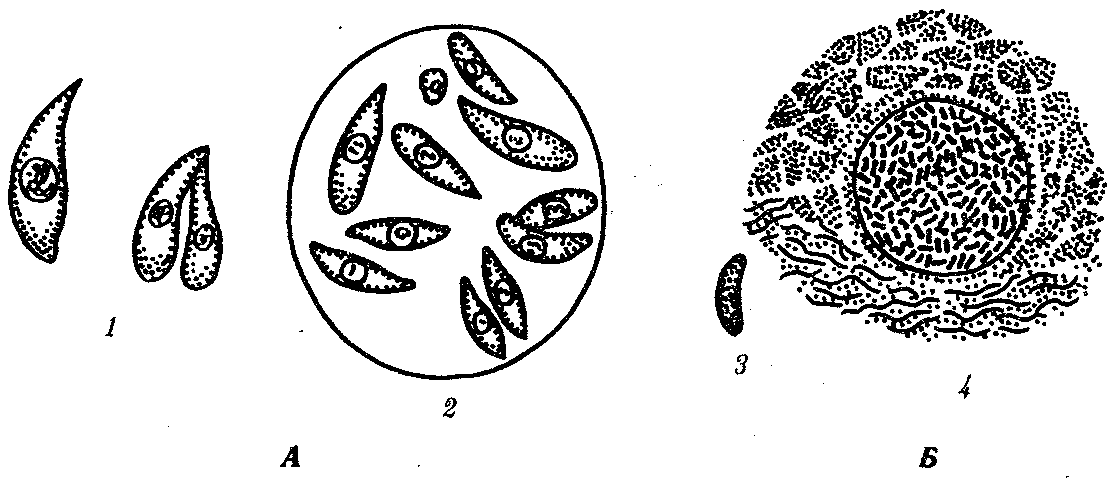 Рис. 19.7. Токсоплазма (Л) и саркоциста (Б): 1 — единичные паразиты, 2 — спорозоиты под общей оболочкой, 3 — изолированная спора, 4— саркоциста в мышечном волокне Токсоплазма поражает огромное количество видов животных и человека. Иммунологические исследования показали, что на Земле токсоплазмами заражено более 500 млн. человек. Жизненный цикл токсоплазмы типичен для споровиков: в нем чередуются стадии шизогонии, гаметогонии и спорогонии. Основные хозяева паразита — домашние кошки и дикие виды сем Кошачьи. Они заражаются, поедая больных грызунов, птиц или инвазированное мясо крупных животных. Паразиты у них сосредоточиваются в клетках кишечника, размножаются шизогонией, а затем образуют гаметы. После копуляции гамет формируются ооцисты, которые выделяются во внешнюю среду. В них происходит спорогония, т. е. деление зиготы под оболочкой. Такие спороцисты со спорозоитами рассеиваются кошками и попадают к промежуточным хозяевам, которыми могут быть человек, почти все млекопитающие, птицы и даже пресмыкающиеся. В клетках большинства их органов происходит бесполое размножение токсоплазм в форме множественного деления. В результате образуются группы, состоящие из многих сотен отдельных паразитов. Эти группы могут распадаться, и тогда отдельные токсоплазмы внедряются с помощью специфической органеллы проникновения — коноида — в непораженные клетки, в которых вновь происходит шизогония. Другие такие группы покрываются плотной оболочкой и формируют цисты. Цисты очень устойчивы и могут длительное время находиться в состоянии покоя в органах хозяев. В окружающую среду они не выделяются. Цикл развития замыкается при поедании кошками органов промежуточных хозяев с цистами. Своеобразной особенностью цикла развития токсоплазм является то, что промежуточные хозяева могут заражаться ими не только от основного хозяина, но и при поедани» друг друга. Так, возможно заражение свиней при поедании ими трупов грызунов, погибших от токсоплазмоза, грызуны же заражаются друг от друга при каннибализме. Возможно и внутриутробное заражение плода от больной беременной самки, когда паразиты проникают через плаценту. Этот способ заражения обеспечивает устойчивое существование природных очагов токсоплазмоза и среди мелких грызунов, не склонных к каннибализму. В соответствии с этим и человек как промежуточный хозяин может заразиться токсоплазмозом разными путями: 1) при поедании мяса инвазированных животных; 2) с молоком и молочными продуктами; 3) через кожу и слизистые оболочки при уходе за больными животными, при обработке шкур и разделке животного сырья; 4) внутриутробно через плаценту; 5) при медицинских манипуляцих переливания крови и лейкоцитарной массы, при пересадках органов, сопровождающихся приемом иммунодепрессивных препаратов. Последнее свидетельствует о том, что общее снижение иммунитета повышает вероятность заражения токсоплазмозом. Обычно паразиты обладают весьма низкой патогенностью, но в некоторых условиях они могут вызвать очень тяжелые нарушения, что зависит как от индивидуальной чувствительности хозяев, так и от путей проникновения токсоплазм в организм человека. Наиболее опасным является трансплацентарное заражение. При этом возможно рождение детей с множественными врожденными пороками развития, в первую очередь головного мозга. При постановке диагноза используют методы иммунологических реакций, обнаружение токсоплазм при прямом микроскопировании материала, взятого от больного человека или трупа. Для исследования используют плаценту, печень, кровь, лимфатические узлы, головной мозг. Применяют также метод биологических проб. В этом случае лабораторным животным вводят кровь или спинномозговую жидкость больного. Мыши заболевают токсоплазмозом при таком способе заражения в острой форме, и обнаружение возбудителя у них не представляет сложности. Профилактика — термическая обработка животных продуктов питания, санитарный контроль на бойнях и мясокомбинатах, предотвращение тесных контактов детей и беременных женщин с домашними животными. Toxoplasma gandi Возбудитель токсоплазмоза. Открыт в 1908 году. Проникает через кожу, слизистые, пищеварительный тракт. Локализуется практически во всех органах. Бывает врожденные формы. Кошачьи – окончательный хозяин, а человек - промежуточный. Смертность очень велика, выжившие люди становятся инвалидами. Все беременные исследуются на носительство. Зооноз с частой природной очаговостью. 138.Саркоцисты. Систематическое положение, морфология, географическое распространение, цикл развития, пути заражения, патогенное действие, обоснование методов лабораторной диагностики, меры профилактики. тип Protozoa класс Sporozoa Несколько близких к токсоплазме паразитов — саркоцисты(Sarcocystis hominis, S. suihominis, S. lindemanni) — являются возбудителями саркоцистозов и имеют сходный с ней цикл развития. Человек для этих паразитов является основным хозяином, а животные — промежуточными. Поэтому у человека, как и у кошки при токсоплазмозе, поражается кишечник. Но степень поражения его очень незначительна. По некоторым данным, частота инвазии людей саркоцистами достигает 7—60%, особенно там, где в соответствии с традициями население употребляет в пищу сырое или полусырое мясо. Врачи обычно не ставят правильного диагноза, а заболевания заканчиваются быстрым самоизлечением. см. альбом! 139.Балантидий кишечный. Систематическое положение, цикл развития, географическое распространение, пути заражения, патогенное действие, методы лабораторной диагностики, меры профилактики. тип Protozoa класс Infusoria Балантидий Balantidium coli (кл. Инфузории) — возбудитель балантидиаза. Это крупное простейшее, длиной до 200 мкм. Сохранены многие признаки свободноживущих инфузорий: все тело покрыто ресничками, имеются цитостом и цитофаринкс. Под пелликулой расположен слой прозрачной эктоплазмы, глубже находится эндоплазма с органеллами и двумя ядрами. Макронуклеус имеет гантелевидную или бобовидную форму, рядом с ним находится маленький микронуклеус. Циста балантидия овальна, до 50—60 мкм в диаметре, покрыта двуслойной оболочкой, ресничек не имеет. Микронуклеус обычно не виден, а в цитоплазме отчетливо выделяется сократительная вакуоль (см. рис. 19.3, Д). Балантидий может жить в кишечнике человека, питаясь бактериями и не принося ему вреда, но иногда внедряется в стенку кишки, вызывая образование язв с гнойным и кровянистым отделением. В этом случае в его цитоплазме часто обнаруживаются форменные элементы крови хозяина. Для заболевания характерны длительные поносы с кровью и гноем, а иногда и перфорация кишечной стенки с перитонитом. Как и при амебной дизентерии, В. coli может попадать в кровеносное русло и оседать в печени, легких и других органах, вызывая там образование абсцессов. Особенностью этих инфузорий является их способность вырабатывать фермент гиалуронидазу, благодаря которой они внедряются и в неповрежденную стенку кишки, где на гистологических препаратах обнаруживаются целые скопления тканевых трофозоитов, морфологически не отличимых от живущих в просвете кишки, но не способных к образованию цист. Кроме человека, балантидий встречается также у крыс и свиней, которые и являются его основным резервуаром. Лабораторная диагностика — обнаружение цист и трофозоитов в мазках фекалий больного. Профилактика — как при лямблиозе, однако в связи с зоонозной природой балантидиаза следует также вести борьбу с грызунами и обеспечивать гигиеническое содержание свиней. Кишечный балантидий. Есть 2 ядра (вегетативное и генеративное), реснички. Деление осуществляется под оболочкой. Питается углеводной пищей. Если углеводов поступает достаточно – не переходит к тканевой форме. Язвы в кишечнике – 3-4 см. главный источник - домашние животные, продукты и вода, зараженные фекалиями крыс, свиней. Инкубационный период длится до 15 лет. Обитают в сигмовидной, прямой, слепой кишках. Диагностика – по обнаружению в фекалиях. 140.ТИП ПЛОСКИЕ ЧЕРВИ. Классификация. Характерные черты организации, медицинское значение. Тип Plathelmintes Плоские черви имеют тело, уплощенное в дорсовентральном направлении. Полость тела отсутствует, внутренние органы погружены в рыхлую соединительную ткань — паренхиму. Кожно-мускульный мешок состоит из покровной ткани — тегумента, который представляет собой многоядерную неклеточную структуру, и трех слоев гладких мышц — продольных, поперечных и дорсовентральных. Движения, осуществляемые ими, медленны и несовершенны. Нервная система состоит из нервных узлов на переднем конце тела, от которых кзади отходят продольные нервные тяжи. Пищеварительная система, если она имеется, построена из глотки и кишечника, который слепо замкнут. Непереваренные остатки пищи выделяются через рот. Половая система гермафродитна и построена очень сложно. Выделение осуществляется с помощью протонефридиальной системы, состоящей из отдельных выделительных клеток — протонефридиев. Они способны захватывать продукты диссимиляции и транспортировать их по внутриклеточным каналам, проходящим в их длинных отростках. Продукты экскреции поступают в собирательные трубочки, а оттуда либо непосредственно, либо через мочевой пузырь — во внешнюю среду. Виды, имеющие медицинское значение, представлены в двух классах: Сосальщики и Ленточные черви. Класс Сосальщики Trematoda Класс Сосальщики включает около 4000 видов. Все они паразиты. Форма тела большинства сосальщиков листовидная. В процессе адаптации к паразитизму выработались мощные присоски — органы прикрепления. Многие сосальщики, кроме того, имеют мелкие шипики, покрывающие все тело и облегчающие им прикрепление к хозяину. Мелкие виды имеют пищеварительную систему в форме мешка или двух слепо замкнутых каналов. У крупных видов пищеварительная система сильно разветвлена и наряду с собственно пищеварением выполняет также транспортную функцию, перераспределяя по организму продукты пищеварения. В остальном сосальщики повторяют организацию плоских червей, описанных выше (рис. 20.1). 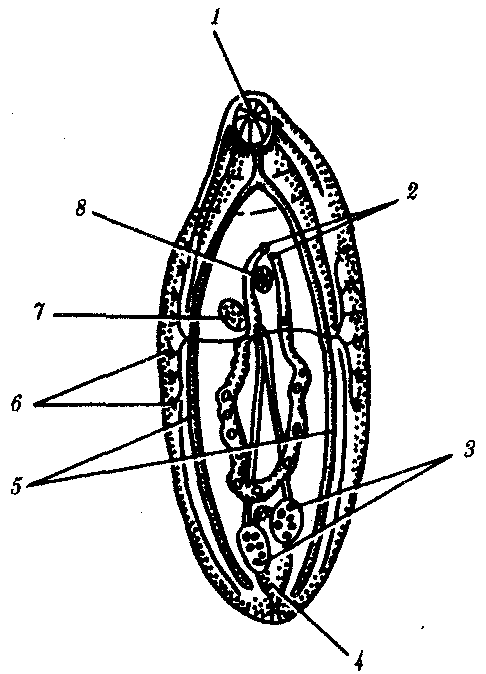 Рис. 20.1. Организация сосальщиков: 1—ротовая присоска, 2—мужские и женские половые отверстия; 3—семенники; 4—мочевой пузырь; 5—ветви кишечника, 6—желточники; 6—яичник; 8—брюшная присоска Сосальщики резко обособлены от других плоских червей своеобразием жизненного цикла, в котором имеет место закономерное чередование поколений, способов размножения и хозяев (рис. 20.2). Половозрелая стадия всегда паразитирует в организме позвоночных животных. Выделяемое яйцо для успешного развития обычно должно попасть в воду. Из него выходит личинка — мирацидий, — снабженная светочувствительными глазками и ресничками, с помощью которых она свободно перемещается. Личинка обычно способна активно отыскивать промежуточных хозяев, используя фото-, гео- и хемотаксис. Мирадиции попадают в организм брюхоногого моллюска определенного вида, строго специфичного для данного сосальщика. Здесь личинка превращается в материнскую спороцисту — стадию, претерпевшую в связи с паразитизмом наиболее глубокую дегенерацию. В ней развиты почти исключительно органы женской половой системы, благодаря которым она размножается партеногенетически. В результате этого образуются многоклеточные редии, которые также способны к партеногенезу. Таким образом, возможно формирование нескольких поколений редий. Последнее из них генерирует церкариев, покидающих организм моллюска и свободно плавающих в поисках основного или второго промежуточного хозяина. 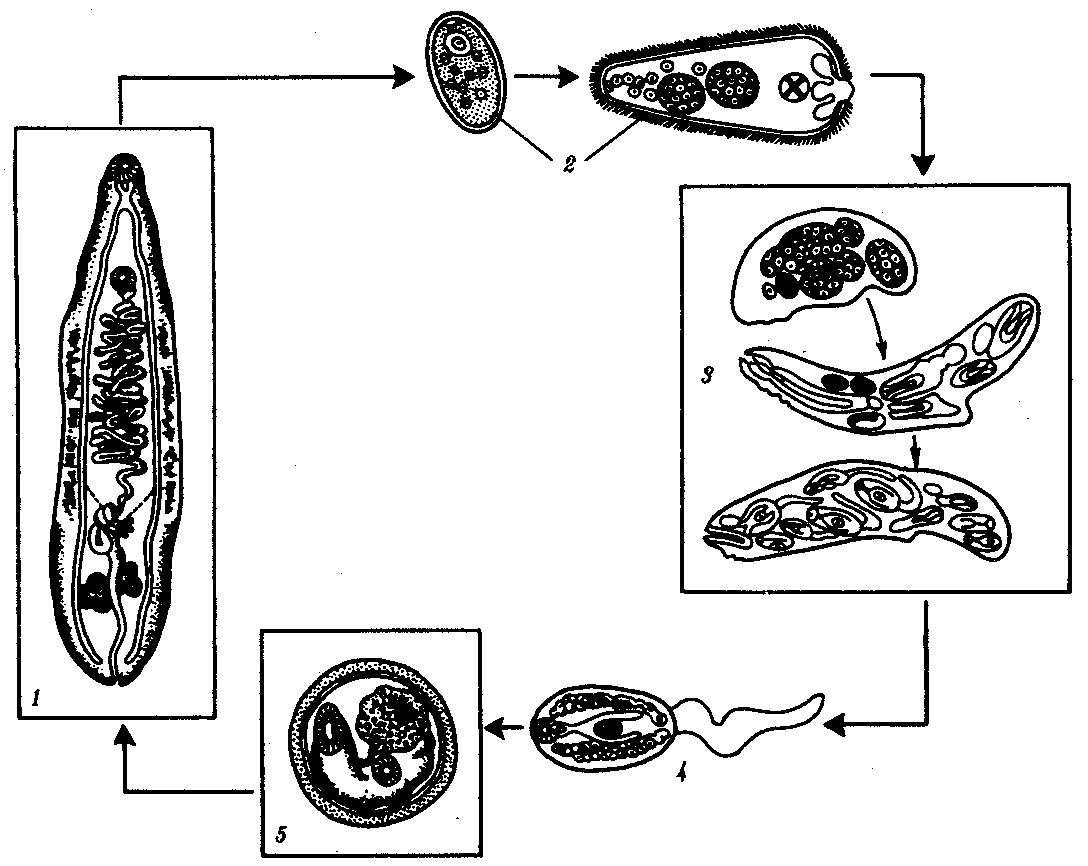 Рис. 20.2. Цикл развития сосальщиков: 1—половозрелая форма в окончательном хозяине, 2—яйцо и мирацидий в воде, 3— личинки, размножающиеся партеногенетически в моллюске, 4—церкарий в воде, 5—метацеркарий во втором промежуточном хозяине В первом случае церкарий либо самостоятельно внедряются в кожу хозяина, либо, инцистируясь на растениях, оказываются проглоченными травоядными животными или человеком. Во втором случае церкарий отыскивают животных, использующихся основными хозяевами для питания, и образуют в них покоящиеся стадии — инцистированные метацеркарий. Церкарий в отличие от мирацидиев не обладают хемотаксисом, а использование только гео- и фототаксиса, а также инцистирование на траве не позволяют им находить специфичных хозяев. Поэтому основная масса церкариев погибает либо не найдя хозяев вообще, либо попав в организмы таких видов, развитие в которых невозможно. После проникновения инвазионных стадий сосальщиков в основного хозяина они мигрируют у него в организме и находят тот орган, где достигнут половой зрелости и будут обитать всю последующую жизнь. Отсутствие свободноживущих видов в классе Сосальщики на фоне общего примитивизма их организации, сложный цикл развития, в котором участвуют специфические промежуточные и основные хозяева, огромная плодовитость, достигающаяся разными способами размножения, и сохранившаяся связь с водной средой обитания свидетельствуют о древности паразитического образа жизни этих организмов. Среди хозяев сосальщиков наиболее специфичными являются именно моллюски: для каждого вида паразита, обитающего на стадии мариты нередко у нескольких видов основных хозяев, первым промежуточным хозяином практически всегда является только один вид улиток. Это означает, что на протяжении эволюции между сосальщиками и моллюсками возникли наиболее совершенные взаимные адаптации. Моллюски были, вероятно, первыми и единственными хозяевами сосальщиков еще в период, предшествующий возникновению позвоночных. Об этом свидетельствует также сохранившийся в цикле развития сосальщиков партеногенез — рудиментарная форма полового размножения, — проходящий именно в организме моллюсков. Наряду с этими чертами в цикле развития имеются такие признаки, которые указывают на рекапитуляции свободного образа жизни: обязательный выход яиц во внешнюю среду и наличие активно плавающих расселительных стадий с органами чувств — мирацидиев и церкарий. Возникновение и дальнейший биологический и морфофизиологи-ческий прогресс позвоночных, освоивших все благоприятные для жизни среды, открыли и сосальщикам широкие возможности адаптивной эволюции за счет приспособления к новым хозяевам. Адаптации сосальщиков к позвоночным как к новым средам обитания не ограничились только использованием их широкого видового разнообразия. Сосальщики адаптировались к обитанию в самых разнообразных органах, тканях и системах — от кожных покровов и органов чувств до кровеносных сосудов внутренних органов. Однако большинство сосальщиков-паразитов человека обитает в пищеварительной системе; некоторые виды живут в легких, другие — в кровеносных сосудах брюшной полости и малого таза. Человек заражается сосальщиками в зависимости от вида разными способами: при контакте с водой и проникновении церкарий через кожу, при поедании продуктов животного происхождения с метацеркариями и при употреблении растений в пищу, если на их листьях инцистированы церкарии паразитов. После попадания в организм человека большинство сосальщиков осуществляют сложные миграции по пути к органам своей окончательной локализации. Миграция происходит по кровеносным сосудам, непосредственно по пространствам между органами и по полости тела. Во время миграции сосальщики вызывают у хозяина тяжелые интоксикации и аллергические состояния, но диагностировать заболевание в этот момент крайне сложно. Заболевания, вызываемые сосальщиками, называют трематодозами. Для диагностики трематодозов используют методы обнаружения яиц в фекалиях, моче или мокроте в зависимости от локализации паразитов, а также аллергические пробы. В связи с тем что сосальщики, обитающие у человека, поражают также и ряд других видов млекопитающих, соответствующие трематодозы относят к природно-очаговым зоонозным заболеваниям, поэтому их полная ликвидация практически невозможна. В зависимости от особенностей цикла развития сосальщиков, паразитирующих у человека, можно разделить на следующие группы: 1) развивающиеся с одним промежуточным хозяином и обитающие в пищеварительной системе; 2) развивающиеся с одним промежуточным хозяином и обитающие в кровеносных сосудах; 3) развивающиеся с двумя промежуточными хозяевами. |
