Общие рекомендации
 Скачать 4.72 Mb. Скачать 4.72 Mb.
|
Практическое значение закона Харди-ВайнбергаВ медицинской генетике закон Харди-Вайнберга позволяет оценить популяционный риск генетически обусловленных заболеваний, поскольку каждая популяция обладает собственным аллелофондом и, соответственно, разными частотами неблагоприятных аллелей. Зная частоты рождения детей с наследственными заболеваниями, можно рассчитать структуру аллелофонда. В то же время, зная частоты неблагоприятных аллелей, можно предсказать риск рождения больного ребёнка. 52.Генеалогический метод изучения генетики человека. Особенности наследования признаков в родословных с аутосомно-доминантным, аутосомно-рецессивным, Х-сцепленным и У-сцепленным типах наследования. В основе этого метода лежит составление и анализ родословных. Родословные человека составлялись на протяжении многих столетий в отношении царствующих семейств в Европе и Азии. Как метод изучения генетики человека генеалогический метод стали применять только с начала XX столетия, когда выяснилось, что анализ родословных, в которых прослеживается передача из поколения в поколение какого-то признака (заболевания), может заменить собой фактически неприменимый в отношении человека гибридологический метод. При составлении родословных исходным является человек — пробанд, родословную которого изучают. Обычно это или больной, или носитель определенного признака, наследование которого необходимо изучить. С помощью генеалогического метода может быть установлена наследственная обусловленность изучаемого признака, а также тип его наследования (аутосомно-доминантный, аутосомно-рецессивный, X-сцепленный доминантный или рецессивный, Y-сцепленный). При анализе родословных по нескольким признакам может быть выявлен сцепленный характер их наследования, что используют при составлении хромосомных карт. Этот метод позволяет изучать интенсивность мутационного процесса, оценить экспрессивность и пенетрантность аллеля. Он широко используется в медико-генетическом консультировании для прогнозирования потомства. Однако необходимо отметить, что генеалогический анализ существенно осложняется при малодетности семей. Родословные при аутосомно-доминантном наследовании. - равная вероятность встречаемости данного признака как у мужчин, так и у женщин. Это обусловлено одинаковой двойной дозой генов, расположенных в аутосомах у всех представителей вида и получаемых от обоих родителей, и зависимостью развивающегося признака от характера взаимодействия аллельных генов. При доминировании признака в потомстве родительской пары, где хотя бы один родитель является его носителем, он проявляется с большей или меньшей вероятностью в зависимости от генетической конституции родителей (рис. 6.25). 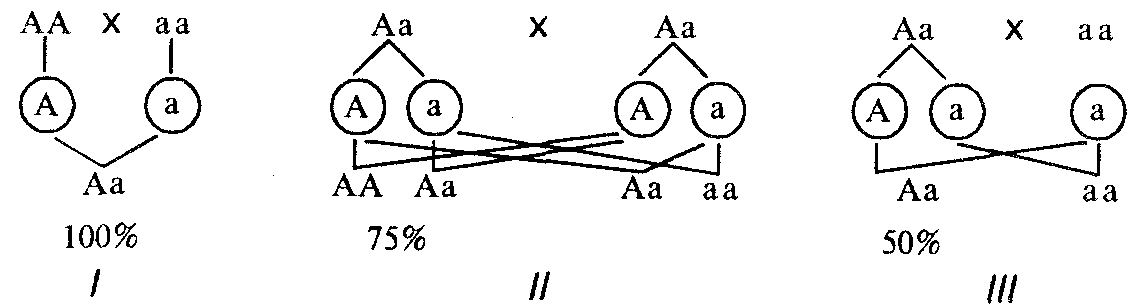 Если анализируется признак, не влияющий на жизнеспособность организма, то носители доминантного признака могут быть как гомо-, так и гетерозиготами. В случае доминантного наследования какого-то патологического признака (заболевания) гомозиготы, как правило, нежизнеспособны, а носители этого признака — гетерозиготы. Таким образом, при аутосомно-доминантном наследовании признак может встречаться в равной мере у мужчин и у женщин и прослеживается при достаточном по численности потомстве в каждом поколении по вертикали. Анализируя родословные, необходимо помнить о возможности неполного пенетрирования доминантного аллеля, обусловленной взаимодействием генов или факторами среды. Показатель пенетрантности может быть вычислен как отношение фактического числа носителей признака к числу ожидаемых носителей этого признака в данной семье. Необходимо также помнить, что некоторые заболевания проявляются не сразу с момента рождения ребенка. Многие болезни, наследуемые по доминантному типу, развиваются лишь в определенном возрасте. Так, хорея Гентингтона клинически проявляется к 35—40 годам, поздно проявляется и поликистоз почек. Поэтому при прогнозировании подобных заболеваний в расчет не принимаются братья и сестры, не достигшие критического возраста. Родословные при аутосомно-рецессивном наследовании. Рецессивные признаки проявляются фенотипически лишь у гомозигот по рецессивным аллелям. Эти признаки, как правило, обнаруживаются у потомков фенотипически нормальных родителей — носителей рецессивных аллелей. Вероятность появления рецессивного потомства в этом случае равна 25%. Если один из родителей имеет рецессивный признак, то вероятность проявления его в потомстве будет зависеть от генотипа другого родителя. У рецессивных родителей все потомство унаследует соответствующий рецессивный признак. Для родословных при аутосомно-рецессивном типе наследования характерно, что признак проявляется далеко не в каждом поколении. Чаще всего рецессивное потомство появляется у родителей с доминантным признаком, причем вероятность появления такого потомства возрастает в близкородственных браках, где оба родителя могут являться носителями одного и того же рецессивного аллеля, полученного от общего предка. Родословные при доминантном Х-сцепленном наследовании признака. Гены, расположенные в Х-хромосоме и не имеющие аллелей в Y-хромосоме, представлены в генотипах мужчин и женщин в разных дозах. Женщина получает две свои Х-хромосомы и соответствующие гены как от отца, так и от матери, а мужчина наследует свою единственную Х-хромосому только от матери. Развитие соответствующего признака у мужчин определяется единственным аллелем, присутствующим в его генотипе, а у женщин он является результатом взаимодействия двух аллельных генов. В связи с этим признаки, наследуемые по Х-сцепленному типу, встречаются в популяции с разной вероятностью у мужского и женского пола. При доминантном Х-сцепленном наследовании признак чаще встречается у женщин в связи с большей возможностью получения ими соответствующего аллеля либо от отца, либо от матери. Мужчины могут наследовать этот признак только от матери. Женщины с доминантным признаком передают его в равной степени дочерям и сыновьям, а мужчины — только дочерям. Сыновья никогда не наследуют от отцов доминантного Х-сцепленного признака. Примером такого типа наследования служит описанная в 1925 г. родословная с фолликулярным кератозом —кожным заболеванием, сопровождающимся потерей ресниц, бровей, волос на голове (рис. 6.30). Характерным является более тяжелое течение заболевания у гемизиготных мужчин, чем у женщин, которые чаще всего являются гетерозиготами. При некоторых заболеваниях наблюдается гибель мужчин-гемизигот на ранних стадиях онтогенеза. Тогда в родословных среди пораженных должны быть только женщины, в потомстве которых отношение пораженных дочерей, здоровых дочерей и здоровых сыновей равно 1:1:1. Мужские доминантные гемизиготы, не погибающие на очень ранних стадиях развития, обнаруживаются в самопроизвольных абортах или среди мертворожденных. Такими особенностями наследования у человека характеризуется пигментный дерматоз. Родословные при рецессивном Х-сцепленном наследовании признаков. Характерной особенностью родословных при данном типе наследования является преимущественное проявление признака у гемизиготных мужчин, которые наследуют его от матерей с доминантным фенотипом, являющихся носительницами рецессивного аллеля. Как правило, признак наследуется мужчинами через поколение от деда по материнской линии к внуку. У женщин он проявляется лишь в гомозиготном состоянии, вероятность чего возрастает при близкородственных браках. Наиболее известным примером рецессивного Х-сцепленного наследования является гемофилия. Другим примером наследования по данному типу является дальтонизм — определенная форма нарушения цветоощущения. Родословные при Y-сцепленном наследовании. Наличие Y-хромосомы только у представителей мужского пола объясняет особенности Y-сцепленного, или голандриче-ского, наследования признака, который обнаруживается лишь у мужчин и передается по мужской линии из поколения в поколение от отца к сыну. Одним из признаков, Y-сцепленное наследование которого у человека все еще обсуждается, является гипертрихоз ушной раковины, или наличие волос на внешнем крае ушной раковины. Предполагают, что в коротком плече Y-хромосомы кроме этого гена находятся гены, определяющие мужской пол. В 1955 г. у мыши описан определяемый Y-хромосомой трансплантационный антиген, названный HY. Возможно, он является одним из факторов половой дифференцировки мужских гонад, клетки которых имеют рецепторы, связывающие этот антиген. Связанный с рецептором антиген активизирует развитие гонады по мужскому типу (см. разд. 3.6.5.2; 6.1.2). Этот антиген в процессе эволюции остался почти неизменным и встречается в организме многих видов животных, в том числе и человека. Таким образом, наследование способности к развитию гонад по мужскому типу определяется голандрическим геном, расположенным в Y-хромосоме (рис. 6.32). Сущность генеалогического метода. -установление наследственной этиологии заболевания - установление типа наследования - установление локализации гена в хромосоме - дифференциация болезней генетической этиологии с близкими к ним ненаследственми формами - дифференциация наследственных заболеваний, несходных по гены наследования. 53.Близнецовый метод изучения генетики человека, возможности метода. Определение соотносительной роли наследственности и среды в развитии признаков и патологических состояний человека. Рождение близнецов – довольно редкое явление. В европейских странах 1-1,2% всех родов – близнецы, в Восточной Европе РФ 1,5%, в Нигерии 4%, в Японии 0,7% у европеоидов – 0,7% у негроидов – 1,1% у монголоидов – 0,2% Эти различия касаются дизиготных близнецов. Зависит от возраста матери (чем старше, тем больше вероятность рождения близнецов), искусственное оплодотворение. Монозиготные близнецы – редкое явление, не зависит от возраста, расы, географического положения и условий жизни. Имеют большое значение для анализа т.к. очень похожи. Близнецовый метод позволяет установить, в какой мере признак зависит от генов и в какой – от внешней среды (т.к. организм взаимодействует с окружающей средой). Используются понятия: конкордантность и дискордантность. Близнецовые методы часто используются для исследования туберкулеза, сахарного диабета, шизофрении, эпилепсии и других болезней и отклонений. Этот метод заключается в изучении закономерностей наследования признаков в парах одно- и двуяйцевых близнецов. Он предложен в 1875 г. Гальтоном первоначально для оценки роли наследственности и среды в развитии психических свойств человека. В настоящее время этот метод широко применяют в изучении наследственности и изменчивости у человека для определения соотносительной роли наследственности и среды в формировании различных признаков, как нормальных, так и патологических. Он позволяет выявить наследственный характер признака, определить пенетрантность аллеля, оценить эффективность действия на организм некоторых внешних факторов (лекарственных препаратов, обучения, воспитания). Суть метода заключается в сравнении проявления признака в разных группах близнецов при учете сходства или различия их генотипов. Монозиготные близнецы, развивающиеся из одной оплодотворенной яйцеклетки, генетически идентичны, так как имеют 100% общих генов. Поэтому среди монозиготных близнецов наблюдается высокий процент конкордантных пар, в которых признак развивается у обоих близнецов. Сравнение монозиготных близнецов, воспитывающихся в разных условиях постэмбрионального периода, позволяет выявить признаки, в формировании которых существенная роль принадлежит факторам среды. По этим признакам между близнецами наблюдается дискордантность, т.е. различия. Напротив, сохранение сходства между близнецами, несмотря на различия условий их существования, свидетельствует о наследственной обусловленности признака. Сопоставление парной конкордантности по данному признаку у генетически идентичных монозиготных и дизиготных близнецов, которые имеют в среднем около 50% общих генов, дает возможность более объективно судить о роли генотипа в формировании признака. Высокая конкордантность в парах монозиготных близнецов и существенно более низкая конкордантность в парах дизиготных близнецов свидетельствуют о значении наследственных различий в этих парах для определения признака. Сходство показателя конкордантности у моно- и дизиготных близнецов свидетельствует о незначительной роли генетических различий и определяющей роли среды в формировании признака или развития заболевания. Достоверно различающиеся, но достаточно низкие показатели конкордантности в обеих группах близнецов дают возможность судить о наследственной предрасположенности к формированию признака, развивающегося под действием факторов среды. Установление соотносительной роли наследственности и среды в развитии различных патологических состояний позволяет врачу правильно оценить ситуацию и проводить профилактические мероприятия при наследственной предрасположенности к заболеванию или осуществлять вспомогательную терапию при его наследственной обусловленности. Трудности близнецового метода связаны, во-первых, с относительно низкой частотой рождения близнецов в популяции (1:86—1:88), что осложняет подбор достаточного количества пар с данным признаком; во-вторых, с идентификацией монозиготности близнецов, что имеет большое значение для получения достоверных выводов. Для идентификации монозиготности близнецов применяют ряд методов. 1. Полисимптомный метод сравнения близнецов по многим морфологическим признакам (пигментации глаз, волос, кожи, форме волос и особенностям волосяного покрова на голове и теле, форме ушей, носа, губ, ногтей, тела, пальцевым узорам). 2. Методы, основанные на иммунологической идентичности близнецов по эритроцитарным антигенам (системы АВО, MN, резусу), по сывороточным белкам (γ-глобулину). 3. Наиболее достоверный критерий монозиготности предоставляет трансплантационный тест с применением перекрестной пересадки кожи близнецов. Несмотря на трудоемкость близнецового метода и возможность ошибок при определении монозиготности близнецов, высокая объективность выводов делает его одним из широко применяемых методов генетических исследований у человека. 54.Цитогенетический метод изучения генетики человека. Денверская и Парижская классификация хромосом. Возможности идентификации хромосом человека. 55.Медико-генетические аспекты брака. Близкородственные браки. Медико-генетическое консультирование Существуют методы пренатальной диагностики. Как правило, пренатальный диагноз ставится в медико-генетических учреждениях. В России 7 центров федерального значения, 10 областных центров, 85 пунктов медико-генетического консультирования. Первая медицинская консультация появилась в 20х годах в Москве благодаря невропатологу Девиденко. Почти все медико-генетические консультации связаны с нервными болезными. Первая медико-генетическая консультация в США возникла при Мачиганском университете в 1941 году. В Воронеже подобная консультация появилась в 1960 году под руководством невропатологов. Медико-генетические консультации обслуживают примерно 1.5 миллионов человек каждая. Врач- генетик затрачивает на прием одного больного около 1,5 – 2 часов, при повторном обращении 30-40 минут. Для подавляющего большинства наследственных болезней эффективных способов лечения не существует. Из этого следует, что в борьбе с наследственной патологией основная роль отводится профилактике рождения аномального потомства. Общий профилактический характер носят мероприятия, направленные на оздоровление окружающей среды, способствующие снижению ее мутагенного воздействия на наследственный материал человеческого организма. В последние десятилетия распространенным и эффективным способом профилактики наследственных болезней является медико-генетическое консультирование. Медико-генетическое консультирование — это один из видов специализированной помощи населению, направленной в первую очередь на предупреждение появления в семье детей с наследственной патологией. С этой целью составляют прогноз рождения в данной семье ребенка с наследственной болезнью, родителям объясняют вероятность этого события и оказывают помощь в принятии решения. В случае большой вероятности рождения больного ребенка родителям рекомендуют либо воздержаться от деторождения, либо провести пренатальную диагностику, если она возможна при данном виде патологии. Консультирование семей, обращающихся к врачу-генетику, включает три основных этапа. Как правило, за консультацией обращаются семьи, где уже имеется ребенок с наследственной патологией, или семьи, в которых имеются больные родственники. На первом этапе консультирования производится уточнение диагноза, что является необходимой предпосылкой любого консультирования. Уточнение диагноза в медико-генетической консультации проводят с помощью генетического анализа. Для этой цели используют генеалогический, цитогенетический, биохимический и другие требуемые методы исследований, которым подвергаются пробанд и его родственники. Точный клинический и генетический диагноз заболевания позволяет установить степень генетического риска и выбор эффективных методов пренатальной диагностики и профилактического лечения. На втором этапе консультирования делают прогноз потомства. Генетический риск может быть определен либо путем теоретических расчетов, основанных на генетических закономерностях, либо с помощью эмпирических данных. Сущность генетического прогноза заключается в определении вероятности появления наследственной патологии в семье. Наиболее эффективным является проспективное консультирование, когда риск рождения больного ребенка определяют до наступления беременности или в ранние ее сроки. Такие консультации чаще проводят в случае кровного родства супругов, при отягощенной наследственности по линии мужа или жены, при воздействии вредных средовых факторов на супругов незадолго до наступления беременности. Ретроспективное консультирование проводят после рождения больного ребенка относительно здоровья будущих детей. Определение прогноза потомства при разных формах наследственной патологии различно. При моногенных, менделирующих болезнях прогноз основывается на расчете вероятности появления потомства в соответствии с генетическими закономерностями. При этом, если известен тип наследования данного заболевания и по родословной удается установить генотип родителей, оценка риска сводится к анализу мевделевского расщепления. Если у пробанда установлена вновь возникшая мутация, то повторный риск рождения ребенка с такой же патологией незначителен. Расчет риска при моногенном заболевании может осложниться при пониженной экспрессивности или неполной пенетрантности гена, позднем проявлении генетической аномалии, генетической гетерогенности заболевания и вообще в случае неточного диагноза. При хромосомных болезнях определение риска повторного рождения потомства с хромосомными аномалиями зависит от того, нормальны ли кариотипы родителей, не обнаружено ли у них мозаицизма, не наблюдается ли семейной формы структурных аномалий хромосом. В случае отсутствия нарушений в кариотипе родителей вероятность повторного рождения второго ребенка с хромосомной аномалией оценивается по эмпирическим данным для каждого вида аномалии с учетом возраста родителей. При мультифакториальных заболеваниях, т.е. заболеваниях с наследственным предрасположением, основой оценки риска являются эмпирические данные о популяционной и семейной частоте каждого из них. Специфический генетический риск до 5% принято считать низким, до 10% —повышенным в легкой степени, до 20% —средним, выше 20% — высоким. Генетический риск средней степени расценивают как противопоказание к зачатию или показание к прерыванию уже имеющейся беременности. Возможность проведения пренатальной диагностики является определяющей для принятия положительного решения в отношении завершения беременности. На третьем этапе консультирования врач-генетик в доступной форме объясняет семье степень генетического риска рождения наследственно аномального потомства, сущность пренатальной диагностики и помогает принять правильное решение в отношении деторождения. Однако окончательное решение этого вопроса остается за родителями. Широкое использование медико-генетического консультирования, разработка способов пренатальной диагностики наследственных заболеваний позволяют существенно уменьшить вероятность появления потомства с наследственной патологией в отдельных семьях. Чаще всего рецессивное потомство появляется у родителей с доминантным признаком, причем вероятность появления такого потомства возрастает в близкородственных браках, где оба родителя могут являться носителями одного и того же рецессивного аллеля, полученного от общего предка. Инбридинг приводит к повышению постоянства фенотипических признаков в потомстве и, в конечном итоге, производится для получения линий генетически идентичных особей (инбредные линии), на которых удобно проводить биологические и медицинские эксперименты. Как известно, организм получает каждый ген в двух экземплярах (аллелях) — от отца и от матери. Если эти гены различаются, то особь называется гетерозиготной (по данному гену), а если не различаются, то гомозиготной. При инбридинге родители являются родственниками и поэтому имеют много одинаковых генов, в результате чего гомозиготность увеличивается с каждым поколением. 56.Пренатальная диагностика наследственных заболеваний человека. Методы пренатальной диагоностики и их возможности. В связи с отсутствием в настоящее время действенных методов лечения, тяжелым поражением здоровья при многих наследственных заболеваниях их ранняя диагностика дает возможность предупредить появление потомства с наследственным нарушением путем прерывания беременности, а иногда начать лечение сразу после рождения или даже в пренатальном периоде. Амниоцентез, с помощью которого на 15—16-й неделе беременности получают амниотическую жидкость, содержащую продукты жизнедеятельности плода и клетки его кожи и слизистых. Забираемый при амниоцентезе материал используют для биохимических, цитогенетических и молекулярно-биологических исследований. Цитогенетическими методами определяют пол плода и выявляют хромосомные и геномные мутации. Изучение амниотической жидкости и клеток плода с помощью биохимических методов позволяет обнаружить дефект белковых продуктов генов, однако не дает возможности определять локализацию мутаций в структурной или регуляторной части генома. Важную роль в выявлении наследственных заболеваний и точной локализации повреждения наследственного материала плода играет использование ДНК-зондов. В настоящее время с помощью амниоцентеза диагностируются все хромосомные аномалии, свыше 60 наследственных болезней обмена веществ, несовместимость матери и плода по эритроцитарным антигенам. С начала 80-х гг. XX в. стало возможным использование для целей медикогенетического диагностирования материала биопсии ворсин хориона. В отличие от амниоцентеза это исследование проводят в первой трети беременности, что позволяет при наличии показаний прерывать ее в более ранние сроки. Для диагностики таких заболеваний, как гемоглобинопатия, используют пункцию сосудов плода с получением клеток его крови. Методы фетоскопии и ультразвуковых исследований позволяют определять пол плода и некоторые пороки его развития путем непосредственного наблюдения. Пренатальная диагностика должна проводиться до 20—22-й недели беременности, когда плод еще нежизнеспособен после ее прерывания. Прерывание беременности в более поздние сроки может привести к рождению живого ребенка и быть опасным для организма матери. Прерывание беременности всегда проводится только с согласия родителей. Так как многие методы пренатального обследования плода не являются абсолютно безвредными, а кроме того, они трудоемки и дорогостоящи, показания к такому обследованию должны быть обоснованы. Пренатальное обследование плода проводят в случаях: 1) обнаружения структурных перестроек хромосом (транслокаций) у одного из родителей; 2) при наличии у родителей доминантного наследственного заболевания; 3) при наличии в семье детей с рецессивным наследственным заболеванием, что свидетельствует о гетерозиготности родителей; 4) при возрасте матери старше 35 лет, что прогрессивно повышает вероятность рождения у нее потомства с наследственной патологией; 5) при привычных выкидышах, вызывающих подозрение на несовместимость матери и плода по эритроцитарным антигенам; 6) при наличии в семье детей с врожденными пороками развития. Благодаря разработке способов пренатальной диагностики удается сократить число рождающихся с наследственными заболеваниями. Существуют 3 вида пренатальной диагностики. - прямые (исследование плода) - непрямые (исследование матери) - дополнительные (УЗИ). Прямые исследования – ранний метод. Используется плодный материал, ставят диагноз до 20 дней. Используются амниоцентез, хондроцентез – взятие крови из пупочных сосудов плода, плацентобиопсия – исследование материала плаценты, хориобиопсия – взятие ворсинок в слизистой матки, определение питания на 8-10 недели беременности. Результат изучается в течение дня, изучается риск абортов и диагностических ошибок. Амниоцентез был предложен немецким гинекологом в 19 веке. На 16 – 17 неделях делается абдоминальный прокол и забирается 10 – 20 мл амниотической жидкости. Вреда не приносит, в околоплодной жидкости имеются 20% жизнеспособных клеток плода – клетки слущенного дыхательного эпителия. Вероятность ошибки 2-3% ( аномальный кариотип). При центрифугировании клетки осаждаются, затем используются различные биохимические методы. Определяется пол плода, проводят кариотипирование. 57.Закономерности наследования внеядерных генов. Наследственные митохондриальные болезни. 58.Общие подходы к лечению наследственных заболеваний человека. 59.Онтогенез как процесс реализации наследственной информации в определенных условиях среды. Этапы, периоды и стадии онтогенеза. Периодизация онтогенеза. 60.Характеристика и значение основных этапов эмбрионального развития: предзиготный период (прогенез), оплодотворение, дробление, гаструляция, первичный органогенез (нейруляция). Дифференцировка зародышевых листков. Образование органов и тканей. 61.Провизорные органы зародышей позвоночных (амнион, хорион, аллантоис, желточный мешок, плацента), их функции. Амнион представляет собой эктодермальный мешок, заключающий зародыша и заполненный амниотической жидкостью. Амниотическая оболочка специализирована для секреции и поглощения амниотической жидкости, омывающей зародыш. Амнион играет первостепенную роль в защите зародыша от высыхания и от механических повреждений, создавая для него наиболее благоприятную и естественную водную среду. Амнион имеет и мезодермальный слой из внезародышевой соматоплевры, который дает начало гладким мышечным волокнам. Сокращения этих мышц вызывают пульсацию амниона, а медленные колебательные движения, сообщаемые при этом зародышу, по-видимому, способствуют тому, что его растущие части не мешают друг другу. Хорион (сероза) — самая наружная зародышевая оболочка, прилежащая к скорлупе или материнским тканям, возникающая, как и амнион, из эктодермы и соматоплевры. Хорион служит для обмена между зародышем и окружающей средой. У яйцекладущих видов основная его функция — дыхательный газообмен; у млекопитающих он выполняет гораздо более обширные функции, участвуя помимо дыхания в питании, выделении, фильтрации и синтезе веществ, например гормонов. Желточный мешок имеет энтодермальное происхождение, покрыт висцеральной мезодермой и непосредственно связан с кишечной трубкой зародыша. У зародышей с большим количеством желтка он принимает участие в питании. У птиц, например в спланхноплевре желточного мешка, развивается сосудистая сеть. Желток не проходит через желточный проток, соединяющий мешок с кишкой. Сначала он переводится в растворимую форму под действием пищеварительных ферментов, продуцируемых энтодермальными клетками стенки мешка. Затем попадает в сосуды и с кровью разносится по всему телу зародыша. У млекопитающих нет запасов желтка и сохранение желточного мешка может быть связано с важными вторичными функциями. Энтодерма желточного мешка служит местом образования первичных половых клеток, мезодерма дает форменные элементы крови зародыша. Кроме того, желточный мешок млекопитающих заполнен жидкостью, отличающейся высокой концентрацией аминокислот и глюкозы, что указывает на возможность обмена белков в желточном мешке. Судьба желточного мешка у разных животных несколько различна. У птиц к концу периода инкубации остатки желточного мешка уже находятся внутри зародыша, после чего он быстро исчезает и к концу 6-х суток после вылупления полностью рассасывается. У млекопитающих желточный мешок бывает развит по-разному. У хищников он сравнительно большой, с сильно развитой сетью сосудов, а у приматов быстро сморщивается и исчезает без остатка до родов. Аллантоис развивается несколько позднее других внезародышевых органов. Он представляет собой мешковидный вырост вентральной стенки задней кишки. Следовательно, он образован энтодермой изнутри и спланхноплеврой снаружи. У рептилий и птиц аллантоис быстро дорастает до хориона и выполняет несколько функций. Прежде всего это вместилище для мочевины и мочевой кислоты, которые представляют собой конечные продукты обмена азотсодержащих органических веществ. В аллантоисе хорошо развита сосудистая сеть, благодаря чему вместе с хорионом он участвует в газообмене. При вылуплении наружная часть аллантоиса отбрасывается, а внутренняя — сохраняется в виде мочевого пузыря. У многих млекопитающих аллантоис тоже хорошо развит и вместе с хорионом образует хориоаллантоисную плаценту. Термин плацента означает тесное наложение или слияние зародышевых оболочек с тканями родительского организма. У приматов и некоторых других млекопитающих энтодермальная часть аллантоиса рудиментарна, а мезодермальные клетки образуют плотный тяж, протягивающийся от клоакального отдела к хориону. По мезодерме аллантоиса к хориону растут сосуды, посредством которых плацента выполняет выделительную, дыхательную и питательную функции. 62.Особенности эмбрионального развития человека. Эмбриональный период. В организмах, размножающихся половым путем, начинается с момента образования зиготы, а заканчивается по-разному: выходом из яйцевых оболочек (свободный личиночный тип эмбриогенеза), выходом из зародышевых оболочек (неличиночный тип), рождением (внутриутробный, вторично личиночный). Развитие разнообразно, но можно сгруппировать по принципу отношений с окружающей средой. Тип эмбриогенеза - совокупность признаков, которые обеспечивают развивающемуся организму связь со средой. Свободный личиночный тип характерен для животных, откладывающих небольшие яйца с маленьким количеством желтка. Наличие личинки – особой формы, отличающейся от взрослого организма. Личинка после метаморфоза превращается во взрослую особь. У многих морских животных, у сосальщиков и других паразитов. Неличиночный тип – яйца крупные, желтка много. Зародыши долгое время находятся под защитой яйцевых оболочек, используя запасы питательных веществ, отложенных в яйцеклетке. Акулы, скаты, круглые и плоские черви, многие насекомые и рептилии, птицы и яйцекладущие млекопитающие. Вторично личиночный тип – яйца мелкие, из яиц выходят подвижные зародыши, способные питаться. Развитие происходит под защитой специальных образований (капсул), в случае живорождения – в организме матери. Живорождение характерно для плацентарных, тропических скорпионов, сумчатых млекопитающих и некоторых рыб и насекомых. В эмбриогенезе человека выделяют 4 периода. 1. Начальный (1 неделя развития, до момента имплантации зародыша в слизистую матки). 2. Эмбриональный (2-8 недели). 3. Предплодный (9-12 недели). 4. Плодный (13 неделя – рождение). В эмбриональном периоде происходят гаструляция, бластуляция, нейруляция. В предплодном имеет место интенсивный органогенез, анатомическая закладка органов. Плодный период характеризуется созданием плода под защитой плодных оболочек. На начальном периоде имеется зигота – 1 клетка зародыша, в ней определяются отдельные участки цитоплазмы, происходят синтез ДНК, белков. Зигота обладает бисимитрическим строением. Постепенно происходит нарушение соотношения ядра и цитоплазмы, в результате происходит стимуляция процесса деления – дробления Стадия дробления – период интенсивных клеточных делений. Размер зародыша не увеличивается, а синтетические процессы идут активно. Происходит интенсивный синтез ДНК, РНК, гистоновых и других белков. Дробление выполняет функции: - образуется достаточное количество клеток, необходимых для формирования тканей и органов. - перераспределение желтка и цитоплазмы между дочерними клетками. 1 и 2 борозды деления идут по меридиану, а 3 по экватору. Ближе к анимальному полюсу. - определяется план зародыша – спинно-брюшная ось, переднее-задняя ось. - нормализуются ядерно-цитоплазматические отношения. Количество ядер растет, объем и масса сохраняются. Постепенно деление замедляется. У женщины через сутки после оплодотворения во второй трети яйцевода начинается дробление. Одновременно с этим процессом зигота перемещается по яйцеводу к полости матки. Образуются клетки 2 типов: более мелкие, в последствии они дают вспомогательную ткань – трофобласт, и более крупные клетки – эмбриобласт – «зачаток зародыша», дадут начало всем клеткам организма и клеткам некоторых вспомогательных частей. На 6-7 день после оплодотворения человеческий зародыш имеет размер 0,5 мм и состоит из 200 клеток. Он начинает прикрепляться к внутренней стенке матки, внедряется в слизистую матки, происходит имплантация. В течение суток погружается наполовину, спустя еще сутки – полностью. Затем мощно развивается трофобласт – образуются ворсинки, выросты, соприкасающиеся с кровью матери, получая питательные вещества и снабжая ими зародыша. На 2 неделе разрастаются внезародышевые части, т.е. те части, которые образованы зародышем, но играют сначала вспомогательную роль – амнион, хорион, желточный мешок. Это провизорные органы – ценогенетические структуры, не принимающие участие в формировании взрослого организма. Клеточный материал, из которого развивается зародыш – зародышевый щиток. На ранних этапах идет подготовительная работа, развивается не сам зародыш, а части, создающие необходимые условия для существования зародыша и обеспечивающие функции дыхания, питания, выведения продуктов метаболизма, создающие жидкую среду вокруг зародыша для защиты его. 3 неделя – формируется плацента, греч. «Лепешка». Состоит из 2 частей – зародышевой и материнской. Зародышевая – трофобласт и некоторые другие ткани (хорион – греч. «оболочка, послед»). Материнская – сильно видоизмененная слизистая оболочка матки. В ней разрушаются сосуды, разрыхляется соединительная ткань, разрушается и эпителий. Ворсинки хориона «купаются» в материнской крови. Площадь плацентарного сплетения 5 квадратных метров, а общая длина ворсинок хориона – 5 км. Материнский и зародышевый организмы не имеют общего кровотока, кровь не смешивается. Питательные вещества идут через стенки хориона. У 3 недельного зародыша появляются пупочные сосуды, врастающие в стенки хориона и выполняющие функции. Питания. 4 неделя. Размеры зародыша вместе с хорионом 5-7 мм. Начинается новый этап. Тело зародыша обособляется от внезародышевых частей. Зародыш приподнимается над амниотической жидкостью, с которой он связан затем только пупочными сосудами. В ходе эмбрионального развития у человека рано возникает желточный мешок - первый орган кроветворения, выполняющий запасание и переработку желтка, первый орган дыхания, питания. Первичные половые клетки начинают формироваться в желточном мешке. Имеется слепо замкнутый с 2 сторон кишечник. Печень – орган кроветворения. Бьется сердце. К концу 4 недели есть зачаток дыхательной системы. Размеры до 30мм. Кишечник растет в длину, в выпрямленном состоянии не помещается и начинает изгибаться. К концу 4 недели появляются лопаточки на боках. В них врастают нервы и мышцы – будущие руки и ноги. К концу недели существует дифференциация на части, к 5 неделе по бокам задней части головы и шеи впячиваются участки зародыша – образуются 4 пары жаберных щелей, изнутри выпячиваются части передней кишки, формируют 4 жаберных кармана. Между жаберными щелями и жаберными карманами нет связи. Из 1 пары жаберных щелей формируется среднее ухо. Из остальных – щитовидная и зобная железы. С 4 недели начинает формироваться нервная система. Образование нервной трубки (нервна пластинка – нервный желобок – нервная трубка). На переднем конце нервной пластинки возникают 3 мозговых пузыря, на 6 неделе уже имеются 5 мозговых пузырей, которые соответствуют отделам мозга, появляются слуховые пузырьки, глазные бокалы, обонятельные ямки. Происходит дифференциация мезодермы. Образуется хвост (34 день) до 10 мм. На 2 месяце закладываются первичные половые железы, куда мигрируют первичные половые клетки из желточного мешка. На 8 неделе происходит быстрое развитие амниотической оболочки и накопление жидкости. 9-10неделя – формирование почек, нефроны образуются в течение всего эмбриогенеза и еще 20 дней после рождения. 7 неделя – формирование зубных пластинок. Начало 3 месяца. Формируется плод. В течение месяца исчезает хвост (гибель клеток под действием лизосомальных ферментов), остаются рудиментарные позвонки. Голова в развитии опережает туловище, затем пропорции восстанавливаются. Начало 4 месяца. Размеры 20-22см. мышечная система сформирована, начинают двигаться. 5 месяц. Все тело покрыто волосяным покровом. Верхние конечности растут быстрее нижних и появляются раньше. 63.Постнатальный онтогенез и его периоды. Основные процессы: рост, формирование дефинитивных структур, половое созревание, репродукция, старение. 64.Старение как закономерный этап онтогенеза. Проявления старения на молекулярно-генетическом, клеточном, тканевом, органном и организменном уровнях. 65.Гипотезы, объясняющие механизмы старения. Влияние генетических факторов, условий и образа жизни на процесс старения. 66.Смерть как биологическое явление. Клиническая и биологическая смерть. Реанимация. Проблемы долголетия. Понятие о геронтологии и гериатрии. Старение – многоэтапный процесс, включающий влияние факторов внешней и внутренней среды. Старение общебиологическая закономерность «увядания» организма, свойственная всем живым существам. Старость - естественный этап онтогенеза, заканчивающийся смертью. Старость – следствие старения. Карл Маркс: « Мы должны рассматривать старение и смерть как естественный завершающий этап индивидуального развития. Жить – значит умирать». У разных биологических видов продолжительность жизни различна (даже у видов, занимающих сходные экологические ниши). Поэтому продолжительность жизни является видовой биологической индивидуальностью, сложившейся в ходе эволюционного процесса, контролируемой генетически. В пределах вида возможны отклонения до 50% средней продолжительности жизни в обе стороны. Кенгуру – 5 лет. Бобр – 50 лет. Тигр – 40 – 50 лет. Осел – 47 лет. Индийский слон – 70 – 77 лет. У человека средняя продолжительность жизни мужчин – 58 – 62 года, у женщин – 74 года (Воронеж). Хронологический возраст – количество прожитых лет человеком по документам. Биологический возраст – показывает, на сколько выглядит человек, (степень окостенения, зубная зрелость, степень развития половых органов). Признаки старения. Старение происходит на всех уровнях
Старость и болезни – единый патологический процесс. Например, наследственные синдромы преждевременного старения (прогерии). Симптомы: поседение, морщинистость кожи, облысение, атеросклероз, инфаркт миокарда, гиперхолестерин и другие симптомы. Могут проявляться в детском возрасте. В 3 – 5 лет имеют вид старческий вид, к 7 годам умирают от старости. Средняя продолжительность жизни таких больных – 12 лет, иногда доживали до 30 лет (максимум – 39 лет). Прогерии – наследственные заболевания, при которых получают резкое развитие один или несколько симптомов есте6ственного старения. Гипотезы старения. Существуют более300 различных гипотез.
Геронтология – наука о старости, изучающая основные закономерности старения на всех уровнях организации от молекулярного до организменного. Гериатрия – наука, изучающая особенности развития, течения, предупреждения заболеваний у людей преклонного возраста. Задача геронтологии – качественное и количественное продление жизни человека. |
