окислители. Окислительновосстановительные реакции Окислители и восстановители
 Скачать 0.87 Mb. Скачать 0.87 Mb.
|
Классификация окислительно-восстановительных реакцийОкислительно-восстановительные реакции обычно разделяют на четыре типа: межмолекулярные, внутримолекулярные, реакции диспропорционирования (самоокисления-самовосстановления), и реакции контрдиспропорционирования. Межмолекулярные реакции протекают с изменением степени окисления разных элементов из разных реагентов. При этом образуются разные продукты окисления и восстановления. 2Al0 + Fe+32O3 → Al+32O3 + 2Fe0, C0 + 4HN+5O3(конц) = C+4O2 ↑ + 4N+4O2 ↑+ 2H2O. Внутримолекулярные реакции – это такие реакции, в которых разные элементы из одного реагента переходят в разные продукты, например: (N-3H4)2Cr+62O7 → N20 ↑+ Cr+32O3 + 4 H2O, 2 NaN+5O-23 → 2 NaN+3O2 + O02↑. Реакции диспропорционирования (самоокисления-самовосстановления) – это такие реакции, в которых окислитель и восстановитель – один и тот же элемент одного реагента, который при этом переходит в разные продукты: 3Br2 + 6 KOH → 5KBr + KBrO3 + 3 H2O, Репропорционирование (конпропорционирование, контрдиспропорционирование) – это реакции, в которых окислитель и восстановитель – это один и тот же элемент, который из разных реагентов переходит в один продукт. Реакция, обратная диспропорционированию. 2H2S-2 + S+4O2 = 3S + 2H2O 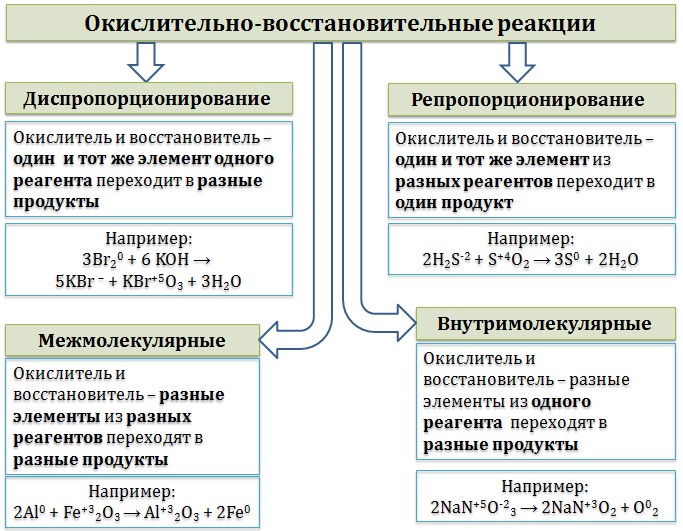 |
