Основные определения Ксенобиотик
 Скачать 0.94 Mb. Скачать 0.94 Mb.
|
|
Теория неионной диффузии Важной характеристикой для прогнозирования токсичности химического вещества является его липофильность. Согласно липидной теории клеточной депрессии, вещества, химически инертные в полярном растворителе – воде, могут оказывать угнетающее действие на клетки, богатые липидами, особенно на клетки центральной нервной системы. При этом воздействие ксенобиотика тем эффективнее, чем выше коэффициент распределения между липофильным растворителем (L) и водой (Н2О): Таким образом, распределение ксенобиотика между органической (липидный слой клеточной мембраны) и водной (внутри- или внеклеточная жидкость) фазами – важная характеристика токсичности. Высокими значениями коэффициента распределения алкильных производных ртути [диметилртуть (СН3)2Hg, диэтилртуть (C2H5)2Hg] и мышьяка [монометимышьяковая кислота (CH3)2AsO(OH)2 и диметилмышьяковая кислота (CH3)2AsO(OH)] объясняются их избирательное накопление в тканях мозга и нейротоксичность. Приближенное значение коэффициента распределения масло/вода можно рассчитать по эмпирической формуле: где И.В. Лазаревым была разработана классификация веществ, в основу которой положена взаимосвязь биологического действия веществ с их липофильностью. Согласно данной системе вещества объединены в группы в соответствии с возрастающими значениями коэффициента распределения: в первую включены неэлектролиты с Вещества первых четырех групп характеризуются плохой растворимостью в жирах и липоидах, хорошей растворимостью в воде, большой сорбционной емкостью организма, медленно проникают в клетки и медленно выводятся из них; последних пяти групп – плохой растворимостью в воде, хорошей растворимостью в жирах и липоидах, малой сорбционной емкостью организма, быстрым проникновением в клетки и быстрым выведением. Коэффициент распределения Большинство органических и неорганических соединений являются электролитами: либо слабыми кислотами, либо основаниями. Поэтому скорость транспорта электролитов через мембраны будет, прежде всего, определяться степенью ионизации молекулы в данных условиях, а затем степенью растворимости нейтральной молекулы в жирах. Степень ионизации органических электролитов является функцией разности отрицательного логарифма константы диссоциации рКа и рН среды. Эта зависимость выражается уравнением Хендерсона-Хассельбаха: для кислот: для оснований: Из закона действующих масс для равновесия следует, при Рассмотрим примеры, демонстрирующие зависимость распределения токсиканта между биологическими средами от его кислотно-основной природы и от рН среды. 1. Токсикант – слабая кислота, подвергающаяся ионизации в соответствии с уравнением НА↔Н+ + А-. Области преобладания (устойчивости, существования) молекулярной и анионной форм кислоты на рН-диаграмме разграничены прямой линией при  В соответствии с уравнением Хендерсона-Хассельбаха: соотношение заряженной и незаряженной форм токсиканта кислотной природы зависит от рН следующим образом: откуда следует, что при В качестве примера рассмотрим равновесные процессы в биологических средах для ксенобиотика кислотной природы-фуросемида (рКа 3,9). Пользуясь рН-диаграммой, нетрудно обнаружить, что в содержимом желудка (рН 1,5-1,8) преобладает незаряженная (протонированная) форма фуросемида НА, хорошо взаимодействующая с липидами (неполярный растворитель). В крови (рН 7,35-7,45) или моче (рН 4,8-7,4) фуросемид подвергается ионизации с образованием анионной формы А-. Синильная кислота рКа 9,2 (аналогично). 2. Токсикант — слабое основание В, протонированная форма которого подвергается ионизации в соответствии с уравнением ВН+↔В+ Н+. Как и в предыдущем примере, области преобладания (устойчивости, существования) молекулярной и анионной форм основания на рН-диаграмме разграничены прямой линией при 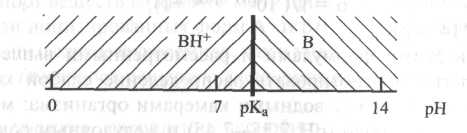 В соответствии с уравнением Хендерсона-Хассельбаха: соотношение заряженной и незаряженной форм токсиканта кислотной природы зависит от рН следующим образом: откуда следует, что при В качестве примера рассмотрим равновесные процессы в биологических средах для ксенобиотика основной природы – эфедрина (рКа 9,6). Из рН-диаграммы следует, что в содержимом желудка, крови и моче преобладает протонированная форма эфедрина ВН+, так как значения рН этих биологических сред ниже рКа эфедрина. Пользуясь этими формулами легко прогнозировать распределение слабой кислоты и слабого основания между водными камерами организма: мочой (рН 4,8-7,4), плазмой крови (рН 7,35-7,45) и желудочным соком (1,5-1,8) (рис.). Например, из рис. видно, что содержание фуросемида в крови значительно превышает его содержание в содержимом желудка, что свидетельствует о чрезвычайно высокой степени его абсорбции. Для эфедрина, напротив, всасывание в кровь незначительно, так как преобладающая форма в содержимом желудка – ионная ВН+. 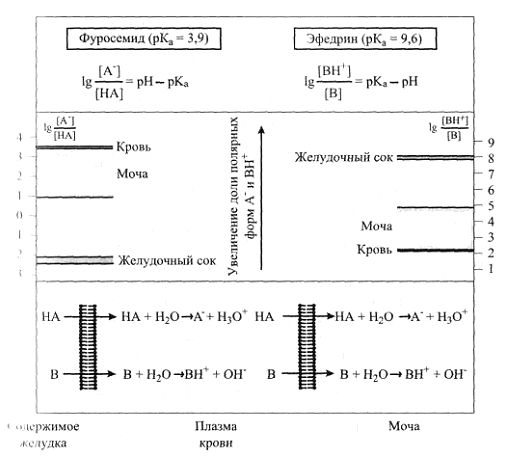 Рис. Распределение слабой кислоты (фуросемид) и слабого основания (эфедрин) между жидкими средами организма Большинство токсикантов – органические вещества с различной растворимостью в липидах; растворимостью определяется их способность проникать через липидный слой. Ионизированные формы слабых органических кислот или оснований (гидрофильные вещества) обычно имеют низкую растворимость в липидах и не способны беспрепятственно преодолеть липидное пространство мембраны (рис.). Напротив, неионизированные формы (гидрофобные/липофильные вещества) хорошо растворимы в липидах и свободно диффундируют через мембраны. ► Незаряженные липофильные вещества могут проникать через липидную сердцевину плазматической мембраны. Некоторые полярные молекулы, в том числе и вода, также способны легко пересекать бислой через межмолекулярные поры. ► Гидрофильные вещества или крупные полярные молекулы, которые нерастворяются в липидах, чтобы пройти сквозь клеточную мембрану, должны взаимодействовать со специальными белками-переносчиками или белком трансмембранного канала. • Физико-химические характеристики токсиканта и биологической среды, влияющие на механизмы токсичности Токсикокинетические характеристики вещества обусловлены как его свойствами, так и особенностями структурно-функциональной организации клеток, органов, тканей и организма в целом. Важнейшие свойства вещества, определяющие его токсикокинетику: ◦ Агрегатное состояние. Биодоступность ксенобиотика, т.е. способность поступать во внутренние среды организма, а также пути проникновения во многом определяются агрегатным состоянием. ◦ Коэффициент распределения в системе «масло-вода». ◦ Размер молекул. ◦ Наличие заряда в молекуле. Ионы плохо проникают через ионные каналы, не проникают через липидные мембраны, не растворяются в липидной фазе клеток и тканей. ◦ Величина константы диссоциации солей, слабых кислот и оснований. Определяет относительную часть молекул токсиканта, диссоциировавших на ионы в условиях внутренней среды. ◦ Растворимость в жидких биосредах. Например, малорастворимые высокодисперсные порошки металлов цинка, меди, свинца, железа или их оксиды независимо от способа поступления в организм проявляют меньшую токсичность, чем хорошо растворимые нитраты или сульфаты данных металлов. Образование малорастворимых соединений в биосреде приводит к снижению их всасывания, что снижает токсичность. Пример: Растворимость оксида мышьяка (III) AS2O3 («белый мышьяк») возрастает в кислой среде (содержимое желудка, соки, вино). При этом образуется устойчивая катионная форма AsO+, которая легко абсорбируется по ионным каналам катионов биогенных элементов. Этим можно объяснить известные исторические факты отравлений вином, в которое добавлен «белый мышьяк». ◦ Химические свойства. Влияют на сродство токсикантов к структурным элементам клеток различных тканей и органов. Важнейшие свойства биосистем: ◦ Соотношение воды и жира. Биологические структуры, ткани, органы могут содержать большое количество липидов (биологические мембраны, жировая ткань, мозг) либо преимущественно состоять из воды (мышечная ткань, соединительная ткань и т.д.). Чем больше жира в структуре, тем в большем количестве в ней накапливаются жирорастворимые вещества. ◦ Окислительно-восстановительный потенциал E0 и pH среды. Жидкие биосреды представляют собой не что иное, как водные растворы биогенных соединений с определенными значениями E0 и pH в локальных точках. Область существования жидких биосред ограничена областью устойчивости воды. Стандартные значения потенциалов, ограничивающие эту область, соответствуют окислительно-восстановительным парам O2/H2O, H2O/H2 и равны соответственно 0,82В и 0,00В. Любой токсикант, область устойчивости которого находится вне области существования жидких биосред, проявляется свойства окислителя или восстановителя по отношению к биогенным соединениями или воде. Например, возможно окисление Fe(II) в гемоглобине до Fe(III) с образованием метгемоглобина веществами разных химических классов. ◦ Наличие молекул, активно связывающих токсикант. • Пути поступления, абсорбция и экскреция ксенобиотиков ♦ Поступление и абсорбция Известно, что одинаковые дозы ксенобиотиков могут давать различные токсические эффекты. Это в первую очередь обусловлено разными способами поступления их в организм, а также особенностями абсорбции, распределения, механизмов биотрансформации и способов экскреции (рис.). 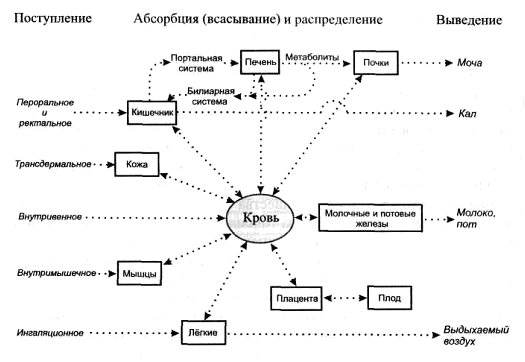 Рис. Пути поступления, абсорбции, распределения и выведения токсикантов Поступление и абсорбция через желудочно-кишечный тракт ЖКТ– один из наиболее важных центров абсорбции ксенобиотиков. Многие токсиканты из окружающей среды входят в пищевые цепи и абсорбируются вместе с компонентами пищи из ЖКТ. Токсичные вещества, за исключением прижигающих ядов, до всасывания в кровоток не оказывают повреждающего действия на организм, и только после всасывания можно говорить о формировании токсического эффекта. Абсорбция токсиканта возможна во всех отделах ЖКТ, от ротовой полости до прямой кишки. Большинство токсикантов всасываются по механизму простой диффузии. Липофильные вещества абсорбируются быстрее и эффективнее, чем водорастворимые соединения. Константы ионизации ксенобиотика, площадь всасывающей поверхности, скорость кровотока — важные параметры процесса абсорбции. В ЖКТ млекопитающих содержатся специальные транспортные системы для абсорбции питательных веществ и электролитов, некоторые из них снижают абсорбцию ксенобиотиков (преобладающее всасывание ряда веществ в различных отделах). Большое значение имеет способность токсичного вещества подвергаться химическому превращению в кислой среде желудка. Если токсикант долго находится в кишечнике, то пропорционально возрастает продолжительность абсорбции. Время пребывания химического вещества в кишечнике зависит от его растворимости и от кишечной моторики. Экспериментально показано, что токсичность некоторых химических соединений возрастает с разведением поглощенного токсичного раствора. Это объясняется более интенсивным всасыванием в результате возрастания поверхности всасывания при увеличении объема токсичного раствора. Пресистемной элиминацией, или эффектом первого прохожденияназывается процесс удаления химического вещества до поступления его в системную циркуляцию (см. рис.). Пресистемной элиминации подвергаются химические вещества, абсорбируемые в ЖКТ. Например, при пероральном поступлении после всасывания в кишечнике ксенобиотик доставляется с кровью по портальной венозной системе в печень, где подвергается внутриклеточной биотрансформации и экскреции гепатоцитами в желчь. Таким образом, при пероральном поступлении проникновение токсиканта в системный кровоток зависит от эффективности абсорбции в желудке и кишечнике, биотрансформации и элиминации в желчь. Пресистемная элиминация обычно уменьшает токсическое действие химического соединения. Ингаляционное поступление токсикантов В альвеолах абсорбируются газы, пары летучих жидкостей и аэрозоли. Площадь активной поверхности альвеол составляет 90-100 м2. Альвеолы имеют мощное кровоснабжение. Прежде чем «летучий» яд попадет в альвеолы, он проходит через носовой ход с носовыми пазухами, в результате чего значительно увеличивается площадь абсорбирующей поверхности. Частицы яда при достаточно хорошей растворимости в воде и высокой реакционной способности могут сохраняться в носовой слизи и удаляться при дыхании и чиханье, не попадая в легкие. ► ♦ При попадании в легкие «летучий» яд диффундирует через альвеолярные мембраны в кровь и растворяется до тех пор, пока не установится равновесие между кровью и газовой фазой альвеол При достижении динамического равновесия скорость переноса молекул «летучего» яда из альвеол в кровь становится равна скорости удаления его молекул из крови в альвеолы. Значение коэффициента распределения зависит в первую очередь от химической природы яда. Для суждения о накоплении веществ в организме используют коэффициент растворимости вода/воздух: где С увеличением Вещества с меньшим коэффициентом растворимости имеют большую активность. Причиной этому служит их лучшая растворимость в липоидах. ♦ Для «летучих» ядов с низкими значениями коэффициента распределения (Скр<<Сальв) абсорбция зависит в основном от скорости кровотока через легкие. ♦ Для летучих веществ с высоким отношением коэффициента распределения (Cкр>>Cальв) абсорбция является функцией частоты и глубины дыхания. ► Кровь переносит молекулы «летучего» яда по всему организму. Молекулы яда перемещаются из крови в ткани. После частичного высвобождения токсиканта в ткани кровь возвращается к легким для дополнительного насыщения. Это продолжается до достижения равновесия между кровью и отдельной тканью: На абсорбцию аэрозолей влияют размер частиц дисперсной фазы и растворимость в воде химических веществ, присутствующих в аэрозоле. Место осаждения частиц зависит от их размера: - частицы размером более 5 мкм обычно оседают в носоглотке и удаляются с носовой слизью при дыхании и чиханье; Покрытые слизью носовые реснички при движении ускоряют перемещение нерастворимых частиц. Растворимые частицы могут растворяться в носовой слизи и также заглатываются или абсорбируются через носовой эпителий в кровь. - частицы размером 1 мкм и меньше попадают в альвеолы, могут абсорбироваться в кровь или удаляться через лимфатическую систему после поглощения альвеолярными макрофагами. Удаление или абсорбция частиц аэрозолей из альвеол протекает по трем основным механизмам: - механически; - фагоцитозом с участием большого числа макрофагов легких, поглощающих частицы экзогенного происхождения; - через лимфатическую систему, причем макрочастицы могут долго оставаться в лимфатических узлах. Полного удаления частиц из альвеол не происходит. Обычно в 1-е сутки удаляется около 20% частиц; оставшиеся частицы выводятся очень медленно. Скорость выведения веществ можно прогнозировать на основании их растворимости в альвеолярной жидкости: чем меньше растворимость, тем медленнее удаление. |
