патфиз шпоры экзамен. Ответы к экзамену по патологической физиологии doc
 Скачать 2.43 Mb. Скачать 2.43 Mb.
|
|
136*. Нарушение функции слюнных желез. Причины и проявления гипо- и гиперсаливации. Нарушения функции слюнных желез. Слюнные железы – пищеварительные железы, выделяющие в полость рта специфический секрет, входящий в состав слюны. Секрет всех слюнных желез, смешанный в полости рта, образует слюну. В норме у человека выделяется до 2,0 л. слюны в сутки. Нарушение саливации: Гиперсаливация характеризуется обильным слюноотделением, возникает рефлекторно, наблюдается у лиц страдающих б-нью Паркинсана, эпидемическим эндефалитом, нарушением мозгового кровообращения, стоматитом, гингивитом, невралгией тройничного нерва, лицевого нерва, токсикозом у беременных, встречается при уремии, отравлении никотином, приеме ряда лекарственных препаратов (пилокарпин и др.). Гиперсаливация может привести к обезвоживанию и истощению организма, нарушению обмена веществ. Обильное количество заглатываемой слюны ведет к нейтрализации кислого желудочного сока, к гипоацидному состоянию, ахилии и соответственно нарушению пищеварения в желудке. Гипосаливация (гипосиалия, сиалопения) и асиалия (т.е. крайняя степень гипосаливация) сопролвождается сухостью слизистой оболочки рта (ксеростомией) – являются симптомами как общих заболеваний (септическое состояние, пневмония, диабет, злокачественная анемия, сыпной и брюшной тиф, при лихорадке), в результате рефлекторного торможения деятельности слюнных желез, так и патологии собственно слюнных желез, их воспаления (сиаладенит), закупорки выводных протоков (сиалолитиаз). Следствием гипосаливации являются недостаточное пропитывание пищевого комка ферментами слюны, затруднение глотания, развитие патогенной микрофлоры и стоматита, нарушение возникновения вкусовых ощущений и в конечном итоге нарушение формирования пищевого комка, аппетита, минерализации эмали зубов, секреторной и моторной функции желудочно-кишечного тракта, процессов пищеварения. 137*. Современные представления об этиологии и патогенезе кариеса зубов. Кариес зубов – патологический процесс, характеризующийся прогрессирующей деструкцией твердых тканей зуба (эмали и дентина) с образованием дефекта в виде полости. Возникновение кариеса обусловлено сочетанными экзогенными и эндогенными воздействиями, а патогенез его определяется взаимодействием общих и местных факторов. Экзогенные факторы: алиментарные: дефицит белков, витаминов В и Д минеральных солей (Са, Р), ряда микроэлементов (селен, магний, кадмий), избыточное потребление углеводов, жиров (несбалансированное питание), а также микрофлора полости рта (зубного налета), патология слюнных желез. Эндогенные факторы: генетические (наследственно-конституционные) факторы, дисгормональные расстройства. Известную этиологическую роль в развитии кариеса зубов играют также гиподинамия и снижение жевательной нагрузки. В патогенезе выделяют две основные группы факторов – общие и местные: нарушения общей метаболической системы обмена организма, включая обмен в обызвествленных тканях с их регуляторными механизмами и нарушение в местной системе (слюнные железы – слюна – ротовая жидкость – зубной налет – ткани зуба – пародонт). Ведущим звеном в патогенезе кариеса зубов является нарушение процессов реминерализации эмали зуба. Белковые матриксы эмалевых призм являются своеобразными нуклеаторами, на которые ориентируются кристаллы гидроксиапатита, основные минеральные компоненты которых – кальций и фосфор – находятся в прямой химической связи с белками эмали. Эти составляющие обеспечивают реминерализацию, гомеостаз и резистентностьэмали зуба. При кариесе нарушается прямая химическая связь между указанными компонентами. Процессы реминеризации возможны только при сохранении функции белковых матриксов эмалевых призм. В соответствии с данными современных морфологических и биохимических исследований кариозного поражения, а также данными о физиологическом состоянии твердых тканей и их взаимодействии с компонентами ротовой жидкости развитие кариеса мы представляем следующим образом. При определенных условиях (избыток сахара в питании, негигиеническое содержание полости рта и др.) на ограниченном участке поверхности или в складках эмали зуба в зубном налете суточной или большей давности рН снижается до критического уровня, который поддерживается длительное время или имеет интермиттирующий характер. Микроорганизмы зубного налета прочно оседают на поверхности зуба и в результате ферментативных процессов лизируют защитную органическую оболочку зуба – пелликулу. Таким образом, создается возможность непосредственного контакта кислот, образующихся в зубном налете, с минеральными веществами эмали. Ионы Н+ в зоне длительного источника кислотообразования, соприкасаясь с апатитами, вызывают их растворение, которое может быть равномерным, если кислотообразование на поверхности эмали происходит достаточно активно, или неравномерным, если образовавшиеся кислоты частично нейтрализуются компонентами слюны. В силу того, что поверхностный слой эмали трудно поддается растворению (в нем больше фторапатитов), ионы Н+ по межкристаллическим пространствам попадают в подповерхностный слой, где вызывают деминерализацию. Проникновение ионов Н+ возможно в те участки подповерхностного слоя эмали, где призмы доходят до поверхности, и невозможно там, где поверхность эмали образована беспризменным слоем. В последнем случае деминерализация происходит по типу равномерного очагового растворения поверхностного слоя эмали. Основными путями проникновения Н+ служат межпризменные микропространства. При этом кристаллы поверхностного слоя эмали частично растворяются образуя микропоры. В подповерхностном слое частичная деминерализация происходит в менее резистентных участках: поперечная исчерченность призм и полосы Ретциуса. Освободившиеся ионы кальция, фосфора и других элементов выходят в ротовую жидкость. Зона деминерализации распространяется параллельно поверхности зуба, так как концентрация Н+ поддерживается за счет кислотообразования на участке поверхности эмали покрытом зубным налетом. Глубокое проникновение ионов в эмаль в начале процесса деминерализации невозможно, потому что они нейтрализуются. При интермиттирующем типе кислотообразования освободившиеся в процессе деминерализации ионы кальция могут вновь из ротовой жидкости проникать в микропространства эмали, где вступают в связь с апатитами или образуют аморфное вещество. При продолжающемся образовании кислоты и процессе деминерализации микропространства в эмали постепенно увеличиваются. В них проникают органические вещества и микроорганизмы, перенося источник кислотообразования внутрь эмали. На этой стадии деминерализация распространяется как параллельно поверхности зуба, так и внутрь, образуя конусовидный очаг поражения. Поверхностный слой эмали над очагом поражения растворяется медленно не только вследствие ее большей устойчивости к растворению из-за наличия фторапатитов, но также из-за большей выраженности процессов реминерализации. Однако при продолжении кислотообразования микропоры в поверхностном слое расширяются, эмаль истончается и проламывается. В дальнейшем процессе  деструкции имеет место как деминерализация так и лизис органической субстанции микроорганизмами. По периферии очага деминерализации образуется зона гиперминерализации ("защитный вал") за счет проникновения в нее освободившихся ионов кальция, фосфора и др. На течение кариозного процесса влияют состав и свойства ротовой жидкости, структурные особенности и биохимический состав твердых тканей зуба, состояние пульпы, функциональное состояние органов и систем организма в период формирования и созревания тканей. деструкции имеет место как деминерализация так и лизис органической субстанции микроорганизмами. По периферии очага деминерализации образуется зона гиперминерализации ("защитный вал") за счет проникновения в нее освободившихся ионов кальция, фосфора и др. На течение кариозного процесса влияют состав и свойства ротовой жидкости, структурные особенности и биохимический состав твердых тканей зуба, состояние пульпы, функциональное состояние органов и систем организма в период формирования и созревания тканей.Кариозный процесс прогрессирует, если снижается скорость слюноотделения, уменьшается количество слюны, повышается ее вязкость. Болезнь может замедляться или приостанавливаться на стадии пятна при нормализации слюноотделения. Быстрому развитию кариеса способствует низкое содержание фтора и высокое содержание карбонатов в эмали. Хорошо выраженная сферичность коронки, гладкая поверхность, толстая эмаль определяют устойчивость к кариесу. Ямки, бороздки, складки, углубления, тонкая эмаль являются зонами, восприимчивыми к кариесу. В зубах с удаленной пульпой (депульпированных) кариес развивается значительно реже, течение его медленнее, а патоморфология несколько отличается от кариеса недепульпированных зубов. Эти особенности можно объяснить нарушением проницаемости в депульпированных зубах 138*. Современные представления об этиологии и патогенезе пародонтитов. Участие аутоиммунных реакций и нейрогенных дистрофий в патогенезе пародонтитов. П 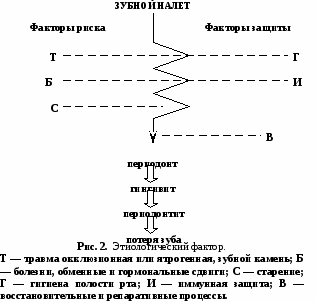 ародонтит – заболевание пародонта, характеризующееся поражением всех его элементов, разрушением зубодесневого соединения и прогрессирующей деструкцией альвеолярных отростков, приводящее без соответсующего лечения к выпадению зубов. ародонтит – заболевание пародонта, характеризующееся поражением всех его элементов, разрушением зубодесневого соединения и прогрессирующей деструкцией альвеолярных отростков, приводящее без соответсующего лечения к выпадению зубов.На протяжении нескольких десятилетий ведущими учеными установлена определяющая взаимосвязь между микробиологическими, иммунологическими, травматическими агентами в развитии болезней периодонта. В многочисленных публикациях приведены факты, свидетельствующие о влиянии местных факторов в развитии патологических состояний тканей периодонта, которые, в дальнейшем, оказывают влияние на организм в целом. Также доказана взаимосвязь между анатомо-физиологическими особенностями периодонтальных тканей, составом их структурных компонентов и микрофлорой полости рта в развитии воспалительных заболеваний периодонта. Особое значение ряд исследователей придают биологической природе заболевания периодонта и считают, что именно местные причины, действующие как стимуляторы воспаления, являются ведущими в этиологии и патогенезе заболеваний периодонта (рис. 2). По мнению этих авторов, полость рта рассматривается, как сбалансированная биологическая система, а заболевания периодонта в большинстве случаев развиваются в результате нарушения равновесия между бактериальным симбиозом и тканями полости рта. Наравне с этим установлено, что ключевыми звеньями в этиологии периодонтальных заболеваний являются три главных фактора:
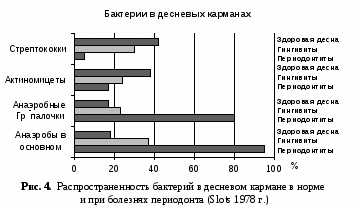 Одним из самых мощных этиологических агентов, вызывающим иммунную реакцию, является микробный фактор, который обуславливает различные клинические проявления заболеваний периодонта. При этом в патогенезе болезней периодонта главное место занимает фактор накопления микроорганизмов зубного налета, его объем, длительность пребывания в участках десны и инвазии в ткани периодонта. Именно влиянием видовой специфичности микробного налета объясняют большинство исследователей развитие воспалительных изменений в периодонте с различными клиническими изменениями. В этом направлении стали более детально изучать состав и специфичность микроорганизмов, механизм образования и прикрепления зубного налета к структурным компонентам тканей ротовой полости и их патогенный потенциал. Всемирная организация здравоохранения определяет понятие зубного налета как «специфическое, но весьма различное по структуре образование на поверхности зуба, обусловленное скоплением и ростом микробов». В целом в полости рта выявлено 300–400 видов микроорганизмов, из них только несколько (7–10) являются вероятными патогенами для тканей периодонта, и называются в литературе как периодонтопатогенные микроорганизмы. Ряд исследователей дает разное описание видового состава микрофлоры периодонта и их связь с расовыми, климатическими, социальными, гигиеническими и возрастными различиями исследуемых групп. Так, доказано, что количество бактерий в единице объема зубного налета очень велико и зависит от возраста, гигиенического воспитания, питания, ятрогенных факторов и факторов риска. Согласно данным литературы в интактном периодонте обнаруживают, главным образом, грамположительные кокки, в частности стрептококки и актиномицеты (рис. 4). За последние годы установлено, что более 70% колоний образуют стрептококки типа Str.salivarius, 15% — вейлонеллы и нейссерии. Остальная флора представлена дифтероидами, лактобактериями, стафилококками, лептотрихиями, фузобактериями, актиномицетами и дрожжеподобными грибами. Микробная флора зубного налета изменчива, как в количественном, так и в качественном отношении и характеризуется различной патогенностью отдельных бактериальных групп и серотипов. Многими исследователями установлено, что основная роль в развитии воспаления десны принадлежит стрептококкам и стафилококкам, но вместе с тем особое место в патологии периодонта занимают бактероиды, фузобактерии, вейлонеллы, спирохеты. Среди них особой патогенностью отличаются грамположительные и грамотрицательные кокки, а также грамположительные бациллы, фузобактерии, спирохеты, актиномицеты и др. Видовая специфичность микроорганизмов зубного налета непостоянна и зависит от эндогенных и, особенно, экзогенных факторов. Так, интенсивность образования зубного налета находится в прямой зависимости от состава слюны, ее вязкости, микрофлоры полости рта, десквамации эпителия слизистой оболочки полости рта, местных воспалительных процессов и особенно от умения чистить зубы, десна и язык. Зубной налет устойчив к смыванию слюной или полосканию рта, так как его поверхность покрыта слизистым полупроницаемым гелем, в виде мукоидной пленки, которая препятствует нейтрализующему действию слюны на бактерии зубного налета. В тоже время микробный состав зубного налета в значительной степени варьирует в различных участках полости рта. Практически важно знать места скапливания зубного налета в полости рта — зубодесневые карманы, ямки, фиссуры на поверхности зубов, участки на слизистой оболочке десны, язык, которые необходимо объяснять пациентам при мотивации. Известно, что степень тяжести периодонтита находится в прямой зависимости от количества зубного налета и общей микробной обсемененности полости рта и в обратной — от эффективности гигиенического режима мероприятий в ротовой полости. Нельзя игнорировать общепризнанный факт вирулентности различных видов микроорганизмов или общую патогенность всей флоры зубного налета. Вирулентность бактерий может выражаться в прямом токсическом воздействии, вызывающим воспаление и деструкцию, а также опосредованно. Эти процессы взаимосвязаны и обусловлены факторами вирулентности микробов, которые распределяются на две группы: Одним из самых мощных этиологических агентов, вызывающим иммунную реакцию, является микробный фактор, который обуславливает различные клинические проявления заболеваний периодонта. При этом в патогенезе болезней периодонта главное место занимает фактор накопления микроорганизмов зубного налета, его объем, длительность пребывания в участках десны и инвазии в ткани периодонта. Именно влиянием видовой специфичности микробного налета объясняют большинство исследователей развитие воспалительных изменений в периодонте с различными клиническими изменениями. В этом направлении стали более детально изучать состав и специфичность микроорганизмов, механизм образования и прикрепления зубного налета к структурным компонентам тканей ротовой полости и их патогенный потенциал. Всемирная организация здравоохранения определяет понятие зубного налета как «специфическое, но весьма различное по структуре образование на поверхности зуба, обусловленное скоплением и ростом микробов». В целом в полости рта выявлено 300–400 видов микроорганизмов, из них только несколько (7–10) являются вероятными патогенами для тканей периодонта, и называются в литературе как периодонтопатогенные микроорганизмы. Ряд исследователей дает разное описание видового состава микрофлоры периодонта и их связь с расовыми, климатическими, социальными, гигиеническими и возрастными различиями исследуемых групп. Так, доказано, что количество бактерий в единице объема зубного налета очень велико и зависит от возраста, гигиенического воспитания, питания, ятрогенных факторов и факторов риска. Согласно данным литературы в интактном периодонте обнаруживают, главным образом, грамположительные кокки, в частности стрептококки и актиномицеты (рис. 4). За последние годы установлено, что более 70% колоний образуют стрептококки типа Str.salivarius, 15% — вейлонеллы и нейссерии. Остальная флора представлена дифтероидами, лактобактериями, стафилококками, лептотрихиями, фузобактериями, актиномицетами и дрожжеподобными грибами. Микробная флора зубного налета изменчива, как в количественном, так и в качественном отношении и характеризуется различной патогенностью отдельных бактериальных групп и серотипов. Многими исследователями установлено, что основная роль в развитии воспаления десны принадлежит стрептококкам и стафилококкам, но вместе с тем особое место в патологии периодонта занимают бактероиды, фузобактерии, вейлонеллы, спирохеты. Среди них особой патогенностью отличаются грамположительные и грамотрицательные кокки, а также грамположительные бациллы, фузобактерии, спирохеты, актиномицеты и др. Видовая специфичность микроорганизмов зубного налета непостоянна и зависит от эндогенных и, особенно, экзогенных факторов. Так, интенсивность образования зубного налета находится в прямой зависимости от состава слюны, ее вязкости, микрофлоры полости рта, десквамации эпителия слизистой оболочки полости рта, местных воспалительных процессов и особенно от умения чистить зубы, десна и язык. Зубной налет устойчив к смыванию слюной или полосканию рта, так как его поверхность покрыта слизистым полупроницаемым гелем, в виде мукоидной пленки, которая препятствует нейтрализующему действию слюны на бактерии зубного налета. В тоже время микробный состав зубного налета в значительной степени варьирует в различных участках полости рта. Практически важно знать места скапливания зубного налета в полости рта — зубодесневые карманы, ямки, фиссуры на поверхности зубов, участки на слизистой оболочке десны, язык, которые необходимо объяснять пациентам при мотивации. Известно, что степень тяжести периодонтита находится в прямой зависимости от количества зубного налета и общей микробной обсемененности полости рта и в обратной — от эффективности гигиенического режима мероприятий в ротовой полости. Нельзя игнорировать общепризнанный факт вирулентности различных видов микроорганизмов или общую патогенность всей флоры зубного налета. Вирулентность бактерий может выражаться в прямом токсическом воздействии, вызывающим воспаление и деструкцию, а также опосредованно. Эти процессы взаимосвязаны и обусловлены факторами вирулентности микробов, которые распределяются на две группы:1 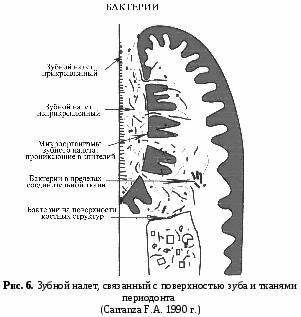 — факторы, определяющие способность микробов прикрепляться к тканям и образовывать колонии; — факторы, определяющие способность микробов прикрепляться к тканям и образовывать колонии;2 — факторы, вызывающие деструкцию тканей организма. Периодонтальные патогены обладают различными механизмами фиксации к тканям, проникновения и фиксации в зубном налете. Токсическое действие бактерий определяется их способностью не только вырабатывать токсины, но и проникать в ткани организма. Последнее свойство называется инвазивностью. С помощью бактериологических, иммунологических и ультраструктурных методов исследований установлено наличие микробов и в межклеточном веществе, и внутри клеток эпителия, и в соединительной ткани десны. Зубной налет, продвигаясь по мере роста под десневой край, вызывает раздражение тканей за счет микроорганизмов и их токсинов, что в дальнейшем приводит к изменению или повреждению эпителия десневой бороздки и воспалению прилежащих тканей (рис. 6). Бактериальный налет быстро растет благодаря наслаиванию новых микробов. Но кроме микробов, в зубном налете имеются погибшие лейкоциты, макрофаги, эпителиальные клетки. Быстрому росту зубного налета особенно способствует мягкая пища с большим количеством легкоферментируемых углеводов. Если мягкий зубной налет не удалить, он превращается в зубной камень, о чем следует информировать пациента. Для врачей-стоматологов важно учитывать, что ответная реакция тканей полости рта на воздействие микробных и других раздражителей, как правило, сопровождается в последующем формированием очагов фокальной инфекции в организме человека. В литературе описаны научно-обоснованные факты о взаимосвязи между воздействием местных факторов и общим уровнем здоровья при заболеваниях периодонта. Все эти процессы видоизменяются и зависят от иммунологической резистентности, в первую очередь, со стороны местных тканей, а также от уровня общей сопротивляемости организма и представлены в виде схемы (по данным Regezi J., 1993 г.):
Механизмы воздействия микробов на ткани периодонта В настоящее время существуют аргументированные мнения относительно механизмов воздействия микроорганизмов на ткани периодонта. Все они базируются на достоверных фактах, указывающих, что микроорганизмы при своей жизнедеятельности выделяют ряд специфичных ингредиентов, которые способны вызывать различные патологические реакции со стороны местных тканей, с последующим изменением системных органов. Доказано, что воспаление десневых тканей начинается именно в пределах поддесневой области, и обусловлено воздействием микроорганизмов на поверхность десневого эпителия и вглубь лежащие ткани в следствии: 1) микробной инвазии тканей; 2) выделения эндотоксинов из микроорганизмов; 3) выделения энзимов из микроорганизмов; 4) наличия зубного налета и образования зубного камня; 5) реакции антиген-антитело. При гингивите и периодонтите в состав микрофлоры могут входить фузобактрии, лептотрихии, грамположительные кокки, бактероиды и др. Кроме того, следует учитывать, что ключевую роль в патогенезе заболеваний периодонта занимают продукты жизнедеятельности микробов — токсины. Известно, что экзотоксины — производные грамположительной микрофлоры, являются обычными для полости рта и не имеют выраженного патогенетического потенциала. В то же время, эндотоксины — производные грамотрицательной микрофлоры, которые устойчивы к температурным воздействиям, могут проявлять свое агрессивное действие на месте прикрепления бактериальной бляшки и стимулируют формирование антител, вызывая тем самым вазомоторные расстройства, что приводит к геморрагическому некрозу чаще в пределах десневой бороздки. С этих позиций многие периодонтологи считают, что деструктивные формы периодонтита следует рассматривать преимущественно как инфекционное заболевание, вызванное грамотрицательными бактериями. В патогенезе заболеваний периодонта существенную роль играют энзимы, которые выделяются микроорганизмами при гибели микробной клетки. Они, благодаря своей метаболической активности, способны вызывать целевую деструкцию тканей и прямо участвовать в механизмах образования периодонтального кармана путем повышения проницаемости сосудов периодонта. За счет повышенной проницаемости сосудистой стенки, воспалительный экссудат проникает через нее в десневую бороздку, и увеличение десневой жидкости является начальным признаком воспаления десны. Клинические проявления повышенной проницаемости сосудов — это отек десны, изменения цвета и рельефа десны с возможным нарушением целостности эпителия. В настоящее время нет сомнений о существовании прямой зависимости между формированием зубного налета и развитием гингивита у лиц со здоровой десной. Как известно, зубной налет, продвигаясь вглубь под десневой край, вызывает раздражение ткани за счет микробных токсинов, что в дальнейшем приводит к повреждению эпителия десневого кармана и воспалению прилежащих тканей. Длительный контакт между микробами и тканями периодонта чреват возникновением аутоиммунных процессов, которые могут обуславливать цепную реакцию, сопровождающуюся прогрессивной альтерацией, что в конечном итоге приводит к образованию периодонтального кармана. При этом происходит нарастание отека и воспалительного экссудата вследствии частичной гибели эпителиального покрова, коллагеновых волокон и связок. Для воспаления характерны пролиферативные процессы с вовлечением структур костной ткани и развитием деструктивных изменений в кортикальной пластинке и в губчатом веществе (см. рис. 6). Образование кармана создает благоприятное условие для вегетирования микрофлоры полости рта. Наличие постоянного очага воспаления способствует дальнейшему развитию периодонтальных карманов и оказывает влияние на состояние околозубных тканей и на организм в целом. Распространяясь с током крови и лимфы, микробные и тканевые токсины могут обуславливать формирование очагов фокальной инфекции в различных органах человека. Современные концепции этиологии и патогенеза болезней периодонта охватывают целый ряд механизмов воздействия микробных раздражителей, включая и «оппортунистическую теорию», основанную на специфичности и патогенности различных видов микроорганизмов, что и отражает клинический аспект этой сложной патологии. Экспериментально и клинически доказано, что если в течение 24 часов или нескольких дней не очищать зубной налет, то он становится причиной развития хронического воспаления десны. Эти факты свидетельствуют о четкой взаимосвязи между неудовлетворительной чисткой зубов и возникновением гингивитов с последующим развитием заболеваний периодонта. Как правило, пренебрежение гигиеной полости рта, употребление мягкой пищи, способствующей накоплению налета, ведут к возникновению гингивитов и с возрастом к прогрессированию болезней периодонта. Огромную роль в патогенезе заболеваний периодонта оказывают курение, алкоголь, некачественные протезы и реставрации, а также образование зубного камня. Зубной камень — это минерализованный зубной налет, прикрепленный к эмали (наддесневой) и к поверхности корня (поддесневой). Минеральные соли откладываются на коллоидной основе путем пропитывания зубного налета кристаллами фосфата кальция, поступающими из слюны. Активное формирование над- и поддесневого камня происходит на зубах, не участвующих в акте жевания, а главное, при нерегулярном и неправильном гигиеническом уходе за полостью рта за 3–4 недели. Так, установлено, что прирост камня происходит в результате накопления зубного налета со временем, что и вызывает непосредственное раздражение эпителия десневой бороздки, а его продвижение по цементу зуба в апикальном направлении приводит к разрушению периодонтального соединения и прогрессированию заболеваний. Наравне с этим, зубные камни, как наддесневые, так и поддесневые, по своей природе — патогенные факторы в развитии болезней периодонта, так как они всегда покрыты слоем микроорганизмов и являются препятствием для проведения гигиенических процедур. |

