ГЛАВА 21 ПАТОФИЗИОЛОГИЯ НЕРВНОЙ СИСТЕМЫ. Патофизиология нервной системы
 Скачать 1.03 Mb. Скачать 1.03 Mb.
|
|
21.3.4. Энергетический дефицит Потребность нейронов в энергообеспечении - самая высокая из всех клеток организма, и нарушение энергообеспечения является одной из распространенных причин патологии нейрона. Энергетический дефицит может быть первичным - при действии метаболических ядов (например, динитрофенола, цианидов) либо вторичным - при различных повреждениях, нарушениях кровообращения, шоке, отеке, общих судорогах, усиленной функциональной нагрузке и др. Дефицит энергии относится к разряду типовых внутриклеточных патологических процессов (см. главу 3). Главными условиями развития энергетического дефицита являются недостаток кислорода и значительное повреждение митохондрий, в которых синтезируется основной носитель энергии - АТФ. Причиной дефицита энергии может быть также недостаток субстрата окисления, в частности глюкозы, которая является для мозга основным субстратом окисления. Нейроны коры не имеют запасов глюкозы и потребляют ее непосредственно из крови (глюкоза свободно проходит ГЭБ), поэтому они особенно чувстви-
тельны к гипогликемии. Мозг потребляет около 20% от всей находящейся в крови глюкозы. Инсулиновые шоки, применяемые для лечения некоторых психозов, связаны с глубокой гипогликемией и протекают с потерей сознания и нередко с судорогами. При ряде патологических состояний (травматический шок, кровопотеря) мозг может дольше обеспечиваться кислородом и глюкозой благодаря перераспределению крови и уменьшению их потребления другими тканями. Для быстрейшего восстановления деятельности мозга после общих судорог необходим достаточно высокий уровень глюкозы в крови. Энергетический дефицит усугубляется нарушением цикла Кребса. При глубоком нарушении окислительного фосфорилирования и синтеза макроэргов источником энергии становится анаэробный гликолиз. Он имеет характер компенсаторного механизма, однако его эффект не может восполнить дефицит энергии, а нарастающее увеличение содержания молочной кислоты в мозгу оказывает отрицательное влияние на деятельность нейронов и усугубляет отек мозга. 21.3.5. Эффекты ишемии и гипоксии В связи с высокой потребностью в энергии нейроны ЦНС нуждаются в значительном кислородном обеспечении. Нейрон коры головного мозга потребляет 250-450 мкл О2/мин (для сравнения - глиоцит и гепатоцит потребляют до 60 мкл О2). Снижение потребления кислорода мозгом всего лишь на 20% может вызвать потерю сознания у человека. Исчезновение импульсной активности нейронов возникает уже в первые десятки секунд ишемии мозга. Через 5-6 мин после начала асфиксии наступает глубокое и нередко необратимое нарушение деятельности мозга. Гибель нейрона при ишемии является результатом осуществления комплекса взаимосвязанных внутриклеточных процессов (рис. 21-5). При аноксии головного мозга в первую очередь страдает кора. Гибель всего мозга означает «мозговую смерть», которая проявляется в полном исчезновении биоэлектрической активности. Филогенетически более старые структуры ЦНС (спинной мозг, ствол головного мозга) менее чувствительны к асфиксии, чем молодые (подкорка и особенно кора). Поэтому при запоздалом оживлении организма может наступить декортикация.
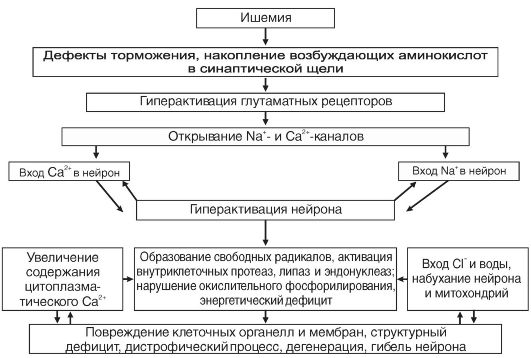 Рис. 21-5. Комплекс внутриклеточных процессов, возникающих при ишемии и вызывающих дегенерацию и гибель мембран Рис. 21-5. Комплекс внутриклеточных процессов, возникающих при ишемии и вызывающих дегенерацию и гибель мембранВесьма чувствительны к аноксии тормозные механизмы. Одним из следствий этого является растормаживание неповрежденных структур ЦНС. На ранних стадиях ишемии, когда нейроны мозга еще способны давать реакцию, они могут гиперактивироваться. На поздних стадиях ишемии гиперактивация нейронов сменяется их инактивацией. С поступлением Na+ в нейрон связана первая, острая фаза поражения нейрона. Возрастание концентрации Na+ в цитозоле нейрона приводит к повышению осмолярности, что обусловливает вход воды в нейрон и его набухание. В дальнейшем повышение осмолярности нейрона связано также с накоплением в нем Са2+, молочной кислоты, неорганического фосфора. С входом Са2+ в нейрон связана вторая фаза повреждения нейрона. Увеличение количества Са2+, поступающего в нейрон, обусловливается активацией глутаматных рецепторов в связи с усиленным выделением глутамата нервными окончаниями при ишемии. Антагонисты глутаматных рецепторов и антагонисты Са2+ (блокаторы Са2+-каналов) способ- ны предотвратить ишемическую дегенерацию нейронов и оказать лечебный эффект. Повреждение нейрона происходит не только во время ишемии, но и в связи с реперфузией мозга и возобновлением циркуляции крови. Именно они могут представлять главную опасность. Большую роль в реперфузионных постишемических повреждениях играют: новая волна поступления Са2+ в нейрон, ПОЛ (перекисное окисление липидов) и процессы свободнорадикального окисления, усиленные в связи с действием поступающего кислорода. Увеличивается содержание молочной кислоты из-за поступления глюкозы в условиях нарушения окислительного фосфорилирования и возросшего анаэробного гликолиза. Происходит отек мозга за счет поступления воды из крови при возобновлении циркуляции.
В сложный комплекс Са2+-индуцируемых внутриклеточных повреждений входят: альтерация внутриклеточных белков, усиленный фосфолипазный гидролиз и протеолиз, разрушение внутриклеточных структур, повреждение цитоплазматической и внутриклеточных мембран, набухание нейронов, нарушение деятельности генома. При критическом возрастании интенсивности этих процессов происходят необратимые повреждения и гибель нейрона, возникает так называемая кальциевая смерть1. На поздних стадиях патологического процесса, вызванного ишемией мозга, а также при хронизации процесса возникает новый комплекс вторичных изменений - дегенеративно-дистрофические процессы, нарушения энзимных и метаболических систем, сосудистые изменения, образование антител к мозговой ткани, аутоиммунная агрессия и др. Они составляют патогенетическую структуру постишемической энцефалопатии, которая может продолжать развиваться (прогредиентное развитие). Эти процессы, а также изменения в других системах и органах с их последствиями имеют место и после реанимации организма, особенно если она была затяжной и поздней. В своей совокупности они составляют патогенетическую структуру постреанимационной болезни (В.А. Неговский) (см. раздел 1.4.2). Гипоксия той или иной степени сопровождает многие (если не все) формы патологии мозга. Являясь типовым и неспецифическим процессом, она, однако, может вносить значительный вклад в его развитие. Вместе с тем умеренная гипоксия может стимулировать метаболические и пластические процессы в нейроне, способствовать адаптации и повышению резистентности, повышать трофический и пластический потенциал нейрона, усиливать адаптационные возможности мозга.
21.3.6. Синаптическая стимуляция и повреждение нейронов Возбуждающая синаптическая стимуляция может играть важную роль в развитии патологии нейрона. Усиленная и длительная синаптическая стимуляция сама по себе вызывает функциональное перенапряжение нейрона, которое может завершиться дегенерацией внутриклеточных структур. Эти повреждения усиливаются при нарушениях микроциркуляции и мозгового кровообращения, действии токсических факторов. Первостепенное значение синаптическая стимуляция имеет при развитии аноксических (ишемических) повреждений. Культура тканей нейронов становится чувствительной к аноксии лишь после установления синаптических контактов между нейронами. Синаптическая стимуляция реализуется через действие возбуждающих аминокислот (глутамат, аспартат, L-гомоцистеинат), причем эти повреждения подобны тем, которые возникают при ишемии и связаны с увеличенным содержанием внутриклеточного Са2+. Этот эффект известен как нейротоксическое (или цитотоксическое) действие возбуждающих аминокислот. С синаптической гиперактивацией, действием возбуждающих аминокислот и гипоксией связаны повреждение и гибель нейронов при эпилептическом статусе и в постишемическом периоде. При этом к патогенному действию указанных факторов присоединяется энергетический дефицит. В связи с изложенным становятся понятными благоприятные эффекты (т.е. ослабление синаптического воздействия) уменьшения функциональной нагрузки, предотвращение дополнительных раздражений, «охранительное», по И.П. Павлову, торможение обратимо поврежденных нейронов. 21.3.7. Нарушение деятельности нейрона при изменении процессов внутриклеточной сигнализации После восприятия рецептором сигнала (связывания рецептором нейромедиатора, гормона и др.) в нейроне возникает каскад цепных метаболических процессов, обеспечивающих необходимую активность нейрона. Важную роль в этих процессах играют так называемые усилительные, или пусковые, ферменты и образующиеся под их влиянием вещества-посредники, вторичные мессенджеры (см. главу 20).
Совокупность каскадных мембранных и внутриклеточных процессов составляет эндогенную усилительную систему нейрона, которая может обеспечить многократное усиление входного сигнала и возрастание его эффекта на выходе из нейрона. Так, каскад метаболических процессов аденилатциклазного пути может усилить эффект стимула в 107-108 раз. Благодаря этому возможны выявление и реализация слабого сигнала, что имеет особое значение в условиях патологии, при нарушении синаптического проведения. Многие изменения функций нейрона связаны с действием патогенных агентов на определенные звенья систем внутриклеточной сигнализации. Фармакологическая коррекция деятельности нейрона и эффекты лечебных средств также реализуются через соответствующие изменения этих систем. Так, холерный и коклюшный токсины действуют на процессы, связанные с активностью мембранных G-белков, активирующих или угнетающих аденилатциклазу. Ксантины (теофиллин, кофеин) обусловливают накопление цАМФ, что приводит к усилению деятельности нейрона. При действии ряда противосудорожных препаратов (например, дифенилгидантоина, карбамазепина, бензодиазепинов) и психотропных средств (например, трифтазина) угнетаются разные пути фосфорилирования белков, благодаря чему снижается активность нейронов. Ионы лития, применяемые при лечении некоторых эндогенных психозов, ослабляют деятельность системы фосфоинозитидов. С усиленным входом Са2+ связана эпилептизация нейронов, блокада этого входа антагонистами Са2+ подавляет эпилептическую активность. 21.3.8. Гиперактивность нейрона Гиперактивность нейрона обусловлена значительным, выходящим из-под контроля нарушением баланса между возбуждением и торможением нейрона в пользу возбуждения. В функциональном отношении она заключается в продуцировании нейроном усиленного потока импульсов, который может иметь различный характер: высокочастотные потенциалы действия; отдельные разряды; разряды, сгруппированные в пачки, и пр. Особый вид гиперактивности представляет собой пароксизмальный деполяризационный сдвиг (ПДС) в мембране, на высоте которого возникает высокочастотный разряд (рис. 21-6). Такой вид гиперактивности рассматривается как проявление эпилептизации нейрона.
Указанный сдвиг баланса между возбуждением и торможением может быть обусловлен либо первичным усиленным возбуждением нейрона, преодолевающим тормозной контроль, либо первичной недостаточностью тормозного контроля. Первый механизм реализуется значительной деполяризацией мембраны и усиленным входом Na+ и Са2+ в нейрон, второй - расстройством механизмов, обеспечивающих гиперполяризацию мембраны: нарушением выхода К+ из нейрона и входа Cl- в нейрон. Существенным эндогенным регулятором активности нейрона является γ-аминомасляная кислота (ГАМК). Она вызывает торможение нейрона при связывании со своим рецептором. В результате усиливается поступление Cl- в нейрон. 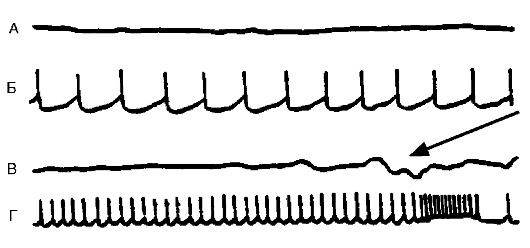 Рис. 21-6. Различные виды спонтанной активности нейрона в эпилептическом очаге, вызванном столбнячным токсином в двигательной зоне коры головного мозга кошки. Кривые А и В - потенциалы, регистрируемые с поверхности мозга в эпилептическом очаге (ЭкоГ). Кривые Б и Г - запись электрической активности нейронов, выполненные с помощью внутриклеточного отведения. Нейрон может генерировать с разной частотой регулярные потенциалы действия. На кривой Г показано завершение потенциала высокочастотными разрядами. В это время на ЭкоГ (кривая В) в зоне очага появляется спайковый разряд (указан стрелкой) Рис. 21-6. Различные виды спонтанной активности нейрона в эпилептическом очаге, вызванном столбнячным токсином в двигательной зоне коры головного мозга кошки. Кривые А и В - потенциалы, регистрируемые с поверхности мозга в эпилептическом очаге (ЭкоГ). Кривые Б и Г - запись электрической активности нейронов, выполненные с помощью внутриклеточного отведения. Нейрон может генерировать с разной частотой регулярные потенциалы действия. На кривой Г показано завершение потенциала высокочастотными разрядами. В это время на ЭкоГ (кривая В) в зоне очага появляется спайковый разряд (указан стрелкой)При растормаживании нейрона в связи с ослаблением торможения и деполяризацией мембраны происходит усиление поступления Са2+ в нейрон. Кроме того, Са2+, находясь уже в цитозоле, нарушает поступление С1- в нейрон, ослабляя, таким образом, изнутри ГАМКергическое торможение. С этим связана эпилептизация нейрона, возникающая под влиянием конвульсантов, которые нарушают ГАМКергическое торможение. Многие конвульсанты (например, пенициллин, коразол и др.) оказывают сложное действие на нейрон, одновременно активируя возбуждающие и инактивируя тормозные механизмы.
Хроническая стимуляция нейрона (например, при прямом электрическом раздражении, синаптическом воздействии, под влиянием возбуждающих аминокислот и др.) даже слабой интенсивности может с течением времени привести к гиперактивации нейрона. С другой стороны, выключение афферентации нейрона также обусловливает его гиперактивацию. Этот эффект объясняется повышением чувствительности нейрона и нарушением тормозных процессов. Таким образом, патологическая гиперактивация нейронов, их эпилептизация представляет сложный комплекс разнообразных мембранных и внутриклеточных процессов. Для подавления эпилептической активности целесообразно комплексное применение веществ, нормализующих основные патогенетические звенья процесса. Среди корригирующих воздействий первостепенное значение имеют блокада поступления Са2+ и восстановление тормозного контроля. 21.4. ГЕНЕРАТОРЫ ПАТОЛОГИЧЕСКИ УСИЛЕННОГО ВОЗБУЖДЕНИЯ (ГПУВ) 21.4.1. Понятие и общая характеристика Расстройство деятельности ЦНС возникает при воздействии достаточно мощного потока импульсов, способного преодолеть механизмы регуляции и тормозного контроля других отделов ЦНС и вызвать их патологическую активность. Столь мощный поток импульсов продуцируется группой гиперактивных нейронов, образующих генератор патологически усиленного возбуждения (Г.Н. Крыжановский). ГПУВ - это агрегат гиперактивных взаимодействующих нейронов, продуцирующий неконтролируемый поток импульсов. Интенсивность и характер этого потока не соответствуют поступающему сигналу и определяются только особенностями структурно-функциональной организации генератора. Вследствие того, что нейроны генератора активируют друг друга, генератор способен самоподдерживать свою активность, не нуждаясь в постоянной дополнительной стимуляции извне.
Возникая при повреждениях нервной системы, генератор становится патогенетическим фактором развития процесса. Его образование имеет характер универсального механизма и является типовым патологическим процессом, осуществляющимся на уровне межнейрональных отношений. Электрофизиологическим выражением деятельности генератора служат суммарные потенциалы составляющих его нейронов. В качестве примера таких потенциалов можно привести электрическую активность, регистрируемую в области генератора в гигантоклеточном ядре продолговатого мозга (рис. 21-7) и в эпилептическом очаге в коре головного мозга, который является одним из видов генератора. Патогенетическое значение ГПУВ. Основное патогенетическое значение генератора заключается в том, что он гиперактивирует тот отдел ЦНС, в котором он возник или с которым он непосредственно связан, вследствие чего этот отдел приобретает значение патологической детерминанты (см. разд. 21.5), формирующей патологическую систему (см. разд. 21.6). Поскольку патологические системы лежат в основе соответствующих нервных расстройств (нейропатологических синдромов), образование генератора является начальным звеном этих расстройств. 21.4.2. Образование и деятельность генераторов патологически усиленного возбуждения Генератор может образовываться при действии разнообразных веществ экзогенной или эндогенной природы, вызывающих либо нарушение механизмов тормозного контроля (что влечет за собой растормаживание и гиперактивацию нейронов), либо непосредственную гиперактивацию нейронов. В последнем случае тормозные механизмы сохранены, но они функционально неэффективны и не способны нормализовать деятельность нейронов. Во всех случаях обязательным условием образования и деятельности гене-
 Рис. 21-7. Характер вызванной активности в гигантоклеточном ядре кошки в норме и при формировании в нем генератора после введения столбнячного токсина: А - реакция на слабое одиночное раздражение икроножного нерва; реакция того же гигантоклеточного ядра на одиночное раздражение той же силы того же нерва при формировании в ядре генератора через 2 ч (Б), 3 ч (В) и 4 ч (Г) после введения в ядро столбнячного токсина: длительные, возрастающие со временем по частоте и амплитуде послеразряды, которые могут продолжаться неопределенное долгое время, - генерирование интенсивного самосдерживающего возбуждения Рис. 21-7. Характер вызванной активности в гигантоклеточном ядре кошки в норме и при формировании в нем генератора после введения столбнячного токсина: А - реакция на слабое одиночное раздражение икроножного нерва; реакция того же гигантоклеточного ядра на одиночное раздражение той же силы того же нерва при формировании в ядре генератора через 2 ч (Б), 3 ч (В) и 4 ч (Г) после введения в ядро столбнячного токсина: длительные, возрастающие со временем по частоте и амплитуде послеразряды, которые могут продолжаться неопределенное долгое время, - генерирование интенсивного самосдерживающего возбужденияратора является недостаточность торможения составляющих его нейронов. Примером образования генератора при первичном нарушении торможения могут быть генераторы, возникающие при действии столбнячного токсина, стрихнина, пенициллина и других конвульсантов. Примером образования генератора при первичной гиперактивации |
