Первый московский государственный медицинский
 Скачать 0.49 Mb. Скачать 0.49 Mb.
|
Лабораторная работа 2.4Определение массы гидроксида натрия в раствореЦель работы: Приобрести навыки выполнения титриметрического анализа. Оборудование и реактивы: Бюретка вместимостью 25 мл, пипетка Мора вместимостью 5 мл, мерная колба вместимостью 100 мл, коническая колба вместимостью 250 мл, конические колбы вместимостью 50 – 100 мл, разбавленные растворы азотной кислоты и гидроксида натрия, раствор метилового оранжевого и фенолфталеина, вода дистиллированная. Сущность работы: Прямое ацидиметрическое определение массы щелочи в растворе по реакции: NaOH + HNO3 NaNO3+ H2O Концентрация щелочи в контрольном растворе рассчитывается по результатам кислотно-основного титрования: с(1/zHNO3)V(HNO3) с(1/zNaOH) = Vаликвотной доли(NaOH) Масса вещества в растворе рассчитывается по формуле: m(NaOH) = c(NaOH) V(NaOH) M(NaOH) Выполнение эксперимента: 1. Приготовить бюретку к работе. 2. Приготовить пробы анализируемого раствора для титрования. 3. Провести титрование проб до трех сходящихся результатов с точностью до 0,1 мл. Экспериментальные данные:
Расчеты: NaOH + HNO3 → NaNO3 + H2O n (1/z NaOH) = n (1/z HNO3) с (НNО3 )=……………… z(NaOH) = ……. z (HNO3) =……….. c (NaOH) Vаликвотной доли( NaOH) = c(HNO3) V(HNO3)= m (NaOH) = c(HNO3) V(HNO3) Vмерной колбы M(NaOH)/ V аликвотной доли = *В выводах указывают полученный результат, метод исследования, используемые индикаторы. Вычисляют относительное отклонение от массы гидроксида натрия, указанной преподавателем. Вывод: Дата ___________ Занятие __________ Перманганатометрия. Семинар. Задания для самостоятельной работы 1.70; 1.75; 1.78 Дата _______ Занятие ___________ МОДУЛЬ №02. Химическая термодинамика. Энергетика химических реакций. I начало термодинамики. Энтальпия. Закон Гесса. Задания для самостоятельной работы2.19; 2.45; 2.57; 2.61 Дата _______ Лабораторная работа 3.1Определение стандартной энтальпии реакции нейтрализации.Цель работы: Научиться калориметрически определять энтальпии реакции нейтрализации. Приборы, оборудование и реактивы: Макет калориметра, термометр с ценой деления 0,1о(10), мерные цилиндры, растворы кислоты и основания. Сущность работы: Теплота реакции нейтрализации определяется калориметрически по измеренному изменению температуры и рассчитанной теплоемкости системы. Лабораторный калориметр 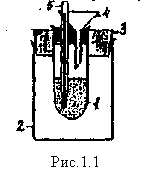 1 – стакан, находящийся в большом термоизоляционном стакане 2, снабженном крышкой 3. С внутренним пространством калориметрического стакана контактируют воронка ; и химический термометр 5. Энтальпия реакции нейтрализации, протекающей между сильными одноосновными кислотами и сильными однокислотными основаниями практически не зависит от их природы, так как реально в растворах протекает одна и та же реакция: Н+(aq) + ОН–(aq) = Н2О(ж) ; DН°r = -57,3 кДж/моль. В случае реакции нейтрализации слабых кислот и слабых оснований такого постоянства не наблюдается, так как часть теплоты расходуется на ионизацию слабой кислоты и слабого основания. Выполнение эксперимента: 1. Измеряют температуру исходных растворов кислоты и щелочи. 2. Измеряют температуру раствора после проведения реакции. Экспериментальные данные.
Концентрации растворов кислоты ________моль/л, щелочи________ моль/л, Объемы растворов реагирующих веществ мл_____ Плотности растворов_______________г/мл_ Масса калориметрического стакана г Справочные величины Суд (воды) = 4,184 Дж/г×К Суд (стекла) = 0,753 Дж/г × К Обработка результатов эксперимента Рассчитывают теплоемкость системы: С = С1 +С2 Теплоемкость раствора С1 рассчитывают по формуле: С1 = [V(р-ра к-ты) × r (р-ра к-ты) + V(р-ра осн.) × r (р-ра осн.) ] × Суд (воды) где V – объемы смешиваемых растворов, мл; r - плотность растворов, г/мл; Суд (р-ра) – удельная теплоемкость раствора, Теплоемкость стакана C2 рассчитывают по формуле: C2 = m × Суд (стекла), где m – масса стакана, г; Суд (стекла) – удельная теплоемкость стекла, Стандартную энтальпию реакции нейтрализации рассчитывают по формуле: С × DТ DН°r = - ------- n где DТ – разница между средним арифметическим значением температур после реакции и средним арифметическим значением температур до реакции; n - количество исходного вещества , взятого в недостатке. Экспериментально определенную величину сравнивают со справочным значением, находят абсолютную и относительную ошибку определения: Абсолютная ошибка: DН°теор – DН°эксп. Относительная ошибка: ½DН°теор – DН°эксп½ ------------------------- ½DН°теор. ½ | |||||||||||||||||||||||||||||||||||||||||||||
