РЕФЕРАТ Атипичные пневмонии.. План реферата тяжелый острый респираторный синдром (торс)
 Скачать 4.37 Mb. Скачать 4.37 Mb.
|
|
ПЛАН РЕФЕРАТА
патогенез ( стр.1).
- ТОРС в педиатрической практике.
Приложение Как известно, заболевание, традиционно обозначаемое термином "атипичная пневмония", не имеет строгой нозологической определенности и рассматривается как клинический синдром. В 1937 г. J.Scadding описал 4 случая необычного течения инфекции нижних дыхательных путей, употребив для их обозначения термин "диссемини-рованная фокальная пневмония". Практически одновременно с ним H.Reimann (1938) описал 8 пациентов со своеобразной клинической картиной нетяжелого респираторного заболевания, весьма близкой к картине так называемой диссеминированной фокальной пневмонии: сухой кашель, затрудненное дыхание/одышка, осиплость голоса, цианоз, заторможенность, профузная потливость, диффузная мелкоочаговая пневмоническая инфильтрация. При попытке этиологической верификации этих случаев заболевания, для которых H.Reimann предложил использовать термин "атипичная пневмония" (этот термин приобретет широкую популярность значительно позже), был выделен фильтрующийся микроорганизм -так называемый агент Итона (Eaton agent). В 1962 г. культуру агента Итона удалось вырастить на агаре, и возбудитель получил современное таксономическое название — «Mycoplasmapneumoniae». С момента первых описаний легионеллезной (Legionellapneumophila) и хламидийной (Chlamydiapneumoniae") пневмонии (1976 и 1986 г., соответственно) было замечено, что вызываемый этими возбудителями симптомокомплекс легочного воспаления весьма схож с таковым микоплазменной пневмонии. Но наиболее широко этот термин внедрился благодаря коронавирусам (coronaviridae), относящихся к подсемейству пневмовирусов. При проникновении этого возбудителя в организм человека в течении некоторого времени ( интервал колеблется в индивидуальном порядке ), развивается комплекс симптомов, происходящих на фоне лихорадки и включающих в себя головную боль, миалгии, анорексию и быстро прогрессирующее поражение респираторного тракта с развитием тяжелой атипичной пневмонии с последующими грозными осложнениями. Эксперты ВОЗ официально назвали новую болезнь дыхательных путей: severeacuterespiratory syndrome(SARS), в русском переводе-тяжелый острый респираторный синдром (ТОРС). ВОЗ ежедневно публиковала кумулятивные данные по распространению ТОРС. В течение марта, апреля и мая болезнь охватила все континенты на земном шаре и стала первой пандемией XXI века. Всего около года назад об этом таинственном заболевании не знал практически никто. Термин « атипичные пневмонии », характеризующий, как уже было упомянуто, целую группу заболеваний, был знаком только специалистам. Затем правительства разных стран стали соревноваться с инфекционистами в предложении как можно более жестоких и универсальных мер по предупреждению распространения грозного заболевания. Статистики Всемирной организации здравоохранения пополняли и продолжают пополнять скорбные списки инфицированных и погибших, врачи, можно сказать судорожно, пытались найти наиболее эффективное средство для борьбы с этим вирусом. В Москве и других крупных городах России была введена ежедневная дезинфекция транспорта, рынков, « особым вниманием » пользуются приезжие из стран, где объявлена эпидемия « атипичной пневмонии » ( или, в международной терминологии –« SARS » ). Этиология и эпидемиология. История открытия и изучения роли коронавируса в патологии человека своими корнями уходит в 1937 год, когда он впервые был выделен у цыплят В 1965 году Tyrell и Вуnoe смогли осуществить культивирование человеческого коронавируса на эмбриональных клетках трахеи. Считается, что около 30% острых простудных заболеваний у человека связано с колонизацией коронавируса в эпителиальных клетках слизистой носа и трахеи. Основным клиническим проявлением острого простудного заболевания, вызванного человеческим коронавирусом, является острый ринит, трахеит. Полагалось, что коронавирус не вызывает поражения нижнего отдела дыхательных путей. Е.О. Балкарова с соавт. (1996-98 гг.) в Институте пульмонологии исследовала вирусный дисбиоз у больных с атоническим синдромом: бронхиальная астма, аллергический ринит, атонический дерматит. Авторы установили, что более чем у четверти больных атоническим синдромом выявляется положительная антигенемия и обнаружены специфические антитела к первому серотипу коронавируса. Помимо коронавируса, у больных также выявлялась персистенция ротавируса и аденовируса, но превалировало носительство коронавируса. Установленный факт вирусного дисбиоза побуждает к проведению дальнейших исследований, целью которых было бы установление причинной связи механизмов атопии и персистенции коронавируса. В истории изучения роли коронавирусов в патологии человека особое место займет пандемия, которая началась в конце 2002 г. и стремительно распространялась в течение первого полугодия 2003 г. В научном обзоре, который представлен ниже, последовательно приводятся данные по эпидемиологии пандемии ТОРС, генетической характеристике нового коронавируса (SARS-CoV), клинической картине, морфологическим изменениям в легочной ткани и основным лечебным программам. Первая пандемия двадцать первого века началась в ноябре 2002 года на юге Китая в провинции Гуангдонг, где проживает более 75 миллионов человек. Население провинции занято преимущественно в агропромышленном комплексе. Многочисленные фермы специализируются на разведении диких животных, которые используются для приготовления деликатесов, добавляемых в пищу и при производстве парфюмерных изделий. Так, на фермах разводят енотовых собак (Raccoondog, Nyctereutesprocyonoides), китайского хорька-барсука (Ferretbadger, Me/oga/emoschata) и, наконец, пятнистое млекопитающее из семейства кошачьих (Palmcivets, Раgита larvata), которое проживает в Африке и Азии (рис. 1). Раствор мускус, получаемый от них, используют в парфюмерной промышленности (Arabiczabad). Как было показано в исследованиях D. Cyranoski, A. Abbot, указанные синатропные и ксенотропные млекопитающие стали источником сформировавшегося зооноза. Первые больные с ТОРС поступили в университетскую клинику города Гуангдонг в конце ноября 2002 года. Первое неофициальное сообщение о том, что врачи встретились с необычной респираторной инфекцией, пришло из Гуангдонга 27 ноября; было рекомендовано изолировать больных с пневмонией. События приобретали драматический характер. Профессор N. Zhong, который возглавил врачебную бригаду в университетской клинике, описывает трагическую смерть врача. Доктор Lx. Deng, 51 года, заведовал блоком интенсивной пульмонологии, в последние два месяца своей жизни занимался больными с ТОРС. Он заболел в начале февраля и умер от тяжелых осложнений, наступивших в результате пневмонии. Официальное сообщение в ВОЗ пришло из Китая 14 февраля 2003 года. В нем сообщалось, что в провинции Гуангдонг госпитализировано 350 больных с атипичной пневмонией; умерло пять больных. Из Гонгконга 19 февраля пришло сообщение о том, что в университетской клинике наблюдаются мужчина 39 лет и мальчик 9 лет, у них грипп, вызванный Avian influenza (H5N1). Это было первое предположение о возможной причине начинающейся эпидемии гриппа. Всемирная Организация Здравоохранения и Центр по контролю распространения инфекционных заболеваний (Атланта, США) взяли на себя роль координаторов центров по организации комплекса мероприятий, целью которых явилось установление этиологии разворачивающейся эпидемии, формирование рекомендаций по организации карантинных мероприятий, проведение серии конференций с обсуждением программ лечения больных ТОРС. ВОЗ ежедневно публиковала кумулятивные данные по распространению ТОРС. В течение марта, апреля и мая болезнь охватила все континенты на земном шаре и стала первой пандемией XXI века. Описано несколько эпидемиологических кластеров ТОРС. Первым явилось описание N. Lee et al. Ниже приводится схема (рис. 2), на которой изображен эпидемиологический кластер, расследованный в Гонконге. 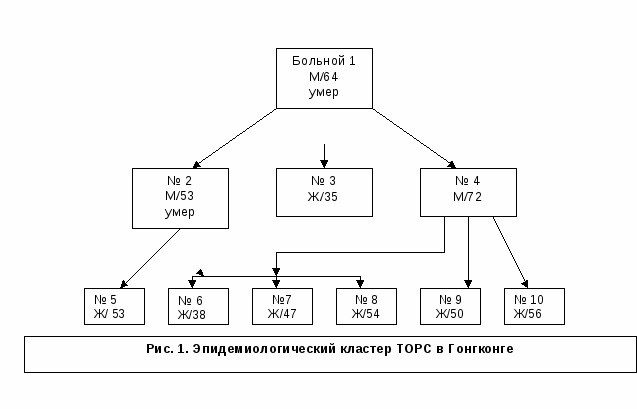 Мужчина 64 лет, по специальности врач-нефролог (больной №1), приехал из Гуангдонга, чтобы осмотреть достопримечательности Гонгконга и навестить своего родственника (больной № 2, мужчина 53 лет). Вместе они находились около 10 часов, посещали парк Атоу. В тяжелом состоянии были доставлены в университетскую клинику, где скончались. Непосредственной причиной смерти явилась прогрессирующая острая неконтролируемая дыхательная недостаточность (респираторный дистресс-синдром). Медицинские сестры (больные №№ 3,5), которые занимались умершими больными, в последующем также поступили в блок интенсивной пульмонологии в связи с развившейся у них клинической картиной ТОРС. Больной мужчина 72 лет (№4) приехал из Торонто (Канада). В холле гостиницы, в которой он остановился (также как и больной №1), они встречались друг с другом. Он поступает в университетскую клинику вместе с больным №1. В гостинице, а в последующем и в госпитале его навещали мужчины (№№ 9,10), которые также заболели. Медицинская сестра (женщина 47 лет, №7), которая занималась мужчиной №4, оказалась инфицированной вирусом ТОРС и поступила с клиническими проявлениями болезни. Наконец, в представленном эпидемиологическом кластере мы видим заболевших женщин (№№ 6,8), которые работали в блоке интенсивной пульмонологии той самой клиники, куда поступали вышеописанные больные. Мужчина 64 лет, по специальности врач-нефролог (больной №1), приехал из Гуангдонга, чтобы осмотреть достопримечательности Гонгконга и навестить своего родственника (больной № 2, мужчина 53 лет). Вместе они находились около 10 часов, посещали парк Атоу. В тяжелом состоянии были доставлены в университетскую клинику, где скончались. Непосредственной причиной смерти явилась прогрессирующая острая неконтролируемая дыхательная недостаточность (респираторный дистресс-синдром). Медицинские сестры (больные №№ 3,5), которые занимались умершими больными, в последующем также поступили в блок интенсивной пульмонологии в связи с развившейся у них клинической картиной ТОРС. Больной мужчина 72 лет (№4) приехал из Торонто (Канада). В холле гостиницы, в которой он остановился (также как и больной №1), они встречались друг с другом. Он поступает в университетскую клинику вместе с больным №1. В гостинице, а в последующем и в госпитале его навещали мужчины (№№ 9,10), которые также заболели. Медицинская сестра (женщина 47 лет, №7), которая занималась мужчиной №4, оказалась инфицированной вирусом ТОРС и поступила с клиническими проявлениями болезни. Наконец, в представленном эпидемиологическом кластере мы видим заболевших женщин (№№ 6,8), которые работали в блоке интенсивной пульмонологии той самой клиники, куда поступали вышеописанные больные.Эпидемиологическое исследование, проведенное группой доктора Le et al., демонстрирует контагиозность острого респираторного заболевания. Однако многое остается непонятным. Так, например, больной, который числился под первым номером, проживал в гостинице вместе со своей супругой. Она осталась здоровой, в то время как медицинская сестра, работавшая в шоковой палате, куда и поступил больной №7, в течение нескольких дней заболела ТОРС. Медицинский персонал оказался подверженным данному заболеванию. Так, среди медицинских работников, которые работали в госпиталях, развернутых для приема больных ТОРС в Китае, заболело около 25%. Высокий процент заболевших был также в госпиталях Гонгконга, Торонто, Сингапура. Анализ эпидемиологических данных демонстрирует, что лица, контактировавшие в домашних или больничных условиях с заболевшими ТОРС, оказались наиболее подверженными возникновению острого респираторного заболевания. Пик заболеваний пришелся на апрель и май 2003 года. В конце июня ВОЗ объявила, что территория Китая свободна от дальнейшего распространения ТОРС. В нескольких лабораториях мира приступили к изучению природы заболевания. Эта была беспрецедентная в мировой практике организованная работа вирусологов, молекулярных биологов, микробиологов, направленная на установление причины ТОРС. Под эгидой ВОЗ осуществлялась координация усилий ученых. Результаты не заставили себя долго ждать. Первые предположения, которые были высказаны: возбудителем нового инфекционного заболевания дыхательных путей у человека является вирус, относящийся к семейству Paramyxoviridae. Это большая группа вирусов, которая подразделена на два подсемейства: Pneumovirinae и Paramyxovirinae. Внимание было сконцентрировано на подсемействе пневмовиринов. В конце прошлого столетия в Австралии, Новой Зеландии и Юго-Восточной Азии отмечались вспышки инфекционных заболеваний с характерной клинической картиной менингоэнцефалита и пневмонии, которые вызывались вирусами Hendra и Nipah. Оба указанных вируса относятся к группе пневмовиринов. Это предположение не получило своего подтверждения при проведении генетических исследований. С  ледующим этапом в изучении природы вируса явилось предположение об этиологической роли метапнев-мовируса человека. Он был выделен совсем недавно группой голландских вирусологов (van den Hoogen et al., 2001). В литературе встречается иногда его первое название: голландский метапневмовирус человека. Он относится к группе РНК-вирусов, филогенетически близок к птичьему метапневмовирусу. Он поражает как взрослых, так и детей. В клинической картине превалируют симптомы гриппоподобного заболевания, в более тяжелых случаях наблюдаются признаки бронхиолита, пневмонии. В Голландии были проведены эпидемиологические исследования по распространенности метапневмовируса человека. В детской популяции было установлено, что более чем у 25% детей выявляются антитела к антигену вируса. В осенне-зимний период отмечалось значительное повышение заболеваемости. Близкие данные голландских авторов были получены в Финляндии, Великобритании и Германии. Так как острое респираторное заболевание, вызванное метапневмовирусом человека, у отдельных больных протекало достаточно тяжело, то при исследовании возникло предположение о том, что он является возможным возбудителем ТОРС. В тяжелых случаях появлялась одышка (83%), сухой кашель (75%), стридор (50%) и высокая температура, т.е. клиническая картина напоминала ту, с которой врачи встретились при пандемии ТОРС. Однако и это предположение не получило своего развития. В конце марта стало очевидным, что пандемия вызвана коронавирусом, который так же, как и указанные выше вирусы, относится к подсемейству пневмовиринов. ледующим этапом в изучении природы вируса явилось предположение об этиологической роли метапнев-мовируса человека. Он был выделен совсем недавно группой голландских вирусологов (van den Hoogen et al., 2001). В литературе встречается иногда его первое название: голландский метапневмовирус человека. Он относится к группе РНК-вирусов, филогенетически близок к птичьему метапневмовирусу. Он поражает как взрослых, так и детей. В клинической картине превалируют симптомы гриппоподобного заболевания, в более тяжелых случаях наблюдаются признаки бронхиолита, пневмонии. В Голландии были проведены эпидемиологические исследования по распространенности метапневмовируса человека. В детской популяции было установлено, что более чем у 25% детей выявляются антитела к антигену вируса. В осенне-зимний период отмечалось значительное повышение заболеваемости. Близкие данные голландских авторов были получены в Финляндии, Великобритании и Германии. Так как острое респираторное заболевание, вызванное метапневмовирусом человека, у отдельных больных протекало достаточно тяжело, то при исследовании возникло предположение о том, что он является возможным возбудителем ТОРС. В тяжелых случаях появлялась одышка (83%), сухой кашель (75%), стридор (50%) и высокая температура, т.е. клиническая картина напоминала ту, с которой врачи встретились при пандемии ТОРС. Однако и это предположение не получило своего развития. В конце марта стало очевидным, что пандемия вызвана коронавирусом, который так же, как и указанные выше вирусы, относится к подсемейству пневмовиринов.Д 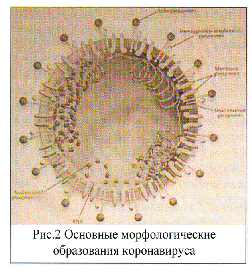 о развернувшейся пандемии было известно три се-ротипа коронавирусов, новый четвертый тип обозначен, как SARScoronavirus. о развернувшейся пандемии было известно три се-ротипа коронавирусов, новый четвертый тип обозначен, как SARScoronavirus.На рисунке 3 схематически изображены серотипы известных коронавирусов. К первому относят человеческий, который маркирован, как HcoV-229E. К этому се-ротипу также относят вирус острого гастроэнтерита свиней, кошачьего перитонита, острой диареи свиней; вторую группу составляют человеческий коронавирус - ОС43, а также вирус гепатита мышей, энцефаломиелита свиней, бычий; к третьей группе серотипа относят коронавирусы бронхита птиц, уток. Таким образом, из многочисленных видов коронавирусов у человека патогенетическую роль играют HcoV-229E и ОС43. С ними связывают вспышки острых вирусных заболеваний верхнего отдела дыхательных путей и остро возникающую диарею. Как правило, активность коронавирусов, поражающих человека, приходится на ранний осенний период. Наиболее характерным проявлением острого вирусного заболевания является клиническая картина острого ринита. Однако не они явились причиной пандемии. На рисунке 1 представлены данные электронной микроскопии. Вирус имеет сферическую форму за счет шиповидных отростков, которые образуют подобие «солнечной короны»; это образное сравнение взято за основу названия - коронавирус (coronavirus). Вирион, как это видно при электронной микроскопии, представляет сферическую форму, его размеры колеблются от 60 до 220 нм. Геном представлен однонитевой РНК. Морфологическая структура представлена шиповидными отростками («солнечная корона»), нуклеокапсидом, липидсодержащей оболочкой, белковой мембраной. На рисунке 5 схематично представлены основные морфологические образования коронавируса. Коронавирусы имеют различные механизмы связи с рецепторами клеток хозяина. Более изученным процессом является связь с рецепторами эпителиальных клеток посредством аминопептидазы (М. Marra et al.). Ведущая роль в процессе связывания с рецепторами клеток хозяина принадлежит гликопротеину шиповидных отростков (S-spikeglycoprotein). Дальнейший процесс проникновения вируса в эндоплазматический ретикулум происходит с участием мембранного белка «М». Большинство известных нейтрализующих антител, а также лимфоциты с цитотоксическим действием реагируют с гликопротеином шиповидных отростков. Он используется для приготовления вакцин против мышиного коронавируса. Одним из отличий коронавирусов первого и второго серотипов является наличие у ОС43 гемагглютининэстеразы, что сближает его с вирусом гриппа. Таким образом, биологическая связь между коронавирусом и рецепторами эпителиальных клеток осуществляется через большой гликопротеин шиповидных отростков. Совместно с трансмембранным белком М он взаимодействует с эндоплазматическим ретикулумом эпителиальных клеток. Следующий этап вирусной инвазии состоит в том, что происходит процесс встраивания этих белковых структур в аппарат Гольджи, копируется РНК по всей своей длине, в последующем нити РНК собираются в белки - нуклеокапсиды. Комплекс РНК в ассоциации с трансмембранным белком достигает мембраны эндоплазматического ретикулума, в котором находится в виде «почек». Вирус мигрирует через аппарат Гольджи и, в конечном счете, элиминируется из клетки посредством механизма экзоцитоза. ВОЗ координировала работу молекулярных генетиков из разных стран мира. В Германии это работу осуществляли в генетической лаборатории Гамбурга и в университетских лабораториях Франкфурта-на-Майне (P.A. Rota et al., Ch. Drosten); в Канаде - в Центре генетических исследований в Ванкувере (М.А. Marra et al.), в США - в Центре по контролю за инфекционными заболеваниями (T.G. Kziazek et al.). Генетические исследования проводились также в других странах, что позволило сделать географическое сопоставление штамма, полученного после смерти Карло Урбани. Он известен в настоящее время, как штамм Урбани. Сравнительный анализ произведен со штаммами, полученными в Торонто, Гонгконге, Гуангдонге, и др. 14 апреля в 10 часов 50 минут по среднеевропейскому времени было завершено чтение нуклеотидных последовательностей нового коронавируса, который явился причиной тяжелого острого респираторного синдрома (ТОРС). Он был маркирован, как уже говорилось выше, - SARS-CoV. Его геномная организация схожа с известными видами коронавирусов. Однако филогенетический анализ и сравнение последовательностей позволяет утверждать, что SARS-CoV не имеет сродства ни с одним из ранее охарактеризованных коронавирусов. Секвенирование установило 29727 нуклеотидных последовательностей, отличия касаются 24 позиций, найдены изменения также в полипротеинах (ORF). Большой гликопреин шиповидных отростков (S-протеин), с которым связывают вирулентность вируса, у нового коронавируса имеет короткий трансмембранный домен и цитоплазматическую часть, если его сравнить с другими известными коронавирусами (52 аминокислоты против 61-74 аминокислот). Различия установлены и при исследовании N-протеина, который содержит 422 аминокислоты, в то время как у других - 377-454 аминокислот. Общее заключение, к которому пришли независимо исследовательские группы - SARS-CoV не происходит от какого-либо другого вируса, и человек с ним встретился впервые. Многочисленные вспышки заболевания показали крайне высокую контагиозность вируса; например, было установлено, что среди медицинского персонала, контактировавшего с больными SARS, индекс контагиозности достиг 50%. В результате было подтверждено, что основной путь передачи вируса — воздушно-капельный, но не исключается передача и при прямом контакте, так как вирус устойчив к факторам окружающей среды и сохраняет свою заразительность до 3 ч на различных предметах при комнатной температуре, до 24 ч — на пластиковых поверхностях и до 4 дней — в фекалиях. Очень значительно колеблется инфек-ционность пациентов с SARS в различные периоды заболевания. Предварительные данные исследования назофарингеального отделяемого методом ПЦР установили, что концентрация вируса максимальна на 10-й день от появления респираторного синдрома и снижается до минимальных значений только к 15-м суткам, с фекалиями и мочой вирус выделяется переболевшими SARS до периода поздней реконвалесценции. Все перечисленное определяет особое место мер индивидуальной защиты при контакте с лицами, потенциально инфицированными вирусом SARS, Это прежде всего индивидуальные маски на персонале и пациенте, резиновые перчатки у персонала, которые не рекомендуется использовать повторно, специальные халаты и шапочки (желательно одноразового применения), а также обязательное мытье рук с мылом перед контактом с больными и после него. Если вода по тем или иным причинам недоступна, можно использовать для обработки рук спиртсодержащие растворы. Все биологические выделения больного тщательно собирают и уничтожают, а предметы окружающей среды обрабатывают раствором гипохлорита. Особое место среди мер защиты от распространения эпидемии SARS принадлежит своевременному выявлению не только больных, но и контактных с ними лиц, а также лиц, прибывших из регионов, признанных очагами этой инфекции, с последующей их изоляцией на срок до 10 сут под медицинским контролем с ежедневной термометрией и осмотром (для раннего выявления заболевших). Среди первых проявлений заболевания — лихорадка, кашель, затрудненное дыхание с быстро нарастающей одышкой. Ведущая роль в мероприятиях по обсервации SARS принадлежит государственным органам. Еще одна загадка, связанная с новоявленным заболеванием – условия, необходимые для его передачи от носителя к здоровому человеку. Иногда одного зараженного хватает , чтобы, как это было в Гонгконге, был инфицирован целый дом или пассажирский самолет. С другой стороны, отмечен целый ряд случаев высокой избирательности вируса, когда люди, непосредственно контактирующие с целым рядом заболевших, остались живы и невредимы. Кроме того, все инфекционные заболевания в первую очередь угрожают двум группам населения – пожилым людям с ослабленной иммунной системой и детям, у которых она еще не достаточно сформирована. В отношении второй категории – детей, вирус оказывается, по крайней мере, в настоящее время практически бессильным. По данным ВОЗ, количество детей среди всех заболевших SARS не превышает 3 %. Так, в Сингапуре среди 126 заболевших оказалось только трое детей ( 2,4 % случаев ). В Гонгконге примерно на тысячу больных атипичной пневмонией взрослых приходится четверо детей ( 0,4 % ), хотя близких контактов между заболевшими SARS взрослыми было довольно много. Официальные представительства Министерства здравоохранения Китая не предоставили информации о количестве детей среди всех больных атипичной пневмонией. Однако они утверждают, что в центральном госпитале южной провинции Гуангдонг, откуда началось распространение болезни, нет ни одного ребенка. Специалисты затрудняются назвать причины устойчивости дктского организма к возбудителю SARS. Некоторые врачи высказывают мнение, что на самом деле количество детей очень велико, но у них заболевание проходит в более легкой форме, и родители просто не обращаются за медицинской помощью. |
