Ответы БХ. Предмет, разделы и задачи биологической химии. Вклад русских и зарубежных учёных в развитие биологической химии
 Скачать 329.13 Kb. Скачать 329.13 Kb.
|
|
Синтез мочевины, место протекания этого процесса, его значение для организма животных. Основным механизмом связывания аммиака в организме является синтез мочевины. Мочевина выводится из организма с мочой в качестве главного конечного продукта белкового, соответственно аминокислотного обмена. На долю мочевины приходится до 80-85 % от всего выводимого из организма азота. Количество выделяемой мочевины зависит от количества белков, поступающих с пищей. Если суточный рацион включает 80–100 г белка, то за сутки образуется и выводится 25–30 г мочевины. Основным местом синтеза мочевины является печень. Синтез мочевины является циклическим метаболическим процессом и носит название орнитинового цикла мочевинообразования Кребса (цикл мочевины Кребса - Хензеляйта). На первом этапе из NН3 и СО2 при участии АТФ синтезируется макроэргическое соединение карбамоилфосфат: На втором этапе цикла мочевинообразования происходит конденсация карбомоилфосфата и орнитина с образованием цитруллина. На следующей стадии вначале происходит связывание одной молекулы NН3 путем восстановительного аминирования с образованием (с затратой молекулы АТФ) аспарагиновой кислоты. Затем цитруллин и аспарагиновая кислота взаимодействуют с образованием аргининосукцината, который распадается на аргинин и фумарат при участии аргининосукцинатлиазы. Аргинин расщепляется под действием фермента аргиназы на орнитин и мочевину. Образовавшийся орнитин может вступать в следующий цикл мочевинообразования. Хотя аргинин есть во всех клетках организма человека, образование мочевины происходит исключительно в клетках печени - единственном органе, где локализован фермент аргиназа. Мочевина из клеток печени поступает в кровь и выводится из организма через почки. Для синтеза одной молекулы мочевины требуется две молекулы NН3, одна молекула СО2 и три молекулы АТФ.
Липиды представляют собой группу веществ, которые характеризуются следующими признаками: нерастворимостью в воде; растворимостью в неполярных растворителях, таких, как эфир, хлороформ или бензол; содержанием высших алкильных радикалов; распространенностью в живых организмах. Строение Молекулы простых липидов состоят из спирта, жирных кислот, сложных — из спирта, высокомолекулярных жирных кислот, возможны остатки фосфорной кислоты, углеводов, азотистых оснований и др. Классификация липидов. Существует несколько классификаций липидов. Наибольшее распространение получила классификация, основанная на структурных особенностях липидов. По этой классификации различают следующие основные классы липидов. Простые липиды: сложные эфиры жирных кислот с различными спиртами.
Сложные липиды: сложные эфиры жирных кислот со спиртами, дополнительно содержащие и другие группы.
а) глицерофосфолипиды (в роли спирта выступает глицерол); б) сфинголипиды (в роли спирта – сфингозин).
Предшественники и производные липидов: жирные кислоты, глице-рол, стеролы и прочие спирты (помимо глицерола и стеролов), альдегиды жирных кислот, углеводороды, жирорастворимые витамины и гормоны. Биологическая роль липидов. Липиды играют важнейшую роль в процессах жизнедеятельности. Будучи одним из основных компонентов биологических мембран, липиды влияют на их проницаемость, участвуют в передаче нервного импульса, создании межклеточных контактов. Жир служит в организме весьма эффективным источником энергии либо при непосредственном использовании, либо потенциально – в форме запасов жировой ткани. В натуральных пищевых жирах содержатся жирорастворимые витамины и «незаменимые» жирные кислоты. Важная функция липидов – создание термоизоляционных покровов у животных и растений, защита органов и тканей от механических воздействий. Структурная. В сочетании фосфолипиды с белками образуют биологические мембраны.
Общие сведения. Жиры и липоиды подвергаются гидролитическому расщеплению в пищеварительном тракте. Нейтральные жиры распадаются на глицерин и жирные кислоты; фосфатиды (лецитины, кефалины, серинфосфатиды и др.) расщепляются на глицерин, жирные кислоты, фосфорную кислоту и азотистые основания — холин, коламин (этаноламин), серин и т. д. При гидролизе стеридов освобождаются холестерин или эргостерин и жирные кислоты. Гидролитический распад жиров катализируется ферментами липазами, которые содержатся в соке желудка, поджелудочной железы и тонкого кишечника. Роль желудочной липазы у взрослого человека весьма невелика, так как фермент катализирует расщепление лишь тонкодиспергированных, предварительно эмульгированных жиров (например, молочного). Значительная роль в переваривании жиров принадлежит липазе поджелудочной железы. Расщепление жиров происходит главным образом в тонком кишечнике. Липаза поджелудочной железы выделяется в малоактивной форме и активируется желчными кислотами. Они являются не только активаторами липазы. Будучи поверхностно-активными веществами, желчные кислоты способствуют эмульгированию жиров, что увеличивает во много раз их поверхность соприкосновения с водным раствором липазы. Слюна не содержит расщепляющих жиры ферментов. Следовательно, в полости рта жиры не подвергаются никаким изменениям. У взрослых людей жиры проходят через желудок также без особых изменений. В желудочном соке содержится липаза, получившая название желудочной. Во-первых, в желудочном соке взрослого человека и других млекопитающих содержание липазы крайне низкое. Во-вторых, рН желудочного сока далек от оптимума действия этого фермента (оптимальное значение рН для желудочной липазы 5,5–7,5). Напомним, что значение рН желудочного сока около 1,5. В-третьих, в желудке отсутствуют условия для эмульгирования триглицеридов, а липаза может активно действовать только на триглицериды, находящиеся в форме эмульсии. Даже незначительное по объему расщепление триглицеридов в желудке приводит к появлению свободных жирных кислот, которые, не подвергаясь всасыванию в желудке, поступают в кишечник и способствуют там эмульгированию жиров, облегчая таким образом воздействие на них липазы панкреатического сока. После того как химус попадает в двенадцатиперстную кишку, прежде всего происходит нейтрализация попавшей в кишечник с пищей соляной кислоты желудочного сока бикарбонатами, содержащимися в панкреатическом и кишечном соках. Выделяющиеся при разложении бикарбонатов пузырьки углекислого газа способствуют хорошему перемешиванию пищевой кашицы с пищеварительными соками. Одновременно начинается эмульгирование жира. Наиболее мощное эмульсирующие действие на жиры оказывают соли желчных кислот, попадающие в двенадцатиперстную кишку с желчью в виде натриевых солей. Большая часть желчных кислот конъюгирована с глицином или таурином. Эмульгирование жиров Жиры составляют до 90% липидов, поступающих с пищей. Переваривание жиров происходит в тонком кишечнике, однако уже в желудке небольшая часть жиров гидролизуется под действием "липазы языка". Этот фермент синтезируется железами на дорсальной поверхности языка и относительно устойчив при кислых значениях рН желудочного сока. Поэтому он действует в течение 1-2 ч на жиры пищи в желудке. Основной процесс переваривания происходит в тонкой кишке. Так как жиры - нерастворимые в воде соединения, то они могут подвергаться действию ферментов, растворённых в воде только на границе раздела фаз вода/жир. Поэтому действию панкреатической липазы, гидролизующей жиры, предшествует эмульгирование жиров. Эмульгирование (смешивание жира с водой) происходит в тонком кишечнике под действием солей жёлчных кислот. Жёлчные кислоты синтезируются в печени из холестерола и секретируются в жёлчный пузырь. Содержимое жёлчного пузыря - жёлчь. Это вязкая жёлто-зелёная жидкость, содержащая главным образом жёлчные кислоты; в небольшом количестве имеются фосфолипиды и холестерол. Жёлчные кислоты представляют собой в основном конъюгированные жёлчные кислоты: таурохолевую, гликохолевую и другие. После приёма жирной пищи жёлчный пузырь сокращается и жёлчь изливается в просвет двенадцатиперстной кишки. Жёлчные кислоты действуют как детергенты, располагаясь на поверхности капель жира и снижая поверхностное натяжение. В результате крупные капли жира распадаются на множество мелких, т.е. происходит эмульгирование жира. Эмульгирование приводит к увеличению площади поверхности раздела фаз жир/вода, что ускоряет гидролиз жира панкреатической липазой. Эмульгированию способствует и перистальтика кишечника. Кроме жиров, с пищей поступают фосфолипиды, эфиры холестерола, однако количество этих липидов в составе пищи значительно меньше, чем жиров (≈10%).
Всасывание липидов. Всасывание происходит в проксимальной части тонкой кишки. Тонкоэмульгированные жиры (величина жировых капель эмульсии не должна превышать 0,5 мкм) частично могут всасываться через стенки кишечника без предварительного гидролиза. Основная часть жира всасывается лишь после расщепления его панкреатической липазой на жирные кислоты, моноглицериды и глицерин. Жирные кислоты с короткой углеродной цепью (менее 10 атомов углерода) и глицерин, будучи хорошо растворимыми в воде, свободно всасываются в кишечнике и поступают в кровь воротной вены, оттуда в печень, минуя какие-либо превращения в кишечной стенке. Более сложно происходит всасывание жирных кислот с длинной углеродной цепью и моноглицеридов. Этот процесс осуществляется при участии желчи и главным образом желчных кислот, входящих в ее состав. В желчи соли желчных кислот, фосфолипиды и холестерин содержатся в соотношении 12,5:2,5:1,0. Жирные кислоты с длинной цепью и моноглицериды в просвете кишечника образуют с этими соединениями устойчивые в водной среде мицеллы. Структура мицелл такова, что их гидрофобное ядро (жирные кислоты, моноглицериды и др.) оказывается окруженным снаружи гидрофильной оболочкой из желчных кислот и фосфолипидов. В составе мицелл высшие жирные кислоты и моноглицериды переносятся от места гидролиза жиров к всасывающей поверхности кишечного эпителия. Происходит постоянная циркуляция желчных кислот между печенью и кишечником. Этот процесс получил название печеночно-кишечной (гепатоэнтеральной) циркуляции. С помощью метода меченых атомов было показано, что в желчи содержится лишь небольшая часть желчных кислот (10–15% от общего количества), вновь синтезированных печенью. Таким образом, основная масса желчных кислот (85–90%) – это желчные кислоты, реабсорбированные в кишечнике и повторно секретируемые в составе желчи. Установлено, что у человека общий пул желчных кислот составляет примерно 2,8–3,5 г, при этом они совершают 6–8 оборотов в сутки. Расщепление и всасывание фосфолипидов и холестерина. Подавляющая часть фосфолипидов содержимого тонкой кишки приходится на фосфатидилхолин (лецитин), основная масса которого поступает в кишечник с желчью (11–12 г/сут.) и меньшая часть (1–2 г/сут.) – с пищей. В зависимости от пищи организм взрослого человека получает ежедневно 300–500 мг холестерина. Основная часть холестерина в неэстерифицированной форме подвергается всасыванию в тонкой кишке в составе смешанных жировых мицелл, состоящих из желчных кислот, жирных кислот, моноглицеридов, фосфолипидов и лизофосфо-липидов. Ресинтез липидов в кишечной стенке. Триглицериды. По современным представлениям, ресинтез триглицеридов происходит в эпителиальных клетках (энтероцитах слизистой оболочки ворсинок тонкой кишки) двумя путями. Первый путь – β-моноглицеридный. Суть его состоит в том, что β-моноглицериды и жирные кислоты, проникающие в процессе всасывания в эпителиальные клетки кишечной стенки, задерживаются в гладком эндоплазматическом ретикулуме клеток. Здесь из жирных кислот образуется их активная форма – ацил-КоА и затем происходит ацилирование β-моноглицеридов с образованием сначала диглицеридов, а затем триглицеридов: β-Моноглицерид + R—СО—S-КоА –> Диглицерид + HS-КоА; Диглицерид + R1—СО—S-КоА –> Триглицерид + HS-КоА. Все реакции катализируются ферментным комплексом – триглицерид-синтетазой, включающим в себя ацил-КоА-синтетазу, моноглицеридацилтрансферазу и диглицеридацилтрансферазу. Второй путь ресинтеза триглицеридов протекает в шероховатом эндоплазматическом ретикулуме эпителиальных клеток и включает следующие реакции: 1) образование активной формы жирной кислоты – ацил-КоА при участии ацил-КоА-синтетазы; 2) образование α-глицерофосфата при участии глицеролкиназы; 3) превращение α-глицерофосфата в фосфатидную кислоту при участии глицерофосфат-ацилтрансферазы; 4) превращение фосфатидной кислоты в диглицерид при участии фосфатидат-фосфогидролазы; 5) ацилирование диглицерида с образованием триглицерида при участии диглицеридацилтрансферазы. Как правило, наличие в эпителиальных клетках избытка β-моноглицеридов тормозит протекание α-глицерофосфатного пути. Ресинтез фосфолипидов в кишечной стенке. В энтероцитах наряду с ре-синтезом триглицеридов происходит также и ресинтез фосфолипидов. В образовании фосфатидилхолинов и фосфатидилэтаноламинов участвует ресинтезированный диглицерид, а в образовании фосфатидилинозитолов – ресинтезированная фосфатидная кислота. Участие этих субстратов в образовании фосфолипидов в стенке кишечника происходит по тем же закономерностям, что и в других тканях. Необходимо подчеркнуть, что в стенке кишечника синтезируются жиры, в значительной степени специфичные для данного вида животного и отличающиеся по своему строению от пищевого жира. В известной мере это обеспечивается тем, что в синтезе триглицеридов (а также фосфолипидов) в кишечной стенке принимают участие наряду с экзогенными и эндогенные жирные кислоты. Однако способность к осуществлению в стенке кишечника синтеза жира, специфичного для данного вида животного, все же ограничена. Образование хиломикронов и транспорт липидов. Ресинтезированные в эпителиальных клетках кишечника триглицериды и фосфолипиды, а также поступивший в эти клетки из полости кишечника холестерин (здесь он может частично эстерифицироваться) соединяются с небольшим количеством белка и образуют относительно стабильные комплексные частицы – хиломикроны (ХМ). Последние содержат около 2% белка, 7% фосфолипидов, 8% холестерина и его эфиров и более 80% триглицеридов. Благодаря большим размерам частиц ХМ не способны проникать из эндотелиальных клеток кишечника в кровеносные капилляры и диффундируют в лимфатическую систему кишечника, а из нее – в грудной лимфатический проток. Затем из грудного лимфатического протока ХМ попадают в кровяное русло, т.е. с их помощью осуществляется транспорт экзогенных триглицеридов, холестерина и частично фосфолипидов из кишечника через лимфатическую систему в кровь. Уже через 1–2 ч после приема пищи, содержащей жиры, наблюдается алиментарная гиперлипемия. Это физиологическое явление, характеризующееся в первую очередь повышением концентрации триглицеридов в крови и появлением в ней ХМ. Пик алиментарной гиперлипемии наблюдается через 4–6 ч после приема жирной пищи. Обычно через 10–12 ч после приема пищи содержание триглицеридов возвращается к нормальным величинам, а ХМ полностью исчезают из кровяного русла. Триглицериды ХМ подвергаются гидролизу на поверхности эндотелия капилляров жировой ткани при участии фермента липопротеидлипазы.
(не нужно!)
β-Окисление - специфический путь катаболизма жирных кислот, при котором от карбоксильного конца жирной кислоты последовательно отделяется по 2 атома углерода в виде ацетил-КоА. Метаболический путь - β-окисление - назван так потому, что реакции окисления жирной кислоты происходят у β-углеродного атома. Окисление жирных кислот (β-окисление). Для преобразования энергии, заключенной в жирных кислотах, в энергию связей АТФ существует метаболический путь окисления жирных кислот до СО2 и воды, тесно связанный с циклом трикарбоновых кислот и дыхательной цепью. Этот путь называется β-окисление, т.к. происходит окисление 3-го углеродного атома жирной кислоты (β-положение) в карбоксильную группу, одновременно от кислоты отщепляется ацетильная группа, включающая С1 и С2 исходной жирной кислоты. Элементарная схема β-окисления. Реакции β-окисления происходят в митохондриях большинства клеток организма (кроме нервных клеток). Для окисления используются жирные кислоты, поступающие в цитозоль из крови или появляющиеся при липолизе собственных внутриклеточных ТАГ. Суммарное уравнение окисления пальмитиновой кислоты выглядит следующим образом: Пальмитоил-SКоА + 7ФАД + 7НАД+ + 7Н2O + 7HS-KoA → 8Ацетил-SКоА + 7ФАД Н2 + 7НАД Н Этапы окисления жирных кислот. 1. Прежде, чем проникнуть в матрикс митохондрий и окислиться, жирная кислота должна активироваться в цитозоле. Это осуществляется присоединением к ней коэнзима А с образованием ацил-S-КоА. Ацил-S-КоА является высокоэнергетическим соединением. Необратимость реакции достигается гидролизом дифосфата на две молекулы фосфорной кислоты. Реакция активации жирной кислоты. 2. Ацил-S-КоА не способен проходить через митохондриальную мембрану, поэтому существует способ его переноса в комплексе с витаминоподобным веществом карнитином. На наружной мембране митохондрий имеется фермент карнитин-ацилтрансфераза I. Карнитин-зависимый транспорт жирных кислот в митохондрию. Карнитин синтезируется в печени и почках и затем транспортируется в остальные органы. Во внутриутробном периоде и в первые годы жизни значение карнитина для организма чрезвычайно велико. Энергообеспечение нервной системы детского организма и, в частности, головного мозга осуществляется за счет двух параллельных процессов: карнитин-зависимого окисления жирных кислот и аэробного окисления глюкозы. Карнитин необходим для роста головного и спинного мозга, для взаимодействия всех отделов нервной системы, ответственных за движение и взаимодействие мышц. Существуют исследования, связывающие с недостатком карнитина детский церебральный паралич и феномен "смерти в колыбели". 3. После связывания с карнитином жирная кислота переносится через мембрану транслоказой. Здесь на внутренней стороне мембраны фермент карнитин-ацилтрансфераза II вновь образует ацил-S-КоА который вступает на путь β-окисления. 4. Процесс собственно β-окисления состоит из 4-х реакций, повторяющихся циклически. В них последовательно происходит окисление (ацил-SКоА-дегидрогеназа), гидратирование (еноил-SКоА-гидратаза) и вновь окисление 3-го атома углерода (гидроксиацил-SКоА-дегидрогеназа). В последней, трансферазной, реакции от жирной кислоты отщепляется ацетил-SКоА. К оставшейся (укороченной на два углерода) жирной кислоте присоединяется HS-КоА, и она возвращается к первой реакции. Все повторяется до тех пор, пока в последнем цикле не образуются два ацетил-SКоА. Расчет энергетического баланса β-окисления. При расчете количества АТФ, образуемого при β-окислении жирных кислот необходимо учитывать: Количество Ацетил-КоА: 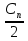 Количество циклов β-окисления: 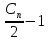
В формуле: 12 – число АТФ из ЦТК, 5 – число АТФ из дыхательной цепи, 1 – затрата АТФ на цикл. количество образуемого ацетил-SКоА – определяется обычным делением числа атомов углерода в жирной кислоте на 2. число циклов β-окисления. Число циклов β-окисления легко определить исходя из представления о жирной кислоте как о цепочке двух углеродных звеньев. Число разрывов между звеньями соответствует числу циклов β-окисления. Эту же величину можно подсчитать по формуле (n/2 -1), где n – число атомов углерода в кислоте. число двойных связей в жирной кислоте. В первой реакции β-окисления происходит образование двойной связи при участии ФАД. Если двойная связь в жирной кислоте уже имеется, то необходимость в этой реакции отпадает и ФАД Н2 не образуется. Количество необразованных ФАД Н2 соответствует числу двойных связей. Остальные реакции цикла идут без изменений. количество энергии АТФ, потраченной на активацию (всегда соответствует двум макроэргическим связям). |