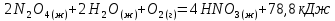отчет по практике. Производство неконцентрированной азотной кислоты. Стадия окисления аммиака. Мощность 380 тыс тг
 Скачать 1.63 Mb. Скачать 1.63 Mb.
|
5МПа и использовании чистого кислорода образуется 97-98%-ная кислота, содержащая до 30% (масс.) растворенных оксидов азота. Целевой продукт получают разгонкой этого раствора. |
| | 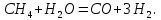 | (1) |
Далее CO подвергается паровой конверсии на железохромовых и медьсодержащих катализаторах:
| | 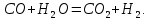 | (2) |
При взаимодействии водорода с азотом воздуха образуется аммиак:
| | 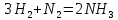 | (3) |
Вследствие каталитической окислении аммиака кислородом воздуха:
| | 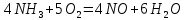 | (4) |
с последующим гомогенным окислением монооксида азота:
| | 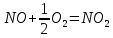 | (5) |
и абсорбцией диоксида азота водой:
| | 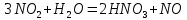 | (6) |
получают азотную кислоту [1].
Промышленные схемы производства неконцентрированной HNO3 отличаются преимущественно по давлению в системе, при котором протекают главные стадии процесса. В соответствии используемого давления их можно условно подразделить на следующие технологические группы:
Унифицированная комплексная линия УКЛ-7, работающая под единым

 давлением 0,716 МПа, производительность агрегата которого составляет 120 тыс. тонн моногидрата в год. Содержание оксидов азота в отходящих газах после каталитической очистки не более 0,005% (об.). Агрегаты УКЛ-7 оснащены приборами автоматизации, которые позволяют управлять процессом из ЦПУ. В подобных агрегатах повышение давления гораздо интенсифицирует все химические реакции, способствует повышению эффективности теплообмена, сокращает объем арматуры и коммуникаций. Следовательно вышеперечисленные факторы снижают капитальные затраты на строительство установок. К недостаткам агрегата можно отнести то, что при повышении давления помимо основной целевой реакции ускоряются побочные реакции, также увеличивается энергозатраты. Решением данной проблемы является путь, по которому тепло, выделяющиеся при окислении аммиака, используется для получения пара энергетических параметров. Схема УКЛ-7 достаточно эффективна так как в этой схеме аппараты размещаются между компрессорной группой и газовой турбиной, что снижает энергозатраты. На таблице 1 приведены некоторые показатели технологического режима [2, 4].
давлением 0,716 МПа, производительность агрегата которого составляет 120 тыс. тонн моногидрата в год. Содержание оксидов азота в отходящих газах после каталитической очистки не более 0,005% (об.). Агрегаты УКЛ-7 оснащены приборами автоматизации, которые позволяют управлять процессом из ЦПУ. В подобных агрегатах повышение давления гораздо интенсифицирует все химические реакции, способствует повышению эффективности теплообмена, сокращает объем арматуры и коммуникаций. Следовательно вышеперечисленные факторы снижают капитальные затраты на строительство установок. К недостаткам агрегата можно отнести то, что при повышении давления помимо основной целевой реакции ускоряются побочные реакции, также увеличивается энергозатраты. Решением данной проблемы является путь, по которому тепло, выделяющиеся при окислении аммиака, используется для получения пара энергетических параметров. Схема УКЛ-7 достаточно эффективна так как в этой схеме аппараты размещаются между компрессорной группой и газовой турбиной, что снижает энергозатраты. На таблице 1 приведены некоторые показатели технологического режима [2, 4].Таблица 1
Основные показатели технологического режима
| Наименование показателя | Нормы |
| Содержание аммиака в аммиачно-воздушной смеси, об. % | 9,5-10,6 |
| Давление воздуха на выходе из компрессора, МПа | 0,23-0,33 |
| Температура воздуха на выходе из компрессора, °С | до 175 |
| Температура, °С: | |
| газообразного аммиака после нагревателя | 80-110 |
| аммиачно-воздушной смеси | 170-230 |
| контактирования | 880-910 |
| Температура нитрозных газов, °С | |
| на выходе из котла-утилизатора | 230-285 |
Продолжение табл. 1
| Наименование показателя | нормы |
| на входе в абсорбционную колонну | 30-50 |
| Давление пара из котлов-утилизаторов, МПа | 1,3-1,5 |
| Концентрация продукционной кислоты, мас. % | 58-60 |
| Платиноидный катализатор (безвозвратные потери), г | 0,155 |
| Вода оборотная, м3 | 159 |
| Природный газ, м3 | 125-135 |
 В схемах УКЛ-7 используется низкотемпературная (селективная) каталитическая восстановление оксидов азота с использованием аммиака, так как высокотемпературная очистка хвостовых газов от оксидов азота с использованием природного газа имеет определенные недостатки. Так, вследствие выделения большого количества тепла при выжигании кислорода его содержание в выхлопных газах ограничивают 2,5-3,0 об.%, значителен расход природного газа, необходимы затраты на утилизацию тепла. В связи с этим был разработан и применяется в различных производствах способ селективного восстановления оксидов азота. Особенностью этого процесса является взаимодействие используемого восстановителя только с оксидами азота. Таким реагентом, применяемым в промышленной практике, является аммиак. Процесс регенерации оксидов азота протекает до молекулярного азота при температурах 200-350°С по реакциям:
В схемах УКЛ-7 используется низкотемпературная (селективная) каталитическая восстановление оксидов азота с использованием аммиака, так как высокотемпературная очистка хвостовых газов от оксидов азота с использованием природного газа имеет определенные недостатки. Так, вследствие выделения большого количества тепла при выжигании кислорода его содержание в выхлопных газах ограничивают 2,5-3,0 об.%, значителен расход природного газа, необходимы затраты на утилизацию тепла. В связи с этим был разработан и применяется в различных производствах способ селективного восстановления оксидов азота. Особенностью этого процесса является взаимодействие используемого восстановителя только с оксидами азота. Таким реагентом, применяемым в промышленной практике, является аммиак. Процесс регенерации оксидов азота протекает до молекулярного азота при температурах 200-350°С по реакциям:| | 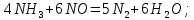 | (7) |
| | 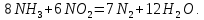 | (8) |
Широкое применение для этой цели получил алюмо-ванадиевый катализатор типа АВК-10, АВК-10М (технические требования, согласно ТУ 28-03-3001-90, приведены в таблице 2) [2, 4].
Таблица 2
 Технические требования на катализатор АВК-10М
Технические требования на катализатор АВК-10М | № п/п | Наименование показателя | Нормы |
| 1 | Внешний вид | Гранулы цилиндрической формы желтого цвета |
| 2 | Массовая доля оксидов ванадия в пересчете на V2O5, % | 13,5 ± 1,5 |
| 3 | Массовая доля оксидов марганца в пересчете на MnO2, % | 0,7 – 1,0 |
| 4 | Насыпная плотность, г/дм3 | 500 - 650 |
| 5 | Активность катализатора – степень восстановления оксидов азота аммиаком, %, не менее | 96,5 |
| 6 | Механическая прочность, %, не менее | 97 |
| 7 | Массовая доля мелочи размером менее 3,00 мм, %, не более | 0,7 |
| 8 | Размеры гранул, мм: | |
| | а) длина, не более | 18 |
| | б) диаметр | 5 ± 1 |