Химия.Шиманович. Решение типовых задач, программированные вопросы для самопроверки и контрольные задания для студентовзаочников инженернотехнических (нехимических) специальностей вузов
 Скачать 10.69 Mb. Скачать 10.69 Mb.
|
|
Гидролиз солей Химическое обменное взаимодействие ионов растворенной соли с водой, приводящее к образованию слабодиссоциирующих продуктов (молекул слабых кислот или оснований, анионов кислых или катионов основных солей) и сопровождающееся изменением рН среды, называется гидролизом. Пример 1. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей: a) KCN; б) Na2CO3; в) ZnS04. Определите реакцию среды растворов этих солей. Решение, а) Цианид калия KCN — соль слабой одноосновной кислоты (см. табл. I приложения) HCN и сильного основания КОН. При растворении в воде молекулы KCN полностью диссоциируют на катионы К+ и анионы CN- . Катионы К не могут связывать ионы ОН- воды, так как КОН — сильный электролит. Анионы же CN- связывают ионы Н+ воды, образуя молекулы слабого электролита HCN. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза CN + Н20 <=> HCN + ОН или в молекулярной форме KCN + Н20 <=>HCN + КОН В результате гидролиза в растворе появляется некоторый избыток ионов OIT, поэтому раствор KCN имеет щелочную реакцию (рН > 7). б) Карбонат натрия Na2C03 — соль слабой многоосновной кислоты и сильного основания. В этом случае анионы соли С032-, связывая водородные ионы воды, образуют анионы кислой соли , а не молекулы Н2С03, так как ионы НСО 3 диссоциируют гораздо труднее, чем молекулы Н2С03. В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза С032-+ H20<=> НСО 3 + ОН- или в молекулярной форме Na2C03 + Н20 <=> NaHC03 + NaOH В растворе появляется избыток ионов ОН-. поэтому раствор Na2C03 имеет щелочную реакцию (рН > 7). в) Сульфат цинка ZnS04 — соль слабого многокислотного основания Zn(OH)2 и сильной кислоты H2S04. В этом случае катионы Zn2+ связывают гидроксильные ионы воды, образуя катионы основной соли ZnOH+. Образование молекул Zn(OH)2 не происходит, так как ионы ZnOH+ диссоциируют гораздо труднее, чем молекулы Zn(OH)2. В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза Zn2+ + Н20<=> ZnOH+ + Н+ или в молекулярной форме 2ZnS04 + 2Н20 <=> (ZnOH)2S04 + H2S04 В растворе появляется избыток ионов водорода, поэтому раствор ZnS04 имеет кислую реакцию (рН < 7). Пример 2. Какие продукты образуются при смешивании растворов Аl (NО3)3 и К2СО3? Составьте ионно-молекулярное и молекулярное уравнение реакции. Решение. Соль Al (N03)3 гидролизуется по катиону, а К2С03 — по аниону: Аl3+ + Н20 <=> АlОН2+ + Н+ СО32- +Н20<=>НСО32- +OH- Если растворы этих солей находятся в одном сосуде, то идет взаимное усиление гидролиза каждой из них, ибо ионы Н+ и ОН-образуют молекулу слабого электролита Н20. При этом гидролитическое равновесие сдвигается вправо и гидролиз каждой из взятых солей идет до конца с образованием Аl (ОН)3 и С02 (Н2С03). Ионно-молекулярное уравнение: 2Аl3+ + 3С032- + 3Н20 = 2Аl (ОН)3 + 3С02 молекулярное уравнение: 2Al (N03)3 + 3К2С03 + 3Н20 = 2Аl (ОН)3 + ЗС02 + 6KNO3 КОНТРОЛЬНЫЕ ВОПРОСЫ 201. Составьте ионно-молекулярное и молекулярное уравнения гидролиза, происходящего при смешивании растворов K2S и СгСl3. Каждая из взятых солей гидролизуется необратимо до конца с образованием соответствующих основания и кислоты.
ния гидролиза соответствующих солей. Какое значение (7 < рН < 7) имеют растворы этих солей?
209. Какое значение рН (7< рН < 7) имеют растворы солей Na3PO4 K2S, CuS04? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей. 210. Составьте ионно-молекулярные и молекулярные уравнения гидролиза сетей CuCl2, Сs2CO3,Cr(NO3)3. Какое значение рН (7 < рН < 7) имеют растворы этих солей? 211. Какие из солей - RbCl, Cr2(SO4)3, Ni(NO3)2, Na2S03 —-подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей. Какое значение рН (7< рН <^ 7) имеют растворы этих солей? 212.К раствору А12(SO4)3 добавили следующие вещества: а)Н2SO4; б)КОН; в) Na2S03; г)Zn SO4/ В каких случаях гидролиз сульфата алюминия усилится? Почему? Составьте ионно-молекулярные уравнения гидролиза соответствующих солей. 213. Какая из двух солей при равных условиях в большей степени подвергается гидролизу: Na2С03 или Na2S03; FeCl3 или FeCl2? Почему? Составьте ионно-молекулярные уравнения гидролиза этих солей. 214. При смешивании растворов А12(SO4)3 и Na2С03 каждая из взятых солей гидролизуется необратимо до конца с образованием соответствующих основания и кислоты. Составьте ионно-молекулярные и молекулярные уравнения происходящего совместного гидролиза. 215. Какая из солей – NaBr, Na2S, K2SО3, CoCl2 – подвергается гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей. Определите рН (7< рН <^ 7) растворов этих солей? 216. Какая из двух солей при равных условиях в большей степени подвергается гидролизу: NaCN или NaClО; Мg Cl2 или ZnCl2? Почему? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей. 217. Составьте ионно-молекулярные и молекулярные уравнения гидролиза соли, раствор которого имеет: а) щелочную реакцию; б)кислую реакцию. 218. Какое значение рН (7< рН < 7) имеют растворы следующих солей: K3РО4, Pb(NO3)2, Na2S? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей. 219. какие из солей - K2СО3, FeCl3, K2SО4, ZnCl2 – подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей. Определите рН (7< рН <^ 7) растворов этих солей? 220. При смешивании растворов А12(SO4)3 и Na2S каждая из взятых солей гидролизуется необратимо до конца с образованием соответствующих основания и кислоты. Выразите этот совместный гидролиз ионно-молекулярным и молекулярным уравнениями. КОНТРОЛЬНОЕ ЗАДАНИЕ № 2 Окислительно-восстановительные реакции Окислительно-восстановительными называют реакции, сопровождающиеся изменением степени окисления атомов, входящих в состав реагирующих веществ. Под степенью окисления (n) понимают условный заряд атома, который вычисляют исходя из предположения, что молекула состоит только из ионов. Иными словами: степень окисления — это условный заряд, который приобрел бы атом элемента, если предположить, что они принял или отдач то или иное число электронов. Окисление-восстановление — это единый, взаимосвязанный процесс. Окисление приводит к повышению степени окисления восстановителя, а восстановление — к ее понижению у окислителя. Повышение или понижение степени окисления атомов отражается в электронных уравнениях: окислитель принимает электроны, а восстановитель их отдает. При этом не имеет значения, переходят ли электроны от одного атома к другому полностью и образуются ионные связи или электроны только оттягиваются к более электроотрицательному атому и возникает полярная связь. О способности того или иного вещества проявлять окислительные, восстановительные или двойственные (как окислительные, так и восстановительные) свойства можно судить по степени окисления атомов окислителя и восстановителя. Атом того или иного элемента в своей высшей степени окисления не может ее повысить (отдать электроны) и проявляет только окислительные свойства, а в своей низшей степени окисления не может ее понизить (принять электроны) и проявляет только восстановительные свойства. Атом же элемента, имеющий промежуточную степень окисления, может проявлять как окислительные, так и восстановительные свойства. Например: 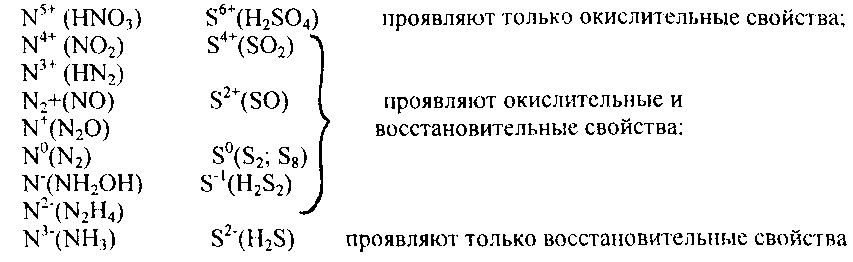 При окислительно-восстановительных реакциях валентность атомов может и не меняться. Например, в окислительно-восстановительной реакции Н02+ С102 = 2Н+С1- валентность атомов водорода и хлора до и после реакции равна единице. Изменилась их степень окисления. Валентность определяет число связей, образованных данным атомом, и поэтому знака заряда не имеет. Степень же окисления имеет знак плюс или минус. Пример 1. Исходя из степени окисления (n) азота, серы и марганца в соединениях NH3, HN02, HNO3, H2S, H2S03, H2S04, Mn02 и KMnО4, определите, какие из них могут быть только восстановителями, только окислителями и какие проявляют как окислительные, так и восстановительные свойства. Решение. Степень окисления азота в указанных соединениях соответственно равна: -3 (низшая), +3 (промежуточная), +5 (высшая); n/(S) соответственно равна: -2 (низшая), +4 (промежуточная), +6 (высшая); n(Мп) соответственно равна: + 4 (промежуточная), +7 (высшая). Отсюда: NH3, H2S — только восстановители; HN03, H2S04, KMn04 — только окислители; HNО2, H2S03, Mn02 — окислители и восстановители. Пример 2. Могут ли происходить окислительно-восстановительные реакции между следующими веществами: a) H2S и HI; б) H2S и H2S03: в) H2S03 и НС1О4? Решение а) Степень окисления в H2S n(S)= -2; в HI n(I) = -1. Так как и сера, и иод находятся в своей низшей степени окисления, то оба вещества проявляют только восстановительные свойства и взаимодействовать друг с другом не могут; б) в H2S n(S) = -2 (низшая), в H2S03 n(S) = +4 (промежуточная). Следовательно, взаимодействие этих веществ возможно, причем H2S()3 является окислителем; в) в H2S03 n(S)= +4 (промежуточная); в НС1О4 n(Сl) = +7 (высшая). Взятые вещества могут взаимодействовать, H2S03 в этом случае будет проявлять восстановительные свойства. Пример 3. Составьте уравнения окислительно-восстановительной реакции, идущей по схеме: Решение. Если в условии задачи даны как исходные вещества, так и продукты их взаимодействия, то написание уравнения реакции сводится, как правило, к нахождению и расстановке коэффициентов. Коэффициенты определяют методом электронного баланса с помощью электронных уравнений. Вычисляем, как изменяют степень окисления восстановитель и окислитель, и отражаем это в электронных уравнениях: восстановитель/ 5 Р3+-2е-= Р5+ процесс окисления окислитель /2 Мn7++5е- = Мn2+ процесс восстановления Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которые присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов десять. Разделив это число на 5, получаем коэффициент 2 для окислителя и продукта его восстановления, а при делении 10 на 2 получаем коэффициент 5 для восстановителя и продукта его окисления. Коэффициент перед веществами, атомы которых не меняют свою степень окисления, находят подбором. Уравнение реакции будет иметь вид: 2КМn04 + 5Н3РОз + 3H2S04 = 2MnS04 + 5Н3Р04 + K2S04 + 3H20 Пример 4. Составьте уравнение реакции взаимодействия цинка с концентрированной серной кислотой, учитывая максимальное восстановление последней. Решение. Цинк, как любой металл, проявляет только восстановительные свойства. В концентрированной серной кислоте окислительная функция принадлежит сере (+6). Максимальное восстановление серы означает, что она приобретает минимальную степень окисления. Минимальная степень окисления серы как p-элемента VIA-группы равна -2. Цинк как металл IIB-группы имеет постоянную степень окисления +2. Отражаем сказанное в электронных уравнениях: |
