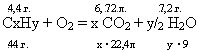Решение задач на вывод химических формул
 Скачать 446 Kb. Скачать 446 Kb.
|
|
19. Определите формулу вещества, если массовая доля азота в нем 30,43%, а кислорода — 69,57 %. 20. Химический анализ показал, что в 17 г соединения алюминия с кислородом содержится 9 г алюминия. Найдите простейшую формулу этого соединения. 21. Найдите простейшую формулу оксида хрома, содержащего 68,4 % хрома. 22. Найдите простейшую формулу вещества, содержащего 43,6 % натрия, 11,3 % углерода и 45,3 % кислорода. 23. При анализе навески 3,16 мт органического вещества обнаружено, что в его составе 0,96 мт углерода, 0,12 мг водорода и 0,8 мт кальция, а остальное приходится на кислород. Найдите простейшую формулу этого соединения. 24. Известно, что оксид некоторого металла содержит 11,11 % кислорода и в его молекуле на один атом кислорода приходится два атом, а металла. Определите, что это за металл, и о каком соединении идет речь. 25. Найдите формулу соединения, если известно, что в его состав входи- 1,59 % водорода, 22,22 % азота, 76,19 % кислорода. 26. Дано: углерода —92,3 %, водорода — 7,7 %, масса 1 л газа при н.у. 1,16 г. Определить молекулярную формулу. 27. Хлорпроизводное предельного углеводорода имеет молекулярную массу 237. Процентный состав этого соединения следующий: хлора — 89,9 %, углерода — 10,1 %. Найдите его молекулярную формулу. 1. Найдем массу хлора 237 237—213 = 24 х : .у=24/12 : 213/35,5=2 : 6=>С2С16. 28. Определите формулы двух оксидов одного и того же элемента, если его массовая доля в этих оксидах равна 88,11 и 84,75%. Этот элемент образует также фторид, содержащий 32,47 % фтора по массе. 29. Элемент ниобий образует более двадцати галогенводородов. Установите две формулы соединений ниобия с одним из галогенов, если содержание металла в них составляет 15,47 и 21,54 % по массе. 30. Относительная плотность по водороду неизвестного газообразного вещества равна 22. Найдите молекулярную формулу этого вещества, если массовая доля (С) в нем 54,55 %, (Н) — 9,09 %, (О) — 36,36 %.31. Найдите простейшую формулу соединения, имеющего следующий состав: Nа —42,1 %, Р — 18,9 %, О — 39,0 %. 8-1. Определите молекулярную формулу органического соединения с составом 80% углерода и 20% водорода, если плотность его по воздуху равна 1,034. 8-2. Определите молекулярную формулу углеводорода, который содержит 85,7% углерода и имеет плотность по водороду 21. 8-3. Органическое вещество содержит 84,21% углерода и 15,79% водорода. Плотность паров вещества по воздуху 3,93. Определить формулу вещества. 8-4. Углеводород содержит 82,76% углерода и 17,24% водорода (по массе). При монохлорировании этот углеводород образует два изомерных алкилхлорида – первичный и третичный. Определить строение исходного углеводорода. 8-5. Органическое вещество содержит 91, 3% углерода и 8,7% водорода. Относительная плотность паров по кислороду равна 2,875. Вывести молекулярную формулу вещества. 8-6. Установите молекулярную формулу углеводорода, молекула которого содержит 40 электронов, а молекулярная масса которого 70. 8-10. Найти молекулярную формулу предельного углеводорода, массовая доля углерода в котором 83,3%. 8-11. Установите молекулярную формулу дибромалкана, содержащего 85,11% брома. 8-12. Установите молекулярную формулу монохлоралкана, содержащего 38,38% хлора. Приведите графические формулы и названия всех соединений, отвечающих данной формуле. 8-13. Монохлорпроизводное предельного углеводорода содержит 38.4% хлора. Определить формулу углеводорода. 8-14. Монохлорпроизводное предельного углеводорода содержит 38,4% хлора по массе. Определите, сколько атомов углерода содержится в молекуле этого вещества. 8-15. В монохлоралкане массовая доля хлора равна 55,04%. Определите формулу монохлоралкана. 8-16. Определите молекулярную формулу фторпроизводного алкана, в 34,27 г которого содержится 17,44 г фтора. 8-17. Определите молекулярную формулу хлорпроизводного алкана, в 35,24 г которого содержится 23,83 г хлора. 8-18. Дихлорпроизводное алкана содержит 5,31% водорода по массе. Определите молекулярную формулу дихлоралкана. Приведите структурную формулу одного из возможных изомеров и назовите его. 8-19. Вещество содержит 36.4% С, 6.1% Н и фтор. Молекулярная масса этого вещества меньше 110. Сколько всего атомов в этой молекуле? 8-20. Органическое вещество содержит 0,2424 доли углерода, 0,0404 доли водорода, 0,7172 хлора. Плотность паров по азоту составляет 3,5357. Определите химическую формулу этого вещества. 8-21. Органическое вещество содержит 0,2975 углерода, 0,0413 водорода, 0,6612 брома. Относительная плотность паров по воздуху равна 4,1724. Вывести молекулярную формулу вещества. 8-22. Хлорпроизводное предельного углеводорода имеет молекулярную массу 257. Процентный состав этого соединения следующий: хлор-89,9%, углерод-10,1%. Определите его молекулярную формулу. 8-23. При монохлорировании углеводорода, содержащего 83,72% С и 16,28% Н, образовалось 2изомерных хлорпроизводных – первичное и третичное. Установите строение углеводорода, составьте формулы продуктов хлорирования 8-25. Содержание брома в соединении, полученном при взаимодействии алкена с бромом, составляет 69,56 мас.%. Определите структурную формулу алкена, если известно, что он может существовать в виде цис- и транс- изомеров. . 15-10. Ароматическое соединение ряда бензола содержит 90.0% углерода. Нарисовать ео возможные изомеры. 15-48. Плотность по водороду вещества равна 22. Вещество имеет следующий состав: углерод - 54,55%, водород - 9,09%, кислород – 36,36% Вещество легко восстанавливает оксид серебра. Определить это вещество. 15-50. Органическое вещество природного происхождения содержит 40 мас.% углерода, 6,67 мас.% водорода и кислород. Сколько всего атомов содержит молекула этого соединения, если известно, что его молярная масса равна 180 г/моль? 15-26. В предельной одноосновной карбоновой кислоте массовая доля кислорода равна 43,24%. Определите формулу кислоты. 15-28. Предельная одноосновная карбоновая кислота содержит 48.6%С. Какая это кислота? 15-30. Установите молекулярную формулу предельной карбоновой кислоты, метиловый эфир которой содержит 9,09% водорода. 15-40. При взаимодействии первичного одноатомного спирта, содержащего 60% углерода и 13,3% водорода, с органической кислотой образовалось вещество, плотность паров которого по водороду равна Определите молекулярную формулу каждого из веществ. 15-41. При взаимодействии одноатомного спирта, содержащего 52,17% углерода и 13,04% водорода, с органической кислотой, образуется вещество, плотность паров которого по водороду равна 51. Определите молекулярную формулу каждого вещества, участвующего в реакции, и дайте им название. 15-42. При взаимодействии одноатомного спирта, содержащего 37,5% углерода, 12,5% водорода, с органической кислотой образуется вещество, плотность паров которого по водороду равна 37. Определите молекулярную формулу каждого вещества, участвующего в реакции, и дайте им название. 15-49. Эфир с молярной массой 130 г/моль при гидролизе образует кислоту, в серебряной соли которой массовая доля серебра составляет 59,66%. Определите число атомов углерода в молекуле спирта, образовавшего эфир. 15-37. Определите молекулярную формулу предельного многоатомного спирта, в 31,25 г которого содержится 14,15 г кислорода. 15-39. Определите молекулярную формулу предельного многоатомного спирта, в 37,67 г которого содержится 16,62 г углерода. 15-14. Путресцин содержит 54,5% (С), 13,6% (Н), остальное приходится на азот. Плотность его паров по водороду равна 44. Установите молекулярную формулу путресцина. 15-15. Одно из важнейших химических соединений реагентов, относящихся к классу диаминов, содержит 40% (С) , 46,7% (N), остальное – водород. Установите молекулярную формулу этого органического соединения. 15-17. Вещество содержит 69,2 % С, 3,85 % Н и азот. Молекулярная масса этого вещества меньше 150. Сколько всего атомов в этой молекуле? 15-20. Предельный амин содержит 31.1% азота. Определите возможное строение этого амина. 15-21. Установите молекулярную формулу предельного третичного амина, содержащего 23,73% азота по массе. 15-29. Массовая доля кислорода в одноосновной аминокислоте равна 42,67%. Установите молекулярную формулу аминокислоты. 1.20 (3) Газообразный углеводород имеет относительную плотность по кислороду 1,375, а массовые доли углерода и водорода в нем составляют соответственно 81,8% и 18,2%. Какое это соединение? 1.21 (3) Относительная плотность паров углеводорода по кислороду равна 2,25. Массовая доля углерода в нем равна 83,33%. Выведите молекулярную формулу этого углеводорода. 1.22 (3) Плотность углеводорода при нормальных условиях равна 1,964 г/л. Массовая доля углерода в нем равна 81,82%. Выведите молекулярную формулу этого углеводорода. 2.9 (3) Относительная плотность паров углеводорода по азоту равна 3. Массовая доля углерода в нем равна 85,71%. Выведите его молекулярную формулу. 2.10 (3) Относительная плотность паров углеводорода по водороду равна 35. Массовая доля водорода в нем равна 14,285%. Выведите молекулярную формулу углеводорода. 3.14 (3) Относительная плотность паров углеводорода по азоту равна 3,5. Массовая доля углерода в нем равна 85,71%. Выведите молекулярную формулу углеводорода. 3.15 Углеводород массой 12,5 г при н. у. занимает объем 5 л. Массовая доля водорода в нем равна 14,29%. Выведите молекулярную формулу углеводорода. 5.15 Относительная плотность паров углеводорода по водороду равна 41. Массовая доля водорода в нем равна 12,2%. Выведите молекулярную формулу углеводорода 5.16 (3) Относительная плотность паров углеводорода по кислороду равна 2,125. Массовая доля углерода в нем равна 88,24%. Выведите молекулярную формулу углеводорода 6.17 (3) Относительная плотность паров углеводорода по углекислому газу равна 2,41. Массовая доля углерода равна 90,6%. Выведите молекулярную формулу углеводорода. 6.21 (1,3) При хлорировании на свету некоторого углеводорода получается единственное монохлорпроизводное, массовая доля хлора в котором равна 22,98%. Назовите исходный углеводород. 6.22 (1,3) При хлорировании на свету некоторого углеводорода получается единственное монохлорпроизводное, массовая доля хлора в котором равна 21,07%. Назовите исходный углеводород. 7.19 (3) Относительная плотность паров органического соединения по кислороду равна 2,75. Массовая доля углерода в этом веществе равна 68,18%, массовая доля водорода равна 13,64%, остальное — кислород. Выведите молекулярную формулу этого вещества. 7.20 (3) Относительная плотность паров органического соединения по воздуху равна 4. Массовая доля углерода в этом веществе равна 72,41%, массовая доля водорода равна 13,79%, массовая доля кислорода равна 13,79%. Выведите молекулярную формулу этого вещества. 8.7 (3) Относительная плотность паров органического вещества по углекислому газу равна 2,41. Массовая доля углерода в этом веществе равна 45,28%, массовая доля водорода равна 9,44%, а остальное приходится на кислород. Выведите молекулярную формулу этого вещества. 8.10 (3) Относительная плотность паров органического вещества по водороду равна 60. Массовая доля углерода в этом веществе равна 50%, массовая доля водорода равна 10%, массовая доля кислорода равна 40%. Выведите молекулярную формулу органического вещества. 9.5 (3) Относительная плотность паров органического соединения по метану равна 7,75. Массовая доля углерода в этом веществе равна 67,74%, массовая доля водорода равна 6,45%, а остальное приходится на кислород. Выведите молекулярную формулу этого соединения. 9.6 (3) Относительная плотность паров органического соединения по азоту равна 4,5. Массовая доля углерода в этом веществе равна 57,14%, массовая доля водорода равна 4,76%, массовая доля кислорода равна 38,10%. Выведите молекулярную формулу этого соединения. 10.16 (3) 10 л газообразного соединения при н. у. имеют массу 13,4 г. Массовые доли углерода и водорода в нем составляют соответственно 40% и 6,7%, остальное — кислород. Установите молекулярную формулу соединения. 10.17 (3) Относительная плотность паров органического соединения по кислороду равна 3,125. Массовая доля углерода в этом веществе равна 72%, массовая доля водорода равна 12%, остальное — кислород. Выведите молекулярную формулу этого соединения. 11.14 (3) Массовая доля углерода в предельной одноосновной карбоновой кислоте составляет 54,5%. Какая это кислота? Какие эфиры будут ее изомерами? 11.16 (3) Относительная плотность паров органического соединения по неону равна 5,4. Массовая доля углерода в этом веществе равна 58,82%, массовая доля водорода равна 9,8%, а остальное — кислород. Выведите молекулярную формулу органического соединения. Предложите возможные структуры. 11.17 (3) Относительная плотность паров органического соединения по кислороду равна 4,5. Массовая доля углерода в этом веществе равна 66,67%, массовая доля водорода равна 11,11%, массовая доля кислорода равна 22,22%. Выведите молекулярную формулу органического соединения. 13.14 (3) Массовая доля углерода в диамине равна 48,65%, массовая доля азота равна 37,84%. Выведите молекулярную формулу диамина. 13.15 (3) Массовая доля углерода в моноамине равна 63,16%, массовая доля азота равна 24,56%. Выведите молекулярную формулу амина. 14.10 (2) Выведите молекулярную формулу моноаминокарбоновой кислоты, массовая доля азота в которой составляет 11,97%. 14.11 (3) Массовая доля кислорода в предельном эфире аминоуксусной кислоты составляет 27,35%. Напишите возможные структурные формулы этого эфира. Вывод формул по продуктам сгорания Задача Какова молекулярная формула углеводорода, имеющего плотность 1,97 г/л, если при сгорании 4,4 г. его в кислороде образовалось 6,72 л. СО2 и 7,2 г. Н2О.
1) При сгорании 3г. углеводорода было получено 8,8 г.углекислого газа,5,4 г. воды. Относительная плотность углеводорода по воздуху равна 1,03. Определите молекулярную формулу углеводорода. 3г. 8,8г. 5,4г. CxHу + О2 = СО2 + Н2О Т.к. -.это углеводород => кроме углерода и водорода в нём больше ничего не содержится. Весь углерод из углеводорода перешёл в 8,8г СО2, а водород в 5,4г Н2О. 1. Рассчитаем Мr (CxHу) Мr (CxHу) = 1,03 2.Рассчитаем массу углерода в 8,8г СО2 3. Рассчитаем массу водорода в 5,4г Н2О. 4. Рассчитаем количество атомов углерода и водорода γ = т/Аr; х : у = 5. Устанавливаем простейшая формула или истинная Мr (С2Н6) = 12 2. При сгорании 1,84г органического вещества образовалось 2,64г углекислого газа и 1,44 г воды. Плотность горючего газа по кислороду равна 2,875. Определите молекулярную формулу вещества. 3. При сгорании 6,8 г газообразного неорганического вещества было получено 3,6 г воды и 12,8 г сернистого газа. Плотность горючего газа по кислороду равна 1,06. Определите молекулярную формулу вещества. 4. При сжигании 5,4 г паров неорганического вещества было получено 2,8 г. азота, 8,8 г углекислого газа и 1,8 г воды. Один литр паров этого вещества весит 1,205 г. Определите молекулярную формулу. 5. При сжигании 5,2 г вещества выделилось 8,96 л углекислого газа и 3,6 г воды. Определите молекулярную формулу вещества. 6. При сжигании 2,5 г вещества образовалось 3,42 г Н20 и 5,57 СО2. В состав вещества, кроме водорода и углерода, входит азот (23 %). Какова молекулярная формула. 7. При сжигании 3,1 г вещества (плотность по водороду 15,5), в котором обнаружены азот, водород и углерод, образуются 4,5 г воды; 4,4 г углекислого газа и 1,4 г азота. Определите молекулярную формулу вещества и процентный состав химических элементов. |