Полушин Ю.С Руководство. Руководство по анестезиологии и реаниматологии под редакцией профессора Ю. С. Полушина
 Скачать 4.32 Mb. Скачать 4.32 Mb.
|
3.2.4. Дыхательная недостаточностьНесмотря на то, что нарушения дыхания могут наступать на любом этапе газообмена, развитие дыхательной недостаточности как клинического синдрома связывают исключительно с патологией внешнего дыхания. Наиболее простое определение ей дал А.П. Зильбер (1996): «Дыхательная недостаточность (ДН) – это состояние организма, при котором возможности легких и аппарата вентиляции обеспечить нормальный газовый состав артериальной крови ограничены». Следует, однако, отметить, что как и в отношении терминологического определения дыхательной недостаточности, так и ее классификации общепринятой точки зрения не выработано. По патогенезу дыхательную недостаточность принято разделять на две основные группы: 1) с преимущественным поражением внелегочных механизмов, 2) с преимущественным поражением легочных механизмов. К развитию дыхательной недостаточности внелегочной природы приводят: - нарушение центральной регуляции дыхания (поражение головного и спинного мозга травматической, метаболической, циркуляторной, токсической, нейроинфекционной этиологии и т.п.,э - нарушение нервно-мышечной передачи (полиомиелит, полирадикулоневрит, миостения, интоксикация, применение курареподобных препаратов и пр.), - патология мышечного аппарата (миодистрофия, травма, коллагенозы и другие расстройства), - поражение грудной клетки (пневмоторакс, реберный клапан, плевральный выпот, кифосколиоз, ревматоидный спондилит и т.д.), - болезни системы крови, сопровождающиеся уменьшением количества гемоглобина, - патология кровообращения, приводящая к нарушению перфузии в легких (кровопотеря, сердечная недостаточность и пр.). Преимущественное поражение легочных механизмов вызывают: - обстукция центральных или периферических дыхательных путей (инородные тела, воспалительные заболевания, постинтубационный отек гортани, анафилаксия, нарушение дренирования мокроты и пр.), - рестрикция альвеолярной ткани (интерстициальный отек, пневмофиброз и т.п.), - диффузные расстройства при утолщении альвеоло-капиллярной мембраны (отек, коллагенозы, фиброз и др.), - поражение легочных капилляров (капилляротоксикоз, микроэмболия и пр.), - сокращение легочной функционирующей ткани (резекция легких, ателектаз, пневмония и пр.). В практической работе широко используется деление бронхолегочной ОДН на вентиляционную, когда нарушена механика дыхания и паренхиматозную, которая обусловлена патологическим процессом в газообменной зоне и интерстициальном пространстве легких. По скорости развития клинических симптомов различают острую и хроническую формы. Острая дыхательная недостаточность (ОДН) возникает в течение нескольких минут или суток. Она может быть излечена или перейти в хроническую дыхательную недостаточность, а та, в свою очередь, при определенных ситуациях может внезапно обостриться и приобрести все черты острой. Быстрота развития недостаточности не должна прямо связываться с ее тяжестью. ОДН не всегда переходит в несостоятельность, а хроническая может быть не менее тяжелой, чем острая. Превращение реаниматологии в междисциплинарную специальность привело к тому, что в отделения реанимации и интенсивной терапии стали поступать пациенты как с одной, так и с другой формой недостаточности. По тяжести течения дыхательную недостаточность предлагается разделять на три формы: а) декомпенсированную, б) компенсированную, в) скрытую (А.П. Зильбер, 1996). Для практики интенсивной терапии наибольшее значение имеют первые две формы. При декомпенсированной дыхательной недостаточности нормальный газовый состав артериальной крови не обеспечивается даже в условиях покоя, несмотря на включение компенсаторных механизмов (гипервентиляции и одышки, ускорения кровотока с тахикардией и повышения сердечного выброса, снижения тканевого метаболизма и пр.). Компенсированная дыхательная недостаточность характеризуется тем, что механизмы компенсации обеспечивают нормальный газовый состав артериальной крови в условиях покоя, но при провоцирующем воздействии (физическая нагрузка и т.п.) может возникнуть декомпенсация. Для этой формы даже в покое характерны изменения режима вентиляции, тахикардия при нормальном газовой составе крови. Скрытая недостаточность проявляется низкими функциональными резервами дыхательной системы, которые выявляются при проведении специальных исследований, в том числе с физическими нагрузочными пробами. О наличии такой формы нарушения газообмена у больного, подвергающегося оперативному вмешательству, анестезиологу важно узнать до операции, так как это может кардинально изменить как тактику анестезии, так и ведение раннего послеоперационного периода. По характеру расстройств газообмена различают гипоксемический и гиперкапнический варианты дыхательной недостаточности. Нарушение выведения углекислого газа значительно легче компенсируется усилением вентиляции, чем нарушением поглощения кислорода. При нормальной альвеолярной вентиляции нарушения газообмена приводят к гипоксемической дыхательной недостаточности, то есть к снижению РaO2 (из-за рефлекторного повышения вентиляции это сопровождается снижением РaCO2). Напротив, снижение альвеолярной вентиляции приводит к одновременному снижению РaO2 и повышению РaCO2, что носит название гиперкапнической дыхательной недостаточности. Важное следствие гиперкапнии - дыхательный ацидоз. Гипоксемическая дыхательная недостаточность определяется, когда преимущественно нарушается оксигенация (РaO2 < 60 мм рт. ст. либо SaO2 < 90%), при этом как правило, РСО2 не превышает 40 мм рт.ст. В диагностике гипоксемической формы ОДН следует обращать внимание на характер дыхания: инспираторный стридор - при нарушениях проходимости верхних дыхательных путей, парадоксальное дыхание - при травме грудной клетки, прогрессирующее тахипноэ и т.д. Другие клинические признаки не выражены. В начале развития ОДН часто отмечается тахикардия с умеренной артериальной гипертензией, неспецифические неврологические проявления: неадекватность мышления, спутанность сознания и речи, заторможенность и т.д. Цианоз не выражен, лишь при прогрессировании гипоксии он становится интенсивным, внезапно нарушается сознание, затем наступает кома (гипоксическая) с отсутствием рефлексов, резко снижается АД и может наступить остановка кровообращения. Продолжительность гипоксемической ОДН может колебаться от нескольких минут (при аспирации, асфиксии) до нескольких часов и дней (РДСВ). Выделяют несколько основных причин развития гипоксемической дыхательной недостаточности: 1) неравномерность вентиляционно-перфузионного отношения; 2) сброс крови «справа налево»; 3) низкое парциальное давление кислорода во вдыхаемом воздухе; 4) нарушение диффузии газов через альвеолярно-капиллярную мембрану; 5) повышенная потребность в кислороде. Неравномерность вентиляционно-перфузионного отношения возникает при множестве заболеваний, например при пневмонии, бронхиальной астме, саркоидозе и т.д. Это самая частая причина гипоксемической дыхательной недостаточности. От участков, где кровоток преобладает над вентиляцией, оттекает кровь, недонасыщенная кислородом, что не компенсируется нормальной или повышенной оксигенацией крови в участках, где вентиляция преобладает над кровотоком. Гипоксемия обычно устраняется при дыхании смесью с высокой концентрацией кислорода. Р(A–a)O2 при этом повышена. Сброс крови справа налево (шунт) можно рассматривать как крайнюю степень неравномерности вентиляционно-перфузионного отношения, когда значительная часть крови протекает через невентилируемые участки легких. Это состояние развивается, например, при ОРДС и кардиогенном отеке легких. При сбросе более 30% гипоксемия не устраняется при дыхании чистым кислородом, Р(A–a)O2 также повышена. Низкое парциальное давление кислорода во вдыхаемом воздухе - редкая причина дыхательной недостаточности. Встречается на больших высотах (например, в горах) и при наличии в воздухе большого количества инородных газов (например, в результате аварии на производстве); Р(A–a)O2 в норме. Нарушение диффузии газов через альвеолярно-капиллярную мембрану встречается довольно часто, например, при интерстициальных заболеваниях легких, однако к гипоксемии приводит редко и обычно выявляется только с помощью нагрузочных проб. Выведение углекислого газа не нарушается, так как он диффундирует значительно быстрее, чем кислород; Р(A–a)O2 может быть повышена. Низкое содержание кислорода в венозной крови бывает при анемии, снижении сердечного выброса, повышенном потреблении кислорода тканями. В норме легкие полностью насыщают кислородом поступающую в них кровь. Однако при выраженном сбросе крови справа налево низкое содержание кислорода в венозной крови может усиливать гипоксемию. Гиперкапническая дыхательная недостаточность (РaCO2 > 55 мм рт. ст.)- результат снижения альвеолярной вентиляции. Клиническими признаками прогрессирующей гиперкапнии являются: нарушения дыхания (одышка, постепенное уменьшение дыхательного и минутного объемов дыхания, бронхиальная гиперсекреция, невыраженный цианоз или гиперемия лица), нарастающая неврологическая симптоматика (безразличие, агрессивность, возбуждение, заторможенность, кома), сердечно-сосудистые нарушения (тахикардия, стойкое повышение АД, затем декомпенсация сердечной деятельности вплоть до гипоксической остановки сердца на фоне гиперкапнии). Гиперкапническая дыхательная недостаточность возникает при уменьшении минутного объема дыхания и увеличении мертвого пространства. В обоих случаях гиперкапнии может способствовать повышенное образование CO2. Уменьшение минутного объема дыхания происходит при поражении центральной и периферической нервной системы (травма спинного мозга, синдром Гийена-Барре, ботулизм, миастения, боковой амиотрофический склероз), мышц (полимиозит, миопатии), грудной клетки (сколиоз), при передозировке некоторых лекарственных средств, гипотиреозе, гипокалиемии и обструкции верхних дыхательных путей. Р(A–a)O2 при этом в норме, за исключением случаев, когда имеются сопутствующие заболевания легких. Увеличение мертвого пространства происходит за счет участков, которые нормально вентилируются, но плохо кровоснабжаются. Этот механизм ответственен за дыхательную недостаточность при таких болезнях легких как ХОЗЛ, бронхиальная астма, муковисцедоз, пневмосклероз (Р(A–a)O2 обычно увеличена). Повышенное образование CO2 происходит, например, при лихорадке, сепсисе, эпилептических припадках и избытке углеводов при парентеральном питании. В клинической практике часто наблюдается смешанная дыхательная недостаточность, причем порой сложно определить ведущий механизм нарушения газообмена. Например, в послеоперационный период оксигенация крови может уменьшаться вследствие множественных ателектазов, развивающихся прежде всего в результате анестезии (снижение дыхательного объема, нарушение кашлевого рефлекса). Играет также роль ограничение подвижности диафрагмы из-за боли или повреждения диафрагмального нерва и обструкция мелких бронхов из-за интерстициального отека. Гиповентиляция - другое следствие снижения подвижности диафрагмы. К смешанной послеоперационной дыхательной недостаточности особенно предрасположены люди с уже имеющимися заболеваниями легких. Терапия дыхательной недостаточности во многом определяется причинами, приведшими к ее развитию, а также тяжестью. Она состоит из множества направлений, ориентированных на улучшение вентиляции легких, газообмена на уровне альвеоло-капиллярной мембраны, легочного кровообращения, микроциркуляции, текучести крови, подавлении инфекции и т.д. Общим элементом в тактике лечения таких больных является быстрое установление диагноза, причинно-следственных отношений и принятие неотложных экстренных мер по устранению гипоксемии или гиперкапнии. Основные лечебные мероприятия в этом направлении предусматривают обеспечение свободной проходимости дыхательных путей, кислородную и лекарственную терапию, ингаляции, применение респираторной поддержки при несостоятельном спонтанном дыхании больного. Важнейшим аспектом интенсивной терапии являются также обеспечение адекватного мониторинга газообмена и других витальных функций. Наиболее широко для обеспечения достаточного газообмена при ОДН используют ингаляцию О2.С этой целью применяют различные устройства, такие как: носовые канюли, негерметичные маски, маски Вентури и др. Недостаток носовых катетеров и обычных лицевых масок в том, что точное значение FiO2 остается неизвестным. Для приблизительной оценки концентрации О2 при использовании носового катетера можно пользоваться следующим правилом: при скорости потока 1 л/мин FiO2 составляет 24%; увеличение скорости на 1 л/мин повышает FiO2 на 4%. Скорость потока не должна превышать 5 л/мин. Маска Вентури обеспечивает точные значения FiO2 (обычно 24, 28, 31, 35, 40 или 50%). Маску Вентури часто используют при гиперкапнии: она позволяет подобрать РaO2 таким образом, чтобы максимально снизить задержку CO2. Маски без возвратного дыхания имеют клапаны, препятствующие смешиванию вдыхаемого и выдыхаемого воздуха. Такие маски позволяют создать FiO2 до 90%. Дыхание под постоянным положительным давлением начинают, если при дыхании через маску без возвратного дыхания РaO2 остается ниже 60 мм рт. ст. Метод можно применять, если больной в сознании, кашлевой рефлекс сохранен, гемодинамика стабильна. Используют плотно прилегающую маску с предохранительным клапаном. Сначала постоянное положительное давление составляет 3-5 см вод. ст. Затем его ступенчато (на 3-5 см вод. ст. за один раз) увеличивают, пока РaO2 не достигнет 60 мм рт. ст. (или SaO2 - 90%), но не более чем до 10-15 см вод. ст. Отказаться от дыхания под постоянным положительным давлением заставляет невозможность устранить гипоксемию, нестабильность гемодинамики, страх замкнутого пространства, который нередко испытывает больной в закрытой маске, и аэрофагия. Решение о начале ИВЛ принимают с учетом обратимости процесса, вызвавшего дыхательную недостаточность, и общего состояния. ИВЛ начинают при выраженном нарушении газообмена, быстром нарастании дыхательной недостаточности, неэффективности вспомогательной вентиляции и усталости дыхательных мышц из-за чрезмерной работы дыхания. Показания для перевода больного на ИВЛ могут быть сформулированы следующим образом: - частота дыхания > 35 мин–1; - максимальное разрежение на вдохе 25 см вод. ст.; - ЖЕЛ < 10-15 мл/кг; - РaO2 < 60 мм рт. ст. при FiO2 > 60%; - РaCO2 > 50 мм рт. ст. при pH < 7,35;. Представленные критерии чаще используются при паренхиматозном повреждении легких. При гиперкапнической ОДН решение об интубации и проведении ИВЛ могут приниматься с учетом уровня сознания, сохранности дыхательного паттерна, длительности основного заболевания и др. 3.3. КровообращениеОсновная функция системы кровообращения – транспорт кислорода в соответствии с метаболическими потребностями организма. Играя существенную роль во всех процессах, обеспечивающих его жизнедеятельность, она обладает как высокой избирательностью по отношению к изменениям внутренней среды, так и адаптационной стабильностью к внешним воздействиям. Система кровообращения выполняет объем работы, во многом превосходящий возможности аналогичных технических устройств. За период жизни сердце производит в среднем около 3 млрд. сокращений. Суммарный объем крови, перемещаемой при этом, составляет около ½ кубического километра, в то время как объем полостных образований сердца измеряется всего лишь миллилитрами. При физической нагрузке значения ударного объема крови (УОК) могут увеличиваться до 200 % и более, а минутного объема кровообращения (МОК) - до 500 %, что свидетельствует о высокой функциональной вариабельности системы кровообращения и ее больших адаптационных возможностях. Одна из задач, решаемая системой кровообращения, заключается в обеспечении множества бассейнов микроциркуляции необходимым количеством крови. Однако функция ее при этом заключается не просто в поддержании определенного объема кровообращения и его рациональном распределении, а в своевременном изменении объемного кровотока в соответствии с постоянно меняющимися потребностями тканей в кислороде. Общая схема распределения объема циркулирующей крови (ОЦК), пульсового давления (ПД) и среднединамического давления (СДД) в основных сосудистых бассейнах представлена на рис.3.15. Из него видно, что гемодинамический процесс весьма сложен и, по крайней мере, не является статичным. В поддержании необходимого уровня гемодинамики ведущая роль отводится транспортно-демпферной (сосудистой) субсистеме кровообращения, насосной функции сердца и объему циркулирующей крови (ОЦК). 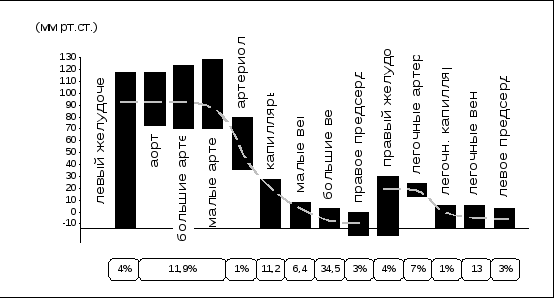 Рис. 3.15. Внутрисосудистое давление и объем крови в различных отделах сосудистого русла. Прерывистая линия — среднее артериальное давление (мм рт. ст.), прямоугольники — пульсовое давление (мм рт. ст.), цифры внизу — объем крови в сосудах (% к общему объему) Интегральным показателем функции кровообращения принято считать показатель минутной производительности сердца, подобно тому, как при оценке функции дыхания наиболее универсальным является уровень оксигенации смешанной венозной крови, оттекающей из малого круга к левому предсердию. Однако ни производительность сердца, ни артериальное давление или частота пульса, когда они берутся изолированно, не могут дать полного представления об адекватности сердечного выброса кислородному обмену, а также о степени функциональной напряженности системы кровообращения. Так, при гиперфункции гемодинамики потребление кислорода растет вместе с минутным объемом в линейной зависимости - взаимосвязь кровообращения с внешним и тканевым дыханием здесь очевидна. В случае снижения производительных параметров кровообращения лимитирующим фактором при подавляющем большинстве патологических состояний оказывается сердечный выброс. Поэтому оценка функции сердечно-сосудистой системы должна учитывать не только параметры, свидетельствующие об уровне ее производительности, но и степень снабжения тканей кислородом и уровень потребления ими последнего. При оценке производительности сердечно-сосудистой системы необходимо учитывать минутный объем кровообращения (МОК), общее потребление кислорода (ПО2) и напряжение (содержание) кислорода в смешанной венозной крови (рО2в). Должные (расчетные) величины сердечной производительности. Величина МОК в значительной мере зависит от антропометрических данных исследуемого, в связи с чем она подвержена большому разбросу. Поэтому для сравнения производительной функции сердца у разных больных применяют сердечный индекс (СИ). СИ отражает МОК, отнесенный к поверхности тела в м2. Единицей размерности СИ является л * мин -1 * м –2, в норме он составляет 3,1 ± 0,7. Современные представления о производительной функции сердца опираются на исследования Н.Н. Савицкого и соавт. (1970, 1974), в которых была продемонстрирована прямая связь между должным основным обменом (ДОО) и должным минутным объемом кровообращения (ДМОК). По данным Н.Н. Савицкого: где: ДМОК – должный минутный объем кровообращения для условий основного обмена (л * мин-1); ДОО – должный основной обмен (ккал/сут); 422 – индекс Савицкого. Расчет ДОО при этом осуществляется раздельно для мужчин и для женщин по формулам, приведенным ниже: где: ДОО – должный основной обмен (ккал/сутки); М – масса тела (кг); Р – рост (см); В – возраст (лет). С учетом того, что условия основного обмена в клинике создать практически невозможно, должный минутный объем кровообращения рассчитывают для условий покоя, применяя для этого индекс Г.П. Звонарева (1974), который составляет 1,35. Формула расчета должного минутного объема кровообращения для условий покоя в этом случае приобретает вид: (Обозначения те же, что и в формуле 3.28). Расчет сердечного индекса осуществляют делением МОК на площадь поверхности тела (ПТ) в м2: где: СИ – сердечный индекс (л * мин-1 * м-2); МОК – минутный объем кровообращения (л * мин-1); ПТ – поверхность тела (м2). В свою очередь расчет ПТ осуществляется по формуле Дюбуа и Дюбуа (1916). где:ПТ –поверхность тела (м2); М – масса тела (кг); Р – рост (см). Уместно напомнить, что уравнение (6) основано на прямом изменении тела только 9 испытуемых. Но, несмотря на это, оно нашло широкое применение и до настоящего времени считается вполне надежным. Энергетика миокарда. Структурно-функциональная специализация сердца призвана обеспечивать его главное предназначение — насосную деятельность. Хотя в реализации кровообращения принимают участие сосудистые и другие механизмы, роль сердечного насоса является определяющей. Сократительная способность миокарда является одним из важнейших компонентов, обеспечивающих нагнетательную функцию и участвующих в регуляции сердечного выброса. Главным условием здесь считается полное соответствие сердечного выброса и венозного возврата крови при стационарном режиме работы сердца и быстрое их выравнивание при меняющихся режимах. Известно, что энергетика сердца значительно отличается от энергетики скелетных мышц преобладанием аэробных процессов, в которых синтезируются макроэргические фосфаты. Важнейшей особенностью сердечного энергообмена является линейная зависимость между механической работой сердца и скоростью потребления миокардом кислорода. В физиологических условиях основная часть энергии сердца получается в результате гидролиза жирных кислот, протекающего только в аэробных условиях (цикл Кребса). Синтезирующиеся при этом ацетилкоэнзим А и пируват окисляются поэтапно до CO2 и ионов Н+. Освобождающиеся атомы водорода переносятся на цепь транспорта электронов цитохромной системой (дыхательная цепь), где используются для восстановления молекулярного кислорода до воды. Образующаяся при переносе электронов на дыхательную цепь энергия идет на ресинтез АТФ. Чем больше длина саркомера перед сокращением, тем больше потенциально возможное возрастание зоны актинмиозинового перекрытия и, следовательно, — больше генерируемый прирост силы. Второй эффект заключается в приросте силы при неизменяемой длине саркомера в ответ на возрастающее сопротивление сокращению. Это приводит к замедлению сокращения, т. е. к зависимости сила - скорость. В этом случае процесс скольжения оказывается замедленным, что увеличивает время контакта головок актинмиозиновых мостиков с активными локусами саркомеров, чем и объясняется прирост силы. Кроме того, существует ряд факторов, оказывающих влияние на силу сокращений через усиленное поступление в саркомеры внеклеточного кальция или увеличение частоты сердечных сокращений (хроноинотропный эффект), а также через катехоламиновые (медиаторные) воздействия. О          сновные механизмы регуляции силы сердечных сокращений достаточно хорошо объясняет теория актинмиозинового скольжения. Первый из таких механизмов реализуется через отношение длина - сила (закон Франка—Старлинга, рис. 3.16.). сновные механизмы регуляции силы сердечных сокращений достаточно хорошо объясняет теория актинмиозинового скольжения. Первый из таких механизмов реализуется через отношение длина - сила (закон Франка—Старлинга, рис. 3.16.).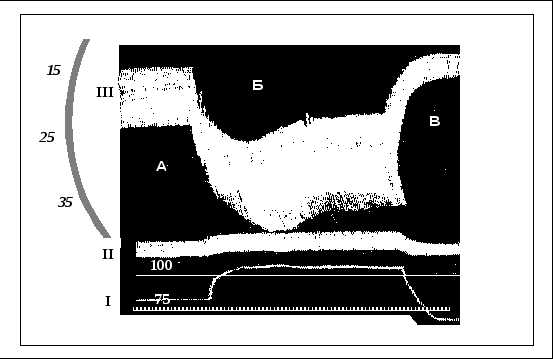 Рис. 3.16. Воспроизведение одной из записей, полученных Старлингом на сердечно-легочном препарате. Запись на закопченной ленте кимографа показывает влияние увеличения венозного давления наполнения (I; без калибровки) на диастолический и систолический объемы сердца. II - артериальное давление в мм рт. ст.; калибровочные отметки (100 и 75 мм рт. ст.) нанесены ниже; III - непрерывная запись объема обоих желудочков, полученная при помощи кардиометра (жесткой латунной камеры, в которую помещены желудочки; во время диастолы воздух из этой камеры вытесняется в измерительный цилиндр); шкала прокалибрована в мл. Отметка времени 1 с. (А). Исходное состояние. Венозное давление 95 мм вод. ст. Производительность желудочков 520 мл-мин-1 (Б). Быстрое повышение венозного давления до 145 мм вод. ст. Обратите внимание на соответствующее увеличение как диастолического объема желудочков, так и их ударного объема. Производительность желудочков 840 мл-мин-1. (В). Быстрое снижение венозного давления до 55 мм вод. ст. Как диастолический, так и ударный объем желудочков падают ниже исходного уровня. Производительность желудочков 200 мл * мин -1. (Patterson, Piper, Starling. The regulation of the heart-beat // J. Physio L., 1914, 48, 465) Одним из критериев эффективности насосной функции является коэффициент полезной деятельности (КПД) сердца. Под ним понимают удельную энергетическую стоимость полезной (внешней) работы. Общие энергетические затраты расходуются сердцем на насосную работу, электромеханическое сопряжение, теплообразование, активный транспорт веществ через мембраны, биосинтез, структурное обновление клеток и т.п. Весь расход энергии сердцем выражается через энергетический эквивалент утилизированного сердцем кислорода или: 2.057 * П02М (3.34), где: 2.057 Ккал/мл - энергетический эквивалент 1,0 мл кислорода, ПО2М - потребление миокардом кислорода за один сердечный цикл. КПД сердца при этом представляется как отношение внешней работы к калорической ценности утилизированного кислорода. Вместе с тем, определить ПО2М даже в условиях клиники сложно. Возможно, поэтому данные о нормальных значениях КПД сердца противоречивы и колеблются от 10 до 40 %. Амплитудно-временнáя организация сердечного цикла. В контексте формирования производительной функции сердечно-сосудистой системы чрезвычайно велико значение амплитудно-временнόй организации сердечного цикла. Наиболее общее разделение цикла сердечной деятельности на систолу и диастолу соответствует начальным представлениям о динамике сердца. Еще Гарвей (Harvey,1628) представлял его работу как цикл, состоящий из трех фаз: систолы, диастолы и паузы. Этой точки зрения придерживались, в частности, и основоположники отечественной физиологии И.П. Павлов (1883), Б.Ф. Вериго (1905), И.М. Сеченов (1923). Дальнейшая дифференциация фазовой структуры сердечного цикла предполагает разделение систолы на период напряжения желудочков (PEP - pre-ejectionperiod) и изгнания из них крови (LVEP - leftventricularejectionperiod), а диастола - на периоды расслабления мускулатуры желудочков (IVRP - isovolumicrelaxationperiod) и наполнения их кровью (FP - filling period). Уиггерс (Wiggers C.J., 1929) разделил сердечный цикл на фазу изометрического сокращения, фазы максимального и редуцированного изгнания, протодиастолу, фазы изометрического расслабления, быстрого и медленного наполнения и систолу предсердий. В настоящее время эта схема дополнена фазой асинхронного сокращения, протосфигматическим и интерсистолическим интервалами. Сердечный цикл, таким образом, может быть разбит на 11 периодов (рис.3.17). Представляют интерес не только абсолютные, но и относительные величины указанных периодов по отношению к длительности сердечного цикла, поскольку наряду с частотной зависимостью, при разных уровнях функционирования гемодинамики происходит изменение конфигурации сердечного цикла. Очевидно, что такое изменение имеет своей целью рациональное перераспределение внутрисердечных объемов крови для большей согласованности между контрактильными возможностями миокарда и уровнем потребления кислорода тканями. Так, по данным импедансометрии, в ответ на стандартную физическую нагрузку (10 присаживаний в постели из положения лежа в положение сидя) помимо прироста разовой производительности сердца и частоты сердечных сокращений (ЧСС), происходит закономерное укорочение периодов сердечного цикла за счет учащения сердцебиений (рис.3.18). Обращает на себя внимание неравномерность такого укорочения. Как показано на рисунке, наибольшей стабильностью отличается период изгнания (LVEP), так как именно в этот период происходит главное событие сердечного цикла - сокращение миокарда. Наименее «устойчивыми» периодами, как правило, являются период расслабления (IVRP) и период наполнения (FP).  Рис.3.17. Временнáя организация сердечного цикла (периоды и интервалы сердечного цикла представлены в миллисекундах для ЧСС = 60 в мин) Р 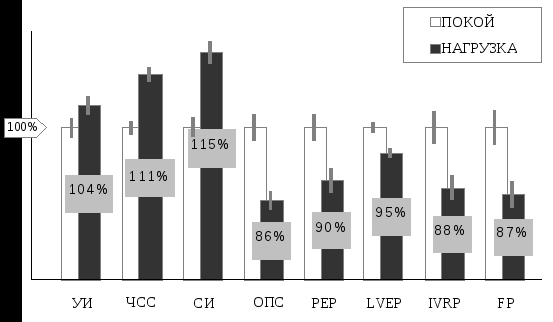 ис.3.18. Изменения показателей гемодинамики и временных интервалов сердечного цикла в ответ на функциональную нагрузку (10 присаживаний в постели без помощи рук) в процентах к исходному состоянию (M±m, n=106) Коронарное кровообращение. Уровень О2 в миокарде, как и в других тканях, зависит от потребности их снабжения и определяется коронарным кровотоком. При этом потребность мышцы сердца в О2 определяется внутрижелудочковым давлением, ЧСС и контрактильностью. Рост систолического давления вызывает рост потребления О2 в соотношении 1:1. Учащение сердечного ритма вдвое увеличивает потребление О2 на 50%. Усиление контрактильности вдвое также увеличивает потребление О2 на 50%. Таким образом, использование сердечных резервов (постнагрузка, ЧСС или инотропизм) связано с увеличением потребления О2 миокардом (В.А. Константинов, 1981). Снабжение О2 любого органа может быть увеличено за счет объемного кровотока, повышения содержания О2 в артериальной крови или усиления его экстракции тканями. Для сердца практически единственным источником дополнительного поступления О2 является увеличение коронарного кровотока, т.к. экстракция его здесь велика даже в покое. Одним из наиболее мощных регуляторов притока крови к сердцу является гипоксия. При ней дилятация венечных сосудов максимальна, а сопротивление в них наименьшее. Однако если гипоксия сопровождается тахисистолией, резервов для увеличения кровотока практически нет. Как результат этого – увеличение тахисистолии сопровождается снижением производительной функции сердца. Кривые давления и кровотока в аорте и кровотока в левой коронарной артерии приведены на рис. 3.19. Обращает на себя внимание то, что во время диастолы через парную артерию протекает значительно больший объем крови, чем во время систолы (Gregg, Fisher, 1962). 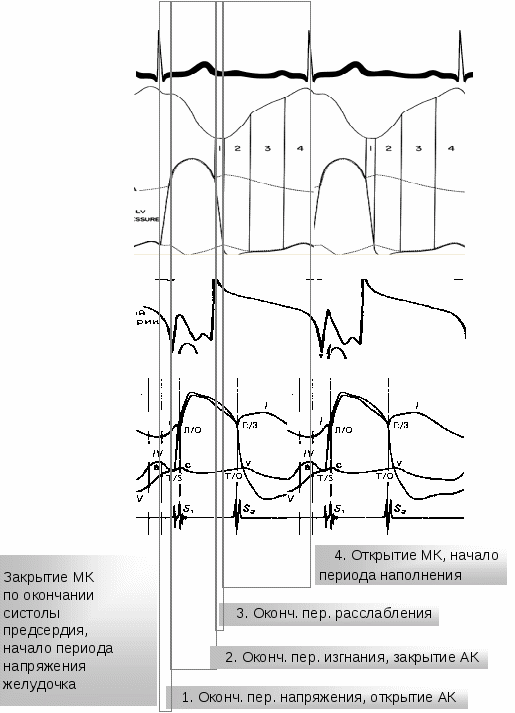 Рис.3.19. Временная организация сердечного цикла. Рисунок составлен на основании данных различных авторов для ЧСС 60 уд. в 1 мин.; вертикальными линиями выделены 11 периодов и интервалов сердечного цикла. Для простоты чтения масштаб по вертикали и амплитудные параметры проигнорированы. Ударный объем крови и факторы, его определяющие. Известно, что изменение числа сердечных сокращений за определенный промежуток времени само по себе не приводит к значимым изменениям производительных параметров работы сердца. Повышение частоты сердечных сокращений вдвое способно привести к повышению производительности сердца всего на несколько процентов, а при ее дальнейшем росте производительность сердца должна снижаться вследствие уменьшения длительности диастолы и, соответственно, степени диастолического наполнения желудочков. С той же долей уверенности можно говорить об отсутствии значимого влияния на производительную функцию сердца артериального сопротивления, формирующегося в артериальной компрессионной камере по мере выхода крови из желудочков. Только очень высокое (240 и более мм рт.ст.) артериальное давление может существенно повлиять на сердечный выброс. Само по себе увеличение силы сокращения желудочков также не в состоянии обеспечить устойчивое увеличение МОК. Рост и частоты, и силы сокращений сердца, снижение постнагрузки – это лишь условия возможности повышения его производительности, для реализации которого необходимо также увеличение притока крови к сердцу. При мышечной работе последнее достигается сочетанием снижения сопротивления сосудов работающих мышц, ограничения роста объема вен (за счет увеличения их жесткости), работы мышечного насоса, повышения центрального венозного давления (ЦВД) и изменения временных характеристик работы сердца. При этом необходимо помнить, что по достижении определенного уровня (обычно 12-14 см вод. ст.) ЦВД перестает влиять на прирост сердечной производительности. В течение ряда лет данный механизм снижения прироста производительности считался основным в развитии сердечной недостаточности, которую приписывали растяжению мышечных волокон сердца сверх каких-то функциональных пределов. В настоящее время данная концепция пересмотрена. Снижение прироста производительности обусловлено нарастанием недостаточности атрио-вентрикулярного клапана - по мере расширения желудочка клапанное отверстие оказывается настолько увеличенным, что часть изгоняемой из желудочка крови возвращается через него в предсердие. Резервы сердечно-сосудистой системы и основные механизмы компенсации. Тахисистолия - один из начальных компенсаторных факторов, быстрых и эффективных. Однако при длительном действии и прогрессировании экономически невыгоден, ухудшает коронарное кровообращение и лимитирует МОК. Увеличение УОК. Реализуется через увеличение венозного тонуса (что приводит к увеличению давления наполнения желудочков и приросту производительности); через венозное увеличение растяжимости сердца; через падение сосудистого сопротивления в артериальной компрессионной камере и, наконец, через увеличение миокардиальной контрактильности. Последнее может быть первичным или реализоваться через медиаторные и гуморальные факторы. Дилятация сердца. В сущности, данный механизм компенсации осуществляется в соответствии с законом Франка-Старлинга. При этом необходимо учитывать, что он повышает количество выполняемой работы и требует увеличения затрачиваемой энергии. Здесь уместно вспомнить закон Лапласа, согласно которому (применительно к желудочку сердца): P = T/R (3.35), где: P – внутрижелудочковое давление, T – напряжение стенки желудочка, R - радиус желудочка. В соответствии с этим законом при дилатации сердца с увеличением радиуса его желудочка для поддержания исходного давления потребуется развивать большее напряжение. Это, в свою очередь, повлечет за собой повышение расхода О2 и, таким образом, эффективность работы сердца снизится. Так как площадь поперечного сечения желудочка сердца равна Гипертрофия миокарда - суммарное увеличение массы сердца за счет увеличения массы отдельных мышечных волокон. По сравнению с дилятацией – более совершенный, но и более длительный тип компенсации. До определенных границ гипертрофия обратима, а в далеко зашедших случаях она приводит к срыву компенсации, так как доказано, что при увеличении толщины миофибрилл в 2 раза диффузия О2 обратно пропорциональна квадрату расстояния, которое О2 должен преодолеть в процессе диффузии. При этом необходимо учитывать, что количество капилляров в гипертрофированном миокарде остается неизменным. Перераспределение кровотока. Происходит при выраженном падении МОК. В этой ситуации нейрорегуляторные механизмы обеспечивают необходимый уровень кровообращения в первую очередь для головного мозга, сердца, щитовидной железы и других жизненно важных органов. Клеточные факторы обеспечивают компенсацию за счет изменения метаболизма, включения анаэробного обмена (в норме встречающегося только в поперечнополосатых мышцах), повышения утилизации О2, увеличения количества циркулирующих эритроцитов за счет мобилизации эритропоэза и т.д. Вместе с тем, необходимо учесть, что степень увеличения минутного объема не беспредельна. Вопросы регуляции нормальной деятельности сердца и проблемы компенсации ее нарушений всегда были в центре внимания физиологов и клиницистов, но до конца они не решены. Известно, что минутный объем слагается из отдельных регионарных кровотоков, величины которых управляются местными и центральными механизмами. Не отрицая роли экстракардиальных механизмов в регуляции сердечной производительности, и в частности, центральной нервной системы, следует все же подчеркнуть, что сердце во многом является саморегулирующейся системой. Подтверждением этому служит опыт пересадки донорского сердца, накопленный хирургами в последние годы и демонстрирующий сохранение адекватности кровообращения, несмотря на денервацию пересаженного органа. МО увеличивается в первую очередь за счет повышения ЧСС. Этот механизм обусловлен симпатической иннервацией и представляет собой наиболее оперативную адаптацию сердечного выброса, хотя и менее экономичную по сравнению с увеличением УОК. Последний также возрастает, но в меньшей степени. При увеличении ЧСС до 160 и более ударов в 1 мин происходит снижение сердечного выброса и МОК. С увеличением ЧСС почти в линейной зависимости растет общее ПО2, что при декомпенсации кровообращения или при выраженной гипертрофии желудочков крайне невыгодно и отрицательно сказывается на производительности сердца. Урежение ЧСС до 40 ударов в 1 мин, равно как и стойкая аритмия, также сопровождаются уменьшением МОК. Оптимум изменений ЧСС при регуляции сердечного выброса находится в широких пределах — от 40 до 160 уд./мин. В условиях патологии рамки данного адаптационного механизма резко сужаются и даже незначительные отклонения ЧСС в ту или иную сторону - от 60 до100 ударов могут сопровождаться снижением МОК. Важно отметить, что у больных искусственное увеличение ЧСС не всегда приводит к повышению МОК. В свете получающей все большее распространение теории об активном механизме диастолы приобретает особый интерес факт, согласно которому диастолическая податливость сердца (комплайнс), или его жесткость, являются функцией ЧСС (Grossman et al., 1973). Таким образом, ритмодиастолическая зависимость выступает как важнейший механизм регуляции сердечного выброса. По-видимому, физиологическое значение ритма не ограничивается только управлением МО, а простирается на интеграцию всех сторон деятельности кардиореспираторной системы, обеспечивая единство функции составляющих ее структур. Управление величиной УОК осуществляется миогенной ауторегуляцией и экстракардиальным контролем. Факторами механизма ауторегуляции являются преднагрузка и постнагрузка. Таким образом, подводя итог сказанному, величина ударного объема крови (УОК) определяется следующими основными факторами: - длиной мышечных волокон миокарда в конце диастолы (механизм Франка-Старлинга или преднагрузка); - контрактильными возможностями миокарда (инотропизм); - величиной сопротивления, преодолеваемого мышечными волокнами миокарда при его сокращении во время систолы (постнагрузка); - временными и амплитудными характеристиками сердечного цикла. Преднагрузка. В опытах на изолированной мышечной клетке, на отдельной мышце и на сердечно-легочном препарате было доказано, что сила сокращений саркомеров (миофибрилл) является функцией их первоначальной длины - иными словами, УОК прямо пропорционален диастолическому наполнению желудочков (Frank, 1895; Starling, 1918). Эту зависимость обозначают как длина - сила, а детерминирующий фактор - длину саркомера - понимают как функцию давления наполнения, или закон Франка—Старлинга. Механизм Франка—Старлинга служит в качестве миогенного гетерометрического регулятора сердечных сокращений, а описание его выражается такими переменными гемодинамики, как конечно-диастолический объем (КДО), конечно-диастолическое давление (КДД) и среднее давление в предсердии. При патологии управление УВ сердца через механизм Франка—Старлинга — один из важнейших практических методов поддержания адекватного сердечного выброса. Механизм влияния преднагрузки тесно связан с гуморальными и нейрогенными механизмами ауторегуляции сердца. Построение функциональных кривых сердца, отражающих зависимость между УОК и КДО для оценки насосной функции, с успехом используют в клинической практике. Постнагрузка. Постнагрузка представляет собой фактор другого механизма миогенной ауторегуляции УОК — гомеометрической регуляции, для реализации которой изменения исходной длины мышечного волокна или объема сердца не обязательны. Сущность этой регуляции, описываемой в виде зависимости давление - сила, проявляется в обратной связи УОК с постнагрузкой. Другими словами, при постоянстве диастолического объема увеличение постнагрузки приводит к уменьшению сердечного выброса. Примечательно, что дать определение самой постнагрузке непросто. Некоторые авторы отождествляют постнагрузку со средним систолическим давлением в аорте (в легочной артерии для правого желудочка). На практике постнагрузку иногда оценивают по общему периферическому сопротивлению (ОПС), что объясняется неразработанностью теоретических основ этого вопроса. Однако ставить знак равенства между понятиями давление и сопротивление неправомерно. ОПС - характеристика стационарного движения жидкости, в то время как сердечно-сосудистая система функционирует в пульсирующем режиме. В действительности еще К.Уиггерс (1929) не напрасно указывал на недостаточную информативность данного показателя в отрыве от компонентов, его формирующих. Однонаправленные изменения среднединамического давления и МОК, даже если они очень выражены, могут взаимно нивелировать показатель ОПС вплоть до нормальных цифр, тем самым нивелируя информационную ценность последнего. Развитием представлений о постнагрузке является предложение характеризовать ее с помощью импеданса — характеристики, описывающей механику жидкости при распространении в ней пульсовых волн давления и скорости (O'Rurk, Taylor, 1967). Однако исследования показали, что для более полноценного суждения о взаимодействии желудочка сердца с сосудистым руслом необходимы физиологические характеристики локальных изменений объема сосуда при прохождении пульсовых волн скорости и давления. Одной из таких характеристик является комплайнс или обратная ей величина - жесткость (Sunagawa et al., 1982). По-видимому, на современном этапе развития физиологии кровообращения дать приемлемое определение постнагрузке, удовлетворяющее как теоретиков, так и практиков, затруднительно. Поэтому для практики пока целесообразно относиться к термину «постнагрузка» как рабочему, подразумевающему совокупную динамическую характеристику взаимодействия желудочка сердца и фрагмента артериального (аортального) русла, принимающего порцию крови во время изгнания. Употребляемый в этом смысле термин «постнагрузка» допускает использование таких оценочных характеристик, как среднее артериальное давление, импеданс, комплайнс и многие другие, оставляя возможность уточнения содержания термина и его объема. При увеличении сосудистого сопротивления повышается потребность миокарда в кислороде, что ухудшает контрактильность и вызывает депрессию МОК или, другими словами, снижение производительности сердца. Внешнее управление компонентами постнагрузки находит широкое применение в клинической практике. Суть инотропии сводится к увеличению силы сердечных сокращений. Хотя данный эффект известен давно (его проявления описал еще в 80-е годы прошлого века И. П. Павлов), механизмы, объясняющие его, до конца не изучены. |
