Сахарный диабет (СД)
 Скачать 0.94 Mb. Скачать 0.94 Mb.
|
|
Сахарный диабет (СД) – это группа метаболических (обменных) заболеваний, характеризующихся хронической гипергликемией, которая является результатом нарушения секреции инсулина, действия инсулина или обоих этих факторов. Хроническая гипергликемия при СД сопровождается повреждением, дисфункцией и недостаточностью различных органов, особенно глаз, почек, нервов, сердца и кровеносных сосудов. Клинические аспекты физиологии углеводного обмена Инсулин синтезируется и секретируется В-клетками островков Лангерганса поджелудочной железы (ПЖЖ). Кроме того, островки Лангерганса секретируют глюкагон (а-клетки), соматостатин (дельта-клетки) и панкреатический полипептид (РР-клетки). Гормоны островковых клеток взаимодействуют между собой: глюкагон в норме стимулирует секрецию инсулина, а соматостатин подавляет секрецию инсулина и глюкагона. Молекула инсулина состоит из двух полипептидных цепей (А-цепь— 21 аминокислота; В-цепь —30 аминокислот). Синтез инсулина начинается с образования препроинсулина, который расщепляется протеазой с образованием проинсулина. В секреторных гранулах аппарата Гольджи проинсулин расщепляется на инсулин и Спептид, которые высвобождаются в кровь в процессе экзоцитоза. Основным стимулятором секреции инсулина является глюкоза. Высвобождение инсулина в ответ на повышение уровня глюкозы в крови происходит двухфазно. Первая, или острая, фаза длится несколько минут, и она связана с высвобождением накопившегося в В-клетке инсулина в период между приемами пищи. Вторая фаза продолжается до тех пор, пока уровень гликемии не достигнет нормального тощакового (3,3—5,5 ммоль/л). Сходным образом на В- клетку воздействую препараты сульфонилмочевины. По портальной системе инсулин достигает печени — своего главного органа-мишени. Печеночные рецепторы связывают половину секретированного гормона. Другая половина, попадая в системный кровоток, достигает мышц и жировой ткани. Большая часть инсулина (80 %) подвергается протеолитическому распаду в печени, остальная — в почках, и лишь незначительное количество метаболизируется непосредственно мышечными и жировыми клетками. В норме ПЖЖ секретирует 35-50Ед инсулина в сутки, что составляет 0,6—1,2 Ед на 1 кг массы тела. Эта секреция подразделяется на пищевую и базальную. Пищевая секреция инсулина соответствует постпрандиальному подъему уровня глюкозы, т.е. за счет нее обеспечивается нейтрализация гипергликемизирующего действия пищи. Количество пищевого инсулина примерно соответствует количеству принятых углеводов — около 1—2,5 Ед на 10-12 г углеводов (1 хлебная единица — ХЕ). Базальная секреция инсулина обеспечивает оптимальный уровень гликемии и анаболизма в интервалах между едой и во время сна. Базальный инсулин секретируется со скоростью примерно 1 Ед/ч, при длительной физической нагрузке или длительном голодании она существенно уменьшается. На пищевой инсулин приходится не менее 50-70 % суточной продукции инсулина Основные физиологические эффекты инсулина  Глюконеогене́з — метаболический путь, приводящий к образованию глюкозы из неуглеводных соединений. Наряду с гликогенолизом, этот путь поддерживает в крови уровень глюкозы, необходимый для работы многих тканей и органов, в первую очередь, нервной ткани и эритроцитов. Исходными соединениями в глюконеогенезе являются аминокислоты мышечной ткани. При длительном голодании это приводит к массивному распаду мышечного белка. Гликогено́лиз — биохимический процесс расщепления гликогена до глюкозы, осуществляется главным образом в печени и мышцах Липо́лиз — метаболический процесс расщепления жиров на составляющие их жирные кислоты под действием липазы Кетогенез (Ketogenesis) — образование кетоновых тел. Основными физиологическими эффектами инсулина являются стимуляция переноса глюкозы через мембраны клеток инсулинзависимых тканей. Основными органами-мишенями инсулина являются печень, жировая ткань и мышцы. К инсулиннезависимым тканям, поступление глюкозы в которые не зависит от эффектов инсулина, в первую очередь относятся центральная и периферическая нервная система, эндотелий сосудов, клетки крови и др. Инсулин стимулирует синтез гликогена в печени и мышцах, синтез жиров в печени и жировой ткани, синтез белков в печени, мышцах и других органах. Все эти изменения направлены на утилизацию глюкозы, что приводит к снижению ее уровня в крови. Физиологическим антагонистом инсулина является глюкагон, который стимулирует мобилизацию гликогена и жиров из депо; в норме уровень глюкагона меняется реципрокно продукции инсулина. Биологические эффекты инсулина опосредованы его рецепторами, которые расположены на клетках-мишенях. Рецептор инсулина представляет собой гликопротеин, состоящий из четырех субъединиц. При высоком уровне инсулина в крови число его рецепторов по принципу понижающей регуляции снижается, что сопровождается снижением чувствительности клетки к инсулину. После связывания инсулина с клеточным рецептором образовавшийся комплекс поступает внутрь клетки. Далее внутри мышечной и жировой клетки инсулин вызывает мобилизацию внутриклеточных везикул, которые содержат транспортер глюкозы GLUT-4. В результате этого везикулы перемешаются к клеточной поверхности, где GLUT-4 выполняет функцию входного отверстия для глюкозы. Аналогичное действие на GLUT-4 оказывает физическая нагрузка. Диагностика сахарного диабета 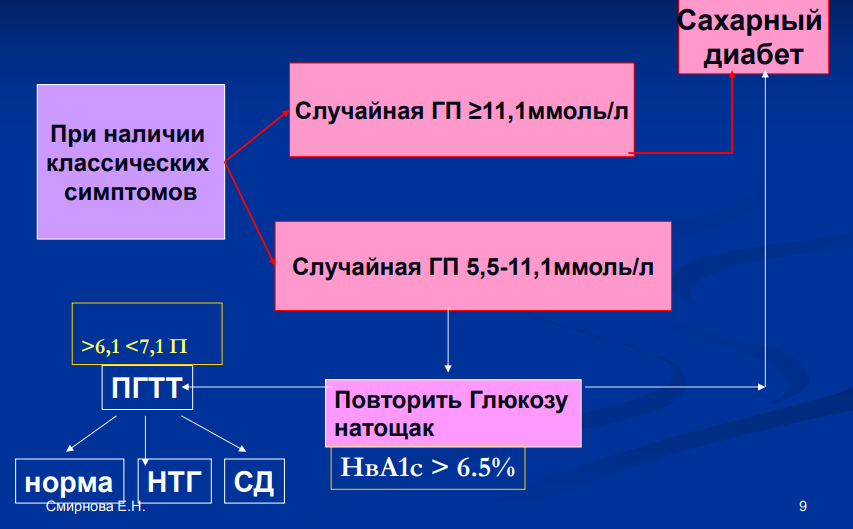 Лабораторная диагностика СД базируется на определении уровня глюкозы крови, при этом критерии диагностики едины для всех типов сахарного диабета, кроме гестационного. Натощак – означает уровень глюкозы крови утром после предварительного голодания в течение не менее 8 часов и не более 14 часов. Случайное – означает уровень глюкозы крови в любое время суток вне зависимости от времени приема пищи. ПГТТ – пероральный глюкозотолерантный тест. Проводится в случае сомнительных значений гликемии для уточнения диагноза. Правила проведения ПГТТ: ПГТТ следует проводить утром на фоне не менее чем 3-дневного неограниченного питания (более 150 г углеводов в сутки) и обычной физической активности. Тесту должно предшествовать ночное голодание в течение 8–14 часов (можно пить воду). Последний вечерний прием пищи должен содержать 30–50 г углеводов. После забора крови натощак испытуемый должен не более чем за 5 мин выпить 75 г безводной глюкозы или 82,5 г моногидрата глюкозы, растворенных в 250–300 мл воды. Для детей нагрузка составляет 1,75 г безводной глюкозы (или 1,925 г моногидрата глюкозы) на кг массы тела, но не более 75 г (82,5 г). В процессе теста не разрешается курение. Через 2 часа осуществляется повторный забор крови 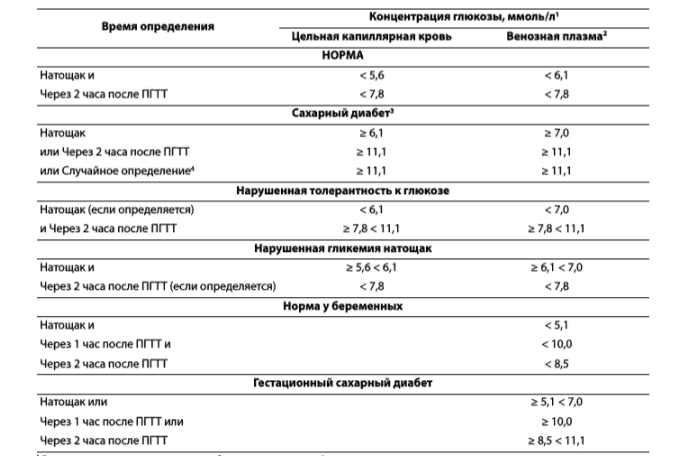 При любом типе СД, а также при значительной нагрузке глюкозой может развиваться глюкозурия, которая является следствием превышения порога реабсорбции глюкозы из первичной мочи. Порог реабсорбции глюкозы значительно индивидуально варьирует («9—10 ммоль/л). Как отдельно взятый показатель глюкозурия для постановки диагноза СД использоваться не должна. В норме, за исключением случаев значительной пищевой нагрузки рафинированными углеводами, глюкозурия не встречается. Продукция кетоновых тел (ацетон, ацетоацетат, р-гидроксибу-тират) значительно интенсифицируется при абсолютном дефиците инсулина. При декомпенсации СД-1 может определяться выраженная кетонурия (исследуется при помощи тест-полосок, которые опускаются в мочу). Легкая (следовая) кетонурия может определяться у здоровых людей при голодании и безуглеводной диете. Дифференциальной диагностики типов СД, а также для выявления формирования дефицита инсулина у пациентов с СД-2, является уровень С-пептида. По уровню Спептида в крови можно косвенно судить об инсулинсекретирующей способности в-клеток ПЖЖ. Основным критерием качества компенсации углеводного обмена при СД является уровень гликированного (гликозилированного) гемоглобина (HbAlc). Последний представляет собой гемоглобин, нековалентно связанный с глюкозой. В эритроциты глюкоза поступает независимо от инсулина, и гликозилирование гемоглобина является необратимым процессом, а его степень прямо пропорциональна концентрации глюкозы, с которой он контактировал на протяжении 120 дней своего существования. Небольшая часть гемоглобина гликозилируется и в норме; при СД она может быть значительно повышена. Уровень HbAlc, в отличие от уровня глюкозы, который постоянно меняется, интегрально отражает гликемию на протяжении последних 3—4 месяцев. Именно с таким интервалом и рекомендуется определение уровня HbAlc с целью оценки компенсации СД. Классификация СД (ВОЗ, 1999, с дополнениями) 1. СД 1 типа • Иммуноопосредованный Деструкция β-клеток поджелудочной железы, обычно приводящая к абсолютной • Идиопатический инсулиновой недостаточности с преимущественной инсулинорезистентностью и относительной инсулиновой 2. СД 2 типа недостаточностью или с преимущественным нарушением секреции инсулина с инсулинорезистентность или без нее 3. Другие специфические типы СД Генетические дефекты действия инсулина (MODY) Генетические дефекты функции β-клеток (Инсулинорезистентность типа А, Лепречаунизм) Заболевания экзокринной части поджелудочной железы (анкреатит, панкреонекроз, травма, опухоли, операции, гемохроматоз, муковисцедоз) Эндокринопатии (акромегалия, гипертиреоз, феохромацитома, альдостерома, синдром Иценко-Кушинга, глюкагонома) СД, индуцированный лекарственными препаратами или химическими веществами Никотиновая кислота, Глюкокортикоиды, Тиреоидные гормоны, α-адреномиметики, β-адреномиметики, β-адреноблокаторы, тиазиды) Инфекции (цитомегаловирус, врожденная краснуха) Необычные формы иммунологически опосредованного СД Другие генетические синдромы, иногда сочетающиеся с СД 4. Гестационный СД Возникает во время беременности Характеристика сахарного диабета 1 типа СД-1 — органоспецифическое аутоиммунное заболевание, приводящее к деструкции инсулинпродуцирующих в-клеток островков ПЖЖ, проявляющееся абсолютным дефицитом инсулина. В ряде случаев у пациентов с явным СД-1 отсутствуют маркеры аутоиммунного поражения Р-клеток (идиопатический СД-1). Этиология. СД-1 является заболеванием с наследственной предрасположенностью, но ее вклад в развитие заболевания невелик (определяет его развитие примерно на Уз) Конкордантность у однояйцевых близнецов по СД-1 составляет всего 36 %. Вероятность развития СД-1 у ребенка при больной матери составляет 1—2 %, отце — 3-6 %, брате или сестре —6 %. Одни или несколько гуморальных маркеров аутоиммунного поражения рклеток, к которым относятся антитела к островкам П Ж Ж ,антитела к глутаматдекарбоксилазе (GAD) и антитела к тирозин-фосфатазе (IA-2 и IA-2P), обнаруживаются у 85-90 % пациентов Патогенез от появления первых клинических симптомов до развития кетоацидоза (вплоть до кетоацидотической комы) может пройти всего несколько недель. 1 стадия – генетическая предрасположенность, которая реализуется у 36% близнецов и у 6 % сибсов 2 стадия - генетический пусковой момент, который вызывает развитие 3 стадии (стресс, инф.б., сомат. Патология, вирусы Коксаки, краснухи, цитомегаловирус, химические вещества, раннее употребление коровьего молока до 3 мес, т.к. казеин коровьего молока инициирует иммунные процессы). 3 стадия –активных иммунологических процессов (наличие 3-х или 4-х типов антител к антигенам островка ПЖ, а также АТ к клеткам других эндокринных органов и тканей (АТ к GAT, к инсулину), но уровень сахара в крови еще в норме. (ниже на фотке) 4 стадия – начальное нарушение угл.обмена, преддиабет при выраженных иммунных нарушениях отмечается снижение секреции инсулина в ответ на введение глюкозы, при этом уровень глюкозы остается нормальным 5 стадия – клиническая манифестация , которая развивается после гибели 80 - 90% бета - клеток. Сохраняется остаточная секреция инсулина МЕДОВЫЙ МЕСЯЦ 6 стадия – полная деструкция бета – клеток   Клинические проявления В основе патогенеза СД-1 лежит абсолютный дефицит инсулина, что и формирует клинику. на фоне избыточного содержания глюкозы в крови возникает тканевой энергодефицит – «голод среди изобилия». Это в свою очередь вызывает активацию липолиза и глюконеогенеза из аминокислот, гликогена. Невозможность поступления глюкозы в инсулинзависимые ткани (жировая и мышечная) приводит к энергетической недостаточности в результате чего интенсифицируется липолиз и протеолиз , с которыми связана потеря массы тела. В крови здорового человека содержание гликозилированного гемоглобина НвА1с не превышает 4 – 5%, то у больного СД его уровень более 6,5% не только уменьшается содержание гемоглобина из-за нарушения механизмов его образования, но и изменяются его функциональные свойства, что имеет существенное значение в развитии тканевой гипоксии, что усугубляет слабость Усиление глюконеогенеза приводит к катаболическим процессам и развитию недостаточности IG = снижение имммунитета Появление инфекционных грибковых процессов на коже, ногтях и т.д Увеличение гипергликемия >10.0 ммоль/л нарушается реабсорбция глюкозы – появляется глюкозурия и дегидратация = полиурия, жажда, зуд в промежности, похудание Продолжающаяся полиурия ведет к системной дегидратации – снижение АД . Увеличение вязкости крови, нарушение микроциркуляции, ДВС Нарушение деятельности ЦНС Повышение уровня гликемии вызывает гиперосмолярность, что сопровождается осмотическим диурезом и выраженным обезвоживанием. В условиях дефицита инсулина и энергетической недостаточности растормаживается продукция контринсулярных гормонов (глюкагон, кортизол, гормон роста), которая, несмотря на нарастающую гликемию, обусловливает стимуляцию глюконеогенеза. Усиление липолиза в жировой ткани приводит к значительному увеличению концентрации свободных жирных кислот. При дефиците инсулина липосинтетическая способность печени оказывается подавленной, и свободные жирные кислоты начинают включаться в кетогенез. Активации кетогенеза и блокирования их расщепления (из-за нарушения цикла Кребса), Накопление в крови кетоновых тел вызывает ряд неблагоприятных последствий: - истощение щелочных резервов крови, снижение рН и развивается метаболический ацидоз; приводит к развитию диабетического кетоза, а в дальнейшем — кетоацидоза. При прогрессирующем нарастании обезвоживания и ацидоза развивается коматозное состояние, которое при отсутствии инсулинотерапии и регидратации неизбежно заканчивается смертью появление ацетона в моче и выдыхаемом воздухе Основное значение инсулина- начать процесс гликолиза (в цикле Кребса) с преобразованием аденозиндифосфата (АДФ) в АТФ т.е. Макроэргов, необходимых для энергетических и анаболических процессов. Т.о. дефицит инсулина приводит к выраженному – энергетическому дефициту – и клинически сильная, немотивированная слабость В типичных случаях, особенно у детей и молодых людей, СД-1 дебютирует яркой клинической картиной, которая развивается на протяжении нескольких месяцев или даже недель. Характерны общие для всех типов СД симптомы, связанные с гипергликемией: полидипсия, полиурия, кожный зуд, но при СД-1 они очень ярко выражены. Так, на протяжении дня пациенты могут выпивать и выделять до 5—10 литров жидкости . Специфичным для СД-1 симптомом, который обусловлен абсолютным дефицитом инсулина, является похудение, достигающее 10—15 кг на протяжении 1-2 месяцев. Характерна выраженная общая и мышечная слабость, снижение работоспособности, сонливость . Вначале заболевания у некоторых пациентов может отмечаться повышение аппетита, которое сменяется анорексией по мере развития кетоацидоза. Последний характеризуется появлением запаха ацетона (или фруктового запаха) изо рта, тош-нотой, рвотой, нередко болями в животе (псевдоперитонит), тяжелым обезвоживанием и заканчивается развитием коматозного состояния. В ряде случаев первым проявлением СД1 является прогрессирующее нарушение сознания вплоть до комы на фоне сопутствующих заболеваний, как правило, инфекционных или острой хирургической патологии. Манифестацию СД-1 могут спровоцировать инфекционные и другие сопутствующие заболевания Характеристика СД 2 типа СД-2 является многофакторным заболеванием с наследственной предрасположенностью. Конкордатность по СД-2 у однояйцевых близнецов достигает 80 % и более. Большинство пациентов с СД-2 указывают на наличие СД-2 у ближайших родственников; при наличии СД-2 у одного из родителей вероятность его развития у потомка на протяжении жизни составляет 40 %. Какого-то одного гена, полиморфизм которого определяет предрасположенность к СД-2, не обнаружено. Большое значение в реализации наследственной предрасположенности к СД-2 Этиология. Сахарный диабет 2 типа относительная недостаточность инсулина в связи с инсулинорезистентностью и дефектом секреции инсулина ИНСУЛИНОРЕЗИСТЕНТНОСТЬ Неспособность клеток утилизировать глюкозу при нормальном количестве инсулина 1 причина – инсулинорезистентность вызывает состояние «относительного дефицита инсулина» в тканях, для преодоления которого дополнительно стимулируется в-клетка ПЖ = развивается хроническая гиперинсулинемия Инсулин усиливает разрастание жировой ткани, что способствует развитию ожирения и атеросклероза. 2 причина – с течением заболевания развивается дисфункция в-клеток - уменьшается секреция инсулина Исчезает первая фаза секреции инсулина играют факторы окружающей среды, в первую очередь, особенности образа жизни. Факторами риска развития СД-2 являются: — ожирение, особенно висцеральное; Инсулин усиливает разрастание жировой ткани, что способствует развитию ожирения и атеросклероза. — этническая принадлежность (особенно при смене традиционного образа жизни на западный); — СД-2 у ближайших родственников; — малоподвижный образ жизни; — особенности диеты (высокое потребление р афинированных углеводов и низкое содержание клетчатки); — артериальная гипертензия. Патогенез  Патогенетически СД-2 представляет собой гетерогенную группу нарушений обмена веществ, именно это и определяет его значительную клиническую неоднородность. В основе его патогенеза лежит инсулинорезистентность ( снижение опосредованной инсулиномутилизации глюкозы тканями ) , которая реализуется на фоне секреторной дисфункции в-клеток. Таким образом, происходит нарушение баланса чувствительности к инсулину и инсулиновой секреции. Секреторная дисфункция в-клеток заключается в замедлении «раннего» секреторного выброса инсулина в ответ на увеличение уровня глюкозы в крови . При этом 1-я (быстрая) фаза секреции , которая заключается в опорожнении везикул с накопленным инсулином, фактически отсутствует ; 2-я (медленная ) фаза секреции осуществляется в ответ на стабилизирующуюся гипергликемию постоянно , в тоническом режиме , и, несмотря на избыточную секрецию инсулина, уровень г ликемии на фоне инсулинорезистентности не нормализуется. Следствием гиперинулинемии является снижение чувствительности и числа инсулиновых рецепторов, а также подавление (инсулинорезистентность). глюкозы в мышечных и жировых клетках (GLUT-4) снижено на 40 % у лиц с висцеральных ожирением и на 80 % — у лиц с СД-2. Вследствие инсулинорезистентности гепатоцитов и портальной гиперинсулинемией происходит гиперпродукция глюкозы печенью, и развивается гипергликемия натощак, которая выявляется у большинства пациентов с СД-2, в том числе и на ранних этапах заболевания. Сама по себе гипергликемия неблагоприятно влияет на характер и уровень секреторной активности в-клеток ( глюкозотоксичность ). Длительно , на протяжении многих лет и десятилетий существующая гипергликемия в конечном счете приводит к истощению продукции инсулина в -клетками и у пациента могут появиться некоторые симптомы дефицита инсулина — похудение, кетоз при сопутствующих инфекционных заболеваниях. Тем не менее, остаточная продукция инсулина, которой оказывается достаточно для предотвращения кетоацидоза, при СД-2 практически всегда сохраняется. Недостаточность инкретиновой секреции. Давно высказывались предположения, что в желудочно-кишечном тракте (ЖКТ) синтезируются вещества, способные снижать уровень глюкозы крови. Эти вещества получили название «инкретины». Наибольшей активностью среди инкретинов обладает глюкагоноподобный пептид-1 (ГПП-1). Он вызывает глюкозозависимую секрецию инсулина и подавление глюкагона, снижает моторику желудка и всасывание глюкозы после еды, способствует быстрому насыщению и снижению массы тела, устраняет инсулинорезистентность. При изучении физиологии инкретинов был обнаружен дефект секреции ГПП-1 у больных с начальными проявлениями СД2 и даже у лиц с предиабетом. Стандартная пищевая нагрузка вызывала на 20–30% меньшую секрецию ГПП-1 при СД 2 по сравнению со здоровыми людьми Клинические проявления  В большинстве случаев, выраженные клинические проявления отсутствуют, и диагноз устанавливается при рутинном определении уровня гликемии. Заболевание обычно манифестирует в возрасте старше 40 лет, при этом у подавляющего большинства пациентов имеет место ожирение и другие компоненты метаболического синдрома. Лечение Лечение любого типа СД базируется на трех основных принципах: сахароснижающая терапия, диета и обучение пациентов. Инсулинотерапия при СД-1 носит заместительный характер и ее целью является максимальная имитация физиологической продукции гормона с целью достижения принятых критериев компенсации Основными компонентами лечения СД-2 являются : диетотерапия, расширение физической активности, сахароснижающая терапия , профилактика и лечение поздних осложнений СД. Поскольку большинство пациентов с СД-2 страдают ожирением, диета должна быть направлена на снижение веса (гипокалорийная) и профилактику поздних осложнений, в первую очередь макроангиопатии (атеросклероза). Гипокалорийная диета необходима всем пациентам с избытком массы тела ( И М Т 25-29 кг/м2) или ожирением ( И МТ > 30 кг/м ). В большинстве случаев следует рекомендовать снижение суточного калоража пищи до 1000—1200 ккал для женщин и до 1200-1600 ккал для мужчин. Рекомендуемое соотношение основных пищевых компонентов при СД-2 аналогично таковому при СД-1 (углеводы — 65 %,белки 10-35 %, жиры до 25-35 %) . Употребление алкоголя необходимо ограничить в связи с тем, что он является существенным источником дополнительных калорий, кроме того, прием алкоголя на фоне терапии препаратами сульфонилмочевины и инсулином может спровоцировать развитие гипогликемии. Рекомендации по расширению физической активности должны быть индивидуализированы. Вначале рекомендуются аэробные нагрузки (ходьба, плаванье) умеренной интенсивности продолжительностью 30—45 минут 3-5 раз в день (около 150 минут в неделю). В дальнейшем необходимо постепенное увеличение физических нагрузок, что в существенной мере способствует снижению и нормализации массы тела. Кроме того, физические нагрузки способствуют снижению инсулинорезистентности показывают гипогликемическое действие. 1. Препараты, способствующие снижению инсулинорезистентности (сенситайзеры). К этой группе относится метформин и тиазолидиндионы. Основными компонентами механизма действия метформина являются: 1. Подавление глюконеогенеза в печени (снижение продукции глюкозы печенью), которое приводит к снижению уровня гликемии натощак. 2. Снижение инсулинорезистентности (увеличение утилизации глюкозы периферическими тканями , прежде всего мышцами) . 3. Активация аннаэробного гликолиза и уменьшение всасывания глюкозы в тонкой кишке. Поскольку метформин не оказывает стимулирующего эффекта на продукцию инсулина, на фоне монотерапии этим препаратом гипогликемии не развиваются (его действие обозначатся как антигипергликемическое, а не как гипогликемическое). Противопоказаниями к назначению метформина являются беременность, тяжелая сердечная, печеночная, почечная и другая органная недостаточность, а также гипоксические состояния другого генеза. Крайне редким осложнением, которое встре- чается при назначении метформина без учета приведенных противопоказаний, является лактатацидоз, являющийся следствием гиперактивации анаэробного гликолиза. Тиазолидиндионы (пиоглитазон,) я вляются агонистами у-рецепторов, активируемых пролифератором пероксисом (PPAR-y). Тиазолидиндионы активируют метаболизм глюкозы и липидов в мышечной и жировой тканях, что приводит к повышению активности эндогенного инсулина, т.е. 2. Препараты, воздействующие на в-клетку и способствующие усилению секреции инсулина (секретогоги). К этой группе относятся препараты сульфонилмочевины и глиниды (прандиальные регуляторы гликемии), которые используют преимущественно для нормализации уровня гликемии после еды. Основной мишенью препаратов сульфонилмочевины (ПСМ) являются в-клетки панкреатических островков. ПСМ связываются на мембране р-клеток со специфическими рецепторами. Это приводит к закрытию АТФ-зависимых калиевых каналов и деполяризации клеточной мембраны, что в свою очередь способствует о ткрытию кальциевых каналов. Поступление кальция внутрь в-клеток приводит к их дегрануляции и выбросу инсулина в кровь. К группе глинидов (прандиальные регуляторы гликемии) относятся репаглинид (производное бензоевой кислоты; суточная доза 0,5—16 мг/сут). После приема препараты быстро и обратимо взаимодействуют с рецептором сульфонилмочевины на (3-клетке, в результате чего происходит короткое повышение уровня инсулина, которое имитирует первую фазу его секреции в норме. Препараты принимаются за 10—20 минут до основных приемов пищи , обычно 3 раза вдень . 3. Препараты с инкретиновой активностью, к этой группе относят 2 класса препаратов: ингибиторы ДПП-4 и агонисты рецепторов ГПП-1. Их эффект основан на инкретиновом ответе. Инкретиновый эффект — это значительное увеличение секреции инсулина в ответ на пероральное поступление углеводов, опосредованное действием инкретиновых гормонов кишечника. У здоровых людей инкретины отвечают за 50–70% всего секретируемого постпрандиального инсулина, т. е. в норме вклад «инкретинового эффекта» в прирост уровня постпрандиального инсулина составляет около 70%, а у пациентов с СД 2 типа он существенно снижен. 1. Ингибиторы ДПП-4 (ситаглиптин, вилдаглиптин, саксаглиптин). К их преимуществам относится: низкий риск гипогликемий; отсутствие влияния на массу тела, доступны в фиксированных комбинациях с метформином; потенциальный протективный эффект в отношении β-клеток 2. Агонисты Рецепторов ГПП-1(эксенатид, лираглутид, ликсисенатид, дулаглутид, семаглутид). К их преимуществам относится: низкий риск гипогликемии; снижение массы тела; снижение АД; потенциальный; протективный эффект в отношении β-клеток; вторичная профилактика у пациентов с АССЗ ; возможно эффективны в качестве первичной профилактики у лиц с сердечно-сосудистыми ФР. Противопоказаны при тяжелой почечной и печеночной недостаточности; кетоацидозе; беременности и лактации. 4. Средства, ингибирующие реабсорбцию глюкозы в почках- Ингибиторы НГЛТ-2 (дапаглифлозин, эмпаглифлозин, канаглифлозин). К их преимуществам относится: низкий риск гипогликемии, снижение массы тела, эффект не зависит от наличия инсулина в крови, умеренное снижение АД, значительное снижение риска госпитализаций по поводу хронической сердечной недостаточности. Но повышают риск гиповолемии, урогенитальных инфекций Алгоритм работы с пациентами с гипергликемией Подтверждение СД - определение гликемии (по стандарту) 1. Определить причину нарушения углеводного обмена (классификация СД) 2. Исходя из причины и типа СД – определить методику лечения. 3. Назначить рациональное питание и физическую нагрузку 4. Выбрать лучшую группу в патогенетическом плане из сахароснижающих препаратов 5. Проверить отсутствие противопоказаний у пациента 6. Оценить возможность развития побочных эффектов 7. Контроль эффективности терапии 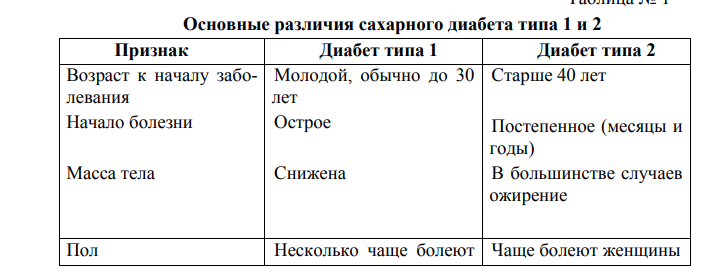 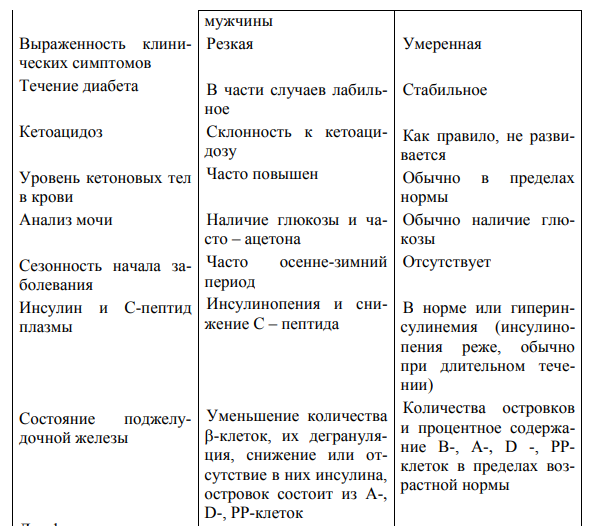 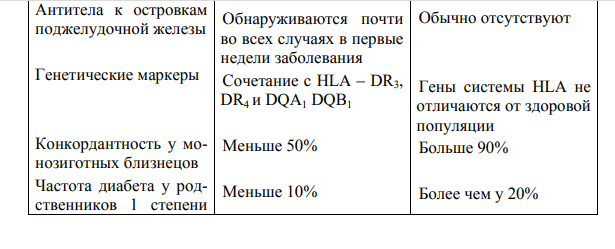  |
